Mierzy się ilość ciepła w układzie SI. Metody i środki pomiaru ilości ciepła
Ciepło- energia przekazywana z cieplejszego ciała do mniej nagrzanego poprzez bezpośredni kontakt lub promieniowanie.
Temperatura jest miarą intensywności ruchu cząsteczek.
Ilość ciepła posiadanego przez ciało w danej temperaturze zależy od jego masy; Na przykład, w tej samej temperaturze w dużej filiżance wody gromadzi się więcej ciepła niż w małej, a w wiadrze zimnej wody może być więcej niż w filiżance gorąca woda(chociaż temperatura wody w wiadrze jest niższa).
Ciepło odgrywa ważną rolę w życiu człowieka, w tym w funkcjonowaniu jego organizmu. Część energii chemicznej zawartej w pożywieniu zamieniana jest na ciepło, dzięki czemu temperatura ciała utrzymywana jest w pobliżu 37°C. Bilans cieplny ludzkiego ciała zależy również od temperatury. środowisko, a ludzie zmuszeni są wydać dużo energii na ogrzewanie pomieszczeń mieszkalnych i przemysłowych zimą i chłodzenie ich latem. Większość tej energii jest dostarczana przez silniki cieplne, takie jak kotłownie i turbiny parowe elektrowni, które zasilane są paliwami kopalnymi (węgiel, olej) i wytwarzają energię elektryczną.
Do końca XVIII wieku. ciepło uważano za substancję materialną, uważając, że temperatura ciała zależy od ilości<калорической жидкости>, lub<теплорода>. Później B. Rumford, J. Joule i inni fizycy tamtych czasów, poprzez dowcipne eksperymenty i rozumowanie, obalili<калорическую>teorii, udowadniając, że ciepło jest nieważkie i można je uzyskać w dowolnej ilości po prostu dzięki ruchowi mechanicznemu. Ciepło samo w sobie nie jest substancją - jest po prostu energią ruchu jej atomów lub cząsteczek. Właśnie takiemu rozumieniu ciepła jest współczesna fizyka.
W tym artykule przyjrzymy się, jak ciepło i temperatura są powiązane i jak te wielkości są mierzone. Przedmiotem naszej dyskusji będą również następujące pytania: przenoszenie ciepła z jednej części ciała do drugiej; przenoszenie ciepła w próżni (przestrzeni, która nie zawiera materii); rola ciepła we współczesnym świecie.
Ciepło i temperatura
Ilość energii cieplnej w substancji nie może być określona przez obserwację ruchu każdej z jej cząsteczek z osobna. Wręcz przeciwnie, tylko badając makroskopowe właściwości materii, można znaleźć charakterystykę mikroskopowego ruchu wielu cząsteczek uśrednionych w pewnym okresie czasu. Temperatura substancji jest średnim wskaźnikiem intensywności ruchu cząsteczek, których energia wynosi energia cieplna Substancje.
Jednym z najbardziej znanych, ale jednocześnie najmniej dokładnych sposobów szacowania temperatury jest dotyk. Dotykając przedmiotu, oceniamy, czy jest gorący, czy zimny, skupiając się na naszych uczuciach. Oczywiście odczucia te zależą od temperatury naszego ciała, co prowadzi nas do pojęcia równowagi termicznej – jednej z najważniejszych przy pomiarze temperatury.
Równowaga termiczna
Równowaga cieplna między ciałami A i B
Oczywiście, jeśli dwa ciała A i B są mocno do siebie dociśnięte, to po ich dotknięciu po wystarczająco długim czasie zauważymy, że ich temperatura jest taka sama. W tym przypadku mówi się, że ciała A i B są ze sobą w równowadze termicznej. Jednak ciała, ogólnie rzecz biorąc, nie muszą być w kontakcie, aby istniała między nimi równowaga termiczna - wystarczy, że ich temperatury są takie same. Można to zweryfikować za pomocą trzeciego ciała C, najpierw doprowadzając je do równowagi termicznej z ciałem A, a następnie porównując temperatury ciał C i B. Ciało C pełni tutaj rolę termometru. W ścisłym ujęciu zasada ta nazywana jest zerową zasadą termodynamiki: jeśli ciała A i B znajdują się w równowadze termicznej z trzecim ciałem C, to ciała te również są ze sobą w równowadze termicznej. To prawo leży u podstaw wszystkich metod pomiaru temperatury.
Pomiar temperatury

Skale temperatury

termometry
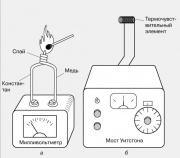
Termometry oparte na efektach elektrycznych
Jeśli chcemy przeprowadzać dokładne eksperymenty i obliczenia, nie wystarczą takie oceny temperatur, jak ciepło, ciepło, zimno, zimno - potrzebujemy stopniowanej skali temperatury. Istnieje kilka takich skal, a jako punkty odniesienia zwykle przyjmuje się punkty zamarzania i wrzenia wody. Na rysunku pokazano cztery najpopularniejsze skale. Skala Celsjusza, według której temperatura zamarzania wody odpowiada 0 °, a wrzenia 100 °, nazywana jest skalą Celsjusza od nazwiska szwedzkiego astronoma A. Celsjusza, który opisał ją w 1742 roku. Uważa się, że Szwedzki przyrodnik K. Linneusz jako pierwszy zastosował tę skalę. Teraz skala Celsjusza jest najbardziej powszechna na świecie. Skala temperatury Fahrenheita, w której temperatury zamarzania i wrzenia wody odpowiadają wyjątkowo niewygodnym liczbom 32 i 212 °, została zaproponowana w 1724 roku przez G. Fahrenheita. Skala Fahrenheita jest szeroko stosowana w krajach anglojęzycznych, ale w literaturze naukowej jest rzadko stosowana. Aby przeliczyć temperaturę Celsjusza (°C) na temperaturę Fahrenheita (°F), istnieje formuła °F = (9/5)°C + 32, a dla tłumaczenia odwrotnego - formuła °C = (5/9) ( °F-32).
Obie skale - zarówno Fahrenheita, jak i Celsjusza - są bardzo niewygodne podczas przeprowadzania eksperymentów w warunkach, w których temperatura spada poniżej punktu zamarzania wody i jest wyrażana jako liczba ujemna. W takich przypadkach wprowadzono bezwzględne skale temperatury, które opierają się na ekstrapolacji do tzw. zera bezwzględnego – punktu, w którym ruch molekularny powinien się zatrzymać. Jedna z nich nazywa się skalą Rankina, a druga nazywa się absolutną skalą termodynamiczną; temperatury są mierzone w stopniach Rankine'a (°R) i kelwinach (K). Obie skale zaczynają się od zera bezwzględnego, a temperatura zamarzania wody odpowiada 491,7 ° R i 273,16 K. Liczba stopni i kelwinów między punktami zamarzania i wrzenia wody w skali Celsjusza i bezwzględnej skali termodynamicznej jest taka sama i równa do 100; dla skal Fahrenheita i Rankine'a jest to również takie samo, ale równe 180. Stopnie Celsjusza są konwertowane na kelwiny za pomocą wzoru K \u003d ° C + 273,16, a stopnie Fahrenheita są konwertowane na stopnie Rankine'a za pomocą wzoru ° R \u003d ° F + 459,7.
Działanie urządzeń przeznaczonych do pomiaru temperatury opiera się na różnych zjawiskach fizycznych związanych ze zmianą energii cieplnej substancji - zmianach oporu elektrycznego, objętości, ciśnienia, charakterystyk radiacyjnych, właściwości termoelektrycznych. Jednym z najprostszych i najbardziej znanych przyrządów do pomiaru temperatury jest szklany termometr pokazany na rysunku. Kulka c w dolnej części termometru jest umieszczana w medium lub dociskana do przedmiotu, którego temperatura ma być mierzona i w zależności od tego, czy kulka nagrzewa się, czy oddaje, rozszerza się lub kurczy, a jej kolumna unosi się lub opada w kapilarny. Jeśli termometr jest wstępnie skalibrowany i wyposażony w skalę, możesz bezpośrednio sprawdzić temperaturę ciała.
Kolejnym urządzeniem, którego działanie opiera się na rozszerzalności cieplnej, jest termometr bimetalicznyprzedstawiony na rysunku. Jego głównym elementem jest spiralna płyta z dwóch lutowanych metali o różnych współczynnikach rozszerzalności cieplnej. Po podgrzaniu jeden z metali rozszerza się bardziej niż drugi, spirala skręca się i obraca strzałkę względem skali. Takie urządzenia są często używane do pomiaru temperatury powietrza wewnątrz i na zewnątrz, ale nie nadają się do określania temperatury lokalnej.
Temperatura lokalna jest zwykle mierzona za pomocą termopary, czyli dwóch drutów z różnych metali przylutowanych na jednym końcu. Kiedy takie złącze jest podgrzewane, na wolnych końcach przewodów powstaje pole elektromagnetyczne, zwykle o wartości kilku miliwoltów. Termopary wykonane są z różnych par metali: żelazo i konstantan, miedź i konstantan, chromel i alumel. Ich termo-EMF zmienia się niemal liniowo wraz z temperaturą w szerokim zakresie temperatur.
Znany jest również inny efekt termoelektryczny - zależność rezystancji materiału przewodzącego od temperatury. Stanowi on podstawę działania termometrów oporowych, z których jeden pokazano na rysunku. Rezystancja małego elementu pomiarowego temperatury (termopary) - zwykle cewek z cienkiego drutu - jest porównywana z rezystancją skalibrowanego rezystora zmiennego za pomocą mostka Wheatstone'a. Instrument wyjściowy może być skalowany bezpośrednio w stopniach.
Pirometry optyczne służą do pomiaru temperatury gorących ciał, które emitują światło widzialne. W jednej z wersji tego urządzenia światło emitowane przez ciało jest porównywane z promieniowaniem żarnika żarówki umieszczonego w płaszczyźnie ogniskowej lornetki, przez którą patrzy się na emitujące ciało. Prąd elektryczny, podgrzewający żarnik lampy, jest zmieniany, aż po wzrokowym porównaniu żaru żarnika i ciała stwierdza się, że między nimi została ustalona równowaga termiczna. Skalę urządzenia można wyskalować bezpośrednio w jednostkach temperatury.
Postęp techniczny ostatnie lata pozwoliło na stworzenie nowych czujników temperatury. Na przykład w przypadkach, w których potrzebna jest szczególnie wysoka czułość, zamiast termopary lub konwencjonalnego termometru oporowego stosuje się urządzenie półprzewodnikowe - termistor. Barwniki i ciekłe kryształy zmieniające swój stan fazowy są również wykorzystywane jako konwertery termiczne, zwłaszcza w przypadkach, gdy temperatura powierzchni ciała zmienia się w szerokim zakresie. Wreszcie stosuje się termografię w podczerwieni, w której obraz obiektu w podczerwieni uzyskuje się w kolorach warunkowych, gdzie każdy kolor odpowiada określonej temperaturze. Ta metoda pomiaru temperatury znajduje najszersze zastosowanie - od diagnostyka medyczna przed sprawdzeniem izolacji termicznej pomieszczeń.
Pomiar ilości ciepła
kalorymetr wodny
Energię cieplną (ilość ciepła) ciała można zmierzyć bezpośrednio za pomocą tak zwanego kalorymetru; Prostą wersję takiego urządzenia pokazano na rysunku. Jest to starannie izolowane naczynie zamknięte, wyposażone w urządzenia do pomiaru temperatury wewnątrz, a niekiedy wypełnione płynem roboczym o znanych właściwościach, takim jak woda. Aby zmierzyć ilość ciepła w małym ogrzanym ciele, umieszcza się je w kalorymetrze i czeka na osiągnięcie przez układ równowagi termicznej. O ilości ciepła przekazywanego do kalorymetru (a dokładniej do napełniającej go wody) decyduje wzrost temperatury wody.
Ilość ciepła uwalnianego podczas reakcji chemicznej, takiej jak spalanie, można zmierzyć, umieszczając mały<бомбу>. W<бомбе>znajduje się próbka, do której podłączone są przewody elektryczne do zapłonu i odpowiednia ilość tlenu. Po całkowitym wypaleniu się próbki i ustaleniu równowagi termicznej określa się, o ile wzrosła temperatura wody w kalorymetrze, a tym samym ilość uwolnionego ciepła.
Jednostki ciepła
Ciepło jest formą energii i dlatego musi być mierzone w jednostkach energii. W międzynarodowym układzie SI jednostką energii jest dżul (J). Dopuszcza się również stosowanie pozasystemowych jednostek ilości ciepła - kalorie: kaloria międzynarodowa to 4,1868 J, kaloria termochemiczna to 4,1840 J. W laboratoriach zagranicznych wyniki badań są często wyrażane za pomocą tzw. Kaloria 15 stopni równa się 4,1855 J. Brytyjska jednostka termiczna (BTU) poza systemem wychodzi z użycia: BTU średnio = 1,055 J.
Źródła ciepła
Głównymi źródłami ciepła są reakcje chemiczne i jądrowe, a także różne procesy konwersji energii. Przykładami reakcji chemicznych z uwolnieniem ciepła są spalanie i rozpad składników żywności. Prawie całe ciepło odbierane przez Ziemię pochodzi z reakcji jądrowych zachodzących w głębinach Słońca. Ludzkość nauczyła się pozyskiwać ciepło za pomocą kontrolowanych procesów rozszczepienia jądra atomowego, a teraz próbuje wykorzystać w tym samym celu reakcje syntezy termojądrowej. Inne rodzaje energii można również przekształcić w ciepło, takie jak praca mechaniczna i energia elektryczna. Należy pamiętać, że energię cieplną (jak każdą inną) można tylko przekształcić w inną formę, ale nie można jej uzyskać.<из ничего>ani nie niszczyć. Jest to jedna z podstawowych zasad nauki zwanej termodynamiką.
Termodynamika
Termodynamika jest nauką o związku między ciepłem, pracą i materią. Współczesne idee dotyczące tych relacji powstały na podstawie prac tak wielkich naukowców z przeszłości, jak Carnot, Clausius, Gibbs, Joule, Kelvin itp. Termodynamika wyjaśnia znaczenie pojemności cieplnej i przewodności cieplnej substancji, rozszerzalność cieplna ciał i ciepło przemian fazowych. Nauka ta opiera się na kilku eksperymentalnie ustalonych prawach - zasadach.
Ciepło i właściwości substancji
Różne substancje mają różną zdolność do gromadzenia energii cieplnej; zależy to od ich struktury molekularnej i gęstości. Ilość ciepła potrzebna do podniesienia temperatury jednostkowej masy substancji o jeden stopień nazywana jest jej pojemnością cieplną właściwą. Pojemność cieplna zależy od warunków, w jakich znajduje się substancja. Na przykład, aby ogrzać jeden gram powietrza w balonie o 1 K, potrzeba więcej ciepła niż ogrzać go w ten sam sposób w szczelnym naczyniu o sztywnych ściankach, ponieważ część energii przekazanej balonowi jest zużywana na rozszerzenie powietrze, a nie na jego ogrzewanie. Dlatego w szczególności pojemność cieplna gazów jest mierzona oddzielnie przy stałym ciśnieniu i przy stałej objętości.
Wraz ze wzrostem temperatury wzrasta intensywność chaotycznego ruchu cząsteczek - większość substancji rozszerza się po podgrzaniu. Nazywa się stopień ekspansji substancji ze wzrostem temperatury o 1 K Współczynnik rozszerzalności cieplnej.
Aby substancja mogła przejść z jednego stanu fazowego do drugiego, na przykład ze stałego do ciekłego (a czasem natychmiastowego do gazowego), musi otrzymać określoną ilość ciepła. Po podgrzaniu solidny, wtedy jego temperatura wzrośnie, aż zacznie się topić; aż do zakończenia topienia temperatura ciała pozostanie stała pomimo dopływu ciepła. Ilość ciepła potrzebna do stopienia masy jednostkowej substancji nazywana jest ciepłem topnienia. Jeśli nadal będziesz dostarczać ciepło, stopiona substancja podgrzeje się do wrzenia. Ilość ciepła potrzebna do odparowania masy jednostkowej cieczy w danej temperaturze nazywana jest ciepłem parowania.
Rola ciepła i jego wykorzystanie
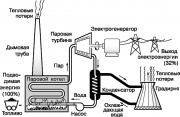
Schemat działania elektrowni z turbiną parową
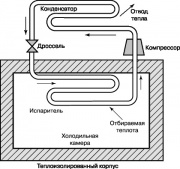
Schemat obiegu chłodniczego
Globalne procesy wymiany ciepła nie sprowadzają się do ogrzewania Ziemi promieniowaniem słonecznym. Ogromne prądy konwekcyjne w atmosferze determinują codzienne zmiany warunków pogodowych na całym świecie. Różnice temperatur w atmosferze między regionami równikowymi i polarnymi, wraz z siłami Coriolisa wynikającymi z rotacji Ziemi, prowadzą do pojawienia się stale zmieniających się prądów konwekcyjnych, takich jak pasaty, prądy strumieniowe oraz fronty ciepłe i zimne.
Przenoszenie ciepła (ze względu na przewodność cieplną) ze stopionego jądra Ziemi na jego powierzchnię prowadzi do erupcji wulkanicznych i pojawienia się gejzerów. W niektórych regionach energia geotermalna jest wykorzystywana do ogrzewania pomieszczeń i wytwarzania energii.
Ciepło jest nieodzownym uczestnikiem prawie wszystkich procesy produkcji. Wymienimy najważniejsze z nich, takie jak wytop i obróbka metali, eksploatacja silników, produkcja żywności, synteza chemiczna, rafinacja ropy naftowej, produkcja szerokiej gamy przedmiotów - od cegieł i naczyń po samochody i urządzenia elektroniczne .
Wiele produkcji przemysłowych i transportowych, a także elektrociepłowni nie mogłoby działać bez silników cieplnych - urządzeń, które zamieniają ciepło w użyteczną pracę. Przykładami takich maszyn są sprężarki, turbiny, silniki parowe, benzynowe i odrzutowe.
Jednym z najbardziej znanych silników cieplnych jest turbina parowa, która realizuje część obiegu Rankine'a stosowanego w nowoczesnych elektrowniach. Uproszczony schemat tego cyklu pokazano na rysunku. Płyn roboczy - woda - jest przekształcany w parę przegrzaną w kotle parowym ogrzewanym spalaniem paliw kopalnych (węgiel, olej lub gaz ziemny). Wysoka para
Gasovik - przemysłowe urządzenia gazowe Katalog GOST, SNiP, PB Jednostki wielkości fizycznych, pojęcia fizykochemiczne, stosunki, skład i charakterystyka gazów
Jednostki miary temperatury i ilości ciepła
Podstawową jednostką pomiaru temperatury był stopień Międzynarodowej Skali Temperatury, co praktycznie odpowiada stopniowi Celsjusza. Wartość ta jest równa 1/100 przedziału temperatur od 0 do 100°C, czyli między punktami topnienia lodu i wrzącej wody pod ciśnieniem 760 mm Hg. Sztuka.
Temperatura bezwzględna to temperatura mierzona od zera bezwzględnego, czyli od -273,16°C i mierzona w stopniach Kelvina (°K). Stopień Kelvina jest taki sam jak stopień Celsjusza. Dlatego temperaturę bezwzględną wyraża się w stopniach Celsjusza w następujący sposób:
T, °K = t, °C + 273,16
W układzie SI jednostką temperatury jest Kelwin. Dopuszcza się wyrażanie praktycznych wyników pomiarów temperatury w stopniach Celsjusza wraz ze stopniami Kelvina, w zależności od pochodzenia (położenia zera) na skali.
Przykład: 250 ±5 °С = 523,16 ±5 °K.
W układzie SI praca, energia i ciepło są mierzone w dżulach (J). Czasami stosuje się większą i wygodniejszą jednostkę do celów praktycznych - kilodżul (kJ), równy 1000 J. Jednostka pracy w SI to praca wykonana przez siłę 1 N przy przemieszczeniu 1 m. Energia - wielkość fizyczna pokazując, ile pracy może wykonać ciało.
Kalorie i kilokalorie mogą być używane jako jednostki ciepła poza systemem. Kaloria to ilość ciepła potrzebna do podniesienia temperatury 1 grama wody o 1°C (19,5 do 20,5°C).
1 cal (kaloria) = 4,1868 J;
1 kcal (kilokaloria) \u003d 1000 cal \u003d 4186,8 J \u003d 4,187 kJ;
1 Mcal (megakaloria) \u003d 10 6 cal \u003d 4,1868 MJ;
1 Gcal (gigakaloria) \u003d 10 9 cal \u003d 4186,8 MJ.
Dla porównania przy ocenie paliwa stosuje się tzw. ciepło warunkowe, którego wartość opałowa do obliczeń przyjmuje warunkowo 7 Mcal/kg lub 7 Gcal/t. W takich przypadkach mówi się odpowiednio o 1 kg lub 1 tonie standardowego paliwa (t.c.f.).
Ciepło odgrywa ważną rolę w życiu człowieka, w tym w funkcjonowaniu jego organizmu. Część energii chemicznej zawartej w pożywieniu zamieniana jest na ciepło, dzięki czemu temperatura ciała utrzymywana jest w pobliżu 37
° C. Bilans cieplny organizmu człowieka zależy również od temperatury otoczenia, a ludzie zmuszeni są do poświęcania dużej ilości energii na ogrzewanie pomieszczeń mieszkalnych i przemysłowych zimą i ich chłodzenie latem. Większość tej energii jest dostarczana przez silniki cieplne, takie jak kotłownie i turbiny parowe elektrowni, które zasilane są paliwami kopalnymi (węgiel, olej) i wytwarzają energię elektryczną.Do końca XVIII wieku. ciepło uważano za substancję materialną, wierząc, że temperatura ciała zależy od ilości zawartej w nim „cieczy kalorycznej” lub „kalorycznej”. Później B. Rumford, J. Joule i inni ówcześni fizycy, poprzez pomysłowe eksperymenty i rozumowanie, obalili teorię „kaloryczną”, udowadniając, że ciepło jest nieważkie i można je uzyskać w dowolnej ilości po prostu dzięki ruchowi mechanicznemu. Samo ciepło nie jest substancją, jest po prostu energią ruchu jej atomów lub cząsteczek. Właśnie takiemu rozumieniu ciepła jest współczesna fizyka. Zobacz też FIZYKA.
W tym artykule przyjrzymy się, jak ciepło i temperatura są powiązane i jak te wielkości są mierzone. Przedmiotem naszej dyskusji będą również następujące pytania: przenoszenie ciepła z jednej części ciała do drugiej; przenoszenie ciepła w próżni (przestrzeni, która nie zawiera materii); rola ciepła we współczesnym świecie.
CIEPŁO I TEMPERATURA Ilość energii cieplnej w substancji nie może być określona przez obserwację ruchu każdej z jej cząsteczek z osobna. Wręcz przeciwnie, tylko badając makroskopowe właściwości materii, można znaleźć charakterystykę mikroskopowego ruchu wielu cząsteczek uśrednionych w pewnym okresie czasu. Temperatura substancji jest średnim wskaźnikiem intensywności ruchu cząsteczek, których energia jest energią cieplną substancji.Jeden z najbardziej znanych, ale też najmniej dokładnych sposobów oceny temperatury dotykiem. Dotykając przedmiotu, oceniamy, czy jest gorący, czy zimny, skupiając się na naszych uczuciach. Oczywiście odczucia te zależą od temperatury naszego ciała, co prowadzi nas do pojęcia równowagi termicznej, jednej z najważniejszych przy pomiarach temperatury.
Bilans cieplny. Oczywiście, jeśli dwa ciała A i B (rys. 1) mocno do siebie dociśnięte, a następnie dotykając ich po wystarczająco długim czasie, zauważymy, że ich temperatura jest taka sama. W tym przypadku mówi się, że ciała są A i B są ze sobą w równowadze termicznej. Jednak ciała, ogólnie rzecz biorąc, nie muszą być w kontakcie, aby istniała między nimi równowaga termiczna, wystarczy, że ich temperatury są takie same. Można to zweryfikować za pomocą trzeciego organu C , doprowadzając go najpierw do równowagi termicznej z ciałem A , a następnie porównanie temperatur ciał C i b. Ciało C tutaj pełni rolę termometru. W ścisłym sformułowaniu zasada ta nazywana jest zerową zasadą termodynamiki: jeśli ciała A i B są w równowadze termicznej z trzecim ciałem C, to ciała te również znajdują się względem siebie w równowadze termicznej. To prawo leży u podstaw wszystkich metod pomiaru temperatury.Pomiar temperatury. Jeśli chcemy przeprowadzać dokładne eksperymenty i obliczenia, to takie wskaźniki temperatury jak ciepło, ciepło, chłodno, zimno nie wystarczą, potrzebujemy stopniowanej skali temperatury. Istnieje kilka takich skal, a jako punkty odniesienia zwykle przyjmuje się punkty zamarzania i wrzenia wody. Cztery najczęstsze skale pokazano na ryc. 2. Skala Celsjusza, zgodnie z którą temperatura zamarzania wody odpowiada 0° , a temperatura wrzenia wynosi 100° , nazywana jest skalą Celsjusza od nazwiska szwedzkiego astronoma A. Celsjusza, który opisał ją w 1742 roku. Uważa się, że jako pierwszy zastosował tę skalę szwedzki przyrodnik K. Linney. Teraz skala Celsjusza jest najbardziej powszechna na świecie. Skala temperatury Fahrenheita, w której temperatury zamarzania i wrzenia wody odpowiadają wyjątkowo niewygodnym liczbom 32 i 212° , został zaproponowany w 1724 r. przez G. Fahrenheita. Skala Fahrenheita jest szeroko stosowana w krajach anglojęzycznych, ale w literaturze naukowej jest rzadko stosowana. Aby przeliczyć temperaturę na stopnie Celsjusza (° C) do temperatury Fahrenheita (° F) istnieje formuła° F = (9/5) ° C + 32, a dla formuły tłumaczenia zwrotnego°C = (5/9) (°F - 32). Obie skale, zarówno Fahrenheita, jak i Celsjusza, są bardzo niewygodne podczas przeprowadzania eksperymentów w warunkach, w których temperatura spada poniżej punktu zamarzania wody i jest wyrażana jako liczba ujemna. W takich przypadkach wprowadzono bezwzględne skale temperatury, które opierają się na ekstrapolacji do tzw. zera bezwzględnego, czyli punktu, w którym ruch molekularny musi się zatrzymać. Jedna z nich nazywa się skalą Rankina, a druga nazywa się absolutną skalą termodynamiczną; temperatury są mierzone w stopniach Rankine'a (° R) i kelwiny (K). Obie skale zaczynają się od zera absolutnego, a temperatura zamarzania wody wynosi 491,7° R i 273,16 K. Liczba stopni i kelwinów między temperaturą zamarzania i wrzenia wody w skali Celsjusza i bezwzględnej skali termodynamicznej jest taka sama i równa 100; dla skal Fahrenheita i Rankine'a jest również taki sam, ale równy 180. Stopnie Celsjusza są przeliczane na kelwiny za pomocą wzoru K \u003d° C + 273,16 i stopnie Fahrenheita na stopnie Rankine'a za pomocą wzoru°R = °F + 459,7. Działanie urządzeń przeznaczonych do pomiaru temperatury opiera się na różnych zjawiskach fizycznych związanych ze zmianą energii cieplnej substancji, zmianami oporu elektrycznego, objętości, ciśnienia, charakterystyk radiacyjnych i właściwości termoelektrycznych. Jednym z najprostszych i najbardziej znanych przyrządów do pomiaru temperatury jest termometr rtęciowy przedstawiony na ryc. 3, a. Kulka z rtęcią w dolnej części termometru jest umieszczana w medium lub dociskana do obiektu, którego temperatura ma być mierzona i w zależności od tego, czy kulka otrzymuje ciepło, czy też się oddaje, rtęć rozszerza się lub kurczy, a jej kolumna unosi się lub spada w kapilarze. Jeśli termometr jest wstępnie skalibrowany i wyposażony w skalę, możesz bezpośrednio sprawdzić temperaturę ciała.Kolejnym urządzeniem, którego działanie opiera się na rozszerzalności cieplnej jest termometr bimetaliczny przedstawiony na ryc.
3, b. Jego główny element spiralna płyta z dwóch lutowanych metali o różnych współczynnikach rozszerzalności cieplnej. Po podgrzaniu jeden z metali rozszerza się bardziej niż drugi, spirala skręca się i obraca strzałkę względem skali. Takie urządzenia są często używane do pomiaru temperatury powietrza wewnątrz i na zewnątrz, ale nie nadają się do określania temperatury lokalnej.Temperatura lokalna jest zwykle mierzona za pomocą termopary, czyli dwóch drutów z różnych metali lutowanych na jednym końcu (rys.
4, a). Kiedy takie złącze jest podgrzewane, na wolnych końcach przewodów powstaje emf, zwykle kilka miliwoltów. Termopary wykonane są z różnych par metali: żelazo i konstantan, miedź i konstantan, chromel i alumel. Ich termo-EMF zmienia się niemal liniowo wraz z temperaturą w szerokim zakresie temperatur.Znany jest również inny efekt termoelektryczny - zależność rezystancji materiału przewodzącego od temperatury. Leży u podstaw działania termometrów oporowych, z których jeden pokazano na ryc.
4, b. Rezystancja małego elementu wrażliwego na temperaturę (czujnika termicznego), zwykle zwojów cienkiego drutu, jest porównywana z rezystancją skalibrowanego rezystora zmiennego za pomocą mostka Wheatstone'a. Instrument wyjściowy może być skalowany bezpośrednio w stopniach.Pirometry optyczne służą do pomiaru temperatury ciał żarowych emitujących światło widzialne. W jednej z wersji tego urządzenia światło emitowane przez ciało jest porównywane z promieniowaniem żarnika żarówki umieszczonego w płaszczyźnie ogniskowej lornetki, przez którą patrzy się na emitujące ciało. Prąd elektryczny, który ogrzewa żarnik lampy, zmienia się, dopóki wizualne porównanie żaru żarnika i ciała nie ujawni, że między nimi została ustalona równowaga termiczna. Skalę urządzenia można wyskalować bezpośrednio w jednostkach temperatury.
Postęp techniczny w ostatnich latach umożliwił stworzenie nowych czujników temperatury. Na przykład w przypadkach, w których potrzebna jest szczególnie wysoka czułość, zamiast termopary lub konwencjonalnego termometru oporowego stosuje się urządzenie półprzewodnikowe, termistor. Barwniki i ciekłe kryształy zmieniające swój stan fazowy są również wykorzystywane jako konwertery termiczne, zwłaszcza w przypadkach, gdy temperatura powierzchni ciała zmienia się w szerokim zakresie. Wreszcie stosuje się termografię w podczerwieni, w której obraz obiektu w podczerwieni uzyskuje się w kolorach warunkowych, gdzie każdy kolor odpowiada określonej temperaturze. Ta metoda pomiaru temperatury znajduje najszersze zastosowanie od diagnostyki medycznej po sprawdzanie izolacji termicznej pomieszczeń. Zobacz też FIZYKA PAŃSTWA SOLIDNEGO; PŁYNNY KRYSZTAŁ.
Pomiar ilości ciepła. Energię cieplną (ilość ciepła) ciała można zmierzyć bezpośrednio za pomocą tak zwanego kalorymetru; Prostą wersję takiego urządzenia pokazano na ryc. 5. Jest to starannie izolowane naczynie zamknięte, wyposażone w urządzenia do pomiaru temperatury w jego wnętrzu i czasami wypełnione płynem roboczym o znanych właściwościach, takim jak woda. Aby zmierzyć ilość ciepła w małym ogrzanym ciele, umieszcza się je w kalorymetrze i czeka na osiągnięcie przez układ równowagi termicznej. O ilości ciepła przekazywanego do kalorymetru (a dokładniej do napełniającej go wody) decyduje wzrost temperatury wody.Ilość ciepła uwalnianego podczas reakcji chemicznej, takiej jak spalanie, można zmierzyć umieszczając małą „bombę” w kalorymetrze. „Bomba” zawiera próbkę, do której podłączone są przewody elektryczne w celu zapłonu, oraz odpowiednią ilość tlenu. Po całkowitym wypaleniu się próbki i ustaleniu równowagi termicznej określa się, o ile wzrosła temperatura wody w kalorymetrze, a co za tym idzie ilość uwolnionego ciepła. Zobacz też KALORYMETRIA.
Jednostki ciepła. Ciepło jest formą energii i dlatego musi być mierzone w jednostkach energii. W międzynarodowym układzie SI jednostką energii jest dżul (J). Dopuszcza się również stosowanie niesystemowych jednostek ilości kalorii cieplnych: międzynarodowa kaloria to 4,1868 J, kaloria termochemiczna to 4,1840 J. W zagranicznych laboratoriach wyniki badań są często wyrażane za pomocą tzw. Kaloria 15 stopni równa się 4,1855 J. Brytyjska jednostka termiczna (BTU) poza systemem wychodzi z użycia: BTU średnio = 1,055 J. Głównymi źródłami ciepła są reakcje chemiczne i jądrowe, a także różne procesy konwersji energii. Przykładami reakcji chemicznych z uwolnieniem ciepła są spalanie i rozpad składników żywności. Prawie całe ciepło odbierane przez Ziemię pochodzi z reakcji jądrowych zachodzących w głębinach Słońca. Ludzkość nauczyła się pozyskiwać ciepło za pomocą kontrolowanych procesów rozszczepienia jądra atomowego, a teraz próbuje wykorzystać w tym samym celu reakcje syntezy termojądrowej. Inne rodzaje energii można również przekształcić w ciepło, takie jak praca mechaniczna i energia elektryczna. Należy pamiętać, że energię cieplną (jak każdą inną) można tylko przekształcić w inną formę, ale nie można jej uzyskać „z niczego” ani zniszczyć. Jest to jedna z podstawowych zasad nauki zwanej termodynamiką. TERMODYNAMIKA Termodynamika to nauka o związku między ciepłem, pracą i materią. Współczesne idee dotyczące tych relacji powstały na podstawie prac tak wielkich naukowców z przeszłości, jak Carnot, Clausius, Gibbs, Joule, Kelvin itp. Termodynamika wyjaśnia znaczenie pojemności cieplnej i przewodności cieplnej substancji, rozszerzalność cieplna ciał i ciepło przemian fazowych. Nauka ta opiera się na kilku eksperymentalnie ustalonych zasadach praw.Początki termodynamiki. Sformułowana powyżej zerowa zasada termodynamiki wprowadza pojęcia równowagi termicznej, temperatury i termometrii. Pierwsza zasada termodynamiki to kluczowe dla całej nauki stwierdzenie: energii nie da się ani zniszczyć, ani uzyskać „z niczego”, a więc całkowita energia Wszechświata jest wartością stałą. W najprostszej postaci pierwszą zasadę termodynamiki można sformułować następująco: energia, którą system otrzymuje, minus energia, którą oddaje, jest równa energii pozostałej w systemie. Na pierwszy rzut oka to stwierdzenie wydaje się oczywiste, ale nie w takim na przykład, sytuacje takie jak spalanie benzyny w cylindrach silnika samochodowego: tutaj odbierana energia jest chemiczna, energia oddawana mechanicznie (praca), a energia pozostająca w układzie jest cieplna.Jest więc jasne, że energia może zmieniać się z jednej formy w drugą i że takie przemiany stale zachodzą w naturze i technologii. Ponad sto lat temu J. Joule udowodnił to w przypadku konwersji energii mechanicznej na energię cieplną za pomocą urządzenia pokazanego na ryc. 6, a. W tym urządzeniu obciążniki opadające i wznoszące obracały wał z łopatkami w kalorymetrze wypełnionym wodą, w wyniku czego woda była podgrzewana. Dokładne pomiary pozwoliły Joule określić, że jedna kaloria ciepła odpowiada 4,186 J pracy mechanicznej. Urządzenie pokazane na ryc.
6, b, wykorzystano do wyznaczenia równoważnika cieplnego energii elektrycznej.Pierwsza zasada termodynamiki wyjaśnia wiele powszechnych zjawisk. Na przykład staje się jasne, dlaczego nie można schłodzić kuchni otwartą lodówką. Załóżmy, że zaizolowaliśmy termicznie kuchnię od otoczenia. Energia jest stale dostarczana do systemu przez przewód zasilający lodówki, ale system nie oddaje żadnej energii. W ten sposób zwiększa się jego całkowita energia, a kuchnia staje się cieplejsza: wystarczy dotknąć rurek wymiennika ciepła (skraplacza) z tyłu lodówki, a zrozumiesz jego bezużyteczność jako urządzenie „chłodzące”. Ale gdyby te rury zostały wyprowadzone z systemu (na przykład przez okno), wtedy kuchnia wydałaby więcej energii niż otrzymała, tj. byłaby chłodzona, a lodówka działała jako klimatyzator okienny.
Pierwsza zasada termodynamiki to prawo natury, które wyklucza tworzenie lub niszczenie energii. Nie mówi jednak nic o tym, jak w przyrodzie przebiegają procesy przekazywania energii. Tak więc wiemy, że gorące ciało ogrzeje zimne, jeśli te ciała się zetkną. Ale czy ciało zimne może samo przenieść rezerwę ciepła na ciało gorące? Ostatnia okazja kategorycznie odrzucone przez drugą zasadę termodynamiki.
Pierwsze prawo wyklucza również możliwość stworzenia silnika o współczynniku przydatne działanie(wydajność) więcej niż 100% (podobne
„wieczny” silnik może wydzielać więcej energii przez dowolnie długi czas niż zużywa). Niemożliwe jest zbudowanie silnika nawet o sprawności równej 100%, ponieważ pewna część dostarczonej do niego energii musi koniecznie zostać przez niego stracona w postaci mniej użytecznej energii cieplnej. Tak więc koło nie będzie się obracać w nieskończoność bez dostarczenia energii, ponieważ z powodu tarcia w łożyskach energia ruchu mechanicznego będzie stopniowo zamieniać się w ciepło, aż koło zatrzyma się.Tendencję do przekształcania „użytecznej” pracy w mniej użyteczną energię cieplną można porównać z innym procesem, który występuje, gdy połączone są dwa zbiorniki zawierające różne gazy. Po dostatecznie długim oczekiwaniu w obu naczyniach znajdujemy jednorodną mieszaninę gazów, które natura działa w taki sposób, że porządek układu maleje. Miarą termodynamiczną tego nieporządku jest entropia, a drugą zasadę termodynamiki można sformułować inaczej: procesy w przyrodzie zawsze przebiegają w taki sposób, że entropia układu i jego otoczenia wzrasta. W ten sposób energia Wszechświata pozostaje stała, a jego entropia stale rośnie.
Ciepło i właściwości substancji. Różne substancje mają różną zdolność magazynowania energii cieplnej; zależy to od ich struktury molekularnej i gęstości. Ilość ciepła potrzebna do podniesienia temperatury jednostkowej masy substancji o jeden stopień nazywamy jej ciepło właściwe. Pojemność cieplna zależy od warunków, w jakich znajduje się substancja. Na przykład, aby ogrzać jeden gram powietrza w balonie o 1 K, potrzeba więcej ciepła niż ogrzać go w ten sam sposób w szczelnym naczyniu o sztywnych ściankach, ponieważ część energii przekazanej balonowi jest zużywana na rozszerzenie powietrze, a nie na jego ogrzewanie. Dlatego w szczególności pojemność cieplna gazów jest mierzona oddzielnie przy stałym ciśnieniu i przy stałej objętości.Wraz ze wzrostem temperatury intensywność chaotycznego ruchu cząsteczek wzrasta, większość substancji rozszerza się po podgrzaniu. Stopień rozszerzalności substancji wraz ze wzrostem temperatury o 1 K nazywany jest współczynnikiem rozszerzalności cieplnej.
Aby substancja mogła przejść z jednego stanu fazowego do drugiego, na przykład ze stałego do ciekłego (a czasem natychmiastowego do gazowego), musi otrzymać określoną ilość ciepła. Jeśli ciało stałe zostanie podgrzane, jego temperatura wzrośnie, aż zacznie się topić; dopóki topienie nie zostanie zakończone, temperatura ciała pozostanie stała, pomimo dopływu ciepła. Ilość ciepła potrzebna do stopienia masy jednostkowej substancji nazywana jest ciepłem topnienia. Jeśli nadal będziesz dostarczać ciepło, stopiona substancja podgrzeje się do wrzenia. Ilość ciepła potrzebna do odparowania masy jednostkowej cieczy w danej temperaturze nazywana jest ciepłem parowania.
Teoria molekularno-kinetyczna. Teoria kinetyki molekularnej wyjaśnia makroskopowe właściwości substancji, biorąc pod uwagę na poziomie mikroskopowym zachowanie atomów i cząsteczek, które tworzą tę substancję. W tym przypadku stosuje się podejście statystyczne i przyjmuje się pewne założenia dotyczące samych cząstek i charakteru ich ruchu. Tak więc molekuły są uważane za kule stałe, które w ośrodkach gazowych poruszają się w sposób ciągły, chaotyczny i pokonują znaczne odległości od jednego zderzenia do drugiego. Zderzenia są uważane za elastyczne i występują między cząstkami, których rozmiar jest niewielki, a liczba bardzo duża. Żaden z gazów rzeczywistych nie odpowiada dokładnie temu modelowi, ale większość gazów jest do niego dość zbliżona, co jest powodem praktycznej wartości teorii kinetyki molekularnej.Opierając się na tych pomysłach i stosując podejście statystyczne, Maxwell wyprowadził rozkład prędkości cząsteczek gazu w ograniczonej objętości, którą później nazwano jego imieniem. Rozkład ten przedstawiono graficznie na ryc. 7 dla danej masy wodoru w temperaturach 100 i 1000
° C. Rzędna reprezentuje liczbę cząsteczek poruszających się z prędkością wskazaną na odciętej. Całkowita liczba cząstek jest równa powierzchni pod każdą krzywą i jest taka sama w obu przypadkach. Z wykresu widać, że większość cząstek ma prędkości bliskie pewnej średniej wartości, a tylko niewielka ich liczba ma bardzo wysokie lub niskie prędkości. Średnie prędkości w tych temperaturach mieszczą się w przedziale 2000-3000 m/s, tj. bardzo duży.Duża liczba takich szybko poruszających się cząsteczek gazu działa z całkowicie mierzalną siłą na otaczające ciała. Mikroskopijne siły, z którymi liczne cząsteczki gazu uderzają w ściany naczynia, sumują się do makroskopowej wielkości zwanej ciśnieniem. Kiedy energia jest dostarczana do gazu (wzrasta temperatura), wzrasta średnia energia kinetyczna jego cząsteczek, cząsteczki gazu częściej i mocniej uderzają o ściany, wzrasta ciśnienie, a jeśli ściany nie są całkowicie sztywne, to rozciągają się i zwiększa się objętość gazu. Zatem mikroskopijne podejście statystyczne leżące u podstaw teorii kinetyki molekularnej umożliwia wyjaśnienie omawianego przez nas zjawiska rozszerzalności cieplnej.
Innym wynikiem teorii kinetyki molekularnej jest prawo opisujące właściwości gazu, który spełnia powyższe wymagania. To jest tak zwane równanie stanu gaz doskonałyłączy ciśnienie, objętość i temperaturę jednego mola gazu i ma postać równości
PV = RT gdzie P nacisk, objętość V, T temperatura i R uniwersalna stała gazowa równa (8,31441± 0,00026) J/(mol H DO). Zobacz też TEORIA MOLEKULARNO-KINETYCZNA; TERMODYNAMIKA. PRZEKAZYWANIE CIEPŁA Przenoszenie ciepła to proces przenoszenia ciepła w ciele lub z jednego ciała do drugiego, ze względu na różnicę temperatur. Intensywność wymiany ciepła zależy od właściwości substancji, różnicy temperatur i jest zgodna z ustalonymi eksperymentalnie prawami natury. Aby tworzyć wydajne systemy ogrzewania lub chłodzenia, różne silniki, elektrownie, systemy izolacji termicznej, trzeba znać zasady wymiany ciepła. W niektórych przypadkach wymiana ciepła jest niepożądana (izolacja termiczna pieców do topienia, statków kosmicznych itp.), a w innych powinna być jak największa (kotły parowe, wymienniki ciepła, naczynia kuchenne).Istnieją trzy główne rodzaje wymiany ciepła: przewodzenie, konwekcja i promieniowanie ciepła.
Przewodność cieplna. Jeżeli wewnątrz ciała występuje różnica temperatur, to energia cieplna przechodzi z jego cieplejszej części do zimniejszej. Ten rodzaj wymiany ciepła, spowodowany ruchami termicznymi i zderzeniami cząsteczek, nazywany jest przewodnością cieplną; w wystarczającym stopniu wysokie temperatury w ciałach stałych można to zaobserwować wizualnie. Tak więc, gdy pręt stalowy jest podgrzewany z jednego końca w płomieniu palnika gazowego, energia cieplna jest przenoszona przez pręt, a poświata rozprzestrzenia się w pewnej odległości od nagrzanego końca (coraz mniej intensywna z odległością od miejsca ogrzewanie).Intensywność wymiany ciepła z powodu przewodności cieplnej zależy od gradientu temperatury, tj. relacje
D T/D x różnica temperatur na końcach pręta do odległości między nimi. Zależy to również od pola przekroju pręta (w m 2 ) i przewodność cieplną materiału[ w odpowiednich jednostkach W/(m Ch K) ] . Związek między tymi wielkościami został wyprowadzony przez francuskiego matematyka J. Fouriera i ma następującą postać: gdzie q Przepływ ciepła, k współczynnik przewodzenia ciepła, oraz A powierzchnia przekroju. Związek ten nazywa się prawem przewodzenia ciepła Fouriera; znak minus wskazuje, że ciepło jest przekazywane w kierunku przeciwnym do gradientu temperatury.Z prawa Fouriera wynika, że strumień ciepła można zmniejszyć poprzez zmniejszenie jednej z wielkości współczynnika przewodnictwa cieplnego, pola powierzchni lub gradientu temperatury. Dla budynku w warunkach zimowych te ostatnie wartości są praktycznie stałe, dlatego w celu utrzymania pożądanej temperatury w pomieszczeniu pozostaje zmniejszenie przewodności cieplnej ścian tj. poprawić ich izolację termiczną.
W tabeli przedstawiono współczynniki przewodzenia ciepła niektórych substancji i materiałów. Z tabeli wynika, że niektóre metale przewodzą ciepło znacznie lepiej niż inne, ale wszystkie są znacznie lepszymi przewodnikami ciepła niż powietrze i materiały porowate.
|
PRZEWODNOŚĆ CIEPLNA NIEKTÓRYCH SUBSTANCJI I MATERIAŁÓW |
|
|
Substancje i materiały |
Przewodność cieplna, W / (m × K) |
| Aluminium | |
| Brązowy | |
| Bizmut | |
| Wolfram | |
| Żelazo | |
| Złoto | |
| Kadm | |
| Magnez | |
| Miedź | |
| Arsen | |
| Nikiel | |
| Platyna | |
| Rtęć | |
| Prowadzić | |
| Cynk | |
|
Inne materiały |
|
| Azbest | |
| Beton | |
| Powietrze | |
| Pióra puchowe (luźne) | |
| Orzech) | |
| Magnezja (MgO) | |
| Trociny | |
| Guma (gąbka) | |
| Mika | |
| Szkło | |
| Węgiel (grafit) | |
Opór cieplny i elektryczny wielu substancji gwałtownie spada, gdy temperatura spada poniżej temperatury ciekłego helu (1,8 K). Zjawisko to, zwane nadprzewodnictwem, jest wykorzystywane do poprawy wydajności wielu urządzeń, od urządzeń mikroelektronicznych po linie energetyczne i duże elektromagnesy. Zobacz też NADprzewodnictwo.
Konwekcja. Jak już powiedzieliśmy, gdy ciepło jest przykładane do cieczy lub gazu, intensywność ruchu cząsteczek wzrasta, aw rezultacie wzrasta ciśnienie. Jeśli objętość cieczy lub gazu nie jest ograniczona, wówczas rozszerzają się; lokalna gęstość cieczy (gazu) maleje, a dzięki siłom wyporu (archimedesowym) nagrzana część medium unosi się w górę (dlatego ciepłe powietrze w pomieszczeniu unosi się od baterii do sufitu). Zjawisko to nazywa się konwekcją. Aby nie marnować na nic ciepła systemu grzewczego, należy zastosować nowoczesne grzejniki, które zapewniają wymuszony obieg powietrza.Konwekcyjny przepływ ciepła z podgrzewacza do ogrzanego medium zależy od początkowej prędkości cząsteczek, gęstości, lepkości, przewodności cieplnej i pojemności cieplnej oraz medium; bardzo ważny jest również rozmiar i kształt grzałki. Stosunek odpowiednich wielkości jest zgodny z prawem Newtona
q = hA( T W- TҐ ), gdzie q przepływ ciepła (mierzony w watach), A powierzchnia źródła ciepła (w m 2), T W oraz T temperatura źródła i jego otoczenia (w kelwinach). Konwekcyjny współczynnik przenikania ciepła h zależy od właściwości ośrodka, prędkości początkowej jego cząsteczek, a także od kształtu źródła ciepła i jest mierzony w jednostkach W/(m 2 godz DO).Wartość
h nie jest tak samo w przypadku, gdy powietrze wokół nagrzewnicy jest nieruchome (konwekcja swobodna) i gdy ta sama nagrzewnica znajduje się w strumieniu powietrza (konwekcja wymuszona). W prostych przypadkach przepływu płynu przez rurę lub opływu płaskiej powierzchni współczynnik h można obliczyć teoretycznie. Jednak nie udało się jeszcze znaleźć analitycznego rozwiązania problemu konwekcji dla turbulentnego przepływu medium. Turbulencja to złożony ruch cieczy (gazu), chaotyczny w skali znacznie przekraczającej molekularne.Jeśli ogrzane (lub odwrotnie zimne) ciało zostanie umieszczone w ośrodku stacjonarnym lub w przepływie, wokół niego powstają prądy konwekcyjne i warstwa graniczna. Temperatura, ciśnienie i prędkość cząsteczek w tej warstwie odgrywają ważną rolę w określaniu współczynnika konwekcyjnego przewodzenia ciepła.
Konwekcja musi być brana pod uwagę przy projektowaniu wymienników ciepła, systemów klimatyzacyjnych, szybkich samolotów i wielu innych zastosowaniach. We wszystkich tego typu układach przewodzenie ciepła odbywa się jednocześnie z konwekcją, zarówno pomiędzy ciałami stałymi, jak iw ich otoczeniu. Na podwyższonych temperaturach Istotną rolę może również odgrywać promieniująca wymiana ciepła.
Promieniowanie wymiany ciepła. Trzeci rodzaj wymiany ciepła przez promieniowanie różni się od przewodzenia ciepła i konwekcji tym, że ciepło w tym przypadku może być przenoszone przez próżnię. Jego podobieństwo do innych metod wymiany ciepła polega na tym, że wynika to również z różnicy temperatur. Promieniowanie cieplne jest jednym z typów promieniowanie elektromagnetyczne. Inne rodzaje fal radiowych, ultrafioletowych i gamma występują przy braku różnicy temperatur.Na ryc. 8 pokazuje zależność energii promieniowania cieplnego (podczerwonego) od długości fali. Promieniowaniu cieplnemu może towarzyszyć emisja światła widzialnego, ale jego energia jest niewielka w porównaniu z energią promieniowania niewidzialnej części widma.
Intensywność wymiany ciepła przez przewodzenie i konwekcję jest proporcjonalna do temperatury, a strumień ciepła promieniowania jest proporcjonalny do czwartej potęgi temperatury i jest zgodny z prawem Stefana Boltzmanna
Przestrzenie mieszkalne i biurowe są często ogrzewane małymi grzejnikami elektrycznymi; czerwonawy blask ich spiral to widzialne promieniowanie cieplne w pobliżu krawędzi podczerwonej części widma. Pomieszczenie ogrzewane jest ciepłem, które przenoszone jest głównie przez niewidzialną, podczerwoną część promieniowania. W noktowizorach
^ Kamera wykorzystuje źródło promieniowania cieplnego oraz czuły na podczerwień odbiornik, który umożliwia widzenie w ciemności.Słońce jest potężnym emiterem energii cieplnej; ogrzewa Ziemię nawet w odległości 150 mln km. Natężenie promieniowania słonecznego rejestrowane rok po roku przez stacje zlokalizowane w wielu częściach globu wynosi około 1,37 W
/ m 2 . Energia słoneczna jest źródłem życia na Ziemi. Trwają poszukiwania sposobów na jak najskuteczniejsze jej wykorzystanie. Panele słoneczne zostały stworzone do ogrzewania domów i wytwarzania energii elektrycznej na potrzeby domowe. ROLA CIEPŁA I JEGO WYKORZYSTANIE Globalne procesy wymiany ciepła nie sprowadzają się do ogrzewania Ziemi promieniowaniem słonecznym. Ogromne prądy konwekcyjne w atmosferze determinują codzienne zmiany warunków pogodowych na całym świecie. Różnice temperatur w atmosferze między regionami równikowymi i polarnymi, wraz z siłami Coriolisa wynikającymi z rotacji Ziemi, prowadzą do pojawienia się stale zmieniających się prądów konwekcyjnych, takich jak pasaty, prądy strumieniowe oraz fronty ciepłe i zimne. Zobacz też KLIMAT; METEOROLOGIA I KLIMATOLOGIA.Przenoszenie ciepła (ze względu na przewodność cieplną) ze stopionego jądra Ziemi na jego powierzchnię prowadzi do erupcji wulkanicznych i pojawienia się gejzerów. W niektórych regionach energia geotermalna jest wykorzystywana do ogrzewania pomieszczeń i wytwarzania energii.
Ciepło jest nieodzownym uczestnikiem niemal wszystkich procesów produkcyjnych. Wymieńmy najważniejsze z nich, takie jak wytop i obróbka metali, eksploatacja silników, produkcja żywności, synteza chemiczna, rafinacja ropy naftowej, produkcja szerokiej gamy przedmiotów od cegieł i naczyń po samochody i urządzenia elektroniczne.
Wiele produkcji przemysłowych i transportowych, a także elektrociepłowni nie mogłoby działać bez silników cieplnych - urządzeń, które zamieniają ciepło w użyteczną pracę. Przykładami takich maszyn są sprężarki, turbiny, silniki parowe, benzynowe i odrzutowe.
Jednym z najbardziej znanych silników cieplnych jest turbina parowa, która realizuje część obiegu Rankine'a stosowanego w nowoczesnych elektrowniach. Uproszczony schemat tego cyklu pokazano na ryc. 9. Woda w płynie roboczym jest przetwarzana na parę przegrzaną w kotle parowym ogrzewanym przez spalanie paliw kopalnych (węgla, ropy naftowej lub gazu ziemnego). Parowy wysokie ciśnienie obraca wał turbiny parowej, która napędza generator wytwarzający energię elektryczną. Para odlotowa skrapla się po schłodzeniu pod bieżącą wodą, która pochłania część ciepła niewykorzystanego w cyklu Rankine'a. Następnie woda podawana jest do chłodni kominowej (chłodniczej), skąd część ciepła jest oddawana do atmosfery. Kondensat jest pompowany z powrotem do kotła parowego i cały cykl się powtarza.
Wszystkie procesy w cyklu Rankine'a ilustrują opisane powyżej zasady termodynamiki. W szczególności, zgodnie z drugim prawem, część energii zużywanej przez elektrownię musi zostać rozproszona w środowisku w postaci ciepła. Okazuje się, że w ten sposób traci się około 68% energii pierwotnie zawartej w paliwach kopalnych. Zauważalny wzrost sprawności elektrowni można było osiągnąć jedynie podnosząc temperaturę kotła parowego (która jest ograniczona wytrzymałością cieplną materiałów) lub obniżając temperaturę medium, do którego trafia ciepło, tj. atmosfera.
Kolejny cykl termodynamiczny mający bardzo ważne w naszym Życie codzienne, jest cyklem chłodzenia sprężarki parowej Rankina, którego schemat pokazano na ryc. 10. W lodówkach i klimatyzatorach domowych energia jest dostarczana z zewnątrz w celu jej dostarczenia. Sprężarka zwiększa temperaturę i ciśnienie substancji roboczej chłodziarki freon, amoniak lub dwutlenek węgla. Przegrzany gaz podawany jest do skraplacza, gdzie jest schładzany i skraplany, oddając ciepło do otoczenia. Ciecz opuszczająca dysze skraplacza przechodzi przez zawór dławiący do parownika, a jej część odparowuje, czemu towarzyszy gwałtowny spadek temperatury. Parownik pobiera ciepło z komory lodówki, która podgrzewa płyn roboczy w dyszach; ciecz ta jest dostarczana przez sprężarkę do skraplacza i cykl się powtarza.
Cykl chłodniczy przedstawiony na ryc. 10 może być również używany w pompie ciepła. Takie pompy ciepła latem oddają ciepło do gorącego powietrza atmosferycznego i klimatyzują pomieszczenie, a zimą odbierają ciepło z zimnego powietrza i ogrzewają pomieszczenie.
Reakcje jądrowe są ważnym źródłem ciepła do celów takich jak wytwarzanie energii i transport. W 1905 r. A. Einstein wykazał, że masa i energia są powiązane relacją
E=mc2 , tj. mogą przechodzić w siebie. prędkość światła c bardzo duże: 300 tys. km/ Z. Oznacza to, że nawet niewielka ilość materii może dostarczyć ogromną ilość energii. Tak więc z 1 kg materiału rozszczepialnego (na przykład uranu) teoretycznie można uzyskać energię, którą na 1000 dni ciągłej pracy zapewnia elektrownia o mocy 1 MW. Zobacz też STRUKTURA ATOMU; PIECE I TECHNOLOGIA PIECOWA; PROMIENIOWANIE ELEKTROMAGNETYCZNE; WYMIENNIK CIEPŁA; TURBINA; JEDNOSTKI MIARY WIELKOŚCI FIZYCZNYCH.LITERATURA Zemansky M. Temperatury bardzo wysokie i bardzo niskie. M., 1968Paweł R. Mechanika, akustyka i doktryna ciepła. M., 1971
Smorodinsky Ya.A. Temperatura. M., 1981
Wentylator J. Maszyny, energia i entropia. M., 1986
Atkins P.V. Porządek i nieporządek w przyrodzie. M., 1987
Kalorymetry płynne
Ten typ kalorymetru, najszerzej stosowany w technologii, jest prosty w konstrukcji i łatwy w utrzymaniu. Ilość ciepła wytworzonego w wyniku reakcji indukowanej zewnętrznie jest najpierw przekazywana do naczynia reakcyjnego (w którym zachodziła reakcja), a następnie do kąpieli ciekłej. Ciecz w kąpieli jest stale mieszana za pomocą wirnika, ślimaka podnoszącego lub pomp, co przyspiesza wyrównanie temperatur. Wanna jest w jak największym stopniu izolowana termicznie (osłonięta) od otoczenia. Zmiana temperatury kąpieli płynnej jest miarą wykrytego ciepła. Pojemność cieplna ogrzewanych mas nie może być zbyt duża, aby zapewnić wystarczającą zmianę temperatury i aby proces pomiaru nie trwał zbyt długo (dzięki czemu zwiększają się straty ciepła).
Rysunek Urządzenie kalorymetru cieczowego.
Przy wysokich wymaganiach co do stałości warunków otoczenia, możliwe jest umieszczenie całego kalorymetru w innej kąpieli i ustabilizowanie w nim temperatury z dużą dokładnością za pomocą pętli sterującej. Jest to konieczne przede wszystkim w przypadkach, gdy wymagane jest przeprowadzenie eksperymentu w temperaturach znacznie różniących się od temperatury otoczenia.
Do analiz w niskich temperaturach (do ok. -150°C) jako czynnik chłodzący stosuje się ciekły azot. W takim przypadku należy zwrócić uwagę na fakt, że przy ich wymianie nie dochodzi do wytrącania się szronu z otaczającego wilgotnego powietrza na próbkach lub naczyniach pomiarowych, gdyż jego warstwa może wpływać na proces pomiarowy. Aby tego uniknąć, gdy kalorymetr jest otwarty, próbka i pojemnik na próbki są przedmuchiwane zimnym gazowym azotem.
Kalorymetry z metalowym korpusem
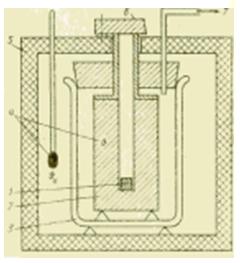
Rysunek Schemat urządzenia metalowego kalorymetru.
Jeśli wymagane jest przeprowadzenie badań kalorymetrycznych w szerszym zakresie temperatur, kalorymetry cieczowe nie są już odpowiednie. W kalorymetrach z metalowym korpusem odpowiednich do tego celu ilość przekazywanego ciepła jest przejmowana przez metalowy blok (srebro, miedź, aluminium), który zwykle znajduje się w temperaturze otoczenia. Taki kalorymetr jest przeznaczony głównie do określania właściwej pojemności cieplnej c, J / (kg * K), substancji ciekłych i stałych.
Próbka jest najpierw schładzana poza kalorymetrem w instalacja chłodnicza lub ogrzewany w piecu i po osiągnięciu stanu ustalonego opuszczany (upuszczany) do otworu w metalowym bloku. Zgodnie z metodą działania takie urządzenie nazywa się kalorymetrem swobodnego spadku, a zgodnie z naturą zachodzących w nim procesów termodynamicznych jest czasami nazywane kalorymetrem przemieszczeniowym.
Ilość ciepła przekazywanego podczas tego mieszania z próbki (o parametrach m1, c1, ) do bloku metalowego (m2, c2, ) powoduje mierzalną zmianę temperatury bloku. Umożliwia to wyznaczenie zwykle nieznanej wartości ciepła właściwego próbki dla idealne warunki(w przypadku braku wymiany ciepła z otoczeniem) z wyrażenia:
Sam metalowy blok znajduje się w ewakuowanym naczyniu Dewara, a czasem w kąpieli płynnej. W tym ostatnim przypadku, aby otrzymać pojemność cieplną kalorymetru Ck, pojemność cieplną kąpieli Cw należy dodać do pojemności cieplnej bloku metalowego C2:
CK=C2+CW=c2m2+cWmW .
KALORYMETRYCZNE METODY POMIARU
Najczęściej kalorymetry są używane w trybie stałych warunków środowiskowych. Dotyczy to przede wszystkim większości kalorymetrów spalinowych, w których czas reakcji jest bardzo krótki.Podczas gdy temperatura wewnętrznych części kalorymetru zmienia się w wyniku reakcji, temperatura otoczenia pozostaje stała.W wielu przypadkach temperatura kontrolowana kąpiel jest wykorzystywana jako środowisko w celu uniknięcia wpływu na mierzoną wartość zakłóceń zewnętrznych – wahań temperatury w pomieszczeniu, promieniowania, przeciągów itp.
Zaletą takiego schematu pomiarowego jest stosunkowo niski koszt sprzętu, który można wykorzystać do wykonywania przeważającej części pomiarów kalorymetrycznych. Za główną wadę należy uznać wymianę ciepła kalorymetru z otoczeniem, co komplikuje interpretację wyników. Ta metoda pomiaru jest zawsze nazywana izoperibolem (diatermicznym). W każdym razie nie można go nazwać izotermicznym, którego istota polega na tym, że temperatura kalorymetru pozostaje stała podczas przebiegu reakcji, tak jak np. kalorymetry przeznaczone do pomiaru przemian fazowych.
metoda adiabatyczna
Jeżeli możliwe jest wykluczenie wymiany ciepła z otoczeniem, tj. zapewnienie adiabatycznego przebiegu procesu, to eksperyment i interpretacja wyników są uproszczone, a wynik pomiaru jest dokładniejszy, ponieważ nie ma potrzeby ciągłego rejestrowania zmiany temperatury i obliczyć poprawki. Ponadto w tym przypadku można tolerować nieco większy wzrost temperatury w naczyniu kalorymetru; w przypadku urządzeń nieadiabatycznych jest to niedopuszczalne ze względu na wzrost strat ciepła.
Aby uniknąć przenoszenia ciepła między naczyniem kalorymetru a jego bezpośrednim otoczeniem (zazwyczaj kąpielą płynną), temperatura kąpieli musi być stale dostosowywana do zmian temperatury w naczyniu. Za pomocą sterownika elektronicznego (obwodu śledzącego) można stale utrzymywać różnicę tych temperatur praktycznie równą zeru. Zwiększa to koszt sprzętu pomiarowego w zależności od wymaganej dokładności pomiaru.
Elementy sprzętowe muszą być szybkie i stabilne przez długi czas (mają minimalny dryf). Strefa martwa śledzącej pętli sterującej powinna mieścić się w zakresie od ±10-3 do ±10-5 K. Jako przyrządy pomiarowe można zastosować dowolne elektryczne termometry kontaktowe szybko reagujące, które włączone w obwód mostkowy dają impuls do sterownika na zmianę mocy grzania. Ogrzewanie odbywa się albo za pomocą elektrycznej cewki oporowej, albo bezpośrednio w kąpieli płynnej, która z powodu słabej dysocjacji działa jak opornik grzejny (tzw. ogrzewanie elektrolityczne). Ta druga metoda jest praktycznie bezwładna. Wynik można uzyskać za pomocą już istniejących środków do elektrycznego pomiaru temperatury lub za pomocą dodatkowo zainstalowanego termometru cieczowego (Beckmann).
Metoda pomiaru adiabatycznego nadaje się do badania głównie powolnych procesów i efektów termicznych. Przy szybkich zmianach ilości ciepła (w kalorymetrach spalinowych) bezwładność wyrównywania temperatury ma tak niekorzystny wpływ, że nie osiąga się nawet dokładności konwencjonalnych metod nieadiabatycznych. Jednak zapewniając małą pojemność cieplną elementów grzejnych i czujników temperatury oraz prowadząc intensywne mieszanie cieczy kąpielowej, możliwe jest uzyskanie niewielkich wartości o różnych stałych czasowych (w celu zmniejszenia bezwładności).
Metoda kompensacji
Stosując kalorymetry różnicowe lub dualne oparte na zasadzie kompensacji można w znacznym stopniu wyeliminować wpływy zewnętrzne na proces pomiarowy. Dwa identyczne naczynia kalorymetryczne z identycznymi akcesoriami umieszczane są w środowisku w tych samych warunkach. W jednym naczyniu zachodzi badany proces z efektem termicznym, a drugie naczynie jest podgrzewane za pomocą układu serwosterowania w taki sposób, aby straty ciepła do otoczenia dla obu naczyń były takie same. W związku z tym wejściową moc grzewczą można wprowadzić wprost proporcjonalnie do ilości ciepła uwalnianego w trakcie badanego procesu. W tym przypadku eksperymentalne zadanie pomiaru przechodzi w inny obszar i sprowadza się do bardzo dokładnego wyznaczenia dostarczonej mocy ogrzewania elektrycznego (W*s, J):
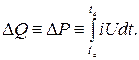
Kalorymetr różnicowy stosuje się w szczególności w adiabatycznych warunkach otoczenia, zwłaszcza gdy należy spodziewać się bardzo małych lub bardzo powolnych zmian ilości ciepła. W procesach endotermicznych wystarczy jedno naczynie kalorymetryczne. Dopływ ciepła jest kontrolowany w taki sposób, aby temperatura w naczyniu pozostawała przez cały czas taka sama (metoda izotermiczna). Wadą kalorymetrów różnicowych jest wysoki koszt sprzętu i przyrządów pomiarowych.
KALORYMETRY SPALANIA
Paliwo stosowane w elektrociepłowniach jest badane w celu określenia jego wartości opałowej H (J/kg). Wskaźnik ten jest potrzebny do określenia współczynników sprawności, badania sprawności i obliczeń energii zużywanej w różnych instalacjach, a także do optymalnej kontroli procesu spalania. Duże wahania składu składników palnych często powodują konieczność ciągłego wyznaczania wartości opałowej.
Kiedy substancja jest całkowicie spalona, uwalniana jest pewna ilość ciepła Q (ciepło spalania). Jeśli podzielimy go przez masę m (lub objętość w normalnych warunkach Vn), otrzymamy (właściwe) ciepło spalania:
W zależności od stanu produktów spalania wyróżnia się dwa rodzaje wartości opałowej: wyższą H0 i niższą H, które nazywane są również ciepłem spalania i wartością opałową. Przy określaniu wartości opałowej Ni, woda powstała podczas reakcje chemiczne musi być w stanie pary. Różnica pomiędzy obydwoma ciepłami H0 - Ni odpowiada ciepłu parowania skroplonej wody (wskaźnik KO - kondensat) r, które wynosi 2,441 MJ/kg.
W przypadku paliw stałych i ciekłych uzyskaną ilość wody można określić na podstawie analizy elementarnej, a przy spalaniu paliw gazowych poprzez pomiar ilości kondensatu.
W piecach przemysłowych temperatura produktów spalania zawsze przekracza temperaturę wrzenia wody. Dlatego tylko wartość opałowa netto Ni jest zwykle interesująca, ponieważ nie można wykorzystać ciepła kondensacji wody.
Kalorymetry spalania dla ciał stałych i cieczy
Dla szybkich procesów spalania opracowano specjalną postać kalorymetru cieczowego – tzw. bombę kalorymetryczną Berthelota (rys. 3).
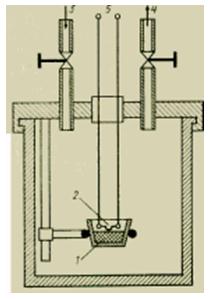
Rysunek Urządzenie bomby kalorymetrycznej.
Spalanie niewielkiej, precyzyjnie odmierzonej ilości substancji następuje w stałej objętości w zamkniętej bombie w atmosferze najczystszego możliwego tlenu pod ciśnieniem ~30 atm (3 MPa). Napełnioną bombę umieszcza się w płynnej kąpieli kalorymetru, która pochłania uwolnione ciepło spalania.
Ciała stałe zwykle sprasowywane w małe brykiety (tabletki) i bardzo dokładnie ważone. Wskazane jest mieszanie słabo palących się substancji z dobrze palącymi się płynami o znanym cieple spalania (na przykład kwas benzoesowy). Substancje płynne umieszcza się w kubkach (łódeczkach) wykonanych z platyny lub kwarcu lub w małych plastikowych kapsułkach. Na pokrywie, przykręconej do korpusu bomby, znajdują się wszystkie niezbędne do badań urządzenia: zawory do dostarczania tlenu i usuwania produktów spalania, uchwyty na próbki oraz zapalnik elektryczny. Zapłon odbywa się poprzez dostarczenie prądu do cienkiego drutu platynowego. Ciepło dostarczane do zapłonu musi być dokładnie zmierzone, aby można je było uwzględnić przy odszyfrowywaniu wyników eksperymentu. W bombie kalorymetrycznej wyznaczana jest najwyższa wartość opałowa H0. Podczas weryfikacji równoważnik termiczny kalorymetru Ck określa się przez spalenie substancji odniesienia (na przykład kwasu benzoesowego) lub za pomocą elektrycznego urządzenia grzewczego.
Kalorymetr spalania substancji gazowych
Aby określić ciepło spalania mediów gazowych, istnieją różne metody. Wszystkie z nich, w przeciwieństwie do bomby kalorymetrycznej na substancje stałe i płynne, opierają się na pomiarze ciągłym. Zastosowana zasada pomiaru jest dość prosta. Gaz testowy jest stale spalany w palniku pod stałym ciśnieniem. Całe ciepło uwalniane podczas spalania jest pochłaniane albo przez przepływ czynnika chłodzącego w wymienniku ciepła (kalorymetr mokry lub wymiennik ciepła), albo przez mieszanie produktów spalania z przepływem powietrza przy znanym natężeniu przepływu (kalorymetr suchy lub mieszany). Zwykle określają wartość opałową netto Hu. Do wyznaczenia ciepła spalania H0 konieczne jest skondensowanie pary wodnej (wskaźnik KO) zawartej w spalinach. Znając masowe natężenia przepływu i różnicę temperatur na wlocie (wskaźnik e) i wylocie (wskaźnik a) kalorymetru, można obliczyć odpowiednią wartość opałową za pomocą równania bilansu cieplnego.
Wymagane przygotowanie gazu jest zasadniczo takie samo we wszystkich kalorymetrach gazowych. Gaz przed spaleniem (wskaźnik G) jest najpierw oczyszczany ze stałych zanieczyszczeń mechanicznych (w filtrze) i nawilżany (do nasycenia wilgocią 100%), a następnie doprowadzany do określonych wartości ciśnienia wstępnego (za pomocą reduktora ciśnienia zaworu) i temperatury czynnika chłodniczego (indeks K) . Powietrze potrzebne do spalania (wskaźnik L) jest również nawilżane i doprowadzane do temperatury czynnika chłodniczego.
W zależności od wymaganej dokładności i dopuszczalnych kosztów oprzyrządowania, niektóre z tych warunków mogą nie być spełnione. Kalorymetry należy zweryfikować gazem odniesienia (np. wodór) w celu określenia odchylenia od równania stanu idealnego kalorymetru. Dla kalorymetru ciepłochronnego (mokrego) powyższe równanie ma postać
gdzie i są masowymi natężeniami przepływu czynnika chłodzącego i paliwa, kg/s; sk - ciepło właściwe medium chłodzącego, J / (kg * K); - wzrost temperatury czynnika chłodzącego, K.
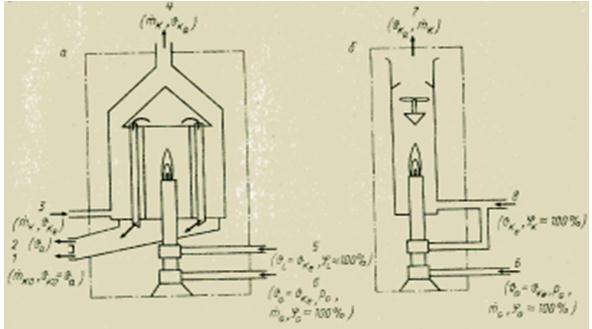
Rysunek Urządzenie kalorymetrów mokrych (a) i suchych (b) dla paliwa gazowego.
Wzrost temperatury wynosi zazwyczaj 5-15 K. Ze względu na dużą masę termiczną kalorymetry wymiany ciepła mają bardzo długą stałą czasową, która może wynosić nawet kilka minut. Dlatego są mniej odpowiednie do zastosowania w zamkniętej pętli regulacji jako czujnik niż kalorymetry suche (mieszające), których stała czasowa wynosi tylko kilka sekund. Z drugiej strony osiągalna dokładność kalorymetrów wymiany ciepła jest stosunkowo wysoka. Ich błąd nie przekracza ±0,25-1%, dzięki czemu mogą być również wykorzystywane do prac laboratoryjnych oraz do weryfikacji. Suche kalorymetry (mieszanie) wykazują błąd od ±1 do ±2% górnej granicy zakresu pomiarowego.
Wersje konstrukcyjne kalorymetrów różnych producentów różnią się przede wszystkim urządzeniami pomocniczymi i zabezpieczającymi, elementami pomiarowymi oraz obwodami obliczeniowymi zapewniającymi kompensację błędów. Tak więc w kalorymetrach ciepłowniczych stosunek natężenia przepływu gazu i czynnika chłodzącego jest utrzymywany w różny sposób (patrz równanie kalorymetru powyżej), dzięki czemu wyższa wartość opałowa H0 zależy bezpośrednio tylko od wzrostu temperatury.
W kalorymetrach suchych wzrost temperatury mierzony jest albo bezpośrednio za pomocą elektrycznych termometrów kontaktowych, albo pośrednio za pomocą czujnika dylatometrycznego - rurki rozprężnej umieszczonej w strumieniu spalin. W kalorymetrze ADOS termiczne wydłużenie rurki dylatometru odpowiada bezpośrednio ciepłu spalania i może być przetworzone na dowolny sygnał za pomocą łącznika i miernika długości. W kalorymetrze Reinecke przedłużenie pręta jest wykorzystywane jako sygnał pomiarowy w obwodzie sterującym, który steruje przepływem powietrza chłodzącego w taki sposób, że wzrost jego temperatury pozostaje prawie stały. W takim przypadku pętla sterowania okazuje się być czysto proporcjonalna, ale pewne odchylenie szczątkowe jest w niej nieuniknione. W tym przypadku zużycie powietrza chłodzącego lub wydłużenie rurki dylatometrycznej (pręta) jest miarą wyznaczonej wartości opałowej. Warunkiem uzyskania wystarczającej dokładności we wszystkich suchych kalorymetrach jest dobre mieszanie powietrza chłodzącego i produktów spalania.
POMIARY PRZEPŁYWU CIEPŁA
Ciepło jako forma energii przekazywane jest na trzy sposoby: przez ciało stałe (przewodnictwo cieplne), media płynne lub gazowe (konwekcja) oraz bez udziału materii (promieniowanie). W technologii wszystkie trzy komponenty prawie zawsze biorą udział w przenoszeniu ciepła; jednak w wielu przypadkach możliwe jest uzyskanie wyników o akceptowalnej dokładności poprzez pomiar tylko jednego składnika.
Pomiar Przepływ ciepła z przewodnością cieplną
Przenikanie ciepła przez ściany przewodzące ciepło ma ogromne znaczenie w wielu dziedzinach techniki (wymienniki wszelkiego rodzaju, izolacje termiczne itp.). Jednocześnie interesująca jest nie tyle bieżąca kontrola wielkości produkcji, ile wyniki pojedynczych pomiarów służących do oceny obciążenia, weryfikacji spełnienia gwarantowanych wskaźników i wydajności.
Zgodnie z prawami stacjonarnego przewodzenia ciepła, strumień ciepła określają następujące wzory (J/s):
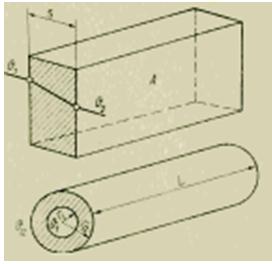
Ponieważ przewodność cieplna ściany [J/(m*s*K)] i jej wymiary geometryczne są znane, pomiar strumienia ciepła sprowadza się do pomiaru różnicy temperatur. Technika ta wymaga jednak bardzo dokładnego określenia temperatury powierzchni. Błędy związane ze zmianami warunków wymiany ciepła podczas instalowania elementów wrażliwych na temperaturę na powierzchniach mogą być dość duże. Dlatego dla dokładniejszych pomiarów zalecane są poniższe metody, w których jednocześnie wykorzystuje się zarówno przewodność cieplną, jak i wymianę ciepła.
Pomiar przepływów ciepła w wymianie ciepła (wymiana ciepła połączona z przewodnictwem ciepła)
Dla płaskiej ściany, o której mowa w poprzednim rozdziale, obowiązuje następujące prawo przenikania ciepła (J/s):
![]() ,
,
gdzie we współczynniku przenikania ciepła k 1J/(m2*s*K)], wraz ze współczynnikiem przenikania ciepła [J/Dm*s*K)], współczynniki przenikania ciepła i [J/(m2*s*K) ] z obu stron ściany są również brane pod uwagę.
Na płaskiej ścianie, przez którą przechodzi zmierzony strumień ciepła, umieszcza się małą cienką płytkę, której temperaturę powierzchni określają wbudowane termopary cienkowarstwowe. Zaletą pomiaru w ten sposób jest to, że nie jest wymagana znajomość właściwości termicznych ściany, a odpowiednie właściwości płyty można zredukować do jednej stałej wartości podczas kalibracji. Takie wrażliwe elementy mają wymiary około 30x30x0,5 mm; zakres pomiarowy obejmuje strumienie ciepła od 10 do 100 000 W/m2; błąd wynosi 2-5%.
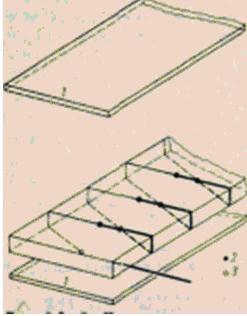
Rysunek Zasada działania miernika strumienia ciepła.
Wraz z udoskonaleniem tej metody pomiaru, zamiast nałożonej płyty stosuje się maty gumowe. Przyklejając je do niepłaskich powierzchni lub owijając wokół zakrzywionej powierzchni, można określić przenoszenie ciepła z powierzchni o stosunkowo dużej powierzchni, np. z rury, naczynia itp. Termopary są wbudowane w obie powierzchnie matę tak, aby ich połączenia ciepłe i zimne były dokładnie względem siebie (rys. 6). I w tym przypadku gęstość strumienia ciepła zgodnie z kalibracją jest proporcjonalna do różnicy temperatur. Jednak zastosowane maty nieco zakłócają początkowy transfer ciepła, co staje się zauważalne przy dokładnych pomiarach. Dlatego ta metoda pomiaru służy głównie do wyznaczania stałych termodynamicznych substancji, gdy naruszenie przepływu ciepła nie wpływa na wynik pomiaru.
Pomiar przepływów ciepła w obecnych środowiskach.
Znaczna część energii cieplnej jest przekazywana przez media płynne lub gazowe (woda, para itp.) poruszające się w zamkniętej sieci rurociągów. Jednak w porównaniu z przesyłaniem energii elektrycznej przewodem, odległość, na jaką może być przesyłana energia cieplna, jest ograniczona. Do badań termotechnicznych wszystkich typów systemów grzewczych i chłodniczych niezbędny jest pomiar wydzielania i zużycia ciepła.
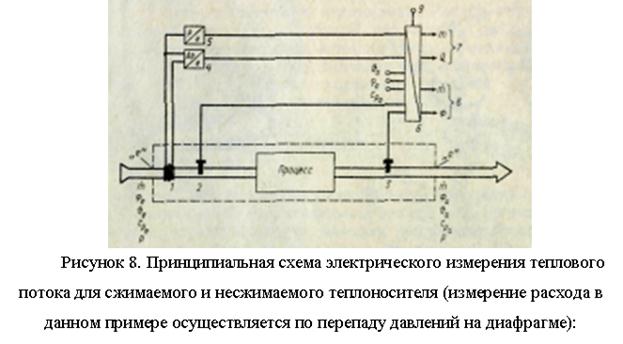
Strumień ciepła F (J/s), przenoszony przez przepływ czynnika - nośnika ciepła (kg/s) przez odcinek regulacyjny o powierzchni A (m2) w określonej strefie, dla której sporządzany jest bilans ciepła (w strefa procesu, rys. 7), jest równa
Ilość ciepła uwolnionego w przedziale czasu t2 - t1 jest określana jako całka (J):
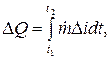
gdzie jest różnicą w zawartości ciepła (entalpie, J/kg) chłodziwa na wlocie (wskaźnik e) i na wylocie (wskaźnik a) strefy bilansu cieplnego.
Ponieważ w ogólnym przypadku wartość entalpii jest interesująca tylko w porównaniu z pewnym poziomem, na przykład z entalpią w temperaturze otoczenia, wszystkie pomiary strumieni ciepła są zasadniczo pomiarami różnicowymi.
Poszczególne entalpie zawarte w ogólnym równaniu można wyrazić w postaci odpowiednich temperatur i właściwych pojemności cieplnych;
Tym samym pomiar przepływu ciepła sprowadza się bezpośrednio do pomiaru temperatury i masowego natężenia przepływu. W wielu przypadkach mierzy się nie masowy, ale objętościowy przepływ chłodziwa; w takim przypadku uzyskany wynik będzie się różnił tylko wartością gęstości chłodziwa р. Właściwe pojemności cieplne, ci, są same w sobie funkcjami temperatury. Jednak ze względu na wąski zakres pomiarowy wielu przyrządów można je zwykle uznać za wartości stałe bez znacznej utraty dokładności. Musi być znana właściwa pojemność cieplna. W przypadku cieczy równanie przepływu ciepła jest jeszcze bardziej uproszczone, ponieważ ich właściwe pojemności cieplne nie polegaj na nacisku:
![]() , J/s.
, J/s.
We wszystkich tego typu równaniach konieczne jest uwzględnienie znaków wielkości w zależności od tego, czy ciepło jest dostarczane czy odprowadzane, czy proces jest endotermiczny czy egzotermiczny, czy występuje chłodzenie czy ogrzewanie.
