เชื้อเพลิง ก๊าซผสม และความจุความร้อน
ในเครื่องยนต์ความร้อน (เครื่องจักร) สารทำงานเป็นส่วนผสมของก๊าซต่างๆ หากไม่ใส่ส่วนประกอบของสารผสมลงไป ปฏิกริยาเคมีระหว่างกัน และแต่ละส่วนประกอบเป็นไปตามสมการสถานะของ Klaiperon ดังนั้นส่วนผสมดังกล่าวจึงถูกพิจารณาว่าเป็นก๊าซในอุดมคติ
ในการคำนวณส่วนผสมจำเป็นต้องกำหนด μ cm - มวลโมลาร์เฉลี่ยและ R c m - ค่าคงที่ของก๊าซเฉพาะของส่วนผสม ในการตรวจสอบพวกเขาจำเป็นต้องทราบองค์ประกอบของส่วนผสมนั่นคือส่วนประกอบใดและปริมาณใดที่ก่อให้เกิดส่วนผสมนี้พารามิเตอร์ใดที่แต่ละส่วนประกอบรวมอยู่ในส่วนผสม
ส่วนประกอบแต่ละส่วนของสารผสมจะทำงานราวกับว่าไม่มีก๊าซอื่นใดในสารผสม ใช้ปริมาตรที่มีอยู่ทั้งหมดซึ่งสารผสมนั้นตั้งอยู่ เป็นไปตามสมการสถานะของมันเอง และออกแรงกดบางส่วนที่เรียกว่าแรงดันบนผนัง ในขณะที่อุณหภูมิ ของส่วนผสมทั้งหมดเท่ากันและเท่ากันกับอุณหภูมิของส่วนผสม
ตามกฎของดาลตัน ความดันของส่วนผสม P เท่ากับผลรวมของความดันบางส่วนของส่วนประกอบแต่ละชนิดที่รวมอยู่ในส่วนผสม:
โดยที่ n คือจำนวนส่วนประกอบของส่วนผสม
ตามกฎของ Amag ปริมาตรของส่วนผสม V เท่ากับผลรวมของปริมาตรบางส่วนของส่วนประกอบแต่ละชนิดที่รวมอยู่ในส่วนผสม ณ อุณหภูมิและความดันของส่วนผสม:
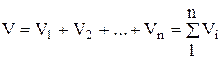 , (1.21)
, (1.21)
ที่ไหน - ปริมาตรบางส่วน ม. 3; V- ปริมาตรของส่วนผสม m 3
ส่วนประกอบของส่วนผสมกำหนดโดยปริมาตร (โมลาร์) หรือเศษส่วนมวล
เศษส่วนปริมาตรของส่วนประกอบ i-thคืออัตราส่วนของปริมาตรบางส่วนของส่วนประกอบต่อปริมาตรของส่วนผสม นั่นคือ ผลรวมของเศษส่วนปริมาตรของส่วนประกอบของส่วนผสมคือ 1 เช่น . หากกำหนดค่าเป็น % ผลรวมของค่านั้น = 100%
เศษส่วนโมลาร์ขององค์ประกอบ i-th n iคืออัตราส่วนของจำนวนกิโลโมลของส่วนประกอบ N i ต่อจำนวนกิโลโมลของส่วนผสม N นั่นคือ โดยที่ ![]() , , เช่น จำนวนกิโลโมลของแต่ละส่วนประกอบและของผสมโดยรวมเท่ากับอัตราส่วนของส่วนประกอบที่สอดคล้องกันและของผสมโดยรวมต่อปริมาตรที่ครอบครองโดยหนึ่งกิโลโมล
, , เช่น จำนวนกิโลโมลของแต่ละส่วนประกอบและของผสมโดยรวมเท่ากับอัตราส่วนของส่วนประกอบที่สอดคล้องกันและของผสมโดยรวมต่อปริมาตรที่ครอบครองโดยหนึ่งกิโลโมล
เมื่อพิจารณาว่าก๊าซในอุดมคติภายใต้เงื่อนไขเดียวกันมีปริมาตรเป็นกิโลโมลเท่ากัน หลังจากการแทนที่เราจะได้: , เช่น สำหรับ ก๊าซในอุดมคติเศษส่วนโมลาร์และปริมาตรมีค่าเท่ากับตัวเลข
เศษส่วนมวลขององค์ประกอบ i-thคืออัตราส่วนของมวลของส่วนประกอบต่อมวลของส่วนผสม: ตามมาด้วยมวลของส่วนผสมเท่ากับผลรวมของมวลของส่วนประกอบ และผลรวมของเศษส่วนมวลของส่วนประกอบก็เท่ากัน เป็น 1 (หรือ 100%)
การแปลงเศษส่วนปริมาตรเป็นเศษส่วนมวลและในทางกลับกันขึ้นอยู่กับอัตราส่วนต่อไปนี้:
![]() ,
,
โดยที่ ρ = μ / 22.4, kg / m 3
ดังนั้นเศษส่วนมวลขององค์ประกอบที่ i จะถูกกำหนดจากความสัมพันธ์:
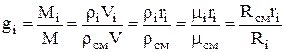 ,
,
โดยที่ความหนาแน่นของส่วนผสมคือ kg / m 3 คือสัดส่วนปริมาตรของส่วนประกอบ i-th
ในอนาคตสามารถกำหนดได้โดยใช้เศษส่วนปริมาตร
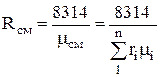 .
.
ความหนาแน่นส่วนผสมของเศษส่วนปริมาตรถูกกำหนดจากความสัมพันธ์
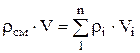 , ที่ไหน
, ที่ไหน 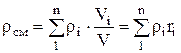 , (1.22)
, (1.22)
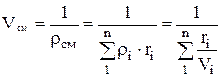 .
.
ความดันบางส่วนถูกกำหนดโดยสูตร:
![]() หรือ
หรือ 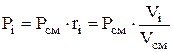 (1.23)
(1.23)
สมการสถานะของส่วนประกอบและของผสมโดยรวมมีรูปแบบ:
![]() ;
;
![]() ,
,
ดังนั้น หลังจากการแปลงร่าง เราได้มา มโหฬารหุ้น
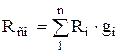 ,
, 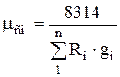 . (1.24)
. (1.24)
ความหนาแน่นและปริมาตรเฉพาะของส่วนผสมสำหรับ มโหฬารแบ่งปัน:
; 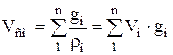 . (1.25)
. (1.25)
ในการคำนวณแรงดันบางส่วน ใช้สูตร:
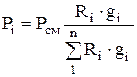 . (1.26)
. (1.26)
การแปลงเศษส่วนมวลเป็นเศษส่วนปริมาตรดำเนินการตามสูตร:
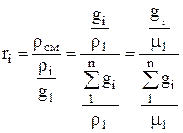 .
.
เมื่อพิจารณาความจุความร้อนของส่วนผสมของก๊าซ จะสันนิษฐานว่าเพื่อให้ความร้อน (เย็น) ส่วนผสมของก๊าซ จำเป็นต้องให้ความร้อน (เย็น) ส่วนประกอบแต่ละส่วนของส่วนผสม
โดยที่ Q i =M i c i ∆t คือความร้อนที่ใช้ในการเปลี่ยนอุณหภูมิของส่วนประกอบที่ i ของส่วนผสม c i คือความจุความร้อนมวลของส่วนประกอบที่ i ของส่วนผสม
ความจุความร้อนของส่วนผสมถูกกำหนดจากอัตราส่วน (หากส่วนผสมถูกกำหนดโดยเศษส่วนมวล)
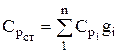 ในทำนองเดียวกัน
ในทำนองเดียวกัน 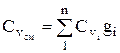 . (1.28)
. (1.28)
ความจุความร้อนโมลาร์และปริมาตรของส่วนผสมที่กำหนดโดยเศษส่วนปริมาตรถูกกำหนดโดย
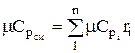 ;
; 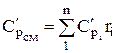 ;
;
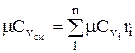 ;
; 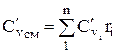
ตัวอย่าง 1.5อากาศแห้งโดยมวลประกอบด้วย g O2 \u003d ออกซิเจน 23.3% และ g N 2 \u003d ไนโตรเจน 76.6% กำหนดองค์ประกอบของอากาศตามปริมาตร (r O2 และ r N 2) และค่าคงที่ของก๊าซของส่วนผสม
การตัดสินใจ.
1. จากตารางที่ 1 เราจะหา กิโลกรัม/กิโลเมตร และ กิโลกรัม/กิโลเมตร
2. กำหนดปริมาตรเศษส่วนของออกซิเจนและไนโตรเจน:
1. ค่าคงที่ของอากาศ (ส่วนผสม) ถูกกำหนดโดยสูตร:
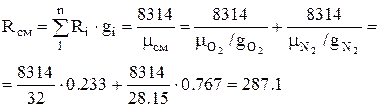 , เจ/กก
, เจ/กก
ตัวอย่าง 1.6. กำหนดปริมาณความร้อนที่ต้องการเพื่อให้ความร้อนแก่ส่วนผสมของก๊าซที่มีมวล M = 2 กก. ที่ P = const ซึ่งมีหน่วยเป็น % โดยน้ำหนัก: , , , , เมื่ออุณหภูมิเปลี่ยนจาก t 1 =900 ° C เป็น t 2 = 1200 องศาเซลเซียส
การตัดสินใจ:
1. กำหนดความจุความร้อนมวลเฉลี่ยของส่วนประกอบที่เป็นส่วนผสมของก๊าซที่ P=const และ t 1 =900 o C (จาก P2):
1.0258 กิโลจูล/กก. K; =1.1045 กิโลจูล/กก. K;
1.1078 กิโลจูล/กก. K; =2.1097 กิโลจูล/กก. K;
2. เรากำหนดความจุความร้อนมวลเฉลี่ยของส่วนประกอบที่ประกอบเป็นส่วนผสมของก๊าซที่ P=const และ t 1 =1200 o C (จาก P2):
1.0509 กิโลจูล/กก. K; =1.153 กิโลจูล/กก. K;
1.1359 กิโลจูล/กก. K; =2.2106 กิโลจูล/กก. K;
3. กำหนดความจุความร้อนมวลเฉลี่ยของส่วนผสมสำหรับช่วงอุณหภูมิ: t 2 \u003d 1200 ° C และ t 1 \u003d 900 ° C:
4. ปริมาณความร้อนเพื่อให้ความร้อน 2 กก. ของส่วนผสมที่ P=const:
กฎข้อที่หนึ่งของอุณหพลศาสตร์กำหนดความสัมพันธ์เชิงปริมาณระหว่างการเปลี่ยนแปลงของพลังงานภายในของระบบและงานเชิงกลที่ดำเนินการกับแรงกดดันภายนอกของสิ่งแวดล้อมอันเป็นผลมาจากการจ่ายความร้อนไปยังของไหลทำงาน
สำหรับระบบอุณหพลศาสตร์แบบปิด สมการของกฎข้อที่หนึ่งมีรูปแบบ
ความร้อนที่ส่งไปยังของไหลทำงาน (หรือระบบ) ถูกใช้เพื่อเพิ่มพลังงานภายใน (dU) เนื่องจากอุณหภูมิของร่างกายเพิ่มขึ้น และเพื่อทำงานภายนอก (dL) เนื่องจากการขยายตัวของของไหลทำงานและการเพิ่มขึ้นของ ปริมาณ.
กฎข้อแรกสามารถเขียนเป็น dH=dq+VdP=dq-dL 0 ,
โดยที่ dL 0 \u003d VdP - งานเบื้องต้นของการเปลี่ยนแปลงแรงดันเรียกว่างานภายนอก (ทางเทคนิค) ที่มีประโยชน์
dU คือการเปลี่ยนแปลงพลังงานภายในของของไหลทำงาน (ระบบ) ซึ่งรวมถึงพลังงานของการเคลื่อนที่ด้วยความร้อนของโมเลกุล (การแปล การหมุน และการสั่น) และพลังงานศักย์ของการทำงานร่วมกันของโมเลกุล
เนื่องจากการเปลี่ยนระบบจากสถานะหนึ่งไปสู่อีกสถานะหนึ่งเกิดขึ้นจากการจ่ายความร้อน ดังนั้นสารทำงานจะร้อนขึ้นและอุณหภูมิจะเพิ่มขึ้น dT และปริมาตรเพิ่มขึ้นโดย dV
การเพิ่มขึ้นของอุณหภูมิของร่างกายทำให้พลังงานจลน์ของอนุภาคเพิ่มขึ้น และการเพิ่มปริมาตรของร่างกายจะนำไปสู่การเปลี่ยนแปลงของพลังงานศักย์ของอนุภาค เป็นผลให้พลังงานภายในร่างกายเพิ่มขึ้น dU ดังนั้นพลังงานภายใน U จึงเป็นฟังก์ชันของสถานะของร่างกายและสามารถแสดงเป็นฟังก์ชันของพารามิเตอร์อิสระสองตัว U=f 1 (P,V); U=f 2 (P,T), U=f 3 (υ,T) การเปลี่ยนแปลงของพลังงานภายในในกระบวนการทางอุณหพลศาสตร์ถูกกำหนดโดยสถานะเริ่มต้น (U 1) และสถานะสุดท้าย (U 2) เท่านั้น เช่น
ในรูปแบบดิฟเฟอเรนเชียลจะเขียนการเปลี่ยนแปลงพลังงานภายใน
ก) เป็นฟังก์ชันของปริมาตรและอุณหภูมิเฉพาะ
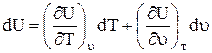
b) เป็นฟังก์ชันของอุณหภูมิตั้งแต่ , แล้ว
สำหรับการคำนวณเชิงปฏิบัติซึ่งจำเป็นต้องคำนึงถึงการเปลี่ยนแปลงใน C v กับอุณหภูมิ มีสูตรเชิงประจักษ์และตารางของพลังงานภายในที่เฉพาะเจาะจง (มักเป็นโมลาร์) สำหรับก๊าซในอุดมคติ พลังงานภายในโมลาร์ของส่วนผสม U m ถูกกำหนดโดยสูตร
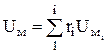 , เจ/กมล
, เจ/กมล
สำหรับส่วนผสมที่กำหนดโดยเศษส่วนมวล ดังนั้น กำลังภายในกิน คุณสมบัติของระบบและกำหนดลักษณะสถานะของระบบ.
เอนทัลปีเป็นฟังก์ชันสถานะความร้อนที่แนะนำโดย Kamerling-Onnes (ผู้ชนะ รางวัลโนเบล, 1913) ซึ่งเป็นผลรวมของพลังงานภายในของระบบ U และผลคูณของความดันของระบบ P และปริมาตร V
เนื่องจากปริมาณที่รวมอยู่ในนั้นเป็นฟังก์ชันสถานะ ดังนั้น H จึงเป็นฟังก์ชันสถานะด้วย เช่น H \u003d f 1 (P, V); H=ฉ 2 (V,T); H=ฉ 3 (P, T)
การเปลี่ยนแปลงของเอนทาลปี dH ในกระบวนการทางอุณหพลศาสตร์ใดๆ ถูกกำหนดโดยสถานะเริ่มต้นของ H 1 และ H 2 สุดท้าย และไม่ขึ้นอยู่กับธรรมชาติของกระบวนการ หากระบบประกอบด้วยสาร 1 กิโลกรัม จะใช้เอนทัลปีเฉพาะ J/กก.
สำหรับแก๊สในอุดมคติ สมการเชิงอนุพันธ์มีรูปแบบดังนี้
ดังนั้นเอนทัลปีเฉพาะจะถูกกำหนดโดยสูตร
สมการของกฎข้อที่หนึ่งของอุณหพลศาสตร์คือ dq=dU+Pdυ เมื่องานประเภทเดียวคืองานขยายตัว Pdυ=d(Pυ)-υdP จากนั้น dq=d(U+Pυ)-υdP ดังนั้น
ในทางปฏิบัติทางวิศวกรรม เรามักจะต้องไม่จัดการกับก๊าซที่เป็นเนื้อเดียวกัน แต่กับส่วนผสมของก๊าซที่ไม่เกี่ยวข้องทางเคมี ตัวอย่างของส่วนผสมของก๊าซ ได้แก่ อากาศในชั้นบรรยากาศ ก๊าซธรรมชาติ ผลิตภัณฑ์ก๊าซจากการเผาไหม้เชื้อเพลิง เป็นต้น
สำหรับส่วนผสมของแก๊ส ให้ปฏิบัติตามข้อกำหนดต่อไปนี้
1. ก๊าซแต่ละชนิดที่เข้าสู่ส่วนผสมมีอุณหภูมิ เท่ากับอุณหภูมิส่วนผสม
2. ก๊าซใด ๆ ที่รวมอยู่ในส่วนผสมจะกระจายไปทั่วปริมาตรของส่วนผสม ดังนั้นปริมาตรของก๊าซแต่ละชนิดจะเท่ากับปริมาตรของส่วนผสมทั้งหมด
3. ก๊าซแต่ละชนิดที่รวมอยู่ในส่วนผสมเป็นไปตามสมการสถานะของมันเอง
4. ส่วนผสมทั้งหมดเป็นเหมือนก๊าซใหม่และเป็นไปตามสมการสถานะของมันเอง
การศึกษาส่วนผสมของแก๊สเป็นไปตามกฎของดาลตัน ซึ่งที่อุณหภูมิคงที่ ความดันของส่วนผสมจะเท่ากับผลรวมของความดันบางส่วนของแก๊สที่รวมอยู่ในส่วนผสม:
โดยที่ p cm คือความดันของส่วนผสม
pi - ความดันบางส่วนของก๊าซ i-th ที่รวมอยู่ในส่วนผสม
n คือจำนวนของก๊าซที่รวมอยู่ในส่วนผสม
ความดันบางส่วนคือความดันที่ก๊าซที่เข้าสู่ส่วนผสมจะออกแรงหากก๊าซเพียงอย่างเดียวครอบครองปริมาตรทั้งหมดของส่วนผสมที่อุณหภูมิเดียวกัน
วิธีการตั้งส่วนผสมของแก๊ส
ส่วนประกอบของส่วนผสมของแก๊สสามารถระบุได้จากมวล ปริมาตร และเศษส่วนของโมล
เศษส่วนมวล. เศษส่วนมวลของก๊าซใดๆ ที่รวมอยู่ในส่วนผสมคืออัตราส่วนของมวลของก๊าซนี้ต่อมวลของส่วนผสม
ม. 1 \u003d ม. 1 / ม. ซม.; ม. 2 \u003d ม. 2 / ม. ซม.; ..........; ม n \u003d ม n / ม ซม.
ที่ไหน ม. 1 , ม. 2 , ..., ม. - เศษส่วนมวลก๊าซ
M 1 , M 2 , ..., M n - มวลของก๊าซแต่ละตัว
M cm คือมวลของส่วนผสม
มันง่ายที่จะเห็นว่า 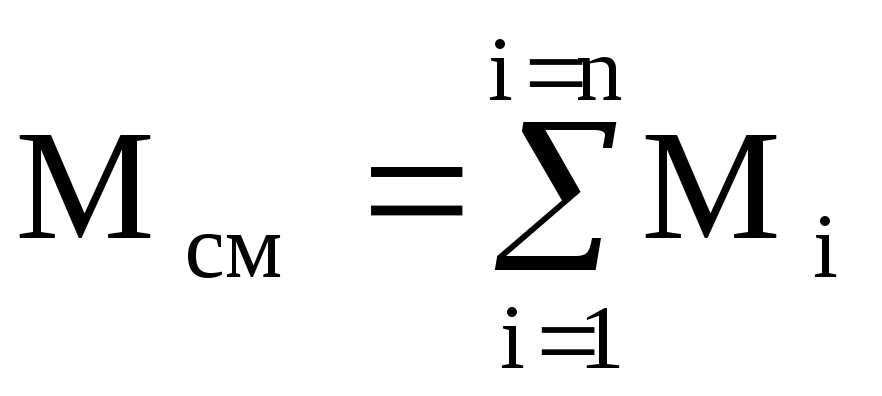 และ
และ 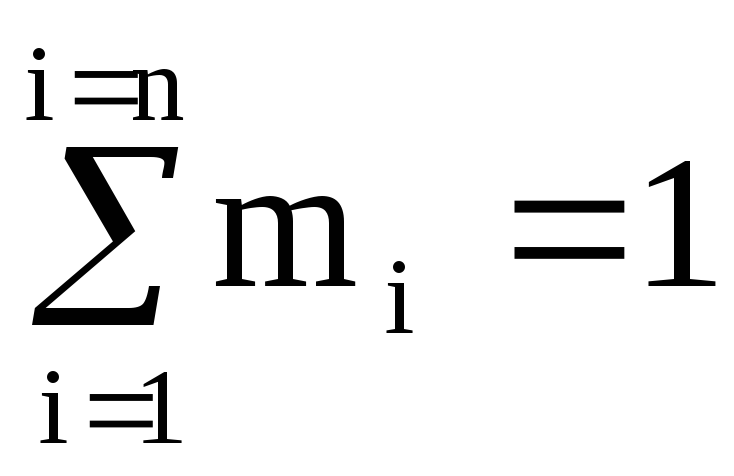 (100%).
(100%).
ปริมาณหุ้น.ส่วนปริมาตรของก๊าซใดๆ ที่รวมอยู่ในส่วนผสมคืออัตราส่วนของปริมาตรที่ลดลง (บางส่วน) ของก๊าซนี้ต่อปริมาตรของส่วนผสม
r 1 \u003d V 1 / V ซม. r 2 \u003d V 2 / V ซม. ........., r n = V n / V cm;
ที่ไหน V 1 , V 2 , ... , V n - ปริมาณก๊าซลดลง
V ซม. คือปริมาตรของส่วนผสม
r 1 , r 2 , ..., r n - ปริมาตรเศษส่วนของก๊าซ
ปริมาตรที่ลดลงคือปริมาตรของก๊าซภายใต้สภาวะของส่วนผสม (ที่อุณหภูมิและความดันของส่วนผสม)
ปริมาตรที่ลดลงสามารถแสดงได้ดังนี้: ถ้าก๊าซทั้งหมดยกเว้นก๊าซหนึ่งถูกเอาออกจากถังบรรจุของผสม และก๊าซที่เหลือถูกบีบอัดไปที่ความดันของส่วนผสมในขณะที่รักษาอุณหภูมิ ปริมาตรของมันจะลดลงหรือบางส่วน
สามารถพิสูจน์ได้ว่าปริมาตรของส่วนผสมจะเท่ากับผลรวมของปริมาตรก๊าซที่ลดลง
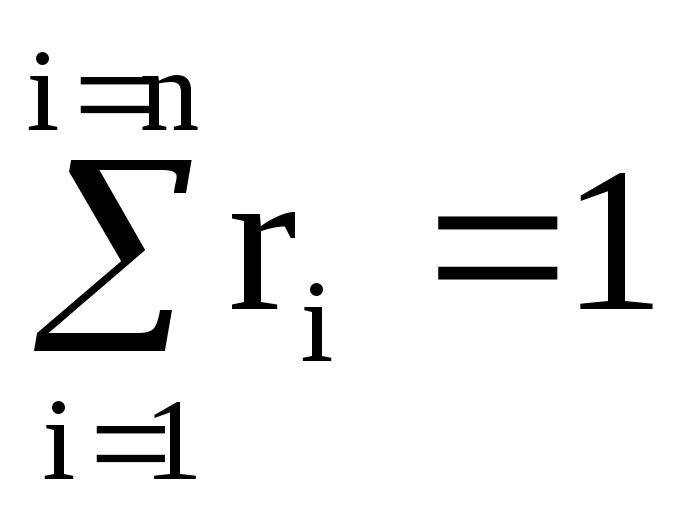 (100%).
(100%).
เศษส่วนโมลส่วนโมลของก๊าซใดๆ ที่รวมอยู่ในส่วนผสมคืออัตราส่วนของจำนวนกิโลโมลของก๊าซนี้ต่อจำนวนกิโลโมลของส่วนผสม
r 1 \u003d n 1 / n cm; r 2 \u003d n 2 / n cm; ........., r n \u003d n n / n cm,
ที่ไหน r 1 , r 2 , ..., r n - เศษส่วนของโมลของก๊าซ
n cm คือจำนวนกิโลโมลของส่วนผสม
n 1 , n 2 , ..., n n คือจำนวนของก๊าซกิโลโมล
การระบุส่วนผสมด้วยเศษส่วนโมลจะเหมือนกับการระบุส่วนผสมด้วยเศษส่วนปริมาตร กล่าวคือ เศษส่วนโมลาร์และปริมาตรมีค่าตัวเลขเท่ากันสำหรับก๊าซแต่ละชนิดที่รวมอยู่ในส่วนผสม
น้ำหนักโมเลกุลคงที่และชัดเจน (เฉลี่ย) ของก๊าซของสารผสมในการคำนวณค่าคงที่ของส่วนผสมของก๊าซที่กำหนดโดยเศษส่วนมวล เราเขียนสมการสถานะ:
สำหรับส่วนผสม
p ซม. × V ซม. = M ซม. R ซม. T; (1.9)
สำหรับก๊าซ
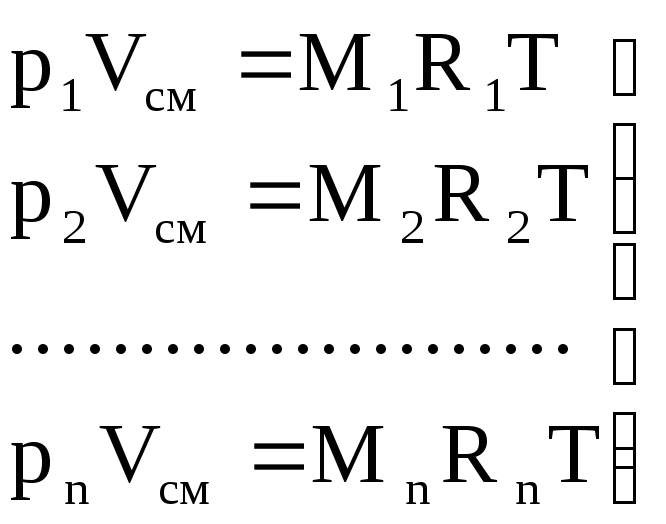 .
(1.10)
.
(1.10)
เรารวมส่วนซ้ายและขวาของสมการ (1.10)
(p 1 + p 2 + .... + p n) V cm = (M 1 R 1 + M 2 R 2 + ..... + M n R n) ต.
เพราะ 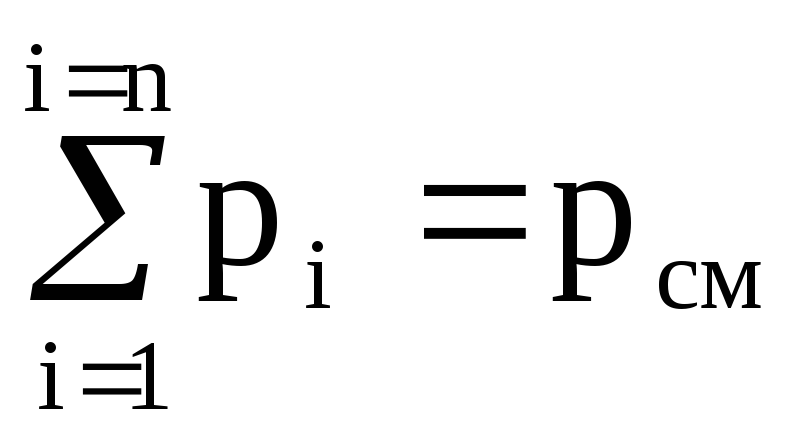 ,
,
แล้ว p cm V cm = (M 1 R 1 + M 2 R 2 + ..... + M n R n) T. (1.11)
สมการ (1.9) และ (1.11) บอกเป็นนัยว่า
M cm R cm T \u003d (M 1 R 1 + M 2 R 2 + ..... + M n R n) ต.
R cm \u003d M 1 / M cm R 1 + M 2 / M cm R 2 + ...... + M n / M cm R n \u003d
M 1 R 1 + m 2 R 2 + ...... + m n R n
หรือ 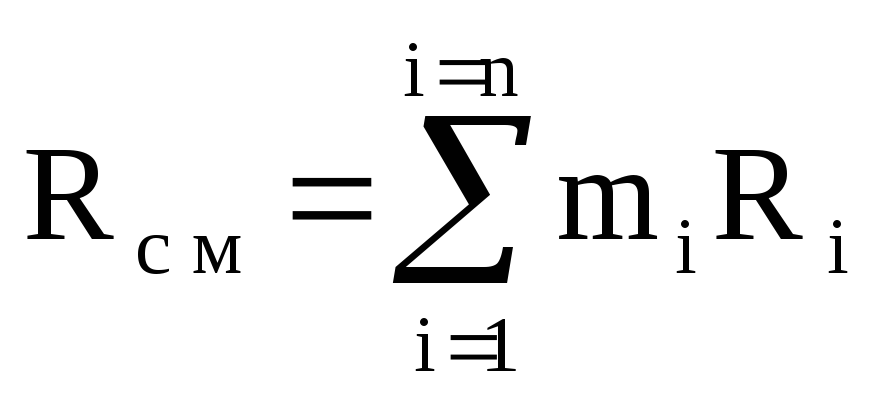 ,
(1.12)
,
(1.12)
โดยที่ R cm คือค่าคงที่ของแก๊สของส่วนผสม
เนื่องจากค่าคงที่ของแก๊ส i-th
R i = 8314 / m ผม ,
จากนั้นสมการ (1.12) จะเขียนใหม่ดังนี้:
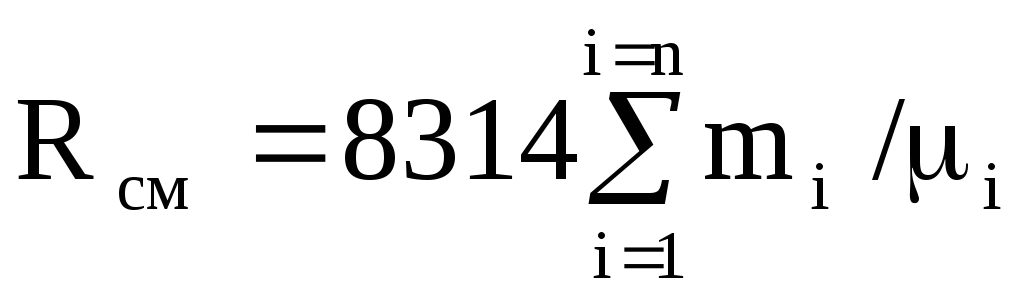 .
(1.13)
.
(1.13)
เมื่อกำหนดพารามิเตอร์ของส่วนผสมของก๊าซ จะสะดวกที่จะใช้ค่าเงื่อนไขบางอย่างที่เรียกว่าน้ำหนักโมเลกุลที่ชัดเจน (เฉลี่ย) ของส่วนผสมของก๊าซ แนวคิดเกี่ยวกับน้ำหนักโมเลกุลที่ชัดเจนของสารผสมช่วยให้เราสามารถพิจารณาสารผสมในรูปของก๊าซที่เป็นเนื้อเดียวกันตามอัตภาพ ซึ่งทำให้การคำนวณง่ายขึ้นอย่างมาก
สำหรับก๊าซที่แยกจากกัน นิพจน์
โดยการเปรียบเทียบสำหรับส่วนผสม เราสามารถเขียนได้
ม ซม. ร ซม = 8314, (1.14)
โดยที่ m cm คือน้ำหนักโมเลกุลที่ปรากฏของสารผสม
จากสมการ (1.14) โดยใช้นิพจน์ (1.12) และ (1.13) เราได้รับ
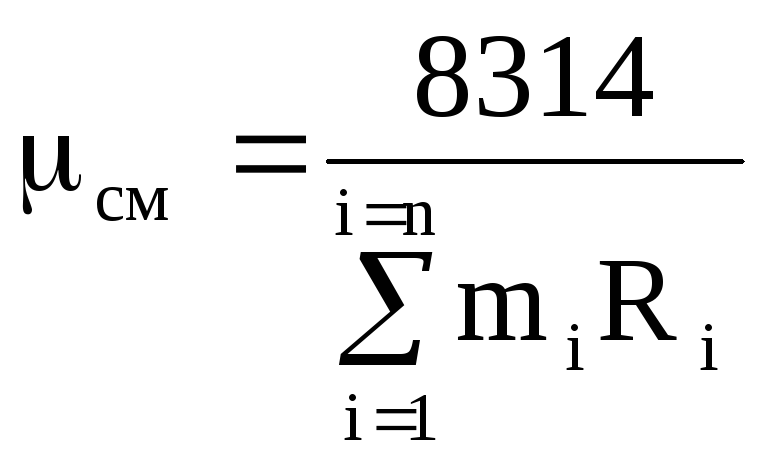 ,
(1.15)
,
(1.15)
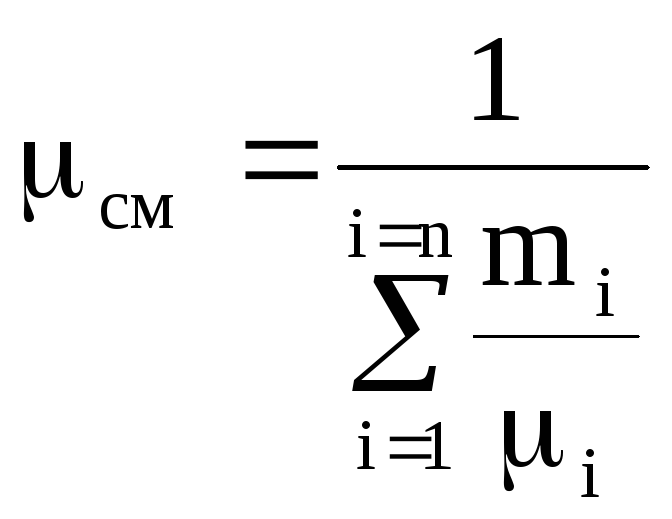 .
(1.16)
.
(1.16)
การโต้เถียงด้วยวิธีนี้ เราสามารถรับสูตรสำหรับการคำนวณ R cm และ m cm ผ่านเศษส่วนปริมาตร สูตรสำหรับการแปลงเศษส่วนมวลเป็นเศษส่วนปริมาตร และในทางกลับกัน เศษส่วนปริมาตรเป็นเศษส่วนมวล สูตรสำหรับการคำนวณปริมาตรเฉพาะของส่วนผสม u cm และ ความหนาแน่นของส่วนผสม r cm ผ่านเศษส่วนมวลและปริมาตร และสุดท้าย สูตรสำหรับคำนวณความดันบางส่วนของก๊าซที่รวมอยู่ในส่วนผสม ผ่านปริมาตรและเศษส่วนมวล เรานำเสนอสูตรเหล่านี้โดยไม่มีแหล่งที่มาในตาราง
สูตรคำนวณส่วนผสมของแก๊ส
|
การตั้งค่าองค์ประกอบของส่วนผสม |
ถ่ายโอนจากองค์ประกอบหนึ่งไปยังอีกองค์ประกอบหนึ่ง |
ความหนาแน่นและปริมาตรเฉพาะของส่วนผสม |
น้ำหนักโมเลกุลที่ชัดเจนของส่วนผสม |
ค่าคงที่ของส่วนผสมของแก๊ส |
ความดันบางส่วน |
|
เศษส่วนมวล |
|
|
|
|
|
|
เศษส่วนปริมาตร |
|
|
|
|
|
ความจุความร้อนของก๊าซ
ความจุความร้อนของร่างกายคือปริมาณความร้อนที่ต้องใช้เพื่อให้ความร้อนหรือทำให้ร่างกายเย็นลง 1 K ความจุความร้อนของสารหนึ่งหน่วยเรียกว่าความจุความร้อนจำเพาะ
ดังนั้น ความจุความร้อนจำเพาะของสสารคือปริมาณความร้อนที่ต้องให้หรือลบออกจากหน่วยของสารเพื่อเปลี่ยนอุณหภูมิ 1 K ในกระบวนการนี้
เนื่องจากความจุความร้อนจำเพาะจะพิจารณาในสิ่งต่อไปนี้ เราจะเรียกความจุความร้อนจำเพาะง่ายๆ ว่าความจุความร้อน
ปริมาณของก๊าซสามารถหาได้จากมวล ปริมาตร และจำนวนกิโลโมล ควรสังเกตว่าเมื่อตั้งค่าปริมาตรก๊าซ ปริมาตรนี้จะเข้าสู่สภาวะปกติและวัดเป็นลูกบาศก์เมตรปกติ (นาโนเมตร 3)
ความจุความร้อนต่อไปนี้ขึ้นอยู่กับวิธีการตั้งค่าปริมาณของก๊าซ:
c - ความจุความร้อนมวล, J / (กก. × K);
c ¢ - ความจุความร้อนเชิงปริมาตร J / (nm 3 × K);
cm - ความจุความร้อนของกราม J / (kmol × K)
ระหว่างความจุความร้อนเหล่านี้มีความสัมพันธ์ดังต่อไปนี้:
ค = ซม. / ม.; กับ ม = กับ × ม;
с¢ = с m / 22.4; ด้วย m = s¢ × 22.4,
จากที่นี่ 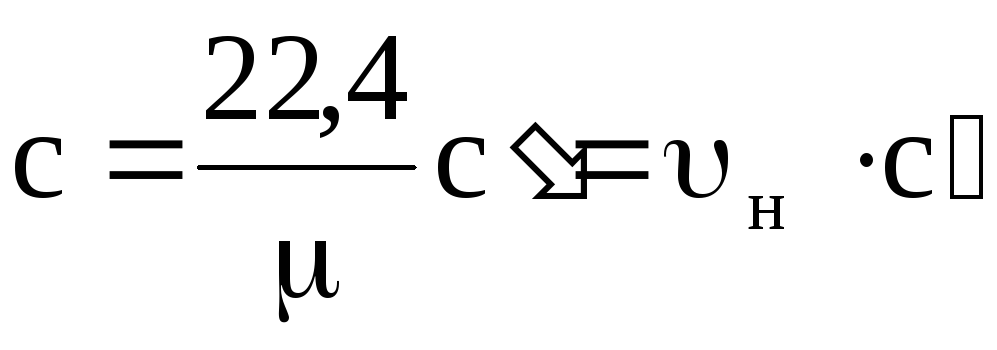 ; s¢ = s × r n
; s¢ = s × r n
โดยที่ คุณ n และ rn - ปริมาตรและความหนาแน่นเฉพาะภายใต้สภาวะปกติ
ความจุความร้อนแบบไอโซโคริกและไอโซบาริก
ปริมาณความร้อนที่จ่ายให้กับของไหลทำงานขึ้นอยู่กับคุณลักษณะของกระบวนการอุณหพลศาสตร์ ความจุความร้อนสองประเภทมีความสำคัญในทางปฏิบัติโดยขึ้นอยู่กับกระบวนการทางอุณหพลศาสตร์: ไอโซคอริกและไอโซบาริก
ความจุความร้อนที่ u = const คือ isochoric
c คุณ - มวลความจุความร้อนไอโซโคริก
ค ยูคือความจุความร้อนไอโซโคริกเชิงปริมาตร
ซี ม ยูคือความจุความร้อนไอโซคอริกของโมลาร์
ความจุความร้อนที่ p = const คือ isobaric
c p - มวลความจุความร้อนไอโซบาริก
c ¢ р - ปริมาตรความจุความร้อนไอโซบาริก
cm p - ความจุความร้อนไอโซบาริกของกราม
ด้วยอุณหภูมิที่เปลี่ยนแปลงเท่ากันในกระบวนการที่ดำเนินการที่ p = const ความร้อนจะถูกใช้มากกว่าในกระบวนการที่ u = const สิ่งนี้อธิบายได้จากข้อเท็จจริงที่ว่าที่ u = const ความร้อนที่ให้แก่ร่างกายจะถูกใช้ไปกับการเปลี่ยนพลังงานภายในเท่านั้น ในขณะที่ p = const ความร้อนจะถูกใช้ทั้งเพื่อเพิ่มพลังงานภายในและในการทำงานของการขยายตัว ความแตกต่างระหว่างความจุความร้อนของมวลไอโซบาริกและมวลไอโซคอริกตามสมการเมเยอร์
ซี พี - ซี ยู=ร. (1.17)
ถ้าด้านซ้ายและขวาของสมการ (1.17) คูณด้วยมวลกิโลโมล m แล้วเราจะได้
ซม. พี - ซม ยู= 8314 เจ/(กโมล×เคล) (1.18)
ในอุณหพลศาสตร์และการใช้งาน อัตราส่วนของความจุความร้อนไอโซบาริกและไอโซคอริกมีความสำคัญอย่างยิ่ง:
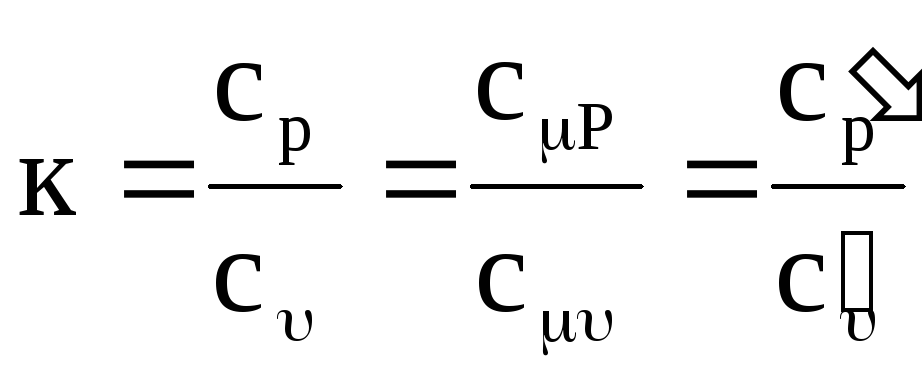 ,
(1.19)
,
(1.19)
โดยที่ k คือเลขชี้กำลังอะเดียแบติก
การคำนวณแสดงว่าสำหรับก๊าซเชิงเดี่ยว k » 1.67, ก๊าซไดอะตอม k » 1.4 และก๊าซไตรอะตอม k » 1.29
มันง่ายที่จะเห็นคุณค่า ถึงขึ้นอยู่กับอุณหภูมิ ตามสมการ (1.17) และ (1.19) ที่ว่า
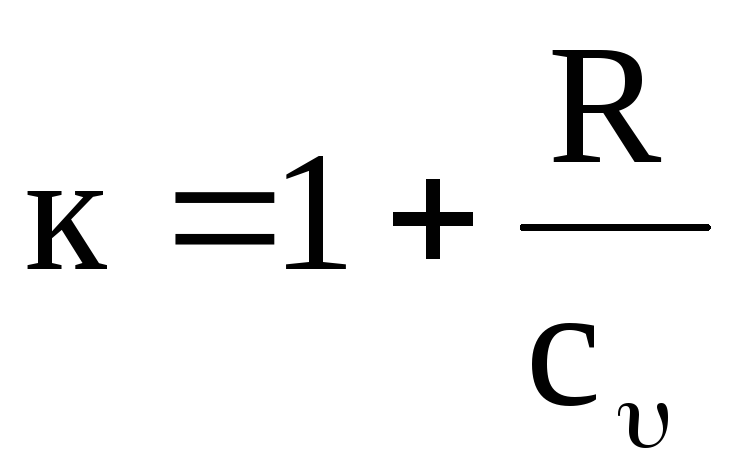 ,
(1.20)
,
(1.20)
และจากสมการ (1.18) และ (1.19)
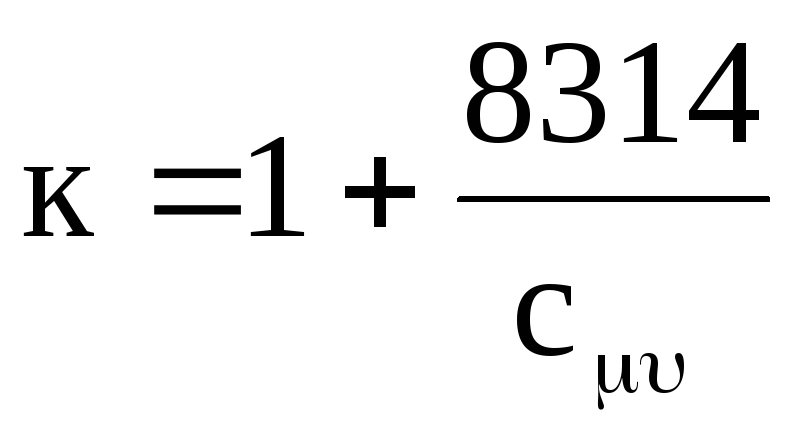 .
(1.21)
.
(1.21)
เนื่องจากความจุความร้อนเพิ่มขึ้นตามอุณหภูมิของก๊าซที่เพิ่มขึ้น ค่าของ k จะลดลง เข้าใกล้เอกภาพ แต่ยังคงมากกว่าค่านั้นเสมอ
เมื่อทราบค่า k เราสามารถกำหนดค่าของความจุความร้อนที่สอดคล้องกัน ตัวอย่างเช่น จากสมการ (1.20) เรามี
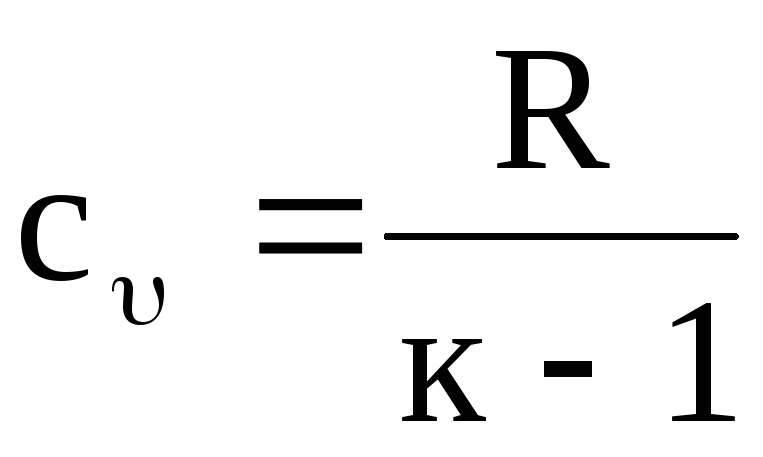 ,
(1.22)
,
(1.22)
และตั้งแต่นั้นเป็นต้นมา ด้วย p = k × s ยูแล้วเราจะได้รับ
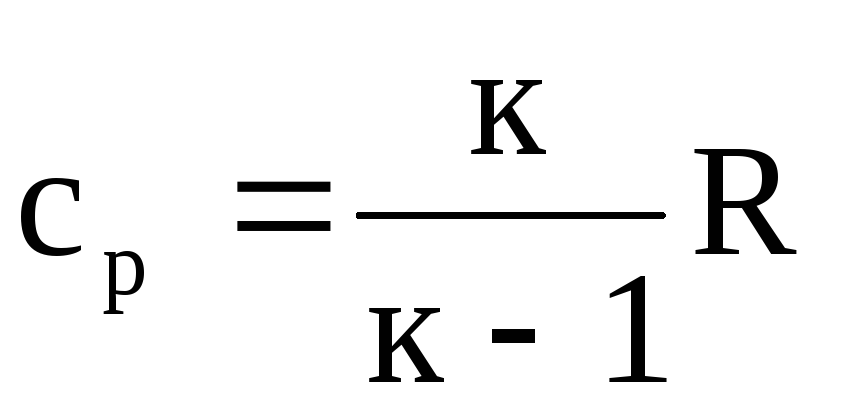 .
(1.23)
.
(1.23)
ในทำนองเดียวกัน สำหรับความจุความร้อนของโมล เราได้รับจากสมการ (1.21)
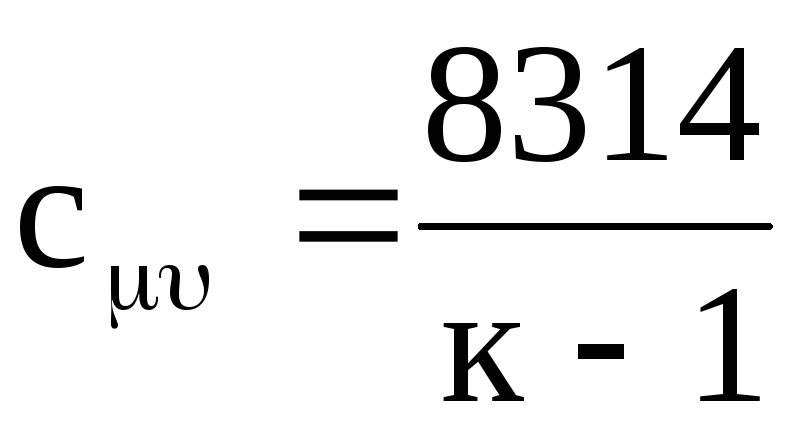 .
(1.24)
.
(1.24)
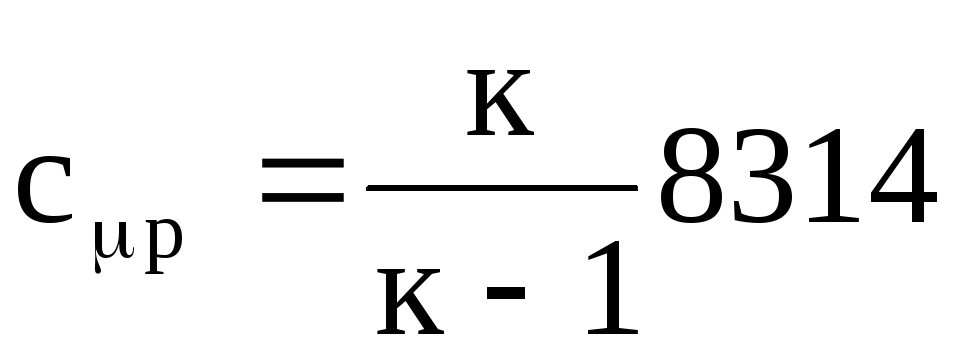 .
(1.25)
.
(1.25)
ความจุความร้อนเฉลี่ยและจริง
ความจุความร้อนของก๊าซขึ้นอยู่กับอุณหภูมิและความดันในระดับหนึ่ง การพึ่งพาความจุความร้อนกับความดันมีน้อยและถูกละเลยในการคำนวณส่วนใหญ่ การพึ่งพาความจุความร้อนต่ออุณหภูมิมีความสำคัญและต้องนำมาพิจารณาด้วย การพึ่งพาอาศัยกันนี้แสดงออกมาได้อย่างแม่นยำในสมการ
ค = เอ + ในเสื้อ + et 2 , (1.26)
ที่ไหน, ในและ e คือค่าคงที่สำหรับก๊าซที่กำหนด
บ่อยครั้งในการคำนวณทางวิศวกรรมความร้อน การพึ่งพาแบบไม่เชิงเส้น (1.26) จะถูกแทนที่ด้วยแบบเชิงเส้น:
ค = เอ + ในที (1.27)
|
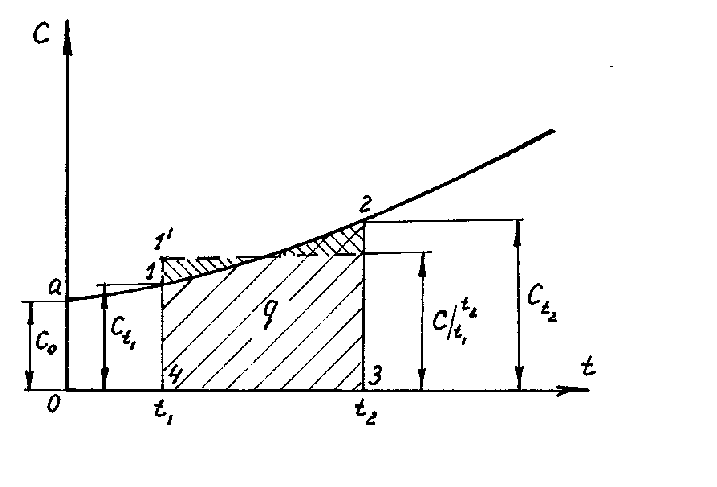
หากเราสร้างกราฟิกการพึ่งพาความจุความร้อนต่ออุณหภูมิตามสมการ (1.26) นี่จะเป็นการพึ่งพาเส้นโค้ง (รูปที่ 1.4) ดังที่แสดงในรูป ค่าอุณหภูมิแต่ละค่ามีค่าความจุความร้อนของตัวเอง ซึ่งโดยทั่วไปเรียกว่าความจุความร้อนที่แท้จริง ในทางคณิตศาสตร์ นิพจน์สำหรับความจุความร้อนที่แท้จริงเขียนได้ดังนี้:
|
|
|
|
ดังนั้น ความจุความร้อนที่แท้จริงคืออัตราส่วนของปริมาณความร้อนเล็กน้อย dq ต่อการเปลี่ยนแปลงอุณหภูมิเล็กน้อย dt กล่าวอีกนัยหนึ่ง ความจุความร้อนที่แท้จริงคือความจุความร้อนของก๊าซ ณ อุณหภูมิที่กำหนด บนมะเดื่อ 1.4 ความจุความร้อนที่แท้จริงที่อุณหภูมิ t 1 จะแสดงด้วย t1 และแสดงเป็นส่วนที่ 1-4 ที่อุณหภูมิ t 2 - ด้วย t2 และแสดงเป็นส่วนที่ 2-3 จากสมการ (1.28) เราได้ dq=ซีดีที (1.29) ในการคำนวณเชิงปฏิบัติ เรากำหนดเสมอ ปริมาณความร้อนที่การเปลี่ยนแปลงครั้งสุดท้าย |
อุณหภูมิ. เห็นได้ชัดว่าปริมาณความร้อน q ซึ่งรายงานเป็นหน่วยปริมาณของสารเมื่อได้รับความร้อนจาก t 1 ถึง t 2 สามารถหาได้จากการอินทิเกรต (1.29) จาก t 1 ถึง t 2
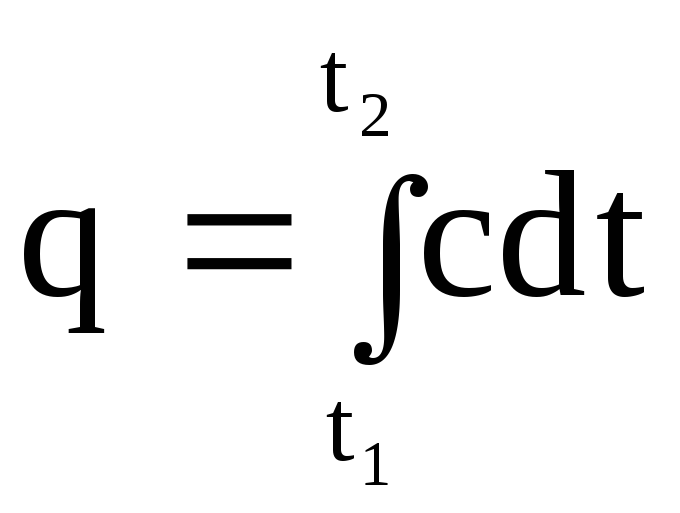 .
(1.30)
.
(1.30)
เชิงกราฟิก อินทิกรัล (1.30) แสดงโดยพื้นที่ 4-1-2-3 หากในการแสดงออก (1.30) เราแทนค่าความจุความร้อนที่แท้จริงตามการพึ่งพาเชิงเส้น (1.27) จากนั้นเราจะได้
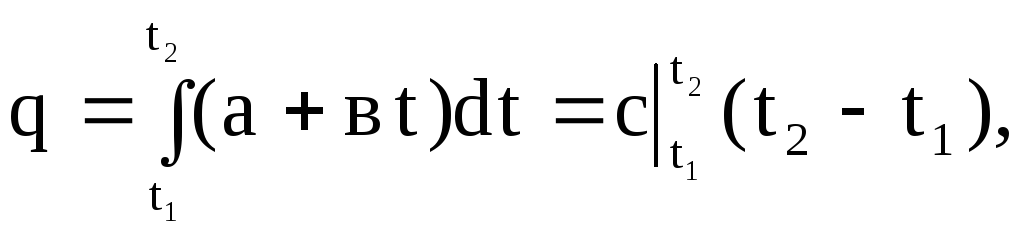 (1.31)
(1.31)
ที่ไหน 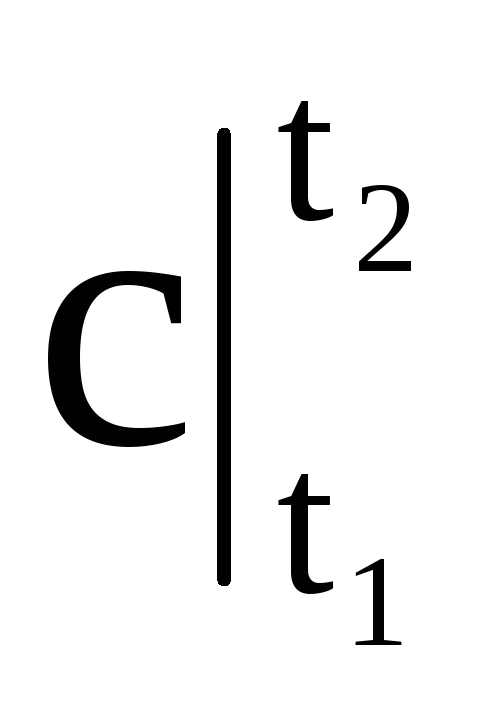 - ความจุความร้อนเฉลี่ยในช่วงอุณหภูมิตั้งแต่ t 1 ถึง t 2
- ความจุความร้อนเฉลี่ยในช่วงอุณหภูมิตั้งแต่ t 1 ถึง t 2
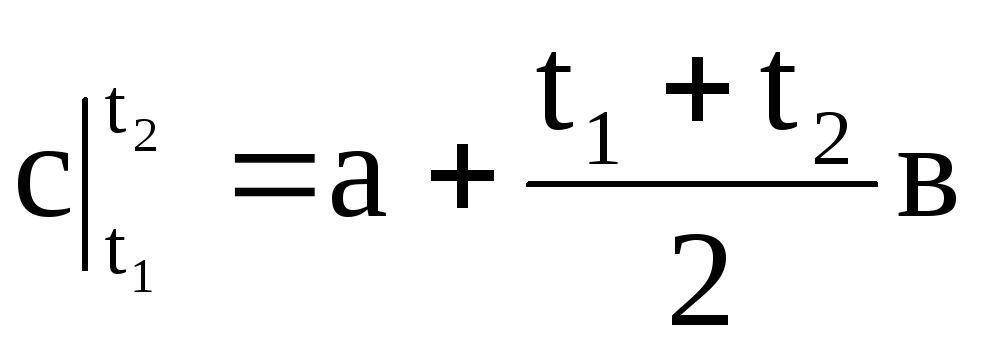 ,
(1.32)
,
(1.32)
ดังนั้นความจุความร้อนเฉลี่ยคืออัตราส่วนของปริมาณความร้อนสุดท้าย q ต่อการเปลี่ยนแปลงอุณหภูมิสุดท้าย เสื้อ 2 - เสื้อ 1:
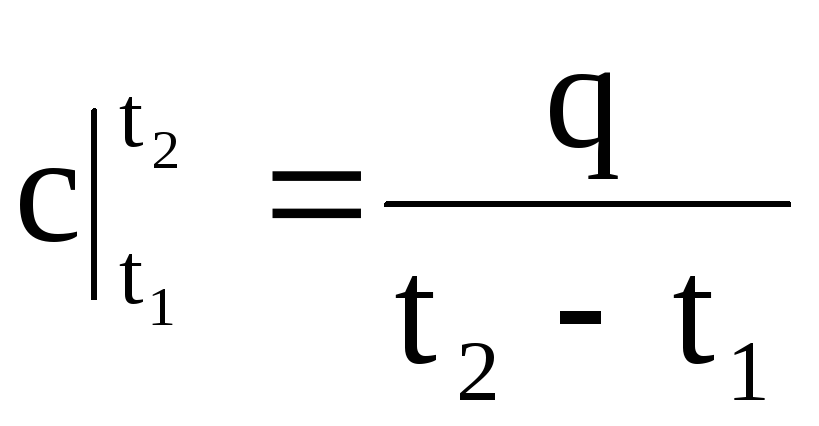 .
(1.33)
.
(1.33)
ถ้าบนพื้นฐานของ 4-3 (รูปที่ 1.4) มีการสร้างสี่เหลี่ยมผืนผ้า 4-1¢-2¢-3 ซึ่งมีขนาดเท่ากับรูปที่ 4-1-2-3 แล้วความสูงของสี่เหลี่ยมผืนผ้านี้จะ เท่ากับความจุความร้อนเฉลี่ย โดยที่ 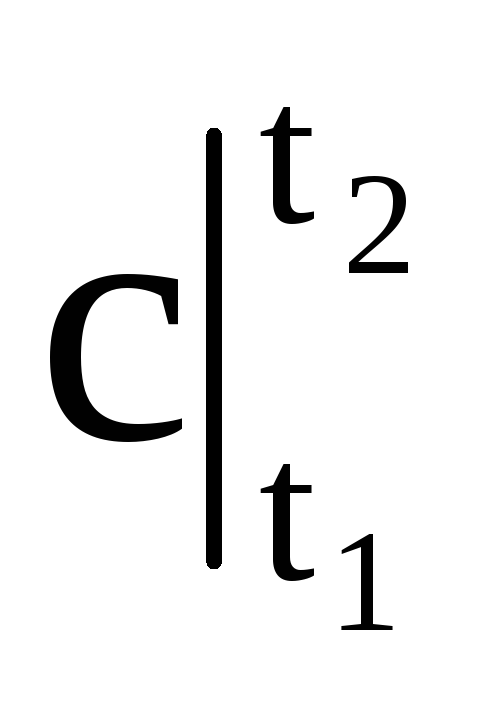 อยู่ในช่วงอุณหภูมิ เสื้อ 1 - เสื้อ 2 .
อยู่ในช่วงอุณหภูมิ เสื้อ 1 - เสื้อ 2 .
โดยปกติค่าความจุความร้อนเฉลี่ยจะได้รับในตารางคุณสมบัติทางอุณหพลศาสตร์ของสาร อย่างไรก็ตาม เพื่อลดปริมาณของตารางเหล่านี้ ค่าความจุความร้อนเฉลี่ยที่กำหนดในช่วงอุณหภูมิตั้งแต่ 0 ° C ถึง t ° C
หากจำเป็นต้องคำนวณค่าความจุความร้อนเฉลี่ยในช่วงอุณหภูมิที่กำหนด t 1 - t 2 สามารถทำได้ดังนี้
พื้นที่ 0a14 ใต้เส้นโค้ง c \u003d f (t) (รูปที่ 1.4) สอดคล้องกับปริมาณความร้อน q 1 ที่จำเป็นในการเพิ่มอุณหภูมิของก๊าซจาก 0 ° C เป็น t 1 ° C
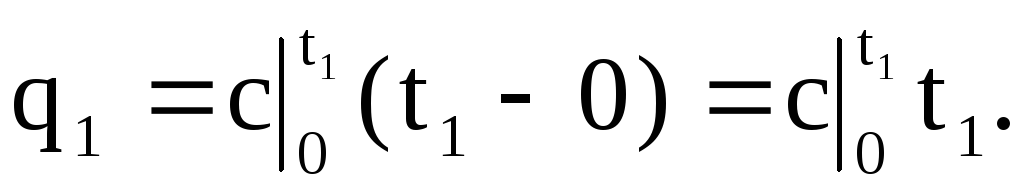
ในทำนองเดียวกัน พื้นที่ 0a23 สอดคล้องกับ q 2 เมื่ออุณหภูมิเพิ่มขึ้นจาก 0 o C ถึง t 2 o C:
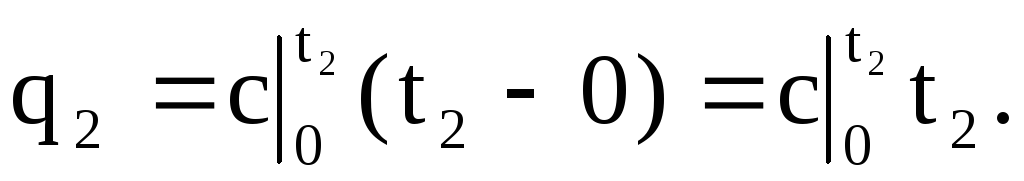
ดังนั้น q \u003d q 2 - q 1 (พื้นที่ 4123) สามารถแสดงเป็น
![]() (1.34)
(1.34)
แทนค่า q ตาม (1.34) เป็นนิพจน์ (1.33) เราได้รับสูตรสำหรับความจุความร้อนเฉลี่ยในช่วงอุณหภูมิใด ๆ :
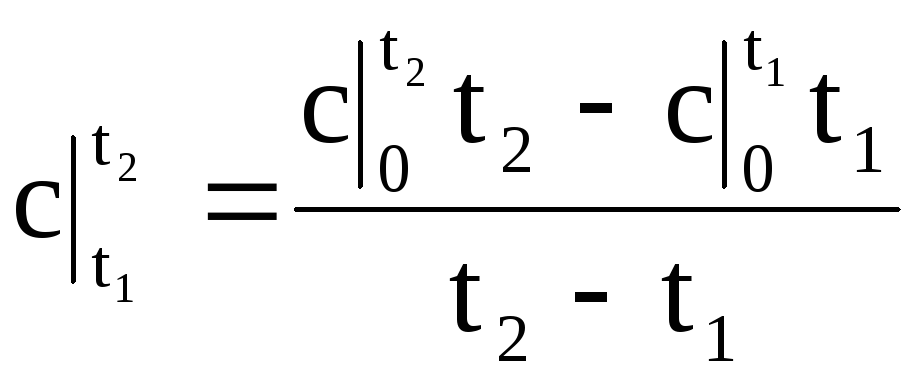 .
(1.35)
.
(1.35)
ดังนั้น ความจุความร้อนเฉลี่ยสามารถคำนวณได้จากความจุความร้อนเฉลี่ยแบบตารางโดยใช้สมการ (1.35) นอกจากนี้ เราได้รับการพึ่งพาแบบไม่เชิงเส้น c = f(t) คุณยังสามารถหาความจุความร้อนเฉลี่ยโดยใช้สมการ (1.32) โดยใช้ความสัมพันธ์เชิงเส้น ค่า a และ ในในสมการ (1.32) สำหรับก๊าซต่าง ๆ มีให้ในเอกสาร
ปริมาณความร้อนที่จ่ายหรือกำจัดออกจากของไหลทำงานสามารถคำนวณได้โดยใช้สมการใดก็ได้:
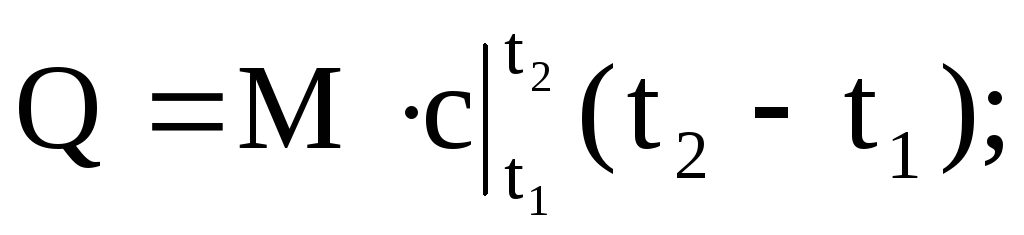 (1.36)
(1.36)
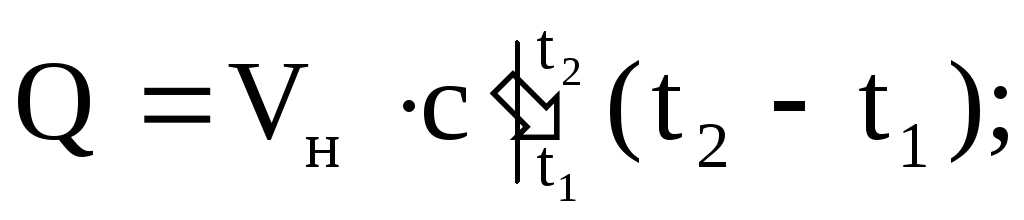 (1.37)
(1.37)
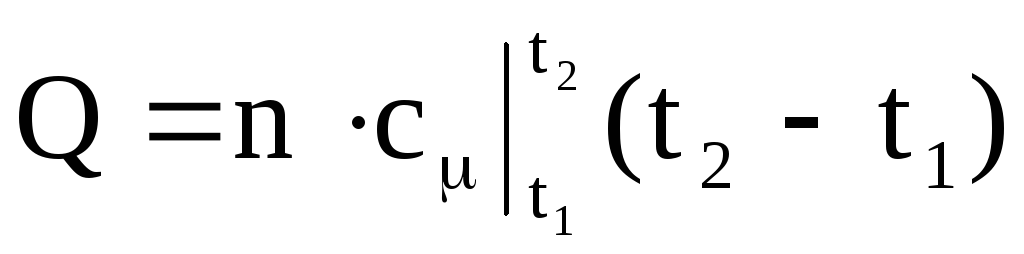 ,
(1.38)
,
(1.38)
ที่ไหน 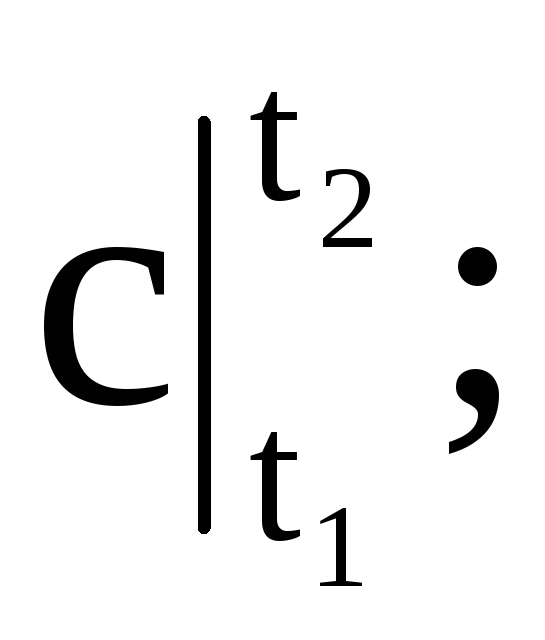
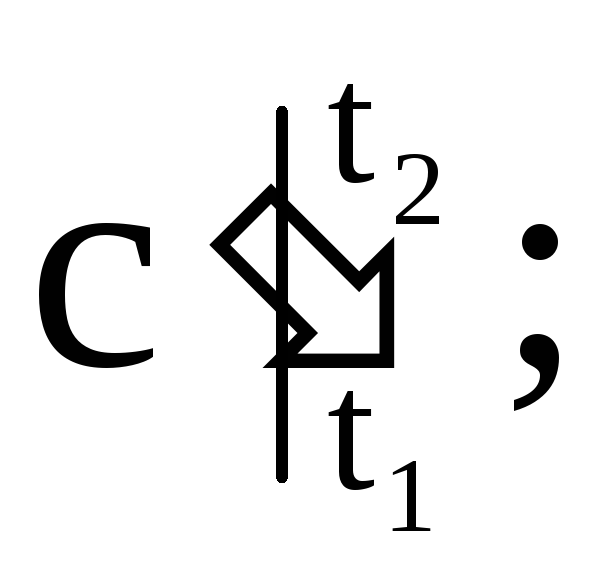
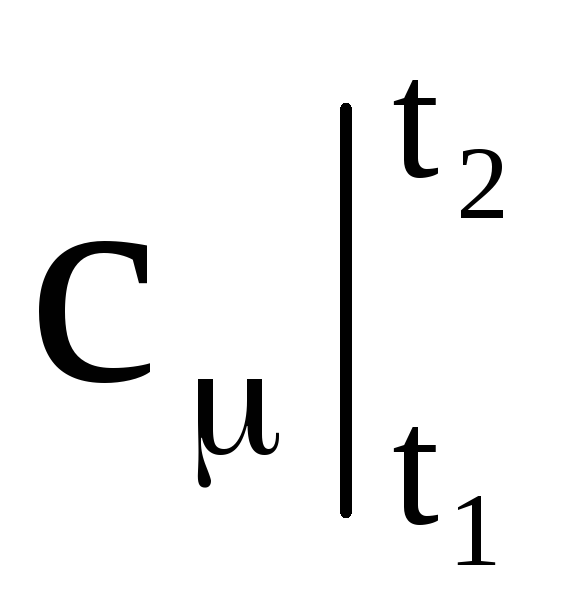 - ตามลำดับ มวลเฉลี่ย ปริมาตร และความจุความร้อนของโมลาร์ M คือมวลของก๊าซ n คือจำนวนกิโลโมลของก๊าซ V n - ปริมาตรของก๊าซภายใต้สภาวะปกติ
- ตามลำดับ มวลเฉลี่ย ปริมาตร และความจุความร้อนของโมลาร์ M คือมวลของก๊าซ n คือจำนวนกิโลโมลของก๊าซ V n - ปริมาตรของก๊าซภายใต้สภาวะปกติ
ปริมาตรของแก๊ส Vn สามารถหาได้ดังนี้ เมื่อเขียนสมการสถานะสำหรับเงื่อนไขที่กำหนด: pV = MRT และสำหรับเงื่อนไขปกติ: p n V n = MRT n เราระบุสมการที่สองกับสมการแรก:
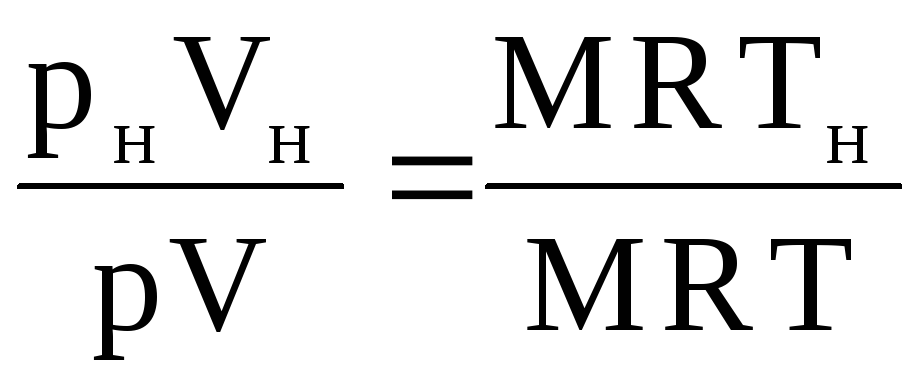 ,
,
จากที่นี่ 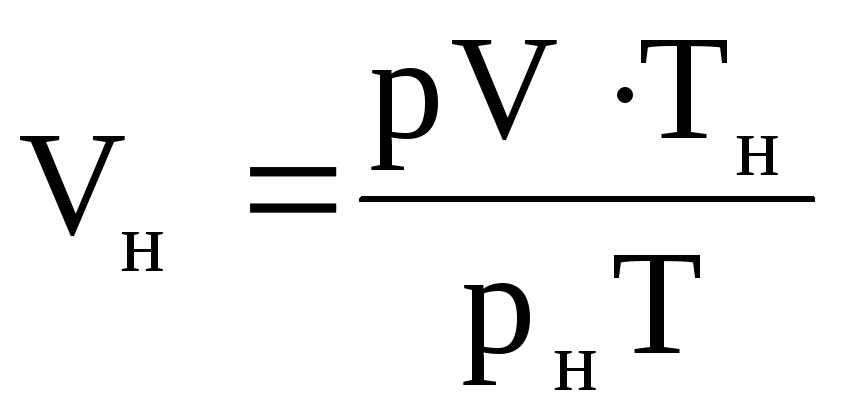 .
(1.39)
.
(1.39)
ความจุความร้อนของแก๊สผสม
สามารถคำนวณความจุความร้อนของส่วนผสมของก๊าซได้หากกำหนดองค์ประกอบของส่วนผสมและทราบความจุความร้อนของส่วนประกอบที่รวมอยู่ในส่วนผสม
ในการอุ่นส่วนผสมมวล M cm ขึ้น 1 K อุณหภูมิของส่วนประกอบแต่ละอย่างจะต้องเพิ่มขึ้น 1 K ด้วย ในเวลาเดียวกัน ปริมาณความร้อนเท่ากับ c i M i จะถูกใช้ในการให้ความร้อนแก่ส่วนประกอบ i-th ของส่วนผสมที่มีมวล М i . ปริมาณความร้อนสำหรับส่วนผสมทั้งหมด 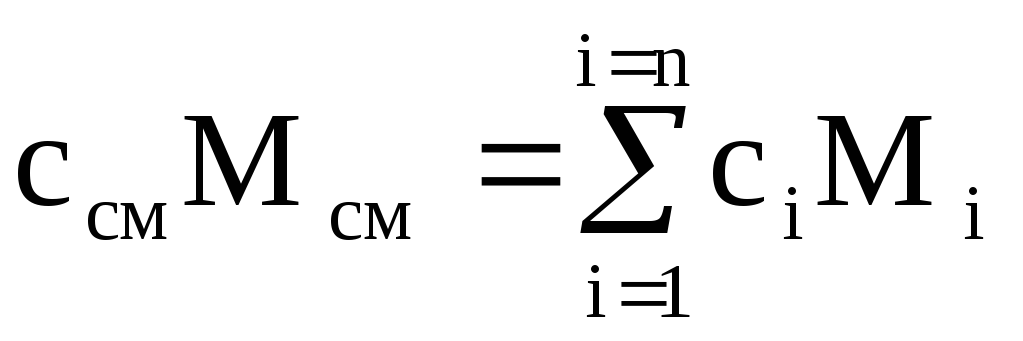 ,
,
โดยที่ c i และ c cm คือความจุความร้อนมวลของส่วนประกอบและของผสมที่ i
การหารนิพจน์สุดท้ายด้วย M cm เราได้สูตรการคำนวณสำหรับความจุมวลความร้อนของส่วนผสม:
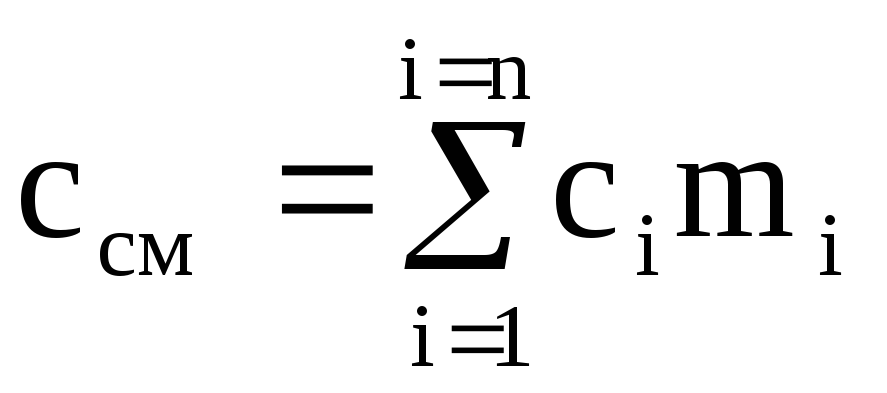 ,
(1.40)
,
(1.40)
โดยที่ m i คือเศษส่วนมวลขององค์ประกอบที่ i
ในทำนองเดียวกัน เราพบความจุความร้อนเชิงปริมาตร c ¢ cm และความจุความร้อนโมลาร์ c m cm ของส่วนผสม:
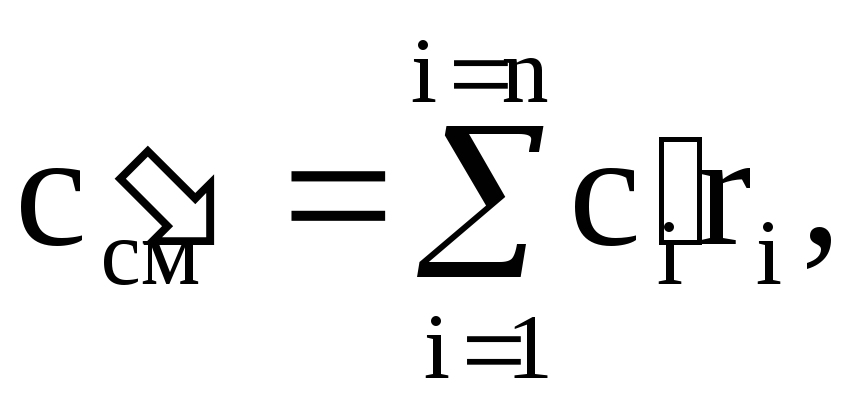 (1.41)
(1.41)
โดยที่ c ¢ i - ความจุความร้อนเชิงปริมาตรของส่วนประกอบ i-th, r i - เศษส่วนปริมาตรของส่วนประกอบ i-th
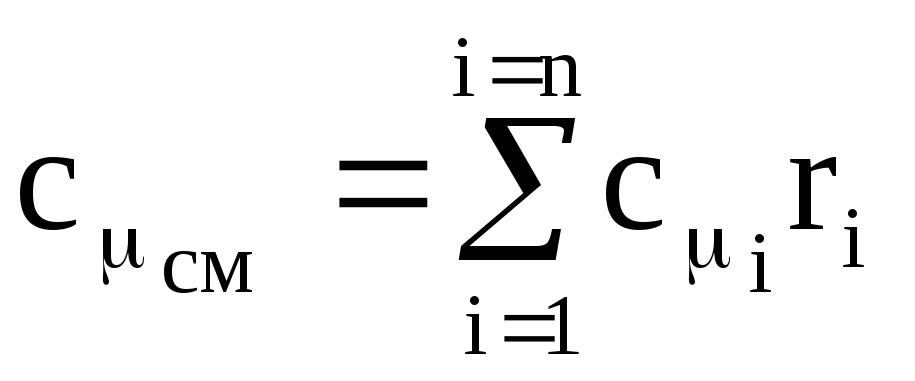 ,
(1.42)
,
(1.42)
โดยที่ c m i คือความจุความร้อนโมลาร์ของส่วนประกอบ i-th
r i - โมล (ปริมาตร) เศษส่วนขององค์ประกอบ i-th
งานจริง№ 2
หัวข้อ: ความจุความร้อน เอนทาลปี ส่วนผสมของก๊าซในอุดมคติ พลังงานภายใน งาน กระบวนการทางอุณหพลศาสตร์
วัตถุประสงค์ของงาน: การรวมความรู้ที่ได้รับระหว่างการฝึกอบรมเชิงทฤษฎีการได้มาซึ่งทักษะในการคำนวณทางวิศวกรรมความร้อน
ฉัน.คำจำกัดความพื้นฐาน สูตร และสมการ
1. ส่วนผสมของก๊าซในอุดมคติ
ส่วนผสมของแก๊สคือส่วนผสมเชิงกลของแก๊สหลายชนิดที่ไม่มีปฏิกิริยาทางเคมีซึ่งกันและกัน ก๊าซแต่ละชนิดในส่วนผสมเรียกว่าส่วนประกอบของก๊าซ ทำตัวราวกับว่าไม่มีก๊าซอื่นใดในส่วนผสม นั่นคือ กระจายอย่างสม่ำเสมอทั่วทั้งส่วนผสม ความดันที่เกิดจากก๊าซของส่วนผสมแต่ละชนิดบนผนังของภาชนะเรียกว่าความดันบางส่วน กฎพื้นฐานสำหรับส่วนผสมของก๊าซในอุดมคติคือกฎของดาลตัน ซึ่งความดันของส่วนผสมจะเท่ากับผลรวมของความดันบางส่วนของก๊าซที่ก่อตัวเป็นส่วนผสม:
2. พลังงานภายใน
พลังงานภายในร่างกายเป็นการรวมกันของพลังงานจลน์ของการเคลื่อนที่ของอนุภาคขนาดเล็กที่ประกอบกันเป็นร่างกายและพลังงานศักย์ของอนุภาคเหล่านั้น กำหนดปฏิสัมพันธ์ แรงดึงดูดหรือแรงผลักซึ่งกันและกัน เป็นไปไม่ได้ที่จะกำหนดค่าสัมบูรณ์ของพลังงานภายใน ดังนั้นในการคำนวณทางอุณหพลศาสตร์ จึงไม่ใช่ค่าสัมบูรณ์ของพลังงานภายในที่คำนวณได้ แต่เป็นการเปลี่ยนแปลง เช่น
![]() หรือ
หรือ ![]()
โดยที่ U 1 และ U 2 - พลังงานภายในของสถานะเริ่มต้นและสถานะสุดท้ายของของไหลทำงาน (แก๊ส)
คุณ 1 และ และ 2 - จังหวะ พลังงานภายในของสถานะเริ่มต้นและสถานะสุดท้ายของของไหลทำงาน
จากนี้ไปการเปลี่ยนแปลงของพลังงานภายในไม่ได้ขึ้นอยู่กับธรรมชาติและเส้นทางของกระบวนการ แต่ถูกกำหนดโดยสถานะของสารทำงานที่จุดเริ่มต้นและจุดสิ้นสุดของกระบวนการเปลี่ยนแปลง
คุณลักษณะของก๊าซในอุดมคติคือการไม่มีแรงอันตรกิริยาระหว่างโมเลกุลในนั้น และด้วยเหตุนี้จึงไม่มีพลังงานศักย์ภายใน กล่าวคือ U n \u003d 0 และ U „ \u003d 0 ดังนั้น พลังงานภายในของก๊าซในอุดมคติ:
U=U k =f(T) unu u=uk =f(T).
ฮ.งานแก๊ส.
ในอุณหพลศาสตร์ การเปลี่ยนแปลงสถานะของของไหลทำงานอันเป็นผลมาจากการแลกเปลี่ยนพลังงานกับ สิ่งแวดล้อมเรียกว่ากระบวนการ ในกรณีนี้พารามิเตอร์หลักของส่วนงานจะเปลี่ยนไป:
การเปลี่ยนแปลงของความร้อนเป็นงานเชิงกลนั้นเกี่ยวข้องกับกระบวนการเปลี่ยนสถานะของของไหลทำงาน กระบวนการเปลี่ยนสถานะของก๊าซอาจเป็นกระบวนการขยายและหดตัว สำหรับมวลโดยพลการของก๊าซ M (กก.) งานจะเท่ากับ:
L \u003d M l \u003d Mp (v 2 - v 1) \u003d, J
โดยที่ l \u003d p (v 2 -v 1) J / kg คืองานของก๊าซ 1 กิโลกรัมหรืองานเฉพาะ
4. ก๊าซเอนทาลปี
เอนทาลปีเป็นพารามิเตอร์ที่แสดงลักษณะพลังงานศักย์ของการเชื่อมต่อของไหลทำงาน (ก๊าซ) กับสิ่งแวดล้อม เอนทัลปีและเอนทัลปีเฉพาะ:
ฉัน \u003d U + pV, J และฉัน ฉัน \u003d และ + pv, J / kg
5. ความจุความร้อน
ความจุความร้อนจำเพาะคือปริมาณความร้อนที่ต้องจ่ายให้กับก๊าซ 1 กิโลกรัมเพื่อให้ความร้อน 1 ° C ในช่วงอุณหภูมิที่กำหนด
ความจุความร้อนจำเพาะคือมวล ปริมาตร และกิโลโมล มีการเชื่อมต่อระหว่างมวล C ปริมาตร C และความจุความร้อนกิโลโมล C:
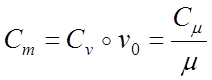 ;
; 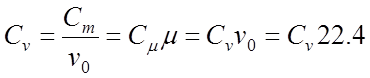
โดยที่ Vo 22.4 m 3 / kmol - เต้น ปริมาตรของก๊าซในสภาวะปกติ
มวลชน ความจุความร้อนของส่วนผสมของก๊าซ:
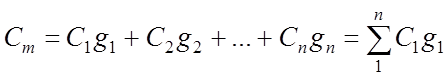
ความร้อนจำเพาะเชิงปริมาตรของส่วนผสมของก๊าซ:
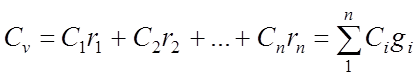
ความร้อนจำเพาะกิโลโมลาร์ของส่วนผสมของก๊าซ:
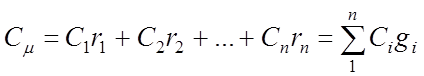
6. สมการสำหรับกำหนดปริมาณความร้อน
ปริมาณความร้อนที่ให้ออกหรือถูกดูดโดยของไหลทำงาน (แก๊ส) สามารถกำหนดได้จากสมการ:
Q \u003d M C m (t 2 -t 1), J หรือ Q \u003d VC (t-t), J โดยที่ M และ V คือน้ำหนักหรือปริมาตรของก๊าซ kg หรือ m 3
t u t - อุณหภูมิของก๊าซที่ส่วนท้ายและจุดเริ่มต้นของกระบวนการ° C;
C และ C - ค่าเฉลี่ยของมวลและปริมาตร ความจุความร้อนของก๊าซ
ที่ t cp \u003d J / kgK หรือ J / m 3 K
7. กฎข้อที่หนึ่งของอุณหพลศาสตร์
กฎหมายนี้พิจารณาถึงการเปลี่ยนแปลงของความร้อนและการทำงานเชิงกล ตามกฎหมายนี้ ความร้อนจะถูกแปลงเป็นงานเชิงกล และในทางกลับกัน งานเชิงกลเป็นความร้อนในปริมาณที่เท่ากันอย่างเคร่งครัด สมการสมมูลของความร้อนและงานมีรูปแบบดังนี้
โดยคำนึงถึงหลักการของความเท่าเทียมกันของความร้อนและการทำงาน สมการสมดุลความร้อนสำหรับมวลของก๊าซโดยพลการ:
Q \u003d U + L และ q \u003d u + l \u003d u -u + l
การแก้ปัญหาครั้งที่สอง
งาน #1 (#1)
อากาศแห้งในบรรยากาศมีองค์ประกอบมวลโดยประมาณดังต่อไปนี้: g 02 =23.2%, g N 2 =76.8%
กำหนดองค์ประกอบเชิงปริมาตรของอากาศ ค่าคงที่ของก๊าซ น้ำหนักโมเลกุลที่ปรากฏ ความดันบางส่วนของออกซิเจนและไนโตรเจน ถ้าอากาศมีค่า P = 101325 Pa โดยใช้บารอมิเตอร์
ฉันกำหนดองค์ประกอบปริมาตรของอากาศ:
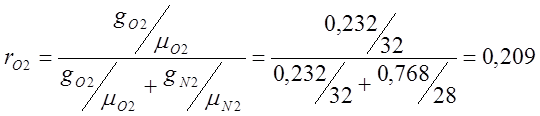 ;
;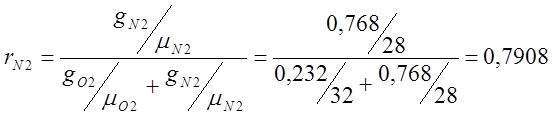 ;
;
โดยที่ r คือเศษส่วนมวล
m คือน้ำหนักโมเลกุลสัมพัทธ์
g คือเศษส่วนปริมาตร
ม. อากาศ. =m O2 r O2 +m N2 r N2 = 32 0.209 + 28 0.7908=6.688+22.14=28.83;
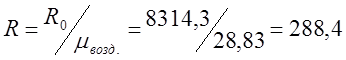
 ;
;
โดยที่ R 0 คือค่าคงที่ของแก๊ส
ฉันกำหนดความดันบางส่วนของก๊าซต่างๆ:
P O 2 \u003d P cm r O2 \u003d 101325 0.209 \u003d 21176.9 (Pa);
PN 2 \u003d P cm r N 2 \u003d 101325 0.7908 \u003d 80127.81 (ป่า);
โดยที่ P O 2 , P N 2 - ความดันบางส่วน
P cm คือความดันของส่วนผสม
งาน #2 (#2)
เรือแบ่งออกเป็น 2 ส่วนโดยปริมาตรคือ V 1 =1.5 ม. 3 และ V 2 =1.0 ม. 3 . ส่วนแรกของปริมาตร V 1 ประกอบด้วย CO 2 ที่ P 1 =0.5 MPa และ t 1 =30°C; ส่วนที่สองของปริมาตร V 2 ประกอบด้วย O 2 ที่ P 2 =0.2 MPa และ t 2 =57°C กำหนดมวลและปริมาตรเศษส่วนของ CO 2 และ O 2 น้ำหนักโมเลกุลที่ปรากฏของส่วนผสมและค่าคงที่ของก๊าซหลังจากถอดพาร์ติชั่นออกและกระบวนการผสมเสร็จสิ้น
ฉันกำหนดค่าคงที่ของก๊าซแต่ละตัว:
ในการทำเช่นนี้ ฉันจะกำหนดน้ำหนักโมเลกุลสัมพัทธ์: m (CO 2) \u003d 32 + 12 \u003d 44; ม.(อ2)=32;
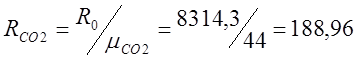
 ;
;
![]()
 ;
;
ตามสมการคุณลักษณะของ Klaiperon ฉันกำหนดมวลของก๊าซ:
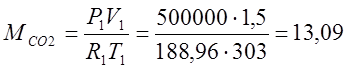 (กิโลกรัม);
(กิโลกรัม);
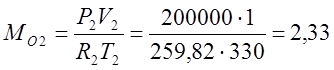 (กิโลกรัม);
(กิโลกรัม);
ฉันกำหนดเศษส่วนมวล:
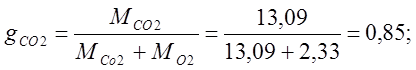
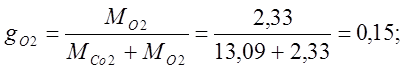
ฉันกำหนดเศษส่วนของปริมาตร:
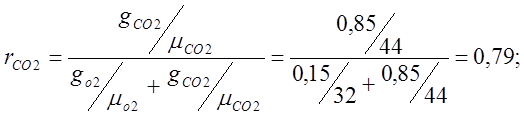
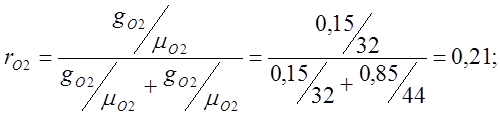
กำหนดน้ำหนักโมเลกุลของอากาศที่ชัดเจน:
ม. อากาศ. \u003d m O2 r O 2 + m CO2 r CO2 \u003d 32 0.21 + 44 0.79 \u003d 6.72 + 34.74 \u003d 41.48;
ฉันกำหนดค่าคงที่ของก๊าซแต่ละตัวสำหรับอากาศ (R):
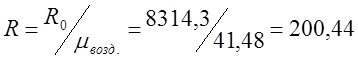
 ;
;
งาน #3 (#6)
ในภาชนะที่มีปริมาตร 300 ลิตรมีออกซิเจนที่ความดัน P 1 \u003d 0.2 MPa และ t 1 \u003d 20 0 C ต้องให้ความร้อนเท่าใดเพื่อให้อุณหภูมิของออกซิเจนเพิ่มขึ้นเป็น t 2 \u003d 300 0 C ? จะสร้างแรงกดดันอะไรในเรือ? ในการคำนวณ ให้ใช้ความร้อนจำเพาะเชิงปริมาตรเฉลี่ยของออกซิเจนที่ n.o. ค 02 \u003d 0.935 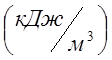
ตามกฎของ Charles ฉันกำหนดแรงกดดันสุดท้ายของกระบวนการ:
; 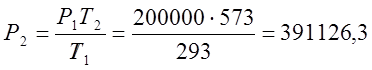 (ป่า);
(ป่า);
โดยที่ P, T คือพารามิเตอร์ของก๊าซ
ฉันกำหนดค่าคงที่ของก๊าซสำหรับออกซิเจน (R):
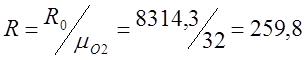
 ;
;
เนื่องจากกระบวนการเป็นแบบไอโซคอริก ฉันกำหนดปริมาณความร้อนที่ต้องป้อนตามสูตรที่เหมาะสม: Q v \u003d M C cv (T 2 -T 1) สำหรับสิ่งนี้ ตามสมการคุณลักษณะของ Claiperon ฉันกำหนดมวล ของแก๊ส
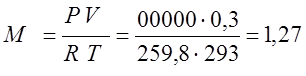 (กิโลกรัม); Q v \u003d MC cv (T 2 -T 1) \u003d 1.27 935 280 \u003d 332486 (J)
(กิโลกรัม); Q v \u003d MC cv (T 2 -T 1) \u003d 1.27 935 280 \u003d 332486 (J)
งาน #4 (#7)
ต้องใช้ความร้อนเท่าใดเพื่อให้ความร้อนแก่อากาศ 2 ม. 3 ที่แรงดันเกินคงที่ P เช่น \u003d 0.2 MPa จากอุณหภูมิ 100 0 C ถึงอุณหภูมิ 500 0 C อากาศจะทำงานอะไรในกรณีนี้ สำหรับการคำนวณ ใช้: ความดันบรรยากาศ P ที่ \u003d 0.1 MPa มวลความจุความร้อนไอโซบาริกเฉลี่ยของอากาศ C pm \u003d 1.022 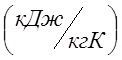 ; คำนวณค่าคงที่ของก๊าซโดยคำนึงถึงน้ำหนักโมเลกุลของอากาศ M อากาศ =29.
; คำนวณค่าคงที่ของก๊าซโดยคำนึงถึงน้ำหนักโมเลกุลของอากาศ M อากาศ =29.
ฉันกำหนดค่าคงที่ของก๊าซแต่ละตัวสำหรับอากาศ:
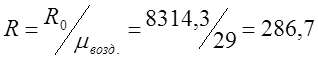
 ;
;
ความดันสัมบูรณ์เท่ากับผลรวมของส่วนเกินและบรรยากาศ P=P est + พี ที่. =0.1+0.2=0.3 เมกะปาสคาล
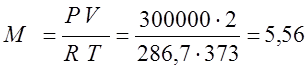 (กิโลกรัม);
(กิโลกรัม);
เนื่องจากกระบวนการนี้เป็นไอโซบาริก ฉันกำหนด Q และ L ตามสูตรที่เกี่ยวข้อง:
ตามกฎหมายเกย์-ลูสแซก ฉันกำหนดปริมาตรสุดท้าย:
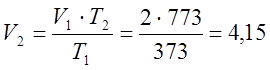 ม.3;
ม.3;
Q \u003d M C น. (T 2 -T 1) \u003d 5.56 1022 400 \u003d 2272928 (J);
L \u003d P (V 2 -V 1) \u003d 300000 2.15 \u003d 645000 (J)
งาน #5 (#8)
มีอากาศอยู่ในกระบอกสูบที่ความดัน P=0.5 MPa และอุณหภูมิ t 1 =400 0 C ความร้อนถูกกำจัดออกจากอากาศที่ P=const ดังนั้นเมื่อสิ้นสุดกระบวนการ อุณหภูมิ t 2 =0 0 C คือ ชุด ปริมาตรของกระบอกสูบที่อากาศ V 1 \u003d 400l
กำหนดปริมาณความร้อนที่ถูกกำจัด ปริมาตรสุดท้าย การเปลี่ยนแปลงของพลังงานภายใน และการทำงานที่สมบูรณ์แบบของการบีบอัด C pm =1.028 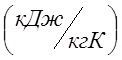 .
.
เนื่องจากกระบวนการนี้เป็น isobaric ดังนั้นตามกฎหมายของ Gay-Lussac ฉันจึงกำหนดปริมาตรสุดท้าย:
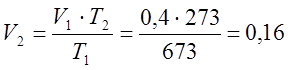 ม.3;
ม.3;
ตามสมการคุณลักษณะของ Klaiperon ฉันกำหนดมวลของก๊าซ:
จากโจทย์ที่แล้ว R=286.7 
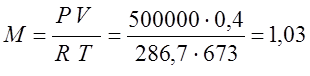 (กิโลกรัม);
(กิโลกรัม);
ฉันกำหนดปริมาณความร้อนที่ปล่อยออกมา:
Q=M C pm (T 2 -T 1)=1.03 1028 (273-673)=-423536 (J);
ฉันกำหนดปริมาณงานที่ใช้ไป:
L=P (V 2 -V 1)= 500,000 (0.16-0.4)=-120,000 (J);
จากสมการที่กำหนดจำนวนทั้งหมดฉันกำหนดการเปลี่ยนแปลงของปริมาณพลังงานภายใน:
![]() ; (เจ)
; (เจ)
ปัญหา #6 (#9)
อากาศที่มีปริมาตร V 1 =0.02 m3 ที่ความดัน P 1 =1.1 MPa และ t 1 =25 s จะขยายตัวในกระบอกสูบด้วยลูกสูบที่เคลื่อนที่ได้จนถึงความดัน P 2 =0.11 MPa ค้นหาปริมาตรสุดท้าย V 2 อุณหภูมิสุดท้าย t 2 งานที่อากาศทำ และความร้อนที่จ่าย ถ้าเกิดการขยายตัวในกระบอกสูบ:
ก) อุณหภูมิคงที่
b) แบบอะเดียแบติกด้วยเลขชี้กำลังแบบอะเดียแบติก k=1.4
c) โพลีทรอปิกที่มีดัชนีโพลีทรอปิก n=1.3
กระบวนการไอโซเทอร์มอล:
ป 1 / ป 2 \u003d V 2 / V 1
V 2 \u003d 0.02 1.1 / 0.11 \u003d 0.2M 3
Q=L=RMT 1 Ln(V 2 /V 1)=P 1 V 1 Ln(V 2 /V 1)=1.1 10 6 0.02Ln(0.2/0.02)=22000 J
กระบวนการอะเดียแบติก:
V 1 / V 2 \u003d (P 2 / P 1) 1 / k
V 2 \u003d V 1 / (P 2 / P 1) 1 / k \u003d 0.02 / (0.11 / 1.1) 1 / 1.4 \u003d 0.1036M 3
T 2 /T 1 \u003d (P 2 /P 1) k-1 / k
T 2 \u003d (P 2 / P 1) k-1 / k T 1 \u003d (0.11 / 1.1) 1.4-1 / 1.4 298 \u003d 20.32k
C v \u003d 727.4 J / kg k
L \u003d 1 / k-1 (P 1 V 1 -P 2 V 2) \u003d (1 / 1.4-1) (1.1 10 6 0.02 -0.11 10 6 0, 1)=2.0275 10 6 J
กระบวนการโพลีโทรปิก:
V 1 / V 2 \u003d (P 2 / P 1) 1 / น
V 2 \u003d V 1 / (P 2 / P 1) 1 / n \u003d 0.02 / (0.11 / 1.1) 1 / 1.3 \u003d 0.118M 3
T 2 /T 1 \u003d (P 2 /P 1) n-1 / n
T 2 \u003d (P 2 / P 1) n-1 / n T 1 \u003d (0.11 / 1.1) 1.3-1 / 1.3 298 \u003d 175k
L \u003d 1 / n-1 (P 1 V 1 -P 2 V 2) \u003d (1 / (1.3-1)) (1.1 10 6 0.02 -0.11 10 6 0.118)=30000J
Q=(k-n/k-1) l M=((1.4-1.3)/(1.4-1)) 30000=7500J
วรรณกรรม:
1. พลังงาน มอสโก 2518
2. Litvin A.M. "รากฐานทางทฤษฎีของวิศวกรรมความร้อน", สำนักพิมพ์ "พลังงาน", มอสโก, 2512
3. Tugunov P.I. , Samsonov A.A. , “ความรู้พื้นฐานของวิศวกรรมความร้อน เครื่องยนต์ความร้อน และโรงไฟฟ้าพลังไอน้ำ” สำนักพิมพ์ Nedra กรุงมอสโก ปี 1970
4. Krutov V.I. , "วิศวกรรมความร้อน" สำนักพิมพ์ "วิศวกรรม" มอสโก 2529
งานปฏิบัติหมายเลข 1
ธีม: ก๊าซในอุดมคติและ ส่วนผสมของแก๊ส. ความจุความร้อนของก๊าซ
เป้า: ให้แนวคิดแก่นักเรียนเกี่ยวกับส่วนผสมของแก๊สและแก๊สในอุดมคติ ตลอดจนความจุความร้อนของแก๊ส
ข้อมูลทางทฤษฎีโดยย่อ
เมื่อคำนวณก๊าซในอุดมคติและส่วนผสมของก๊าซ ตลอดจนความจุความร้อนของก๊าซ จำเป็นต้องรู้และใช้สูตรต่อไปนี้:
สมการสถานะของก๊าซในอุดมคติ:
– สำหรับแก๊ส 1 กก
, (1.1)
- สำหรับ มกิโลกรัมของก๊าซ
, (1.2)
- สำหรับแก๊ส 1 โมล
, (1.3)
ปริมาตรโมลาร์อยู่ที่ไหน ม 3 /โมล; คือค่าคงที่ของก๊าซสากล (โมลาร์) J/(โมล K)
ค่าคงที่ของก๊าซสากล = 8.314 J/(mol. ถึง).
ค่าคงที่ของก๊าซเฉพาะ J/(kg K)
, (1.4)
มวลโมลาร์อยู่ที่ไหน กก./โมล
, (1.4a)
น้ำหนักโมเลกุลสัมพัทธ์ของสารอยู่ที่ไหน
อุณหภูมิอุณหพลศาสตร์, K,
, (1.5)
อุณหภูมิอยู่ที่ไหนในองศาเซลเซียส 0 ค.
เป็นเรื่องปกติที่จะนำปริมาตรของก๊าซไปสู่สภาวะปกติซึ่งความดันก๊าซ \u003d 101.3 kPa และอุณหภูมิ \u003d 0 0 ค.
ความดันส่วนผสมของแก๊ส
, (1.6)
ความดันบางส่วนของส่วนประกอบอยู่ที่ไหน
สำหรับส่วนผสมของแก๊ส
, (1.7)
มวลของส่วนประกอบอยู่ที่ไหน
, (1.7a)
โดยที่ปริมาตรบางส่วน (ลดลง) ของส่วนประกอบ ม 3 .
ความหนาแน่นของส่วนผสมของแก๊ส
, (1.8)
ส่วนปริมาตรของส่วนประกอบอยู่ที่ไหน คือความหนาแน่นของส่วนประกอบนี้ kg/m 3 ;
, (1.8a)
เศษส่วนมวลของส่วนประกอบอยู่ที่ไหน
มวลโมลาร์ที่เห็นได้ชัดของของผสมของก๊าซในอุดมคติ
, (1.9)
มวลโมลาร์ของส่วนประกอบอยู่ที่ไหน
. (1.9a)
อัตราส่วนระหว่างเศษส่วนของมวลและปริมาตร
. (1.10)
ความดันบางส่วนของส่วนประกอบ
. (1.11)
ความจุความร้อนกำหนดปริมาณความร้อนที่ต้องป้อนให้กับร่างกาย (ไปยังระบบ) เพื่อเพิ่มอุณหภูมิ 1 0 C (ต่อ 1 K)
มีความสัมพันธ์เชิงหน้าที่ระหว่างความจุความร้อนเหล่านี้
. (1.12)
สิ่งที่สำคัญเป็นพิเศษในการคำนวณทางความร้อนคือความจุความร้อนของก๊าซในกระบวนการที่ความดันคงที่และปริมาตรคงที่ - ความจุความร้อนแบบไอโซบาริกและไอโซคอริก ตามลำดับ พวกมันเชื่อมโยงกันด้วยสมการเมเยอร์:
– สำหรับแก๊ส 1 กก
, (1.13)
ที่ไหนและคือความจุความร้อนจำเพาะของไอโซบาริกและไอโซโคริก
– ต่อแก๊ส 1 โมล
, (1.13ก)
ที่ไหนและคือความจุความร้อนของโมลาร์ไอโซบาริกและไอโซโคริก
อัตราส่วนของความจุความร้อนเหล่านี้เรียกว่าเลขชี้กำลังอะเดียแบติก
. (1.14)
ความจุความร้อนเฉลี่ยในช่วงอุณหภูมิตั้งแต่ ถึง มักจะคำนวณเป็น
, (1.15)
ที่ไหนและคือความจุความร้อนเฉลี่ยในช่วงอุณหภูมิตั้งแต่ 0 ถึง 0 Сและจาก 0 ถึง 0 С
ความจุความร้อนของส่วนผสมของก๊าซ:
- เฉพาะเจาะจง
, (1.16)
ที่ไหน - ความจุความร้อนจำเพาะส่วนประกอบ;
– ปริมาตร
, (1.16a)
ที่ไหน คือความจุความร้อนเชิงปริมาตรของส่วนประกอบ
– ฟันกราม
, (1.16ข)
ความจุความร้อนโมลาร์ของส่วนประกอบอยู่ที่ไหน
หลักเกณฑ์เพื่อแก้ปัญหา
งานหมายเลข 1
คอมเพรสเซอร์สูบลมในปริมาณ 4 ม 3 /นาทีที่ 17 0 C และความดัน 100 kPa ลงในถังที่มีปริมาตร 10 m 3 . นานแค่ไหนที่ความดันในถังจะเพิ่มขึ้นจาก 0.1 เป็น 0.9 MPa เมื่อคำนวณให้ถือว่าอุณหภูมิอากาศในถังไม่เปลี่ยนแปลงและเท่ากับ 17 0 ค.
การตัดสินใจ
มวลของอากาศในถังที่จุดเริ่มต้นของการทำงานของคอมเพรสเซอร์ตามสูตร (1.2)
กิโลกรัม,
ที่ได้รับการยอมรับ:
287 กิโลจูล/(กก. K) - ค่าคงที่ของก๊าซเฉพาะของอากาศ (ภาคผนวก B);
17 + 273.15 = 290.15 K - ตามสมการ (1.5)
มวลของอากาศในถังเมื่อถึงความดันสุดท้าย = 0.9 MPa ตามสูตร (1.2)
กิโลกรัม.
ความหนาแน่นของอากาศที่พารามิเตอร์เริ่มต้นตามการพึ่งพา (1.1)
กก. / ลบ.ม.
ตามเงื่อนไขของปัญหา กำหนดปริมาณการไหลของคอมเพรสเซอร์ = 4 ม 3 /นาที จำเป็นต้องกำหนดอัตราป้อนมวลของมัน
กก./นาที
เวลาทำงานของคอมเพรสเซอร์เมื่ออากาศถูกดันเข้าไปในถัง
นาที
ตอบ: ใน 20 นาที ความดันในถังจะเพิ่มขึ้นจาก 0.1 เป็น 0.9 MPa
งานหมายเลข 2
กำหนดความจุความร้อนจำเพาะและปริมาตรของอากาศในกระบวนการที่ความดันและปริมาตรคงที่ โดยสมมติว่าความจุความร้อนคงที่ ความหนาแน่นของอากาศภายใต้สภาวะปกติ = 1.29 กก./ม 3 .
การตัดสินใจ
เราเขียนน้ำหนักโมเลกุลสัมพัทธ์ของอากาศ = 28.96 (ภาคผนวก B) และค่าของความจุความร้อนโมลสำหรับก๊าซไดอะตอม = 29.1 J / (โมล. K) และ \u003d 20.8 J / (โมล K) (ภาคผนวก B).
ตามสูตร (1.4a) กำหนด:
– มวลโมลาร์ของอากาศ
กก./โมล
คำนวณตามสูตร (1.12):
– ความร้อนจำเพาะไอโซบาริก
J / (กก. K) \u003d 1.005 kJ / (กก. K)
– ความจุความร้อนเชิงปริมาตรไอโซบาริก
kJ / (ม. 3. K),
– ความร้อนเฉพาะไอโซโคริก
J / (กก. K) \u003d 0.718 kJ / (กก. ถึง),
– ความจุความร้อนเชิงปริมาตรไอโซโคริก
kJ / (ม. 3. K).
ตอบ: ความจุความร้อนจำเพาะ 0.718 กิโลจูล/(กก . K) และความจุความร้อนเชิงปริมาตรคือ 0.926 kJ / (m๓.เค).
งานสำหรับ การตัดสินใจที่เป็นอิสระ
งานหมายเลข 1
ค้นหาความหนาแน่นของคาร์บอนไดออกไซด์ภายใต้สภาวะปกติ
งานหมายเลข 2
ปริมาตรของไนโตรเจน 100 กก. ที่ 70 คืออะไร 0 C และความดัน 0.2 MPa?
งานหมายเลข 3
กำหนดมวลของอากาศในหอประชุมที่มีพื้นที่ 120 ม 2 และความสูง 3.5 ม. อุณหภูมิอากาศในผู้ชมคือ 18 0 C และความดันบรรยากาศคือ 100 kPa
งานหมายเลข 4
กำหนดจำนวนอะตอมในโมเลกุลออกซิเจนหากมีปริมาตร 10 ลิตรที่อุณหภูมิ 30 0 C และความดัน 0.5 MPa มีออกซิเจน 63.5 กรัม
งานหมายเลข 5
ในถังที่มีความจุ 8 ม 3 มีอากาศที่ความดัน 10 MPa และที่อุณหภูมิ 27 0 C. หลังจากใช้อากาศบางส่วนจนหมด ความดันลดลงเหลือ 5 MPa และอุณหภูมิเหลือ 20 0 ค. หามวลอากาศที่ใช้.
งาน #6
คอมเพรสเซอร์ปั๊มแก๊สลงในถังขนาด 10 ม 3 . ในกรณีนี้ ความดันในอ่างเก็บน้ำเพิ่มขึ้นจาก 0.2 เป็น 0.7 MPa ที่อุณหภูมิก๊าซคงที่ 20 0 C. กำหนดเวลาการทำงานของคอมเพรสเซอร์หากจ่ายไฟ 180 ม 3 /ชม ฟีดถูกกำหนดภายใต้สภาวะปกติ
งานหมายเลข 7
คอมเพรสเซอร์สูบอากาศเข้าไปในถังขนาด 7 ม 3 ในขณะที่ความดันในถังเพิ่มขึ้นจาก 0.1 เป็น 0.6 MPa อุณหภูมิยังเพิ่มขึ้นจาก 15 เป็น 50 0 C. กำหนดเวลาทำงานของคอมเพรสเซอร์หากอัตราการไหลอยู่ที่ 30 ม 3 /h สัมพันธ์กับสภาวะปกติ: 0.1 MPa และ 0 0 ค.
งานหมายเลข 8
ในการกำหนดความร้อนของการเผาไหม้เชื้อเพลิงจะใช้ระเบิดความร้อนขนาด 0.4 ลิตรที่เต็มไปด้วยออกซิเจน ในระหว่างการชาร์จ แรงดันออกซิเจนในระเบิดจะถึง 2.2 MPa ออกซิเจนมาจากถังขนาด 6 ลิตร จะมีประจุออกซิเจนเพียงพอในกระบอกสูบเท่าใดหากความดันเริ่มต้นคือ 12 MPa เมื่อคำนวณให้ใช้อุณหภูมิของออกซิเจนทั้งในกระบอกสูบและขณะชาร์จระเบิดเท่ากับ 20 0 ค.
งานหมายเลข 9
การสตาร์ทเครื่องยนต์ที่อยู่กับที่จะดำเนินการโดยใช้อากาศอัดจากกระบอกสูบขนาด 40 ลิตร ใช้อากาศ 0.1 ลบ.ม. ต่อการสตาร์ท 1 ครั้ง 3 กำหนดภายใต้สภาวะปกติ กำหนดจำนวนเครื่องยนต์ที่สตาร์ทหากความดันในกระบอกสูบลดลงจาก 2.5 เป็น 1 MPa ใช้อุณหภูมิของอากาศเท่ากับ 10 0 ค.
งานหมายเลข 10
ผลิตภัณฑ์ที่เป็นก๊าซจากการเผาไหม้เชื้อเพลิงจะถูกทำให้เย็นลงในกระบวนการไอโซบาริกจากอุณหภูมิหนึ่งไปอีกอุณหภูมิหนึ่ง องค์ประกอบของก๊าซจะได้รับในส่วนปริมาตร: , และ จงหาปริมาณความร้อนที่ปล่อยออกมา 1 เมตร 3 ผลิตภัณฑ์การเผาไหม้ ปริมาณถูกกำหนดภายใต้สภาวะปกติ
นำข้อมูลเริ่มต้นตามตาราง 1.1 ขึ้นอยู่กับรหัส (หมายเลขตัวเลือก) การคำนวณดำเนินการโดยใช้ความจุความร้อนเฉลี่ย
ตารางที่ 1.1. ข้อมูลเบื้องต้น
ควบคุมคำถาม
1. ให้คำจำกัดความของก๊าซในอุดมคติและระบุความแตกต่างจากก๊าซจริง
2. อะไรคือความแตกต่างระหว่างค่าคงที่ของก๊าซและค่าคงที่ของก๊าซสากล?
3. ความดันบางส่วนของก๊าซในส่วนผสมเรียกว่าอะไร มีอยู่จริงหรือไม่ และกำหนดได้อย่างไร
4. อะไรเรียกว่าปริมาตรบางส่วนของก๊าซในสารผสม มีอยู่จริงหรือไม่ และจะกำหนดได้อย่างไร
5. จะทราบสัดส่วนปริมาตรของก๊าซในของผสมได้อย่างไรหากทราบสัดส่วนของมวล
6. ลักษณะใดของก๊าซในอุดมคติที่กำหนดค่าตัวเลขของความจุความร้อนของไอโซบาริกและไอโซคอริกเฉพาะของโมลาร์
ส่งงานที่ดีของคุณในฐานความรู้เป็นเรื่องง่าย ใช้แบบฟอร์มด้านล่าง
นักศึกษา บัณฑิต นักวิทยาศาสตร์รุ่นเยาว์ที่ใช้ฐานความรู้ในการศึกษาและการทำงานจะขอบคุณมาก
โฮสต์ที่ http://www.allbest.ru/
กระทรวงศึกษาธิการและวิทยาศาสตร์แห่งสหพันธรัฐรัสเซีย
สถาบันการศึกษางบประมาณของรัฐบาลกลาง
อุดมศึกษา
มหาวิทยาลัยเทคนิคแห่งรัฐวอลโกกราด
คณะภาคค่ำคิรอฟ
ภาคการศึกษาเกี่ยวกับระเบียบวินัย:
วิศวกรรมความร้อน
ในหัวข้อ:
เชื้อเพลิง ก๊าซผสม และความจุความร้อน
เสร็จสิ้นโดย: นักเรียน gr.TVB-385
เชลุดเชนโก บี.ดี.
ตรวจสอบโดย: รศ. Goryunov V.A.
โวลโกกราด 2015
เงื่อนไข
ตัวออกซิไดเซอร์อุณหภูมิการเผาไหม้เชื้อเพลิง
ในเตาอุตสาหกรรม เชื้อเพลิง (เอธานอล) จะถูกเผาด้วยแรงดันคงที่ อากาศถูกใช้เป็นสารออกซิแดนท์ที่อุณหภูมิ ต 1 =660K. ค่าสัมประสิทธิ์ของอากาศส่วนเกินจะได้รับ: a= 1.0 และค่าสัมประสิทธิ์ความสมบูรณ์ของการเผาไหม้เชื้อเพลิง w=0.9 กำหนดค่าทางทฤษฎีของอุณหภูมิการเผาไหม้สูงสุด Tg ไม่สนใจความร้อนที่เกิดจากเชื้อเพลิง
แท็บ หมายเลข 1 องค์ประกอบและค่าความร้อนของเชื้อเพลิง
แท็บ หมายเลข 2 สูตรสำหรับความจุความร้อนของมวลไอโซโคริกเฉลี่ย (c v)
|
ความจุความร้อน kJ/kg*K |
|||
|
0.691 + 7.1 * 10 - 5 ต |
|||
|
0.775 + 11.7 * 10 -5 ต |
|||
|
1.328+28.07*10 -5 ต |
|||
|
0.716 + 7.54 * 10 -5 ต |
|||
|
0.628 + 6.75 * 10 -5 ต |
แท็บ หมายเลข 3 ผลการคำนวณ
อุณหภูมิการเผาไหม้สูงสุดตามทฤษฎีหาได้จากสมการสมดุลความร้อน :
zhQ H +Q o \u003d Q p.sg
ที่ไหน: Q o - ความร้อนที่ตัวออกซิไดเซอร์นำมาใช้
Qh - ค่าความร้อนสุทธิของเชื้อเพลิง
g - ค่าสัมประสิทธิ์ความสมบูรณ์ของการเผาไหม้เชื้อเพลิง
ถาม Cr- ความร้อนที่ได้รับจากการเผาไหม้
เราพบความร้อนที่ปล่อยออกมาระหว่างการเผาไหม้เชื้อเพลิง (lQ h)
จากตารางที่ 2 ค่าของ Q h จะถูกนำมา:
Q ชั่วโมง \u003d 27100 kJ / kg
จากตารางที่ 1 ค่าของ w จะถูกนำมาใช้ (ในเวอร์ชันของฉัน w = 0.9)
และ*Q H \u003d 0.9 * 27100 \u003d 24390 kJ / kg
ค้นหาความร้อนที่เกิดจากตัวออกซิไดซ์:
ถาม o \u003d C หน้า อากาศ *m อากาศ* T 1
เรากำหนดความจุความร้อนมวลไอโซโคริกเฉลี่ยของอากาศตามสูตรที่กำหนดในตารางที่ 2
c v air \u003d 0.691 + 7.1 * 10 -5 * 660 \u003d 0.73786 kJ / kg * K
เราคำนวณความจุความร้อนมวลไอโซบาริกเฉลี่ยโดยใช้สูตร Mayer:
Av air \u003d cv air +R \u003d 0.73786 + 0.287 \u003d 1.02486 kJ / kg * K
เรากำหนดมวลอากาศที่จำเป็นทางทฤษฎี:
m อากาศ \u003d 2.67 * C p + 8H p - O p / 0.23 \u003d (2.67 * 0.52 + 8 * 0.13-0.35) / 0.23 \u003d (1.3884 + 1 .04-0.35)/0.23=2.0784/0.23=9.0365 กก./กก
กำหนดมวลที่แท้จริงของอากาศ:
ม. อากาศ \u003d a * ม. อากาศ \u003d 1.0 * 9.0365 \u003d 9.0365 Kg / Kg
กำหนด Q o:
ถาม o \u003d C หน้า อากาศ * ม. อากาศ * T 1 \u003d 1.02486 * 9.0365 * 660 \u003d 6112.36 kJ / kg
เราคำนวณความร้อนที่เกิดจากตัวออกซิไดเซอร์และเชื้อเพลิงที่เผาไหม้:
zhQ H +Q o \u003d 24390 + 6112.36 \u003d 30502.36 kJ / kg
เราพบความร้อนของผลิตภัณฑ์จากการเผาไหม้ (Qn.Сг):
ถาม n Cr \u003d CR, p. sg * m p, sg * T 2.
ก) กำหนดมวลของผลิตภัณฑ์การเผาไหม้:
m p, sg \u003d 1 + m อากาศ \u003d 1 + 9.0365 \u003d 10.0365
b) เราคำนวณเศษส่วนมวลของส่วนประกอบในผลิตภัณฑ์การเผาไหม้:
g co 2 \u003d m co 2 / m p, sg \u003d 3.67 * C P / m p, sg \u003d 3.67 * 0.52 / 10.0365 \u003d 0.1901
g H 2 o \u003d m H 2 o / m p, sg \u003d 9 * H p / m p, sg \u003d 9 * 0.13 / 10.0365 \u003d 0.1166
g o2 \u003d m o2 / m p, sg \u003d 0.23 * (a-1) * m o air / m p, sg \u003d 0.23 * (1.0-1) * 9.0365 / 10.0365 \u003d 0
g N2 \u003d m N2 / m p, sg \u003d 0.77 * a * m o อากาศ / m p, sg \u003d 0.77 * 1.0 * 9.0365 / 10.0365 \u003d \u003d 0.693
ค) ค้นหาความจุมวลความร้อนไอโซบาริกเฉลี่ยของผลิตภัณฑ์การเผาไหม้โดยใช้สูตร:
C P, p. sg \u003d g (co 2) * C p (co 2) + g (H 2 o) * C p (H 2 O) + g (o 2) * C p (O 2) + g ( N 2) * C p (N 2) \u003d
เราพบความจุความร้อน isobaric ของส่วนประกอบของผลิตภัณฑ์การเผาไหม้:
ก) cv (co 2) \u003d 0.775 + 11.7 * 10 -5 * T 2
ข) cv (H2 o) \u003d 1.328 + 28.07 * 10 -5 * T 2
ค) cv (O 2) \u003d 0.628 + 6.75 * 10 -5 * T 2
ง) cv (N 2) \u003d 0.716 + 7.54 * 10 -5 * T 2
เมื่อใช้สูตรของ Mayer เราจะพบกับ p :
1. C p (co 2) \u003d c v (co 2) + R \u003d 0.775 + 11.7 * 10 -5 * T 2 +0.189 \u003d 0.964 + 11.7 * 10 -5 * T 2
2. C p (H2O) \u003d c v (H2 o) + R \u003d 1.328 + 28.07 * 10 -5 * T 2 +0.462 \u003d 1.79 + 28.07 * 10 -5 * T 2
3. C p (O 2) \u003d c v (O 2) + R \u003d 0.628 + 6.75 * 10 -5 * T 2 + 0.260 \u003d 0.888 + 6.75 * 10 -5 * T 2
4. C p (N 2) \u003d c v (N 2) + R \u003d 0.716 + 7.54 * 10 -5 * T 2 + 0.297 \u003d 1.013 + 7.54 * 10 -5 * T 2
ดังนั้นเราจึงพบความจุความร้อนมวลไอโซบาริกเฉลี่ยของผลิตภัณฑ์การเผาไหม้ตามสูตร:
C P, p. sg \u003d g (co 2) * C p (co 2) + g (H 2 o) * C p (H 2 O) + g (o 2) * C p (O 2) + g ( N 2) * C p (N 2) \u003d 0.1901 * (0.964 + 11.7 * 10 -5 * T 2) + 0.1166 * (1.79 + 28.07 * 10 -5 * T 2) + 0 * (0.888 + 6.75 * 10 - 5 * T 2) + 0.693 * (1.013 + 7.54 * 10 -5 * T 2) \u003d 0.1832 + 2.2242 * 10 -5 * T 2 + 0.2087 + 3.2729 * 10 -5 * T 2 +0 + 0.702 + 5.2252 * 10 -5 * T 2 = 1.0939 + 10.7223 * 10 -5 * T 2 = 1.0939 + 10.7223 * 10 -5 * 3934.89 = = 1.516
ค้นหาความร้อนของผลิตภัณฑ์จากการเผาไหม้ Q n . เอสจี:
ถาม n Cr \u003d C R, p.sg * m p, sg * T 2 \u003d (1.0939 + 10.7223 * 10 -5 * T 2) * 10.0365 * T 2
ใช้สมการสมดุลความร้อนกำหนดอุณหภูมิการเผาไหม้ตามทฤษฎีสูงสุด (T 2):
และถาม ชม.= ถาม น . เอสจี
24390=(1.0939+10.7223*10 -5 *T 2) *10.0365*T 2 ตัดทั้งสองข้างด้วย 10.0365:
10.7223*10 -5 *(ท 2) 2 +1.09369*ท 2 - 2430.13=0
1.09369 + 1.495/0.000214=1875 เคลวิน
โฮสต์บน Allbest.ru
เอกสารที่คล้ายกัน
การหามวล ปริมาตร และความจุความร้อนโมลาร์ของแก๊สผสม การคำนวณค่าสัมประสิทธิ์การพาความร้อนและการพาความร้อน การไหลของความร้อนจากท่อแอร์เข้าโรงรถ การคำนวณตามสูตร D.I. Mendeleev ของค่าความร้อนต่ำสุดและสูงสุดของน้ำมันเชื้อเพลิง
ทดสอบเพิ่ม 01/11/2015
ส่วนผสมของแก๊ส ความจุความร้อน การคำนวณโมลาร์เฉลี่ยและความจุความร้อนจำเพาะ รอบเครื่องยนต์เบื้องต้น สันดาปภายใน. ค่าสัมประสิทธิ์ความร้อน การกระทำที่เป็นประโยชน์รอบดีเซล ไอน้ำ โรงไฟฟ้าพลังไอน้ำ. แนวคิดทั่วไปของวัฏจักรแรงคิน
ภาคนิพนธ์ เพิ่ม 11/01/2555
ความร้อนจำเพาะ- อัตราส่วนของความร้อนที่ได้รับจากหน่วยปริมาณของสารต่อการเปลี่ยนแปลงของอุณหภูมิ ปริมาณความร้อนขึ้นอยู่กับลักษณะของกระบวนการและความจุความร้อน - ตามเงื่อนไขของหลักสูตร กระบวนการทางอุณหพลศาสตร์กับก๊าซในอุดมคติ
บทคัดย่อ เพิ่ม 01/25/2009
การกำหนดค่าความร้อนสำหรับเชื้อเพลิงก๊าซเป็นผลรวมของผลิตภัณฑ์จากผลกระทบทางความร้อนของส่วนประกอบของก๊าซที่ติดไฟตามปริมาณ การไหลของอากาศที่จำเป็นในทางทฤษฎีสำหรับการเผาไหม้ก๊าซธรรมชาติ การกำหนดปริมาตรของผลิตภัณฑ์การเผาไหม้
ทดสอบเพิ่ม 11/17/2010
มวลโมลาร์และความจุความร้อนมวลของส่วนผสมของก๊าซ กระบวนการสถานะอะเดียแบติก พารามิเตอร์ของร่างกายการทำงานที่จุดของวงจร อิทธิพลของอัตราส่วนการอัด การเพิ่มความดัน และการขยายตัวของไอโซบาริกที่มีต่อประสิทธิภาพทางความร้อนของวัฏจักร กระบวนการกำจัดความร้อนตามไอโซชอร์
ภาคนิพนธ์ เพิ่ม 03/07/2010
การกำหนดการไหลของอากาศและปริมาณของผลิตภัณฑ์การเผาไหม้ การคำนวณองค์ประกอบของฝุ่นถ่านหินและค่าสัมประสิทธิ์ของอากาศส่วนเกินระหว่างการเผาอะลูมิเนียมในเตาเผาแบบหมุน ใช้สูตรกึ่งเชิงประจักษ์ของ Mendeleev เพื่อคำนวณความร้อนของการเผาไหม้ของเชื้อเพลิง
ทดสอบเพิ่ม 02/20/2014
วิธีการคำนวณการเผาไหม้เชื้อเพลิงในอากาศ: การกำหนดปริมาณออกซิเจนในอากาศ, ผลิตภัณฑ์จากการเผาไหม้, ค่าความร้อนเชื้อเพลิง แคลอริเมตริก และอุณหภูมิการเผาไหม้จริง การเผาไหม้ของเชื้อเพลิงในอากาศที่อุดมด้วยออกซิเจน
ภาคนิพนธ์ เพิ่ม 12/08/2554
อุณหพลศาสตร์เป็นสาขาหนึ่งของฟิสิกส์ที่ศึกษากระบวนการเปลี่ยนความร้อนเป็นงานและพลังงานประเภทอื่นๆ ลักษณะของคุณสมบัติที่สำคัญของวงจรเทอร์โมมิเตอร์แก๊ส การพิจารณาคุณสมบัติพื้นฐานของก๊าซในอุดมคติ สาระสำคัญของแนวคิดของ "ความจุความร้อน"
งานนำเสนอ เพิ่ม 04/15/2014
คำอธิบายของชุดหม้อไอน้ำก่อนเปลี่ยนไปใช้เชื้อเพลิงประเภทอื่น ลักษณะของหัวเผาที่รับติดตั้ง การปรับอุณหภูมิของไอเสีย การคำนวณปริมาตรของอากาศและผลิตภัณฑ์จากการเผาไหม้ระหว่างการเผาไหม้ของเชื้อเพลิงสองประเภท สมดุลความร้อนและการสิ้นเปลืองเชื้อเพลิง
วิทยานิพนธ์, เพิ่ม 06/13/2015
วัตถุประสงค์ของเครื่องอบแห้งแบบอุโมงค์ องค์ประกอบของเชื้อเพลิงและการคำนวณอากาศสำหรับการเผาไหม้ การกำหนดปริมาตรรวมของผลิตภัณฑ์การเผาไหม้ระหว่างการเผาไหม้เชื้อเพลิงและอุณหภูมิตามทฤษฎี การคำนวณทางเทคโนโลยีของอุโมงค์อบแห้ง การคำนวณทางเทอร์โมเทคนิคของกระบวนการทำให้แห้ง

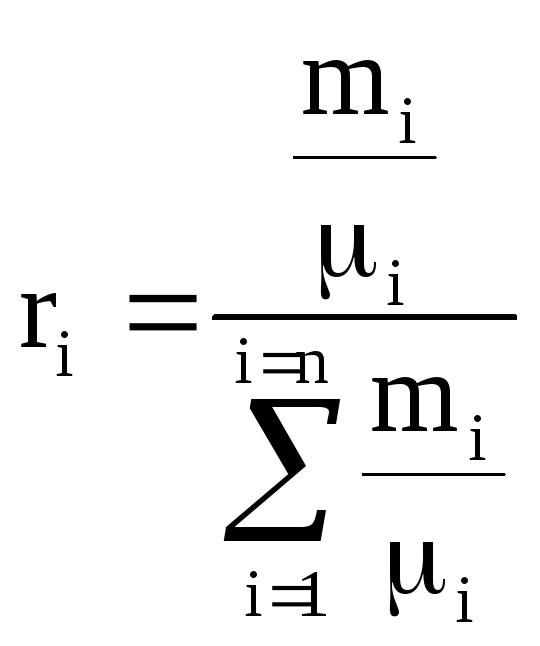
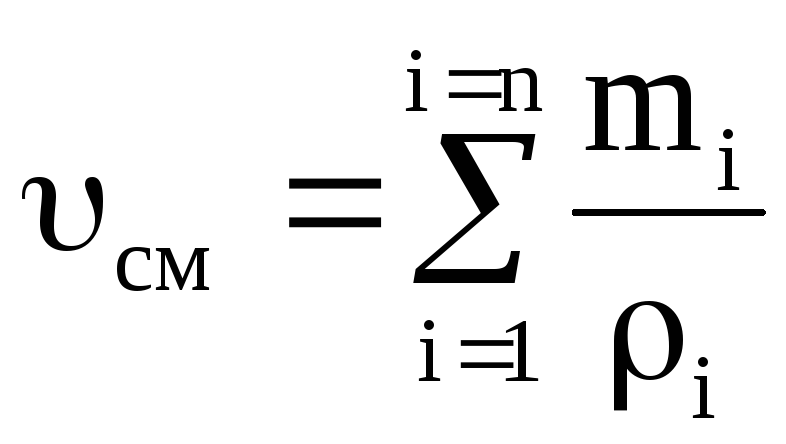
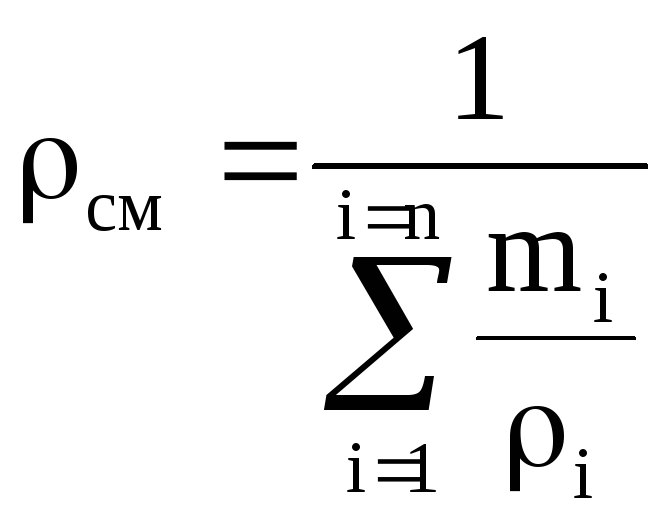
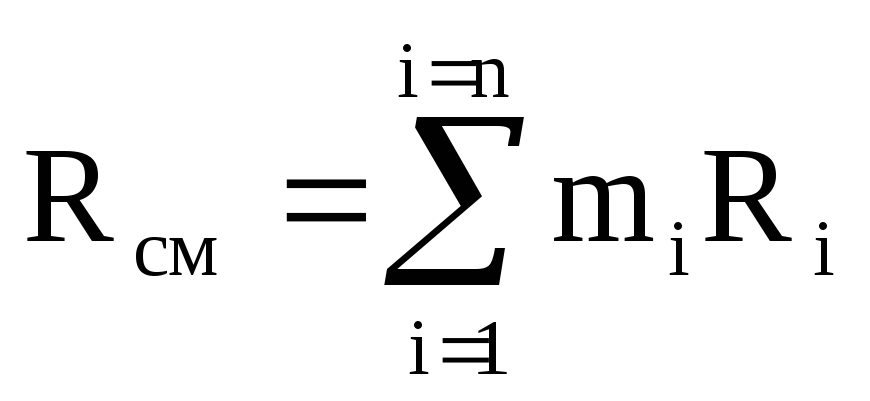

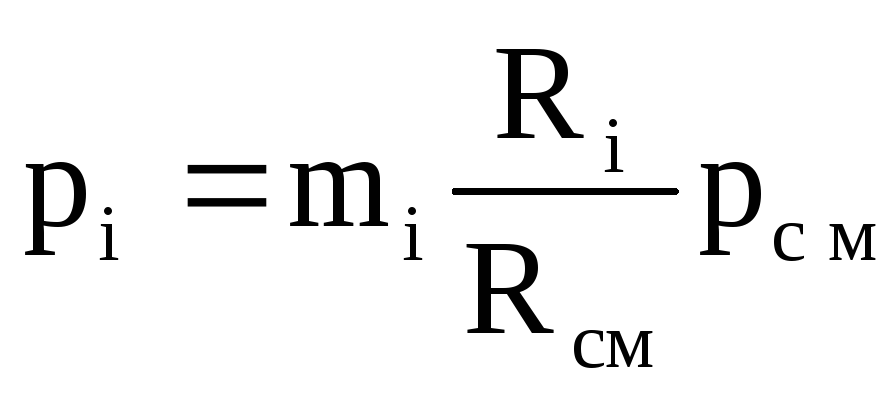
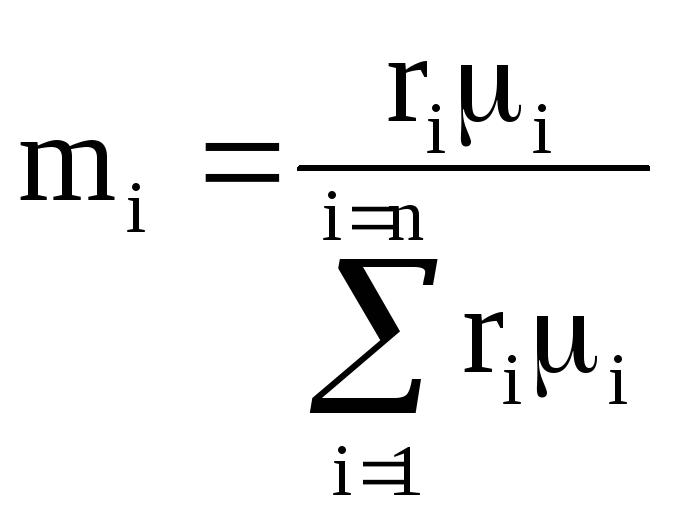
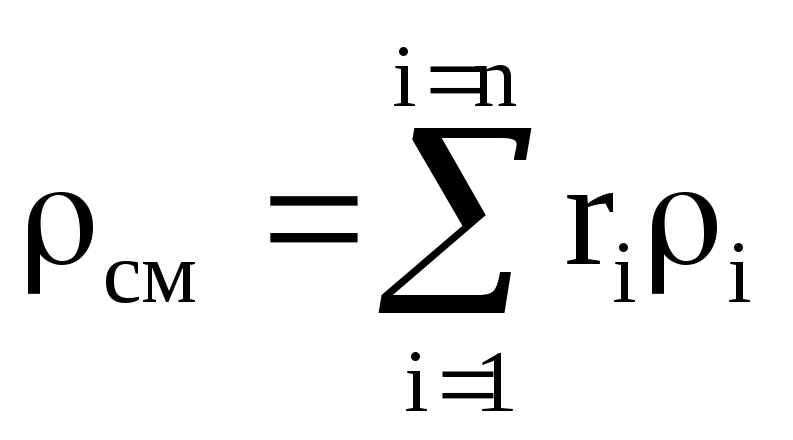
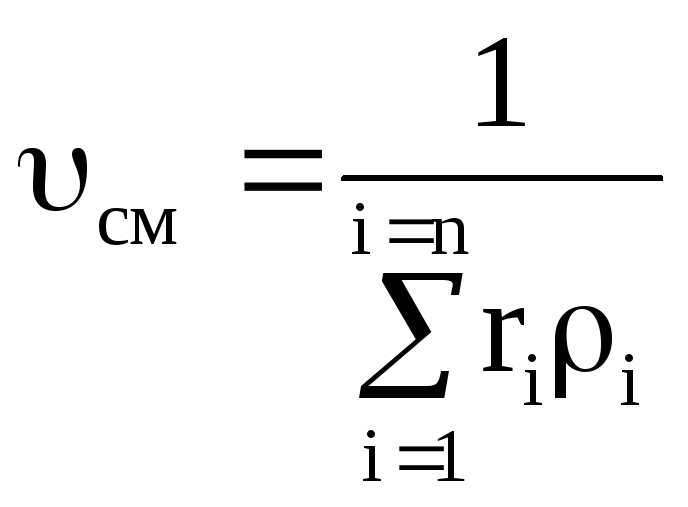
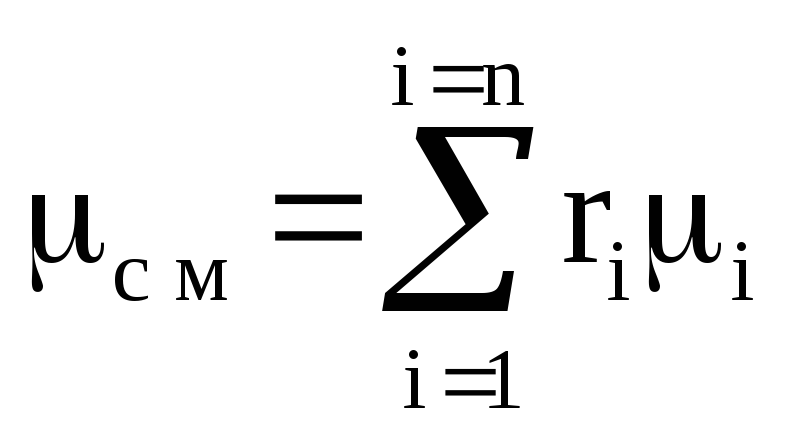
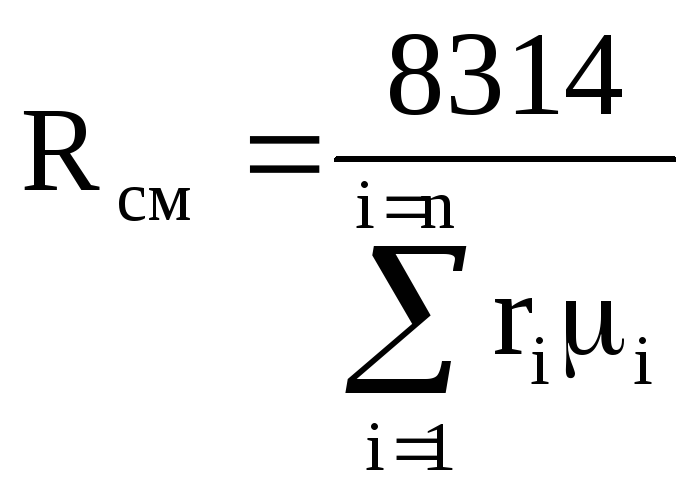
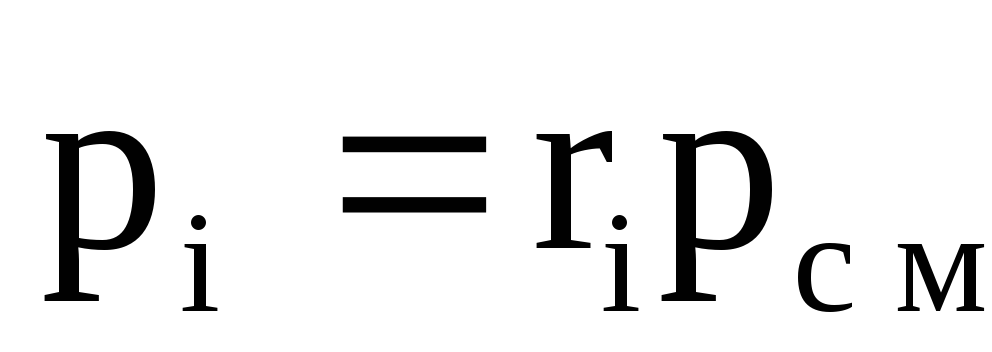
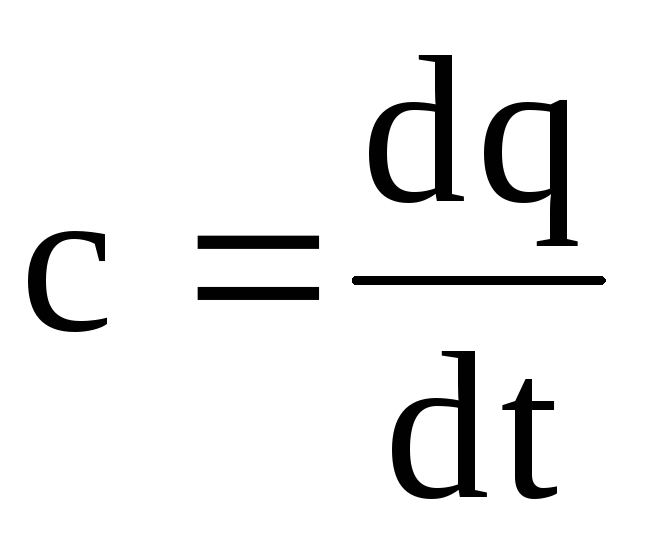 .
(1.28)
.
(1.28)