SI 系の熱量を測定します。 熱量を測定する方法と手段
熱- 直接接触または放射によって、より高温の物体からより加熱されていない物体に伝達されるエネルギー。
温度は、分子運動の強さの尺度です。
特定の温度で物体が保有する熱量は、その質量に依存します。 たとえば、同じ温度では、小さなカップよりも大きなカップの水に多くの熱が蓄えられます。 お湯(バケツの水の温度は低いですが)。
熱は、体の機能を含め、人間の生活において重要な役割を果たしています。 食物に含まれる化学エネルギーの一部が熱に変換されるため、体温は 37 °C 近くに維持されます。 人体の熱バランスも温度に依存します。 環境、そして人々は、冬には住宅や工業施設を暖房し、夏には冷房に多くのエネルギーを費やすことを余儀なくされています. このエネルギーのほとんどは、ボイラー プラントや発電所の蒸気タービンなど、化石燃料 (石炭、石油) で稼働し、電気を生成する熱機関によって供給されます。
18世紀の終わりまで。 体の温度は、<калорической жидкости>、 また<теплорода>. 後に、B. ラムフォード、J. ジュール、その他の当時の物理学者は、機知に富んだ実験と推論を通じて反論しました。<калорическую>この理論により、熱は無重力であり、機械的な動きだけで任意の量を得ることができることが証明されました。 熱自体は物質ではなく、原子や分子の動きのエネルギーです。 現代の物理学が固執するのは、この熱の理解です。
この記事では、熱と温度がどのように関係し、これらの量がどのように測定されるかを見ていきます。 私たちの議論の主題は、次の質問にもなります。体のある部分から別の部分への熱の伝達。 真空(物質を含まない空間)での熱伝達; 現代世界における熱の役割。
熱と温度
物質の熱エネルギーの量は、その分子のそれぞれの動きを個別に観察することによって決定することはできません。 それどころか、物質の巨視的な性質を研究することによってのみ、ある期間にわたって平均化された多くの分子の微視的な運動の特徴を見つけることができます。 物質の温度は、分子の動きの強さの平均的な指標であり、そのエネルギーは 熱エネルギー物質。
最もよく知られているが、温度を推定する最も正確でない方法の 1 つは触覚です。 私たちは物に触れて、それが熱いか冷たいかを自分の感覚で判断します。 もちろん、これらの感覚は私たちの体の温度に依存します。これは、温度を測定する上で最も重要な概念の 1 つである熱平衡の概念につながります。
熱平衡
物体 A と物体 B の間の熱平衡
明らかに、2 つの物体 A と B が互いに強く押し付けられている場合、十分に長い時間接触した後、それらの温度が同じであることがわかります。 この場合、物体 A と B は互いに熱平衡状態にあると言われます。 ただし、一般的に言えば、物体間に熱平衡が存在するために物体が接触している必要はありません。温度が同じであれば十分です。 これは、第 3 の物体 C を使用して検証できます。最初に物体 A と熱平衡状態にし、次に物体 C と B の温度を比較します。ここで物体 C は温度計の役割を果たします。 厳密な定式化では、この原理は熱力学のゼロ次法則と呼ばれます。物体 A と B が第 3 の物体 C と熱平衡状態にある場合、これらの物体も互いに熱平衡状態にあります。 この法則は、温度を測定するすべての方法の根底にあります。
温度測定

温度目盛り

体温計
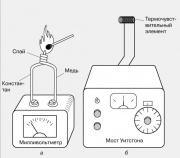
電気効果に基づく温度計
正確な実験と計算を行いたい場合は、高温、高温、低温、低温などの温度定格では不十分です。段階的な温度スケールが必要です。 そのような目盛りはいくつかあり、通常は水の凝固点と沸点が基準点として取られます。 最も一般的な 4 つのスケールを図に示します。 水の凝固点が 0 °、沸点が 100 ° に相当する摂氏目盛りは、1742 年にスウェーデンの天文学者 A. セルシウスが記述したことにちなんで、摂氏目盛りと呼ばれています。スウェーデンの博物学者 K. リンネがこの尺度を最初に適用しました。 現在、摂氏スケールは世界で最も一般的です。 水の凝固点と沸点が 32 と 212 ° の非常に不快な数値に対応する華氏温度スケールは、1724 年に G. 華氏によって提案されました。 華氏スケールは英語圏の国で広く使用されていますが、科学文献ではほとんど使用されていません. 摂氏温度 (°C) を華氏温度 (°F) に変換するには、式 °F = (9/5)°C + 32 があり、逆変換 - 式 °C = (5/9) ( °F- 32)。
華氏と摂氏の両方のスケールは、温度が水の凝固点を下回り、負の数として表される条件で実験を行う場合、非常に不便です。 このような場合、絶対温度スケールが導入されました。これは、分子運動が停止する点である、いわゆる絶対零度への外挿に基づいています。 そのうちの 1 つはランキン スケールと呼ばれ、もう 1 つは絶対熱力学スケールと呼ばれます。 温度はランキン度 (°R) とケルビン (K) で測定されます。 どちらのスケールも絶対零度から始まり、水の凝固点は 491.7°R と 273.16 K に対応します。摂氏スケールと絶対熱力学スケールでの水の凝固点と沸点の間の度数とケルビン数は同じで等しいです。 100まで; 華氏とランキンのスケールも同じですが、180に等しくなります。摂氏は式K \u003d°C + 273.16を使用してケルビンに変換され、華氏は式°R \u003dを使用してランキン度に変換されます°F + 459.7。
温度を測定するように設計されたデバイスの動作は、物質の熱エネルギーの変化に関連するさまざまな物理現象 (電気抵抗、体積、圧力、放射特性、熱電特性の変化) に基づいています。 最も単純で最も身近な温度測定器の 1 つは、図に示すガラス温度計です。 温度計下部の球 c は、媒質中に入れたり温度を測定したい対象物に押し付けたりして、球が熱を受けるか放出するかによって膨張または収縮し、円柱が上昇または下降します。毛細血管。 温度計が事前に校正され、スケールが装備されている場合は、体温を直接知ることができます。
熱膨張に基づいて動作する別のデバイスは、図に示すバイメタル温度計です。 その主な要素は、熱膨張係数の異なる 2 つのはんだ付けされた金属のスパイラル プレートです。 加熱すると、金属の 1 つが他の金属よりも膨張し、らせんがねじれて、目盛りに対して矢印が回転します。 このようなデバイスは、屋内外の気温を測定するためによく使用されますが、局所的な温度を決定するのには適していません。
局所温度は通常、熱電対を使用して測定されます。熱電対は、一方の端がはんだ付けされた異種金属の 2 本のワイヤです。 このような接合部が加熱されると、ワイヤの自由端に通常数ミリボルトの EMF が発生します。 熱電対は、鉄とコンスタンタン、銅とコンスタンタン、クロメルとアルメルなど、さまざまな金属のペアから作られています。 それらの熱起電力は、広い温度範囲で温度に対してほぼ直線的に変化します。
別の熱電効果も知られています - 導電性材料の抵抗の温度依存性です。 電気抵抗温度計の動作の根底にあるもので、その1つが図に示されています。 小さな温度検出素子 (熱電対) (通常は細いワイヤのコイル) の抵抗は、ホイートストン ブリッジを使用して校正された可変抵抗器の抵抗と比較されます。 出力インストゥルメントは、度単位で直接目盛ることができます。
光高温計は、可視光を放射する高温物体の温度を測定するために使用されます。 この装置の 1 つのバージョンでは、体から放射された光が、双眼鏡の焦点面に配置された白熱灯のフィラメントの放射と比較されます。 ランプのフィラメントを加熱する電流を変化させ、フィラメントと本体の輝きを視覚的に比較すると、それらの間に熱平衡が確立されていることがわかります。 デバイスのスケールは、温度の単位で直接目盛りを付けることができます。
技術の進歩 近年新しい温度センサーを作成できます。 たとえば、特に高い感度が必要な場合は、熱電対や従来の抵抗温度計の代わりに、半導体デバイス、サーミスタが使用されます。 相状態を変化させる色素や液晶は、特に体表面温度が広範囲に変化する場合に、熱変換器としても使用されます。 最後に、赤外線サーモグラフィを使用します。この方法では、物体の赤外線画像が条件付きの色で取得されます。各色は特定の温度に対応します。 この温度測定方法は、最も幅広いアプリケーションを見つけます。 医療診断建物の断熱をチェックする前に。
熱量の測定
水熱量計
物体の熱エネルギー (熱量) は、いわゆる熱量計で直接測定できます。 このようなデバイスの単純なバージョンを図に示します。 慎重に断熱された密閉容器で、内部の温度を測定するための装置が装備されており、時には水などの既知の特性を持つ作動流体で満たされています。 小さな加熱体の熱量を測定するには、熱量計に入れ、システムが熱平衡になるのを待ちます。 熱量計 (より正確には、熱量計を満たしている水) に伝達される熱量は、水温の上昇によって決まります。
燃焼などの化学反応中に放出される熱量は、小さなものを置くことで測定できます。<бомбу>. で<бомбе>点火用の電線が接続されているサンプルと、それに対応する酸素の量が配置されています。 サンプルが完全に燃え尽きて熱平衡が確立された後、熱量計内の水の温度がどれだけ上昇したか、したがって放出される熱量が決定されます。
ヒートユニット
熱はエネルギーの一種であるため、エネルギーの単位で測定する必要があります。 国際的な SI システムでは、エネルギーの単位はジュール (J) です。 また、熱量のシステム外単位であるカロリーを使用することも許可されています。国際カロリーは4.1868 J、熱化学カロリーは4.1840 Jです。外国の研究所では、研究結果はいわゆるを使用して表現されることがよくあります。 15 度のカロリーは 4.1855 J に相当します。オフシステムの英国熱量単位 (BTU) は使用されなくなりつつあります: BTU 平均 = 1.055 J.
熱源
主な熱源は、化学反応と核反応、およびさまざまなエネルギー変換プロセスです。 熱の放出を伴う化学反応の例は、燃焼と食品成分の分解です。 地球が受け取るほとんどすべての熱は、太陽の深部で発生する核反応によって提供されます。 人類は、核分裂の制御されたプロセスの助けを借りて熱を得る方法を学び、現在、同じ目的のために熱核融合反応を使用しようとしています. 機械的仕事や電気エネルギーなど、他の種類のエネルギーも熱に変換できます。 熱エネルギーは(他のものと同様に)別の形にしか変換できず、取得できないことを覚えておくことが重要です。<из ничего>、破壊することもありません。 これは、熱力学と呼ばれる科学の基本原理の 1 つです。
熱力学
熱力学熱、仕事、物質の間の関係の科学です。 これらの関係についての現代的な考え方は、カルノー、クラウジウス、ギブス、ジュール、ケルビンなどの過去の偉大な科学者の業績に基づいて形成されました. 熱力学は、物質の熱容量と熱伝導率の意味を説明します,物体の熱膨張、および相転移の熱。 この科学は、実験的に確立されたいくつかの法則、つまり原則に基づいています。
物質の熱と性質
さまざまな物質熱エネルギーを蓄積する能力が異なります。 それは分子構造と密度に依存します。 物質の単位質量の温度を 1 度上げるのに必要な熱量は、その比熱容量と呼ばれます。 熱容量は、物質が置かれている条件によって異なります。 たとえば、気球内の 1 グラムの空気を 1 K 加熱するには、気球に与えられたエネルギーの一部が気球の膨張に費やされるため、壁が固い密閉容器内で同じように加熱するよりも多くの熱が必要です。空気ではなく、加熱してください。 したがって、特に、ガスの熱容量は、一定の圧力と一定の体積で別々に測定されます。
温度が上昇すると、分子の混沌とした動きの強度が増します。ほとんどの物質は、加熱すると膨張します。 温度が1 K上昇したときの物質の膨張の程度は呼ばれます 熱膨張係数.
物質がある相状態から別の相状態へ、たとえば固体から液体へ (時にはすぐに気体へ) 移行するためには、一定量の熱を受け取る必要があります。 加熱した場合 個体、その後、溶け始めるまで温度が上昇します。 溶融が完了するまで、熱入力にもかかわらず本体の温度は一定のままです。 物質の単位質量を溶かすのに必要な熱量は、融解熱と呼ばれます。 熱を供給し続けると、溶けた物質は沸騰するまで加熱されます。 特定の温度で単位質量の液体を蒸発させるのに必要な熱量は、蒸発熱と呼ばれます。
熱の役割とその利用
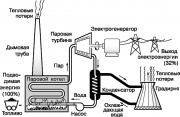
蒸気タービン発電所の運転スキーム
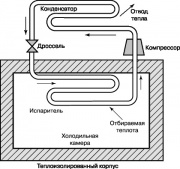
冷凍サイクル図
地球全体の熱伝達プロセスは、太陽放射による地球の加熱に還元されません。 大気中の大規模な対流は、世界中の気象条件の日々の変化を決定します。 赤道域と極域の間の大気の温度差は、地球の自転によるコリオリ力とともに、貿易風、ジェット気流、温暖前線や寒冷前線など、絶えず変化する対流の出現につながります。
地球の溶融コアからその表面への熱の伝達 (熱伝導率による) は、火山噴火と間欠泉の出現につながります。 一部の地域では、暖房や発電に地熱エネルギーが使用されています。
暖かさは、ほとんどすべてにおいて不可欠な参加者です 生産工程. 金属の製錬と加工、エンジンの操作、食料生産、化学合成、石油精製、レンガや食器から自動車や電子機器に至るまで、さまざまな品目の製造など、最も重要なものに言及します。 .
多くの工業生産と輸送、および火力発電所は、熱機関 (熱を有用な仕事に変換する装置) なしでは機能しません。 このような機械の例としては、圧縮機、タービン、蒸気、ガソリン、およびジェット エンジンがあります。
最もよく知られている熱機関の 1 つは、現代の発電所で使用されるランキン サイクルの一部を実装する蒸気タービンです。 このサイクルの簡略図を図に示します。 作動流体 - 水 - は、化石燃料 (石炭、石油、または天然ガス) の燃焼によって加熱された蒸気ボイラーで過熱蒸気に変換されます。 スチームハイ
Gasovik - 工業用ガス機器 GOST、SNiP、PB 物理量の単位、物理化学的概念、ガスの比率、組成および特性のディレクトリ
温度と熱量の測定単位
温度測定の基本単位は、実質的に摂氏に対応する国際温度目盛りの度でした。 この値は、0 ~ 100 °C の温度間隔の 1/100 に相当します。 760 mm Hg の圧力での氷と沸騰水の融点の間です。 美術。
絶対温度は、絶対零度、つまり -273.16 ° C から測定された温度であり、ケルビン度 (° K) で測定されます。 ケルビン度は摂氏度と同じです。 したがって、絶対温度は次のように摂氏で表されます。
T、°K = t、°C + 273.16
SI システムでは、温度の単位はケルビンです。 スケールの原点 (ゼロの位置) に応じて、摂氏度とケルビン度を使用して温度測定の実際の結果を表すことができます。
例: 250 ±5 °С = 523.16 ±5 °K。
SI システムでは、仕事、エネルギー、および熱はジュール (J) で測定されます。 実用的な目的のために、より大きくて便利な単位が使用されることがあります - キロジュール (kJ)、1000 J に等しい. SI の仕事の単位は、1 m の変位で 1 N の力によって行われる仕事です. エネルギー - 物理量体がどれだけの仕事をすることができるかを示します。
カロリーとキロカロリーは、システム外の熱単位として使用できます。 カロリーとは、水 1 グラムの温度を 1 ℃ (19.5 ~ 20.5 ℃) 上げるのに必要な熱量です。
1cal(カロリー)=4.1868J;
1 kcal (キロカロリー) \u003d 1000 cal \u003d 4186.8 J \u003d 4.187 kJ;
1 Mcal (メガカロリー) \u003d 10 6 cal \u003d 4.1868 MJ;
1 Gcal (ギガカロリー) \u003d 10 9 cal \u003d 4186.8 MJ.
比較のために、燃料を評価するとき、いわゆる条件付き熱が使用され、計算のための発熱量は条件付きで7Mcal / kgまたは7 Gcal / tに等しいと仮定されます。 このような場合、それぞれ 1 kg または 1 トンの標準燃料 (t.c.f.) について話します。
熱は、体の機能を含め、人間の生活において重要な役割を果たしています。 食物に含まれる化学エネルギーの一部が熱に変換されるため、体温は 37 付近に維持されます。
° C. 人体の熱収支は周囲温度にも依存し、人々は住宅や工業施設の冬の暖房と夏は冷房に多くのエネルギーを費やさなければなりません。 このエネルギーのほとんどは、ボイラー プラントや発電所の蒸気タービンなど、化石燃料 (石炭、石油) で稼働し、電気を生成する熱機関によって供給されます。18世紀の終わりまで。 体の温度はそれに含まれる「カロリー液体」または「カロリー」の量によって決定されると信じて、熱は物質的な物質と考えられていました。 その後、B. ラムフォード、J. ジュール、その他の当時の物理学者は、巧妙な実験と推論を通じて「熱量」理論に反論し、熱には無重力があり、機械的な動きだけで任意の量を得ることができることを証明しました。 熱自体は物質ではなく、原子や分子の動きのエネルギーです。 現代の物理学が固執するのは、この熱の理解です。 こちらもご覧ください物理。
この記事では、熱と温度がどのように関係し、これらの量がどのように測定されるかを見ていきます。 私たちの議論の主題は、次の質問にもなります。体のある部分から別の部分への熱の伝達。 真空(物質を含まない空間)での熱伝達; 現代世界における熱の役割。
熱と温度 物質の熱エネルギーの量は、その分子のそれぞれの動きを個別に観察することによって決定することはできません。 それどころか、物質の巨視的な性質を研究することによってのみ、ある期間にわたって平均化された多くの分子の微視的な運動の特徴を見つけることができます。 物質の温度は、分子の動きの強さの平均的な指標であり、そのエネルギーは物質の熱エネルギーです。最もよく知られている方法の 1 つですが、触って温度を評価する方法としては最も正確ではありません。 私たちは物に触れて、それが熱いか冷たいかを自分の感覚で判断します。 もちろん、これらの感覚は私たちの体の温度に依存しているため、温度を測定する上で最も重要な概念の 1 つである熱平衡の概念に導かれます。
熱バランス。 明らかに、2体なら と B (図1)互いにしっかりと押し付けられ、十分に長い時間後にそれらに触れると、それらの温度が同じであることがわかります。 この場合、遺体は と B 互いに熱平衡状態にあります。 ただし、一般的に言えば、物体間に熱平衡が存在するために物体が接触している必要はなく、温度が同じであれば十分です。 これは、3 番目のボディを使用して検証できます。 ハ 、最初に体との熱平衡状態にします あ 、そして体の温度を比較します Cと b. 体 ハ ここで温度計の役割を果たします。 厳密な定式化では、この原理は熱力学のゼロ次法則と呼ばれます。 物体 A と B が第 3 の物体 C と熱平衡状態にある場合、これらの物体も互いに熱平衡状態にあります。この法則は、温度を測定するすべての方法の根底にあります。温度測定。 正確な実験と計算を行いたい場合は、高温、高温、低温、低温などの温度定格では不十分で、目盛り付きの温度スケールが必要です。 そのような目盛りはいくつかあり、通常は水の凝固点と沸点が基準点として取られます。 最も一般的な 4 つのスケールを図に示します。 2. 水の凝固点が 0 に相当する摂氏目盛り° 、沸点は100° は、1742 年にスウェーデンの天文学者 A. セルシウスにちなんでセルシウス スケールと呼ばれます。このスケールを最初に使用したのは、スウェーデンの博物学者 K. リニーであると考えられています。 現在、摂氏スケールは世界で最も一般的です。 水の凝固点と沸点が非常に不快な数字の 32 と 212 に対応する華氏温度スケール° 、1724 年に G. ファーレンハイトによって提案されました。 華氏スケールは英語圏の国で広く使用されていますが、科学文献ではほとんど使用されていません. 温度を摂氏に変換するには (° C) から華氏温度 (° F) 公式がある° F = (9/5) ° C + 32、および逆変換式の場合°C = (5/9)(°F - 32)。 華氏と摂氏の両方のスケールは、温度が水の凝固点を下回り、負の数で表される状況で実験を行う場合、非常に不便です。 このような場合、絶対温度スケールが導入されました。これは、いわゆる絶対零度 (分子運動が停止しなければならないポイント) への外挿に基づいています。 そのうちの 1 つはランキン スケールと呼ばれ、もう 1 つは絶対熱力学スケールと呼ばれます。 温度はランキン度で測定されます (° R) とケルビン (K)。 どちらの目盛りも絶対零度から始まり、水の凝固点は 491.7 です。° R および 273.16 K。摂氏スケールと絶対熱力学スケールでの水の凝固点と沸点の間の度数とケルビン数は同じで、100 に等しい。 華氏とランキン スケールの場合も同じですが、180 に等しくなります。摂氏度は、式 K \u003d を使用してケルビンに変換されます。° C + 273.16、および式を使用した華氏からランキン度への度数°R = °F + 459.7。 温度を測定するように設計されたデバイスの動作は、物質の熱エネルギーの変化、電気抵抗、体積、圧力、放射特性、および熱電特性の変化に関連するさまざまな物理現象に基づいています。 温度を測定するための最も単純で最もよく知られている器具の 1 つは、図 1 に示すガラス中水銀温度計です。 3, を。 温度計の下部に水銀を入れた球を、媒質中に入れたり、温度を測定したい対象物に押し付けたりして、球が熱を受けるか放出するかによって、水銀が膨張または収縮し、その柱が上昇または上昇します。毛細血管に落ちます。 温度計が事前に校正され、スケールが装備されている場合は、体温を直接知ることができます。熱膨張に基づいて動作するもう 1 つのデバイスは、図 1 に示すバイメタル温度計です。
3, b. その主な要素 熱膨張係数の異なる 2 つのはんだ付けされた金属のスパイラル プレート。 加熱すると、金属の 1 つが他の金属よりも膨張し、らせんがねじれて、目盛りに対して矢印が回転します。 このようなデバイスは、屋内外の気温を測定するためによく使用されますが、局所的な温度を決定するのには適していません。局所温度は通常、熱電対を使用して測定されます。熱電対は、一方の端がはんだ付けされた異種金属の 2 本のワイヤです (図 1)。
4, a)。 このような接合部が加熱されると、ワイヤの自由端に通常数ミリボルトの起電力が発生します。 熱電対は、鉄とコンスタンタン、銅とコンスタンタン、クロメルとアルメルなど、さまざまな金属のペアから作られています。 それらの熱起電力は、広い温度範囲で温度に対してほぼ直線的に変化します。別の熱電効果も知られています - 導電性材料の抵抗の温度依存性です。 電気抵抗温度計の動作の根底にあるもので、そのうちの1つを図1に示します。
4, b. 小さな温度感知素子 (熱センサー) の抵抗は、通常は細いワイヤのコイルで、ホイートストン ブリッジを使用して校正済みの可変抵抗器の抵抗と比較されます。 出力インストゥルメントは、度単位で直接目盛ることができます。光高温計は、可視光を発する白熱体の温度を測定するために使用されます。 この装置の 1 つのバージョンでは、体から放射された光が、双眼鏡の焦点面に配置された白熱灯のフィラメントの放射と比較されます。 ランプのフィラメントを加熱する電流は、フィラメントと本体のグローを視覚的に比較して、それらの間に熱平衡が確立されていることが明らかになるまで変更されます。 デバイスのスケールは、温度の単位で直接目盛りを付けることができます。
近年の技術的進歩により、新しい温度センサーの作成が可能になりました。 例えば、特に高い感度が必要な場合は、熱電対や従来の測温抵抗体の代わりに、半導体デバイスであるサーミスタが使用されます。 相状態を変化させる色素や液晶は、特に体表面温度が広範囲に変化する場合に、熱変換器としても使用されます。 最後に、赤外線サーモグラフィを使用します。この方法では、物体の赤外線画像が条件付きの色で取得されます。各色は特定の温度に対応します。 この温度測定方法は、医療診断から部屋の断熱チェックまで、最も幅広い用途があります。 こちらもご覧ください固体の物理学; 液晶。
熱量の測定。 物体の熱エネルギー (熱量) は、いわゆる熱量計で直接測定できます。 このようなデバイスの単純なバージョンを図 1 に示します。 5. これは慎重に断熱された密閉容器で、内部の温度を測定するための装置が装備されており、場合によっては水などの既知の特性を持つ作動流体で満たされています。 小さな加熱体の熱量を測定するには、熱量計に入れ、システムが熱平衡になるのを待ちます。 熱量計 (より正確には、熱量計を満たしている水) に伝達される熱量は、水温の上昇によって決まります。燃焼などの化学反応中に放出される熱量は、熱量計に小さな「爆弾」を配置することで測定できます。 「爆弾」には、点火用の電線が接続されたサンプルと、対応する量の酸素が含まれています。 サンプルが完全に燃え尽きて熱平衡が確立された後、熱量計内の水の温度がどれだけ上昇したか、つまり放出された熱の量が決定されます。 こちらもご覧ください熱量測定。
ヒートユニット。 熱はエネルギーの一種であるため、エネルギーの単位で測定する必要があります。 国際的な SI システムでは、エネルギーの単位はジュール (J) です。 熱カロリー量の非全身単位を使用することも許可されています。国際カロリーは4.1868 J、熱化学カロリーは4.1840 Jです。外国の研究所では、研究結果はいわゆるを使用して表現されることがよくあります。 15 度のカロリーは 4.1855 J に相当します。オフシステムの英国熱量単位 (BTU) は使用されなくなりつつあります: BTU 平均 = 1.055 J. 主な熱源は、化学反応と核反応、およびさまざまなエネルギー変換プロセスです。 熱の放出を伴う化学反応の例は、燃焼と食品成分の分解です。 地球が受け取るほとんどすべての熱は、太陽の深部で発生する核反応によって提供されます。 人類は、核分裂の制御されたプロセスの助けを借りて熱を得る方法を学び、現在、同じ目的のために熱核融合反応を使用しようとしています. 機械的仕事や電気エネルギーなど、他の種類のエネルギーも熱に変換できます。 熱エネルギーは(他のものと同様に)別の形にしか変換できないことを覚えておくことが重要ですが、「何もないところから」取得したり破壊したりすることはできません. これは、熱力学と呼ばれる科学の基本原理の 1 つです。 熱力学 熱力学は、熱、仕事、物質の間の関係の科学です。 これらの関係についての現代的な考え方は、カルノー、クラウジウス、ギブス、ジュール、ケルビンなどの過去の偉大な科学者の業績に基づいて形成されました. 熱力学は、物質の熱容量と熱伝導率の意味を説明します,物体の熱膨張、および相転移の熱。 この科学は、実験的に確立されたいくつかの法則の原則に基づいています。熱力学の始まり。 上で定式化された熱力学のゼロ次法則は、熱平衡、温度、および温度測定の概念を導入します。 熱力学の第 1 法則は、すべての科学全体にとって非常に重要な声明です。エネルギーは「何もないところから」破壊することも取得することもできないため、宇宙の総エネルギーは一定の値です。 熱力学の第 1 法則は、最も単純な形で次のように述べることができます。システムが受け取るエネルギーから、システムが放棄するエネルギーを差し引いたものが、システムに残っているエネルギーに等しくなります。 一見すると、このステートメントは明白に見えますが、そうではありません。, 自動車エンジンのシリンダー内でのガソリンの燃焼のような状況: ここで受け取るエネルギーは化学的であり、放出されるエネルギーは機械的 (仕事) であり、システムに残っているエネルギーは熱です。したがって、エネルギーはある形態から別の形態に変化する可能性があり、そのような変化が自然と技術で絶えず起こっていることは明らかです。 100 年以上前に、J. Joule は、図 1 に示すデバイスを使用して、機械エネルギーを熱エネルギーに変換する場合についてこれを証明しました。 6, a. この装置では、下降および上昇するおもりが、水で満たされた熱量計でブレード付きのシャフトを回転させ、その結果、水が加熱されました。 正確な測定により、ジュールは 1 カロリーの熱が 4.186 J の機械的仕事に相当することを決定することができました。 図に示すデバイス。
6, b は、電気エネルギーの熱当量を決定するために使用されました。熱力学の第一法則は、多くの一般的な現象を説明しています。 たとえば、開いた冷蔵庫でキッチンを冷やすことができない理由が明らかになります。 キッチンを環境から断熱したとしましょう。 エネルギーは冷蔵庫の電源線を介してシステムに継続的に供給されますが、システムはエネルギーを放出しません。 したがって、その総エネルギーが増加し、キッチンが暖かくなります。冷蔵庫の背面にある熱交換器(コンデンサー)のチューブに触れるだけで、「冷却」デバイスとしての役に立たないことがわかります。 しかし、これらのパイプがシステムの外に持ち出された場合(たとえば、窓の外)、キッチンは受け取ったよりも多くのエネルギーを放出します。 冷やされ、冷蔵庫は窓用エアコンとして機能しました。
熱力学の第一法則は、エネルギーの生成または破壊を妨げる自然の法則です。 しかし、エネルギー伝達のプロセスが自然界でどのように進行するかについては何も述べていません。 したがって、これらの物体が接触すると、熱い物体が冷たい物体を加熱することがわかります。 しかし、冷たい体はそれ自体でその蓄熱量を熱い体に移すことができますか? 最後の機会熱力学第二法則によって断固として拒絶されます。
最初の法則は、係数を持つエンジンを作成する可能性も排除します 有用なアクション(効率) 100%以上 (類似)
" 永遠 " エンジンは、消費するよりも任意の長い時間、より多くのエネルギーを放出する可能性があります)。 エンジンに供給されるエネルギーの一部は、あまり役に立たない熱エネルギーの形で必然的に失われる必要があるため、100% の効率でもエンジンを構築することは不可能です。 したがって、ホイールは、ベアリングの摩擦により、ホイールが停止するまで徐々に熱に変わるため、エネルギーの供給がなければ無期限に回転しません。「有用な」仕事を有用性の低いエネルギー熱に変える傾向は、異なるガスを含む2つの容器が接続されたときに発生する別のプロセスと比較できます. 十分に待った後、両方の容器でガスの均一な混合物がシステムの秩序を低下させるように作用することがわかりました。 この障害の熱力学的尺度はエントロピーと呼ばれ、熱力学の第 2 法則は別の方法で定式化できます。自然界のプロセスは、システムとその環境のエントロピーが増加するように常に進行します。 したがって、宇宙のエネルギーは一定のままですが、そのエントロピーは絶えず増加しています。
物質の熱と性質。 物質が異なれば、熱エネルギーを蓄える能力も異なります。 それは分子構造と密度に依存します。 物質の単位質量の温度を 1 度上昇させるのに必要な熱量は、その熱量と呼ばれます。 比熱. 熱容量は、物質が置かれている条件によって異なります。 たとえば、気球内の 1 グラムの空気を 1 K 加熱するには、気球に与えられたエネルギーの一部が気球の膨張に費やされるため、壁が固い密閉容器内で同じように加熱するよりも多くの熱が必要です。空気ではなく、加熱してください。 したがって、特に、ガスの熱容量は、一定の圧力と一定の体積で別々に測定されます。温度が上昇すると、分子の無秩序な動きの強度が増加し、ほとんどの物質は加熱されると膨張します。 温度が1 K上昇したときの物質の膨張の程度は、熱膨張係数と呼ばれます。
物質がある相状態から別の相状態へ、たとえば固体から液体へ (時にはすぐに気体へ) 移行するためには、一定量の熱を受け取る必要があります。 固体を加熱すると、溶け始めるまで温度が上昇します。 融解が完了するまで、熱の供給にもかかわらず、体の温度は一定のままです。 物質の単位質量を溶かすのに必要な熱量は、融解熱と呼ばれます。 熱を供給し続けると、溶けた物質は沸騰するまで加熱されます。 特定の温度で単位質量の液体を蒸発させるのに必要な熱量は、蒸発熱と呼ばれます。
分子動力学理論。 分子動力学理論は、この物質を構成する原子や分子の挙動を微視的なレベルで考察することにより、物質の巨視的な特性を説明します。 この場合、統計的アプローチが使用され、粒子自体とその動きの性質についていくつかの仮定が行われます。 したがって、分子は固体のボールであると考えられます。これは、ガス状の媒体では連続的な無秩序な動きをしており、衝突ごとにかなりの距離を移動します。 衝突は弾性的であると考えられ、サイズが小さく数が非常に多い粒子間で発生します。 このモデルに正確に対応する実在の気体はありませんが、ほとんどの気体はこのモデルに非常に近く、これが分子動力学理論の実用的な価値の理由です。これらのアイデアに基づいて、統計的アプローチを使用して、マクスウェルは、後に彼にちなんで名付けられた、限られた体積内のガス分子の速度の分布を導き出しました。 この分布は、図にグラフで示されています。 温度 100 および 1000 で水素の特定の質量に対して 7
° C. 縦軸は、横軸に示された速度で移動する分子の数を表します。 粒子の総数は、各曲線の下の面積に等しく、どちらの場合も同じです。 グラフから、ほとんどの粒子はある平均値に近い速度を持ち、ごく少数の粒子のみが非常に高速または低速であることがわかります。 これらの温度での平均速度は、2000 ~ 3000 m/s の範囲にあります。 非常に大きい。このような急速に移動する多数のガス分子は、周囲の物体に完全に測定可能な力で作用します。 多数のガス分子が容器の壁に衝突する微視的な力は、圧力と呼ばれる巨視的な量になります。 ガスにエネルギーが供給されると (温度が上昇する)、その分子の平均運動エネルギーが増加し、ガス粒子が壁に衝突する頻度が高くなり、圧力が上昇します。ガスの量が増えます。 このように、分子動力学理論の根底にある微視的統計的アプローチにより、これまで議論してきた熱膨張の現象を説明することが可能になります。
分子動力学理論のもう 1 つの結果は、上記の要件を満たすガスの特性を記述する法則です。 これがいわゆる状態方程式 理想気体 1モルのガスの圧力、体積、温度を結び、等式の形をしています
PV = RT ここで P プレッシャー、 Vボリューム、 T 温度、および R (8.31441 に等しい普遍的なガス定数± 0.00026) J/(mol H に)。 こちらもご覧ください分子動力学理論;熱力学。 熱伝達 熱伝達とは、温度差により、物体内または物体間で熱が移動するプロセスです。 熱伝達の強度は、物質の特性、温度差に依存し、実験的に確立された自然の法則に従います。 効率的な加熱または冷却システム、さまざまなエンジン、発電所、断熱システムを作成するには、熱伝達の原理を知る必要があります。 熱交換が望ましくない場合 (溶解炉、宇宙船などの断熱) もあれば、可能な限り大きくする必要がある場合 (蒸気ボイラー、熱交換器、台所用品) もあります。熱伝達には、伝導、対流、放射熱伝達の 3 つの主なタイプがあります。
熱伝導率。 体内に温度差があると、熱エネルギーは熱い部分から冷たい部分へと移動します。 分子の熱運動と衝突によるこのタイプの熱伝達は、熱伝導率と呼ばれます。 十分に 高温固体では視覚的に観察できます。 そのため、ガスバーナーの炎の中で鋼棒が一方の端から加熱されると、熱エネルギーが棒を介して伝達され、加熱された端から一定の距離で輝きが広がります(場所からの距離に応じて強度が弱くなります)暖房)。熱伝導率による熱伝達の強さは、温度勾配に依存します。 関係
D T/D バツ ロッドの両端の温度差とそれらの間の距離。 また、ロッドの断面積にも依存します(m 2 ) と材料の熱伝導率[ 対応する単位で W/(m Ch K) ] . これらの量の間の関係は、フランスの数学者 J. フーリエによって導き出され、次の形式をとっています。どこ q 熱流、 k 熱伝導率、および あ 断面積。 この関係はフーリエの熱伝導の法則と呼ばれます。 その中のマイナス記号は、熱が温度勾配とは反対の方向に伝達されることを示します。フーリエの法則から、熱伝導係数、面積、または温度勾配のいずれかの量を減らすことで熱流束を減らすことができることがわかります。 冬の状態の建物の場合、後者の値は実質的に一定であるため、部屋の温度を維持するために、壁の熱伝導率を下げる必要があります。 断熱性を向上させます。
この表は、いくつかの物質と材料の熱伝導率係数を示しています。 この表は、一部の金属が他の金属よりもはるかに熱を伝導することを示していますが、それらはすべて空気や多孔質材料よりもはるかに優れた熱伝導体です.
|
いくつかの物質と材料の熱伝導率 |
|
|
物質と材料 |
熱伝導率、W / (m × K) |
| アルミニウム | |
| ブロンズ | |
| ビスマス | |
| タングステン | |
| 鉄 | |
| 金 | |
| カドミウム | |
| マグネシウム | |
| 銅 | |
| 砒素 | |
| ニッケル | |
| 白金 | |
| 水星 | |
| 鉛 | |
| 亜鉛 | |
|
その他の資料 |
|
| アスベスト | |
| コンクリート | |
| 空気 | |
| アイダーダウン(緩い) | |
| 木の実) | |
| マグネシア (MgO) | |
| おがくず | |
| ゴム(スポンジ) | |
| 雲母 | |
| ガラス | |
| カーボン(グラファイト) | |
多くの物質の熱抵抗と電気抵抗は、温度が液体ヘリウムの温度 (1.8 K) を下回ると急激に低下します。 超電導と呼ばれるこの現象は、マイクロ電子デバイスから電力線、大型電磁石まで、多くのデバイスの効率を改善するために使用されます。 こちらもご覧ください超伝導性。
対流。 すでに述べたように、液体または気体に熱が加えられると、分子の運動の強度が増し、その結果、圧力が増加します。 液体または気体の体積が制限されていない場合、それらは膨張します。 液体 (気体) の局所的な密度が低くなり、浮力 (アルキメデス) の力により、媒体の加熱された部分が上に移動します (これが、室内の暖かい空気が電池から天井まで上昇する理由です)。 この現象は対流と呼ばれます。 暖房システムの熱を無駄にしないためには、強制空気循環を提供する最新のヒーターを使用する必要があります。ヒーターから加熱された媒体への対流熱流は、分子の初速度、密度、粘度、熱伝導率と熱容量、および媒体に依存します。 ヒーターのサイズと形状も非常に重要です。 対応する量の比率はニュートンの法則に従います
q = hA ( TW- )、ここで q 熱流(ワットで測定)、 あ 熱源の表面積(m 2), TWと T ソースとその環境の温度 (ケルビン単位)。 対流熱伝達係数 時間 媒体の特性、分子の初期速度、および熱源の形状に依存し、単位は W/(m 2時間 に)。価値
時間 は、ヒーターの周囲の空気が静止している場合 (自然対流) と、同じヒーターが空気の流れの中にある場合 (強制対流) では異なります。 パイプを通る流体の流れまたは平らな表面の周りの流れの単純なケースでは、係数 時間 理論的に計算できます。 しかし、媒体の乱流の対流の問題に対する解析的な解決策を見つけることはまだ可能ではありませんでした。 乱流は液体(気体)の複雑な動きであり、分子のものを大幅に超えるスケールで混沌としています。加熱された(または逆に冷たい)物体が静止媒体または流れの中に置かれると、対流と境界層がその周囲に形成されます。 この層内の分子の温度、圧力、および速度は、対流熱伝達係数を決定する上で重要な役割を果たします。
対流は、熱交換器、空調システム、高速航空機、その他多くのアプリケーションの設計において考慮する必要があります。 このようなすべてのシステムでは、熱伝導は固体間およびその環境の両方で対流と同時に発生します。 で 高温放射熱伝達も重要な役割を果たします。
放射熱伝達。 3番目のタイプの熱伝達放射熱伝達は、この場合の熱は真空を介して伝達できるという点で、熱伝導および対流とは異なります。 他の熱伝達方法との類似点は、温度差によるものでもあるということです。 熱放射はタイプの 1 つです。 電磁放射. 他のタイプの電波、紫外線、ガンマ線は、温度差がない場合に発生します。図上。 図8は、波長に対する熱(赤外線)放射のエネルギーの依存性を示す。 熱放射は可視光の放出を伴うことがありますが、そのエネルギーはスペクトルの目に見えない部分の放射エネルギーと比較して小さいです。
熱伝導と対流による熱伝達の強さは温度に比例し、放射熱流束は温度の 4 乗に比例し、ステファン ボルツマンの法則に従います。
住宅やオフィスのスペースは、多くの場合、小型の電気ヒーターで加熱されています。 それらの渦巻きの赤みを帯びた輝きは、スペクトルの赤外線部分の端に近い目に見える熱放射です。 部屋は、主に放射の目に見えない赤外線部分によって運ばれる熱によって加熱されます。 暗視装置で
^ このカメラは、熱放射源と赤外線に敏感な受信機を使用しているため、暗闇でも見ることができます。太陽は熱エネルギーの強力なエミッターです。 1 億 5000 万 km の距離でも地球を加熱します。 地球上の多くの場所にある観測所で毎年記録されている太陽放射の強度は、約 1.37 W です。
/m2 . 太陽エネルギーは地球上の生命の源です。 それを最も効果的に使用する方法が模索されています。 住宅を暖房し、家庭のニーズに合わせて電力を生成するために、ソーラー パネルが作成されました。 熱の役割とその利用 地球全体の熱伝達プロセスは、太陽放射による地球の加熱に還元されません。 大気中の大規模な対流は、世界中の気象条件の日々の変化を決定します。 赤道域と極域の間の大気の温度差は、地球の自転によるコリオリ力とともに、貿易風、ジェット気流、温暖前線や寒冷前線など、絶えず変化する対流の出現につながります。 こちらもご覧ください気候; 気象学と気候学。地球の溶融コアからその表面への熱の伝達 (熱伝導率による) は、火山噴火と間欠泉の出現につながります。 一部の地域では、暖房や発電に地熱エネルギーが使用されています。
熱は、ほぼすべての生産プロセスに不可欠な要素です。 金属の製錬と加工、エンジンの操作、食料生産、化学合成、石油精製、レンガや皿から自動車や電子機器に至るまで、さまざまな物の製造など、それらの中で最も重要なものに言及しましょう。
多くの工業生産と輸送、および火力発電所は、熱機関 (熱を有用な仕事に変換する装置) なしでは機能しません。 このような機械の例としては、コンプレッサー、タービン、蒸気、ガソリン、ジェット エンジンなどがあります。
最も有名な熱機関の 1 つは、現代の発電所で使用されるランキン サイクルの一部を実装する蒸気タービンです。 このサイクルの簡略図を図 1 に示します。 9. 作動流体の水は、化石燃料 (石炭、石油、または天然ガス) の燃焼によって加熱された蒸気ボイラーで過熱蒸気に変換されます。 蒸気 高圧電気を発生させる発電機を駆動する蒸気タービンのシャフトを回転させます。 排気蒸気は、ランキン サイクルで使用されなかった熱の一部を吸収する流水によって冷却されると凝縮します。 次に、水は冷却塔(冷却塔)に供給され、そこから熱の一部が大気中に放出されます。 凝縮液は蒸気ボイラーにポンプで戻され、サイクル全体が繰り返されます。
ランキン サイクルのすべてのプロセスは、上記の熱力学の原理を示しています。 特に、第 2 法則によれば、発電所で消費されるエネルギーの一部は、熱の形で環境に放散されなければなりません。 このようにして、化石燃料にもともと含まれていたエネルギーの約68%が失われていることが判明。 発電所の効率の顕著な向上は、蒸気ボイラーの温度を上げるか(材料の熱抵抗によって制限されます)、または熱が移動する媒体の温度を下げることによってのみ達成できます。 雰囲気。
を有する別の熱力学的サイクル 非常に重要私たちの中で 日常生活、ランキン蒸気圧縮機冷凍サイクルであり、その図を図1に示します。 10. 冷蔵庫や家庭用エアコンでは、エネルギーを外部から供給して提供しています。 コンプレッサーは、冷蔵庫のフレオン、アンモニア、または二酸化炭素の作動物質の温度と圧力を上昇させます。 過熱されたガスはコンデンサーに供給され、そこで冷却されて凝縮され、環境に熱を放出します。 凝縮器のノズルを出た液体は、絞り弁を通って蒸発器に入り、その一部が蒸発します。これには、温度の急激な低下が伴います。 蒸発器は冷凍室から熱を奪い、ノズル内の作動流体を加熱します。 この液体はコンプレッサーによってコンデンサーに供給され、サイクルが再び繰り返されます。
図に示す冷凍サイクル。 10はヒートポンプにも使用できます。 このようなヒートポンプは、夏は暖かい空気に熱を放出して室内を調湿し、冬は逆に冷たい空気から熱を奪って部屋を暖めます。
核反応は、発電や輸送などの目的のための重要な熱源です。 1905 年に、A. アインシュタインは、質量とエネルギーが次の関係によって関連付けられることを示しました。
E=mc2 、つまり 互いに通過することができます。 光の速度 c 非常に大きい: 30 万 km/ と。 これは、少量の物質でも膨大な量のエネルギーを提供できることを意味します。 したがって、1kgの核分裂性物質(ウランなど)からエネルギーを得ることが理論的には可能であり、これは1000日間の連続運転で1MWの容量の発電所によって提供されます。 こちらもご覧ください原子構造; 炉および炉技術; 電磁放射;熱交換器; タービン; 物理量の測定単位。文学 ゼマンスキー M. 気温が非常に高く、非常に低い. M.、1968ポール R. 力学、音響学、および熱の教義. M.、1971
スモロディンスキー 温度. M.、1981
ファン J. 機械、エネルギー、エントロピー. M.、1986
アトキンス P.V. 自然界の秩序と無秩序。 M.、1987
液体熱量計
このタイプの熱量計は、テクノロジーで最も広く使用されており、設計がシンプルで保守が容易です。 外部から誘導された反応によって生成された熱量は、最初に反応容器 (反応が行われた) に伝達され、次に液体槽に伝達されます。 浴槽内の液体は、インペラー、昇降スクリュー、またはポンプによって連続的に攪拌され、温度の均一化が促進されます。 バスは可能な限り環境から断熱 (シールド) されています。 液体槽の温度変化は、検出された熱量の尺度です。 十分な温度変化を確保し、測定プロセスが長くなりすぎないようにするために (熱損失が増加するため)、加熱される質量の熱容量が高すぎてはなりません。
図 液体熱量計のデバイス。
周囲条件の一定性に対する高い要件により、熱量計全体を別の槽に配置し、制御ループを使用して高精度で温度を安定させることができます。 これは、周囲温度と大幅に異なる温度で実験を行う必要がある場合にまず必要です。
低温(約-150℃まで)での分析では、冷却媒体として液体窒素が使用されます。 この場合、それらを交換するときに、その層が測定プロセスに影響を与える可能性があるため、周囲の湿った空気からの霜がサンプルまたはサンプル容器に沈殿しないことに注意する必要があります。 これを避けるために、熱量計が開いているとき、サンプルとサンプル容器は冷たい窒素ガスでパージされます。
金属体熱量計
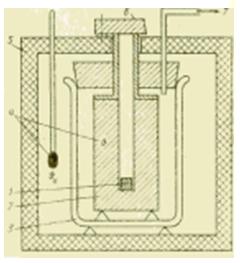
図 金属熱量計のデバイスのスキーム。
より広い温度範囲で熱量分析を行う必要がある場合、液体熱量計はもはや適していません。 この目的に適した金属体熱量計では、伝達される熱量は、通常周囲温度の金属ブロック (銀、銅、アルミニウム) によって吸収されます。 このような熱量計は、主に比熱容量c、J /(kg * K)、液体および固体物質を決定することを目的としています。
サンプルは、最初に熱量計の外で冷却されます。 冷凍プラントまたは炉で加熱し、定常状態に達した後、金属ブロックの穴に降ろします(落とします)。 操作方法によれば、このようなデバイスは自由落下熱量計と呼ばれ、その中の熱力学的プロセスの性質に応じて、変位熱量計と呼ばれることもあります。
この混合中にサンプル (パラメーター m1、c1、 ) から金属ブロック (m2、c2、 ) に伝達される熱量は、ブロックの温度に測定可能な変化を引き起こします。 これにより、サンプルの比熱容量の通常未知の値を決定することができます。 理想的な条件(環境との熱交換がない場合)式から:
金属ブロック自体は、真空のデュワー容器内にあり、場合によっては液体槽内にあります。 後者の場合、熱量計 Ck の熱容量を得るには、浴の熱容量 Cw を金属ブロック C2 の熱容量に追加する必要があります。
CK=C2+CW=c2m2+cWmW .
熱量測定法
ほとんどの場合、熱量計は一定の環境条件のモードで使用されます。 これは、反応時間が非常に短いほとんどの燃焼熱量計に最初に適用されます. 熱量計の内部部品の温度は反応によって変化しますが、周囲温度は一定のままです. 多くの場合、温度制御された外部干渉の測定値への影響を避けるために、環境としてバスが使用されます - 室内の温度変動、放射線、ドラフトなど。
この測定方式の利点は、熱量測定の大部分を実行するために使用できる機器のコストが比較的低いことです。 主な欠点は、結果の解釈を複雑にする環境との熱量計の熱交換を考慮する必要があります。 この測定方法は常に isoperibol (diathermic) と呼ばれます。 いずれにせよ、それは等温とは言えません。その本質は、例えば相転移を測定するように設計された熱量計のように、反応の過程で熱量計の温度が一定のままであるという事実にあります。
断熱法
環境との熱交換を排除できる場合、つまり、プロセスの断熱過程を確保することができれば、実験と結果の解釈が簡素化され、継続的に記録する必要がないため、測定結果がより正確になります。温度変化を計算し、補正を計算します。 さらに、この場合、熱量計容器内の温度が多少上昇しても許容できます。 非断熱デバイスの場合、熱損失が増加するため、これは受け入れられません。
熱量計容器とその周囲 (通常は液体浴) との間の熱伝達を避けるために、容器内の温度変化に応じて浴の温度を常に調整する必要があります。 電子コントローラー(追跡回路)の助けを借りて、これらの温度差を実質的にゼロに常に維持することができます。 これにより、必要な測定精度に応じて測定機器のコストが増加します。
ハードウェア要素は、高速で長時間安定している必要があります (ドリフトが最小限に抑えられている)。 トラッキング制御ループの不感帯は、±10-3 ~ ±10-5 K の範囲内にある必要があります。測定デバイスとして、ブリッジ回路に含まれている場合、応答の速い電気接触式温度計を使用できます。コントローラーへの衝動が加熱電力を変更します。 加熱は、電気抵抗コイルを使用するか、液体槽内で直接実行されます。これは、弱い解離による加熱抵抗器として機能します (いわゆる電解加熱)。 この 2 番目の方法は、実質的に慣性がありません。 結果は、既存の電気温度測定手段を使用するか、追加で設置された液体温度計 (Beckmann) を使用して取得できます。
断熱測定法は、主に遅いプロセスと熱効果の研究に適しています。 (燃焼熱量計での)熱量の急激な変化により、温度均一化の慣性は、従来の非断熱方法の精度でさえ達成できないほどの不利な効果をもたらします。 ただし、発熱体と温度センサーの熱容量を小さくし、浴液の集中的な混合を行うと、さまざまな時定数の小さな値を得ることができます(慣性を減らすため)。
補償方法
補償の原理に基づく示差熱量計またはデュアル熱量計を使用すると、測定プロセスに対する外部の影響を大幅に排除できます。 同一のアクセサリを備えた 2 つの同一の熱量測定容器が、同じ条件下の環境に置かれています。 一方の容器では、熱効果を伴う調査プロセスが発生し、もう一方の容器は、両方の容器の環境への熱損失が同じになるように、サーボ制御システムを使用して加熱されます。 したがって、入力加熱電力は、研究中のプロセス中に放出される熱量に正比例することができます。 この場合、測定の実験的タスクは別の領域に入り、供給された電気加熱電力(W * s、J)の非常に正確な決定に縮小されます。
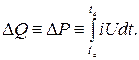
示差熱量計は、特に断熱周囲条件下で、特に熱量の変化が非常に小さいか非常に遅いことが予想される場合に使用されます。 吸熱プロセスでは、熱量測定容器が 1 つあれば十分です。 熱入力は、容器内の温度が常に同じに保たれるように制御されます (等温法)。 示差熱量計の欠点は、機器や測定器のコストが高いことです。
燃焼熱量計
熱電設備で使用される燃料を調べて、その発熱量H(J/kg)を求めます。 この指標は、効率係数を決定し、さまざまな設備で消費されるエネルギーの効率と計算を研究し、燃焼プロセスを最適に制御するために必要です。 可燃性成分の組成が大きく変動する場合は、発熱量を継続的に測定する必要があります。
物質が完全に燃焼すると、一定量の熱Q(燃焼熱)が放出されます。 それを質量 m (または通常の状態での体積 Vn) で割ると、(比) 燃焼熱が得られます。
燃焼生成物の状態により、高H0と低Hの2種類の発熱量が区別され、燃焼熱や発熱量とも呼ばれます。 Ni の正味の発熱量を決定する際に、生成された水 化学反応蒸気状態でなければなりません。 両方の熱 H0 - Ni の差は、凝縮水の気化熱 (インデックス KO - 凝縮液) r に対応し、これは 2.441 MJ / kg に相当します。
固体燃料と液体燃料の場合、結果として生じる水の量は、元素分析に基づいて決定できます。また、気体燃料を燃焼させる場合は、凝縮物の量を測定することによって決定できます。
工業炉では、燃焼生成物の温度は常に水の沸点を超えています。 したがって、水の凝縮熱は使用できないため、通常は正味発熱量 Ni のみが重要です。
固体と液体の燃焼熱量計
高速燃焼プロセスのために、特別な形式の液体熱量計が開発されました-いわゆるBerthelot熱量計ボンベ(図3)。
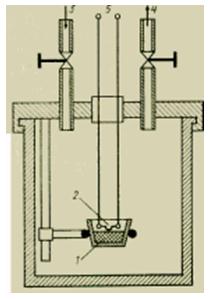
Figure カロリメトリック爆弾の装置。
正確に測定された少量の物質の燃焼は、密閉されたボンベ内で、圧力が約 30 気圧 (3 MPa) の可能な限り純粋な酸素の雰囲気内で一定の体積で発生します。 充填されたボンベは熱量計の液体槽に入れられ、放出された燃焼熱を吸収します。
固体通常、小さなブリケット (錠剤) に圧縮され、非常に正確に計量されます。 燃焼しにくい物質と、既知の燃焼熱を持つよく燃焼する液体(安息香酸など)を混合することをお勧めします。 液体物質は、プラチナまたはクォーツで作られたカップ(ボート)または小さなプラスチックカプセルに入れられます。 爆弾の本体にボルトで固定されたカバーには、研究に必要なすべてのデバイスがあります。酸素を供給し、燃焼生成物を除去するためのバルブ、サンプルホルダー、電気点火器です。 点火は細い白金線に通電することで行います。 点火に供給される熱は、実験結果を解読する際に考慮できるように、正確に測定する必要があります。 熱量爆弾では、最高発熱量 H0 が決定されます。 検証中、熱量計 Ck の熱当量は、参照物質 (安息香酸など) を燃焼させるか、電気加熱装置を使用して決定されます。
ガス状物質の燃焼熱量計
気体媒体の燃焼熱を決定するには、さまざまな方法があります。 それらはすべて、固体および液体物質の比色爆弾とは対照的に、連続測定に基づいています。 使用される測定原理は非常に単純です。 テストガスは、一定の圧力でバーナーで連続的に燃焼されます。 燃焼中に放出されるすべての熱は、熱交換器内の冷却媒体の流れによって (湿式または熱交換熱量計)、または既知の流量で燃焼生成物を空気流と混合することによって (乾式または混合熱量計) 吸収されます。 通常、正味の発熱量 Hu を決定します。 総発熱量 H0 を求めるには、排ガスに含まれる水蒸気 (指数 KO) を凝縮する必要があります。 熱量計の入口 (インデックス e) と出口 (インデックス a) での質量流量と温度差がわかれば、熱収支方程式を使用して対応する発熱量を計算することができます。
必要なガス準備は、基本的にすべてのガス熱量計で同じです。 燃焼前に、ガス(インデックスG)は最初に(フィルター内の)固体の機械的不純物が取り除かれ、湿らせられ(水分で飽和するまで、100%)、次に予備圧力の指定された値になります(減圧を使用)バルブ) と冷却媒体の温度 (インデックス K) 。 燃焼に必要な空気 (インデックス L) も加湿され、冷却媒体の温度になります。
必要な精度と許容される計測コストによっては、これらの条件の一部が満たされない場合があります。 熱量計は、熱量計の理想的な状態の方程式からの偏差を決定するために、基準ガス (水素など) で検証する必要があります。 熱交換 (湿式) 熱量計の場合、上記の式は次の形式になります。
ここで、 と は冷却媒体と燃料の質量流量、kg/s です。 sk - 冷却媒体の比熱容量、J / (kg * K); - 冷却媒体の温度の上昇、K.
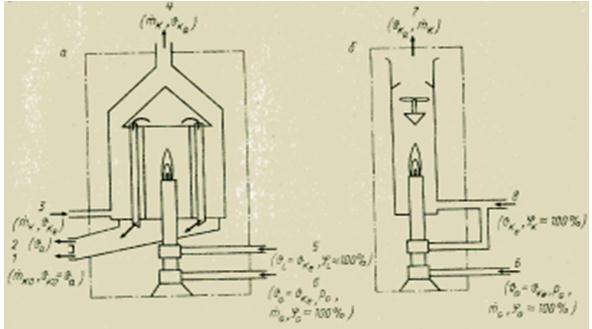
図 気体燃料用の湿式 (a) および乾式 (b) 熱量計の装置。
温度上昇は通常 5 ~ 15 K です。熱量が大きいため、伝熱熱量計の時定数は非常に長く、最大で数分かかる場合があります。 したがって、時定数がわずか数秒の乾式 (混合) 熱量計よりも、クローズド制御ループでのセンサーとしての使用には適していません。 一方、熱交換熱量計の達成可能な精度は比較的高いです。 誤差は±0.25~1%を超えないため、実験室での作業や検証にも使用できます。 乾式熱量計(混合)は測定範囲上限の±1~±2%の誤差があります。
さまざまなメーカーの熱量計の設計バージョンは、主に補助デバイスと安全デバイス、検出要素、および誤差補正を提供する計算回路が異なります。 したがって、熱交換熱量計では、ガスと冷却媒体の流量の比率はさまざまな方法で維持されます (上記の熱量計の式を参照)。これにより、より高い発熱量 H0 は温度上昇のみに直接依存します。
乾式熱量計では、温度上昇は、電気接触温度計を使用して直接測定するか、膨張計センサー (排気ガス流に配置された膨張管) を使用して間接的に測定します。 ADOS熱量計では、膨張計チューブの熱伸びは燃焼熱に直接対応し、リンケージと長さゲージを使用して任意の信号に変換できます。 ライネッケ熱量計では、温度の上昇がほぼ一定に保たれるように冷却空気の流れを制御する制御回路で、ロッドの伸びが測定信号として使用されます。 この場合、制御ループは純粋に比例することがわかりますが、ある程度の残留偏差は避けられません。 この場合、冷却空気の消費量または膨張チューブ (ロッド) の伸びが、決定された発熱量の尺度となります。 すべての乾式熱量計で十分な精度を得るための前提条件は、冷却空気と燃焼生成物の良好な混合です。
熱流測定
エネルギーの形態としての熱は、固体 (熱伝導)、液体または気体媒体 (対流)、および物質の関与なし (放射) の 3 つの方法で伝達されます。 テクノロジーでは、ほとんどの場合、3 つのコンポーネントすべてが熱の伝達に関与しています。 ただし、多くの場合、1 つのコンポーネントのみを測定することで、許容できる精度の結果を得ることができます。
計測 熱流熱伝導率あり
熱伝導壁を介した熱伝達は、多くの技術分野 (あらゆる種類の熱交換器、断熱材など) で非常に重要です。 同時に、関心のあるのは生産量の現在の制御ではなく、負荷を評価し、保証された指標と効率の達成を検証するために使用される単一の測定の結果です。
定常熱伝導の法則によると、熱流束は次の式 (J/s) によって決定されます。
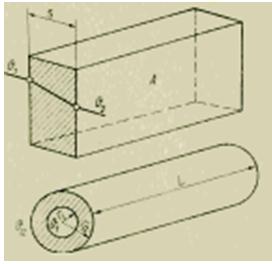
壁の熱伝導率 [J/(m*s*K)] とその幾何学的寸法が既知であるため、熱流束の測定は温度差の測定に還元されます。 ただし、この手法では、表面温度を非常に正確に測定する必要があります。 温度に敏感な要素を表面に取り付けるときの熱伝達条件の変化に関連するエラーは、非常に大きくなる可能性があります。 したがって、より正確な測定を行うには、熱伝導率と熱伝達を同時に使用する次の方法が推奨されます。
伝熱(熱伝導を伴う伝熱)における熱流の測定
前のセクションで説明した平らな壁の場合、次の熱伝達法則 (J/s) が有効です。
![]() ,
,
ここで、熱伝達係数 k 1J/(m2*s*K)]、熱伝達係数 [J/Dm*s*K)]、熱伝達係数および [J/(m2*s*K)壁の両側の ] も考慮されます。
測定された熱流束が通過する平らな壁に小さな薄いプレートが置かれ、その表面温度は内蔵の薄膜熱電対によって決定されます。 この方法で測定する利点は、壁の熱特性を知る必要がなく、対応するプレートの特性をキャリブレーション中に単一の一定値に減らすことができることです。 このような敏感な要素のサイズは約 30x30x0.5 mm です。 測定範囲は、10 ~ 100,000 W/m2 の熱流束をカバーします。 誤差は 2 ~ 5% です。
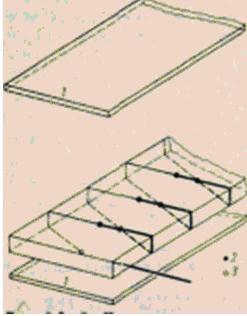
図 熱流束計の動作原理。
この測定方法の改良により、重ね板の代わりにゴムマットが使用されます。 それらを非平面に接着したり、曲面に巻き付けたりすることにより、パイプ、容器などの比較的広い面積の表面からの熱伝達を決定することができます。熱電対は両方の表面に組み込まれていますマットのホット ジャンクションとコールド ジャンクションが互いに正確に接するようにします (図 6)。 そしてこの場合、校正による熱流束密度は温度差に比例します。 ただし、適用されたマットは、正確な測定で目立つようになる初期の熱伝達をいくらか妨げます。 したがって、この測定方法は、熱流の違反が測定結果に影響を与えない場合に、主に物質の熱力学的定数を決定するために使用されます。
現在の環境における熱流の測定。
熱エネルギーの大部分は、閉じたパイプライン ネットワーク内を移動する液体または気体の媒体 (水、蒸気など) によって伝達されます。 ただし、電線による電気エネルギーの伝送と比較して、熱エネルギーを伝送できる距離は限られています。 あらゆるタイプの加熱および冷却システムの熱工学研究では、熱の放出と消費を測定する必要があります。
媒体の流れによって伝達される熱流束 F (J/s) - 熱収支がまとめられている特定のゾーン内の領域 A (m2) の制御セクションを通る熱媒体 (kg/s) (kg/s)プロセス ゾーン、図 7) は次のようになります。
時間間隔 t2 - t1 の間に放出される熱量は、積分 (J) として決定されます。
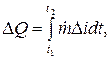
ここで、 は、熱平衡ゾーンの入口 (インデックス e) と出口 (インデックス a) での冷媒の熱量 (エンタルピー、J/kg) の差です。
一般に、エンタルピーの値は、たとえば周囲温度でのエンタルピーなど、特定のレベルと比較する場合にのみ重要であるため、熱流束のすべての測定値は本質的に差分測定値です。
一般式に含まれる個々のエンタルピーは、対応する温度と比熱容量で表すことができます。
したがって、熱流の測定は、温度と質量流量の測定に直接還元されます。 多くの場合、冷媒の質量ではなく体積流量が測定されます。 この場合、得られる結果は、冷媒密度 р の値だけ異なります。 比熱容量 ci は、それ自体が温度の関数です。 ただし、多くの機器の測定範囲が狭いため、通常、精度をあまり損なうことなく一定の値と見なすことができます。 比熱容量を知る必要があります。 液体の場合、熱流方程式はさらに単純化されます。 比熱容量圧力に依存しない:
![]() 、J/s。
、J/s。
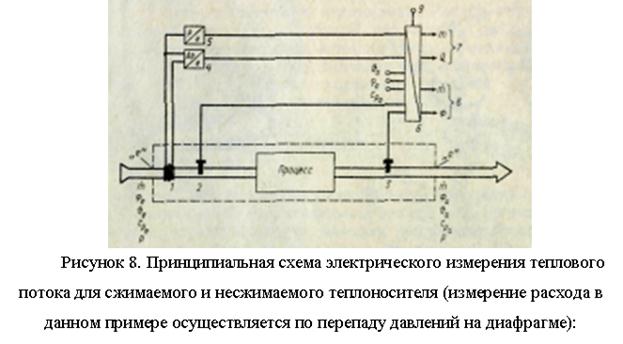
このタイプのすべての方程式では、熱が供給されるか除去されるか、プロセスが吸熱か発熱か、冷却または加熱が発生するかどうかに応じて、量の符号を考慮する必要があります。
