Jumlah panas dalam sistem SI diukur. Metode dan cara mengukur jumlah panas
Panas- energi yang ditransfer dari benda yang lebih panas ke benda yang kurang panas melalui kontak langsung atau radiasi.
Suhu adalah ukuran intensitas gerakan molekul.
Jumlah panas yang dimiliki oleh suatu benda pada suhu tertentu tergantung pada massanya; Misalnya, pada suhu yang sama, lebih banyak panas disimpan dalam secangkir besar air daripada di yang kecil, dan dalam seember air dingin bisa lebih banyak daripada di cangkir. air panas(walaupun suhu air dalam ember lebih rendah).
Panas memegang peranan penting dalam kehidupan manusia, termasuk dalam fungsi tubuhnya. Bagian dari energi kimia yang terkandung dalam makanan diubah menjadi panas, sehingga suhu tubuh dipertahankan mendekati 37 ° C. Keseimbangan panas tubuh manusia juga tergantung pada suhu. lingkungan, dan orang-orang terpaksa menghabiskan banyak energi untuk memanaskan tempat tinggal dan industri di musim dingin dan mendinginkannya di musim panas. Sebagian besar energi ini dipasok oleh mesin panas, seperti pembangkit boiler dan turbin uap pembangkit listrik yang menggunakan bahan bakar fosil (batubara, minyak) dan menghasilkan listrik.
Sampai akhir abad ke-18. panas dianggap sebagai zat material, percaya bahwa suhu tubuh ditentukan oleh jumlah<калорической жидкости>, atau<теплорода>. Belakangan, B. Rumford, J. Joule dan fisikawan lain pada masa itu, melalui eksperimen dan penalaran yang cerdas, membantah<калорическую>teori, membuktikan bahwa panas tidak berbobot dan dapat diperoleh dalam jumlah berapa pun hanya karena gerakan mekanis. Panas itu sendiri bukanlah suatu zat - itu hanya energi dari pergerakan atom atau molekulnya. Pemahaman tentang panas inilah yang dianut oleh fisika modern.
Pada artikel ini, kita akan melihat bagaimana panas dan suhu terkait dan bagaimana kuantitas ini diukur. Subjek diskusi kita juga akan menjadi pertanyaan berikut: perpindahan panas dari satu bagian tubuh ke bagian lain; perpindahan panas dalam ruang hampa (ruang yang tidak mengandung materi); peran panas di dunia modern.
Panas dan suhu
Jumlah energi panas dalam suatu zat tidak dapat ditentukan dengan mengamati pergerakan masing-masing molekulnya secara terpisah. Sebaliknya, hanya dengan mempelajari sifat makroskopik materi, seseorang dapat menemukan karakteristik gerakan mikroskopis dari banyak molekul yang dirata-ratakan selama periode waktu tertentu. Suhu suatu zat adalah indikator rata-rata intensitas pergerakan molekul, yang energinya adalah energi termal zat.
Salah satu cara yang paling akrab, tetapi juga paling tidak akurat untuk memperkirakan suhu adalah dengan sentuhan. Menyentuh suatu objek, kita menilai apakah itu panas atau dingin, dengan fokus pada perasaan kita. Tentu saja, sensasi ini bergantung pada suhu tubuh kita, yang membawa kita pada konsep kesetimbangan termal - salah satu yang paling penting dalam mengukur suhu.
Kesetimbangan termal
Kesetimbangan termal antara benda A dan B
Jelas, jika dua benda A dan B ditekan erat satu sama lain, maka, setelah menyentuhnya setelah waktu yang cukup lama, kita akan melihat bahwa suhunya sama. Dalam hal ini, benda A dan B dikatakan dalam kesetimbangan termal satu sama lain. Namun, benda, secara umum, tidak harus bersentuhan agar keseimbangan termal ada di antara mereka - cukup suhunya sama. Ini dapat diverifikasi menggunakan benda ketiga C, pertama-tama membawanya ke kesetimbangan termal dengan benda A, dan kemudian membandingkan suhu benda C dan B. Benda C di sini berperan sebagai termometer. Dalam formulasi yang ketat, prinsip ini disebut hukum termodinamika ke-nol: jika benda A dan B berada dalam kesetimbangan termal dengan benda ketiga C, maka benda-benda ini juga berada dalam kesetimbangan termal satu sama lain. Hukum ini mendasari semua metode pengukuran suhu.
Pengukuran suhu

Skala suhu

termometer
Termometer berdasarkan efek listrik
Jika kita ingin melakukan eksperimen dan perhitungan yang akurat, maka peringkat suhu seperti panas, hangat, dingin, dingin tidak cukup - kita memerlukan skala suhu bertingkat. Ada beberapa skala seperti itu, dan titik beku dan titik didih air biasanya diambil sebagai titik acuan. Empat skala yang paling umum ditunjukkan pada gambar. Skala celcius, yang menyatakan titik beku air sesuai dengan 0 °, dan titik didih hingga 100 °, disebut skala Celsius yang dinamai A. Celsius, seorang astronom Swedia yang menggambarkannya pada tahun 1742. Dipercaya bahwa Naturalis Swedia K. Linnaeus pertama kali menerapkan skala ini. Sekarang skala Celcius adalah yang paling umum di dunia. Skala suhu Fahrenheit, di mana titik beku dan titik didih air sesuai dengan angka 32 dan 212 ° yang sangat merepotkan, diusulkan pada tahun 1724 oleh G. Fahrenheit. Skala Fahrenheit banyak digunakan di negara-negara berbahasa Inggris, tetapi hampir tidak digunakan dalam literatur ilmiah. Untuk mengubah suhu Celcius (°C) ke suhu Fahrenheit (°F), ada rumus °F = (9/5)°C + 32, dan untuk terjemahan terbalik - rumus °C = (5/9) ( °F-32).
Kedua skala - baik Fahrenheit dan Celsius - sangat merepotkan saat melakukan eksperimen dalam kondisi di mana suhu turun di bawah titik beku air dan dinyatakan sebagai angka negatif. Untuk kasus seperti itu, skala suhu absolut diperkenalkan, yang didasarkan pada ekstrapolasi ke apa yang disebut nol absolut - titik di mana gerakan molekul harus berhenti. Salah satunya disebut skala Rankin, dan yang lainnya disebut skala termodinamika absolut; suhu diukur dalam derajat Rankine (°R) dan kelvin (K). Kedua skala dimulai dari nol mutlak, dan titik beku air sesuai dengan 491,7 ° R dan 273,16 K. Jumlah derajat dan kelvin antara titik beku dan titik didih air pada skala Celcius dan skala termodinamika mutlak adalah sama dan sama sampai 100; untuk skala Fahrenheit dan Rankine juga sama, tetapi sama dengan 180. Derajat Celcius dikonversi ke kelvin menggunakan rumus K \u003d ° C + 273,16, dan derajat Fahrenheit dikonversi ke derajat Rankine menggunakan rumus ° R \u003d ° F + 459,7.
Pengoperasian perangkat yang dirancang untuk mengukur suhu didasarkan pada berbagai fenomena fisik yang terkait dengan perubahan energi panas suatu zat - perubahan hambatan listrik, volume, tekanan, karakteristik radiasi, sifat termoelektrik. Salah satu alat pengukur suhu yang paling sederhana dan paling dikenal adalah termometer kaca yang ditunjukkan pada gambar. Bola c di bagian bawah termometer ditempatkan dalam medium atau ditekan terhadap benda yang suhunya ingin diukur, dan tergantung pada apakah bola menerima panas atau melepaskannya, memuai atau mengerut dan kolomnya naik atau turun. kapiler. Jika termometer sudah dikalibrasi dan dilengkapi dengan timbangan, maka Anda bisa langsung mengetahui suhu tubuh.
Perangkat lain yang tindakannya didasarkan pada ekspansi termal adalah termometer bimetal yang ditunjukkan pada gambar. Elemen utamanya adalah pelat spiral dari dua logam yang disolder dengan koefisien ekspansi termal yang berbeda. Ketika dipanaskan, salah satu logam mengembang lebih dari yang lain, spiral memutar dan memutar panah relatif terhadap skala. Perangkat semacam itu sering digunakan untuk mengukur suhu udara dalam dan luar ruangan, tetapi tidak cocok untuk menentukan suhu lokal.
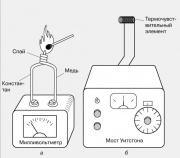
Temperatur lokal biasanya diukur menggunakan termokopel, yaitu dua kabel dari logam berbeda yang disolder di salah satu ujungnya. Ketika sambungan tersebut dipanaskan, EMF muncul di ujung kabel yang bebas, biasanya beberapa milivolt. Termokopel terbuat dari pasangan logam yang berbeda: besi dan konstantan, tembaga dan konstantan, kromel dan alumel. Termo-EMF mereka berubah hampir secara linier dengan suhu pada rentang suhu yang luas.
Efek termoelektrik lain juga diketahui - ketergantungan resistansi bahan konduktif pada suhu. Hal tersebut mendasari pengoperasian termometer hambatan listrik, salah satunya ditunjukkan pada gambar. Resistansi elemen penginderaan suhu kecil (termokopel) - biasanya gulungan kawat tipis - dibandingkan dengan resistansi resistor variabel yang dikalibrasi menggunakan jembatan Wheatstone. Instrumen keluaran dapat diluluskan secara langsung dalam derajat.
Pirometer optik digunakan untuk mengukur suhu benda panas yang memancarkan cahaya tampak. Dalam satu versi perangkat ini, cahaya yang dipancarkan oleh tubuh dibandingkan dengan radiasi filamen lampu pijar yang ditempatkan di bidang fokus teropong yang melaluinya tubuh pemancar dilihat. Arus listrik, yang memanaskan filamen lampu, diubah sampai, ketika secara visual membandingkan pancaran filamen dan bodi, ditemukan bahwa keseimbangan termal telah ditetapkan di antara keduanya. Skala perangkat dapat diluluskan secara langsung dalam satuan suhu.
Kemajuan teknis tahun terakhir diizinkan untuk membuat sensor suhu baru. Misalnya, dalam kasus di mana sensitivitas tinggi diperlukan, alih-alih termokopel atau termometer resistansi konvensional, perangkat semikonduktor digunakan - termistor. Pewarna dan kristal cair yang mengubah keadaan fasanya juga digunakan sebagai konverter termal, terutama dalam kasus di mana suhu permukaan tubuh bervariasi dalam rentang yang luas. Akhirnya, termografi inframerah digunakan, di mana gambar inframerah suatu objek diperoleh dalam warna bersyarat, di mana setiap warna sesuai dengan suhu tertentu. Metode pengukuran suhu ini menemukan aplikasi terluas - dari diagnosa medis sebelum memeriksa isolasi termal tempat.
Mengukur jumlah panas
kalorimeter air
Energi termal (jumlah panas) suatu benda dapat diukur secara langsung dengan apa yang disebut kalorimeter; Versi sederhana dari perangkat semacam itu ditunjukkan pada gambar. Ini adalah bejana tertutup yang diisolasi dengan hati-hati, dilengkapi dengan perangkat untuk mengukur suhu di dalamnya, dan kadang-kadang diisi dengan fluida kerja yang sifatnya diketahui, seperti air. Untuk mengukur jumlah panas dalam tubuh kecil yang dipanaskan, itu ditempatkan dalam kalorimeter dan menunggu sistem mencapai kesetimbangan termal. Jumlah panas yang ditransfer ke kalorimeter (lebih tepatnya, ke air yang mengisinya) ditentukan oleh peningkatan suhu air.
Jumlah panas yang dilepaskan selama reaksi kimia, seperti pembakaran, dapat diukur dengan menempatkan<бомбу>. PADA<бомбе>sampel berada, di mana kabel listrik untuk pengapian terhubung, dan jumlah oksigen yang sesuai. Setelah sampel benar-benar terbakar dan kesetimbangan termal tercapai, ditentukan berapa banyak suhu air dalam kalorimeter telah meningkat, dan karenanya jumlah panas yang dilepaskan.
Satuan panas
Kalor adalah salah satu bentuk energi dan oleh karena itu harus diukur dalam satuan energi. Dalam sistem SI internasional, satuan energi adalah joule (J). Juga diperbolehkan untuk menggunakan unit di luar sistem dari jumlah panas - kalori: kalori internasional adalah 4,1868 J, kalori termokimia adalah 4,1840 J. Di laboratorium asing, hasil penelitian sering dinyatakan menggunakan apa yang disebut. Kalori 15 derajat sama dengan 4,1855 J. British Thermal Unit (BTU) di luar sistem tidak digunakan lagi: BTU avg = 1,055 J.
Sumber panas
Sumber utama panas adalah reaksi kimia dan nuklir, serta berbagai proses konversi energi. Contoh reaksi kimia dengan pelepasan panas adalah pembakaran dan pemecahan komponen makanan. Hampir semua panas yang diterima oleh Bumi disediakan oleh reaksi nuklir yang terjadi di kedalaman Matahari. Umat manusia telah belajar bagaimana memperoleh panas dengan bantuan proses fisi nuklir terkontrol, dan sekarang mencoba menggunakan reaksi fusi termonuklir untuk tujuan yang sama. Jenis energi lain juga dapat diubah menjadi panas, seperti kerja mekanik dan energi listrik. Penting untuk diingat bahwa energi panas (seperti yang lainnya) hanya dapat diubah menjadi bentuk lain, tetapi tidak dapat diperoleh.<из ничего>, juga tidak merusak. Ini adalah salah satu prinsip dasar ilmu yang disebut termodinamika.
Termodinamika
Termodinamika adalah ilmu tentang hubungan antara panas, kerja, dan materi. Ide-ide modern tentang hubungan ini dibentuk atas dasar karya para ilmuwan besar di masa lalu seperti Carnot, Clausius, Gibbs, Joule, Kelvin, dan lain-lain.Termodinamika menjelaskan arti kapasitas panas dan konduktivitas termal suatu zat, ekspansi termal benda, dan panas transisi fase. Ilmu ini didasarkan pada beberapa hukum - prinsip yang ditetapkan secara eksperimental.
Panas dan sifat zat
Berbagai zat memiliki kemampuan yang berbeda untuk mengakumulasi energi panas; itu tergantung pada struktur molekul dan kepadatannya. Jumlah panas yang diperlukan untuk menaikkan suhu satu satuan massa suatu zat sebesar satu derajat disebut kapasitas panas spesifiknya. Kapasitas panas tergantung pada kondisi di mana zat itu berada. Misalnya, untuk memanaskan satu gram udara dalam balon sebesar 1 K, lebih banyak panas diperlukan daripada memanaskannya dengan cara yang sama dalam bejana tertutup dengan dinding kaku, karena sebagian energi yang diberikan ke balon dihabiskan untuk memperluas udara, dan bukan dengan memanaskannya. Oleh karena itu, khususnya, kapasitas panas gas diukur secara terpisah pada tekanan konstan dan pada volume konstan.
Dengan peningkatan suhu, intensitas pergerakan molekul yang kacau meningkat - sebagian besar zat mengembang saat dipanaskan. Derajat pemuaian zat dengan kenaikan suhu 1 K disebut koefisien ekspansi termal.
Agar suatu zat berpindah dari satu keadaan fase ke fase lainnya, misalnya, dari padat ke cair (dan kadang-kadang segera menjadi gas), ia harus menerima sejumlah panas. Jika dipanaskan padat, maka suhunya akan naik sampai mulai mencair; sampai peleburan selesai, suhu tubuh akan tetap konstan meskipun ada masukan panas. Banyaknya kalor yang diperlukan untuk melebur satu satuan massa suatu zat disebut kalor peleburan. Jika Anda terus memasok panas, maka zat cair akan memanas hingga mendidih. Jumlah panas yang diperlukan untuk menguapkan satu satuan massa cairan pada suhu tertentu disebut panas penguapan.
Peran panas dan penggunaannya
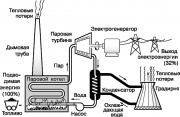
Skema operasi pembangkit listrik turbin uap
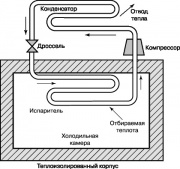
Diagram siklus pendinginan
Proses perpindahan panas global tidak direduksi menjadi pemanasan Bumi oleh radiasi matahari. Arus konveksi besar-besaran di atmosfer menentukan perubahan harian dalam kondisi cuaca di seluruh dunia. Perbedaan suhu di atmosfer antara daerah khatulistiwa dan kutub, bersama dengan gaya Coriolis akibat rotasi Bumi, menyebabkan munculnya arus konveksi yang terus berubah, seperti angin pasat, aliran jet, dan front hangat dan dingin.
Perpindahan panas (karena konduktivitas termal) dari inti cair Bumi ke permukaannya menyebabkan letusan gunung berapi dan munculnya geyser. Di beberapa daerah, energi panas bumi digunakan untuk pemanas ruangan dan pembangkit listrik.
Kehangatan adalah peserta yang sangat diperlukan di hampir semua proses produksi. Kami akan menyebutkan yang paling penting dari mereka, seperti peleburan dan pemrosesan logam, pengoperasian mesin, produksi makanan, sintesis kimia, penyulingan minyak, pembuatan berbagai barang - dari batu bata dan piring hingga mobil dan perangkat elektronik.
Banyak produksi dan transportasi industri, serta pembangkit listrik termal, tidak dapat bekerja tanpa mesin panas - perangkat yang mengubah panas menjadi pekerjaan yang bermanfaat. Contoh mesin tersebut adalah kompresor, turbin, uap, bensin, dan mesin jet.
Salah satu mesin panas yang paling terkenal adalah turbin uap, yang mengimplementasikan bagian dari siklus Rankine yang digunakan di pembangkit listrik modern. Diagram yang disederhanakan dari siklus ini ditunjukkan pada gambar. Fluida kerja - air - diubah menjadi uap super panas dalam ketel uap yang dipanaskan dengan membakar bahan bakar fosil (batubara, minyak atau gas alam). uap tinggi
Gasovik - peralatan gas industri Direktori GOST, SNiP, PB Satuan besaran fisika, konsep fisika-kimia, rasio, komposisi dan karakteristik gas
Satuan pengukuran untuk suhu dan jumlah panas
Unit dasar pengukuran suhu adalah derajat Skala Suhu Internasional, yang secara praktis sesuai dengan derajat Celcius. Nilai ini sama dengan 1/100 interval suhu antara 0 dan 100 ° C, yaitu antara titik leleh es dan air mendidih pada tekanan 760 mm Hg. Seni.
Suhu mutlak adalah suhu yang diukur dari nol mutlak, yaitu dari -273,16°C, dan diukur dalam derajat Kelvin (°K). Derajat Kelvin sama dengan derajat Celcius. Oleh karena itu, suhu mutlak dinyatakan dalam derajat celcius sebagai berikut:
T, °K = t, °C + 273,16
Dalam sistem SI, satuan suhu adalah Kelvin. Diperbolehkan untuk menyatakan hasil praktis pengukuran suhu menggunakan derajat Celcius bersama dengan derajat Kelvin, tergantung pada asal (posisi nol) pada skala.
Contoh: 250 ±5 °С = 523,16 ±5 °K.
Dalam sistem SI, kerja, energi, dan panas diukur dalam joule (J). Kadang-kadang unit yang lebih besar dan lebih nyaman digunakan untuk tujuan praktis - kilojoule (kJ), sama dengan 1000 J. Satuan kerja dalam SI adalah kerja yang dilakukan oleh gaya 1 N pada perpindahan 1 m.Energi - kuantitas fisik menunjukkan berapa banyak pekerjaan yang dapat dilakukan tubuh.
Kalori dan kilokalori dapat digunakan sebagai unit panas di luar sistem. Kalori adalah jumlah kalor yang diperlukan untuk menaikkan suhu 1 gram air sebesar 1°C (19,5 hingga 20,5°C).
1 kal (kalori) = 4,1868 J;
1 kkal (kilokalori) \u003d 1000 kal \u003d 4186.8 J \u003d 4.187 kJ;
1 Mcal (megakalori) \u003d 10 6 kal \u003d 4.1868 MJ;
1 Gkal (gigakalori) \u003d 10 9 kal \u003d 4186,8 MJ.
Sebagai perbandingan, ketika mengevaluasi bahan bakar, yang disebut panas bersyarat digunakan, nilai kalor yang untuk perhitungan diasumsikan bersyarat sama dengan 7 Mcal/kg atau 7 Gkal/t. Dalam kasus seperti itu, seseorang berbicara, masing-masing, tentang 1 kg atau 1 ton bahan bakar standar (t.c.f.).
Panas memegang peranan penting dalam kehidupan manusia, termasuk dalam fungsi tubuhnya. Bagian dari energi kimia yang terkandung dalam makanan diubah menjadi panas, sehingga suhu tubuh dipertahankan mendekati 37
° C. Keseimbangan panas tubuh manusia juga tergantung pada suhu lingkungan, dan orang terpaksa menghabiskan banyak energi untuk memanaskan tempat tinggal dan industri di musim dingin dan mendinginkannya di musim panas. Sebagian besar energi ini dipasok oleh mesin panas, seperti pembangkit boiler dan turbin uap di pembangkit listrik yang menggunakan bahan bakar fosil (batubara, minyak) dan menghasilkan listrik.Sampai akhir abad ke-18. panas dianggap sebagai zat material, percaya bahwa suhu tubuh ditentukan oleh jumlah "cairan kalori" atau "kalori" yang terkandung di dalamnya. Belakangan, B. Rumford, J. Joule dan fisikawan lain pada masa itu, melalui eksperimen dan penalaran yang cerdik, membantah teori "kalori", membuktikan bahwa panas tidak memiliki bobot dan dapat diperoleh dalam jumlah berapa pun hanya karena gerakan mekanis. Panas itu sendiri bukanlah suatu zat melainkan hanya energi dari pergerakan atom atau molekulnya. Pemahaman tentang panas inilah yang dianut oleh fisika modern. Lihat juga FISIKA.
Pada artikel ini, kita akan melihat bagaimana panas dan suhu terkait dan bagaimana kuantitas ini diukur. Subjek diskusi kita juga akan menjadi pertanyaan berikut: perpindahan panas dari satu bagian tubuh ke bagian lain; perpindahan panas dalam ruang hampa (ruang yang tidak mengandung materi); peran panas di dunia modern.
PANAS DAN SUHU Jumlah energi panas dalam suatu zat tidak dapat ditentukan dengan mengamati pergerakan masing-masing molekulnya secara terpisah. Sebaliknya, hanya dengan mempelajari sifat-sifat makroskopik materi, seseorang dapat menemukan karakteristik gerak mikroskopis dari banyak molekul yang dirata-ratakan selama periode waktu tertentu. Suhu suatu zat adalah indikator rata-rata intensitas pergerakan molekul, yang energinya adalah energi panas suatu zat.Salah satu cara yang paling akrab, tetapi juga paling tidak akurat untuk menilai suhu dengan sentuhan. Menyentuh suatu objek, kita menilai apakah itu panas atau dingin, dengan fokus pada perasaan kita. Tentu saja, sensasi ini bergantung pada suhu tubuh kita, yang membawa kita pada konsep kesetimbangan termal, salah satu yang paling penting dalam mengukur suhu.
Keseimbangan termal. Jelas, jika dua tubuh A dan B (Gbr. 1) saling menempel erat, kemudian, setelah menyentuhnya setelah waktu yang cukup lama, kita akan melihat bahwa suhunya sama. Dalam hal ini, mayat dikatakan A dan B berada dalam kesetimbangan termal satu sama lain. Namun, benda, secara umum, tidak harus bersentuhan agar keseimbangan termal ada di antara mereka, cukup suhunya sama. Ini dapat diverifikasi menggunakan badan ketiga C , membawanya terlebih dahulu ke dalam kesetimbangan termal dengan tubuh SEBUAH , dan kemudian membandingkan suhu tubuh C dan b. Tubuh C di sini memainkan peran termometer. Dalam formulasi yang ketat, prinsip ini disebut hukum ke-nol termodinamika: jika benda A dan B berada dalam kesetimbangan termal dengan benda ketiga C, maka benda-benda ini juga berada dalam kesetimbangan termal satu sama lain. Hukum ini mendasari semua metode pengukuran suhu.Pengukuran suhu. Jika kita ingin melakukan eksperimen dan perhitungan yang akurat, maka peringkat suhu seperti panas, hangat, dingin, dingin tidak cukup, kita memerlukan skala suhu bertingkat. Ada beberapa skala seperti itu, dan titik beku dan titik didih air biasanya diambil sebagai titik acuan. Empat skala yang paling umum ditunjukkan pada gambar. 2. Skala Celcius, di mana titik beku air sesuai dengan 0° , dan titik didihnya adalah 100° , disebut skala Celsius yang dinamai A. Celsius, seorang astronom Swedia yang menggambarkannya pada tahun 1742. Diyakini bahwa naturalis Swedia K. Linney adalah orang pertama yang menggunakan skala ini. Sekarang skala Celcius adalah yang paling umum di dunia. Skala suhu Fahrenheit, di mana titik beku dan titik didih air sesuai dengan angka yang sangat tidak nyaman 32 dan 212° , diusulkan pada tahun 1724 oleh G. Fahrenheit. Skala Fahrenheit banyak digunakan di negara-negara berbahasa Inggris, tetapi hampir tidak digunakan dalam literatur ilmiah. Untuk mengubah suhu ke Celcius (° C) ke suhu Fahrenheit (° F) ada rumusnya° F = (9/5) ° C + 32, dan untuk rumus terjemahan terbalik°C = (5/9)(°F - 32). Kedua skala, baik Fahrenheit maupun Celsius, sangat merepotkan saat melakukan eksperimen dalam kondisi di mana suhu turun di bawah titik beku air dan dinyatakan sebagai angka negatif. Untuk kasus seperti itu, skala suhu absolut telah diperkenalkan, yang didasarkan pada ekstrapolasi ke apa yang disebut nol absolut, titik di mana gerakan molekul harus berhenti. Salah satunya disebut skala Rankin, dan yang lainnya disebut skala termodinamika absolut; suhu diukur dalam derajat Rankine (° R) dan kelvin (K). Kedua skala mulai dari nol mutlak dan titik beku air adalah 491,7° R dan 273,16 K. Jumlah derajat dan kelvin antara titik beku dan titik didih air pada skala Celcius dan skala termodinamika absolut adalah sama dan sama dengan 100; untuk skala Fahrenheit dan Rankine, itu juga sama, tetapi sama dengan 180. Derajat Celcius dikonversi ke kelvin menggunakan rumus K \u003d° C + 273,16, dan derajat Fahrenheit ke derajat Rankine menggunakan rumus°R = °F + 459.7. Pengoperasian perangkat yang dirancang untuk mengukur suhu didasarkan pada berbagai fenomena fisik yang terkait dengan perubahan energi panas suatu zat, perubahan hambatan listrik, volume, tekanan, karakteristik radiasi, dan sifat termoelektrik. Salah satu instrumen paling sederhana dan paling dikenal untuk mengukur suhu adalah termometer air raksa dalam gelas yang ditunjukkan pada gambar. 3, sebuah. Bola dengan air raksa di bagian bawah termometer ditempatkan dalam medium atau ditekan ke benda yang suhunya ingin mereka ukur, dan tergantung pada apakah bola menerima panas atau melepaskannya, air raksa memuai atau menyusut dan kolomnya naik atau jatuh di kapiler. Jika termometer sudah dikalibrasi dan dilengkapi dengan timbangan, maka Anda bisa langsung mengetahui suhu tubuh.Perangkat lain yang operasinya didasarkan pada ekspansi termal adalah termometer bimetal yang ditunjukkan pada gambar.
3, b. Elemen utamanya pelat spiral dari dua logam yang disolder dengan koefisien ekspansi termal yang berbeda. Ketika dipanaskan, salah satu logam mengembang lebih dari yang lain, spiral memutar dan memutar panah relatif terhadap skala. Perangkat semacam itu sering digunakan untuk mengukur suhu udara dalam dan luar ruangan, tetapi tidak cocok untuk menentukan suhu lokal.Temperatur lokal biasanya diukur dengan menggunakan termokopel, yaitu dua kabel logam berbeda yang disolder pada salah satu ujungnya (Gbr.
4, sebuah). Ketika sambungan seperti itu dipanaskan, ggl muncul di ujung bebas kabel, biasanya beberapa milivolt. Termokopel terbuat dari pasangan logam yang berbeda: besi dan konstantan, tembaga dan konstantan, kromel dan alumel. Termo-EMF mereka berubah hampir secara linier dengan suhu pada rentang suhu yang luas.Efek termoelektrik lain juga diketahui - ketergantungan resistansi bahan konduktif pada suhu. Ini mendasari pengoperasian termometer hambatan listrik, salah satunya ditunjukkan pada Gambar.
4, b. Resistansi elemen sensitif suhu kecil (sensor termal) biasanya gulungan kawat tipis dibandingkan dengan resistansi resistor variabel yang dikalibrasi menggunakan jembatan Wheatstone. Instrumen keluaran dapat diluluskan secara langsung dalam derajat.Pirometer optik digunakan untuk mengukur suhu benda pijar yang memancarkan cahaya tampak. Dalam satu versi perangkat ini, cahaya yang dipancarkan oleh tubuh dibandingkan dengan radiasi filamen lampu pijar yang ditempatkan di bidang fokus teropong yang melaluinya tubuh pemancar dilihat. Arus listrik yang memanaskan filamen lampu diubah sampai perbandingan visual dari pancaran filamen dan benda menunjukkan bahwa keseimbangan termal telah terbentuk di antara keduanya. Skala perangkat dapat diluluskan secara langsung dalam satuan suhu.
Kemajuan teknis dalam beberapa tahun terakhir telah memungkinkan untuk membuat sensor suhu baru. Misalnya, dalam kasus di mana sensitivitas sangat tinggi diperlukan, perangkat semikonduktor, termistor, digunakan sebagai pengganti termokopel atau termometer resistansi konvensional. Pewarna dan kristal cair yang mengubah keadaan fasanya juga digunakan sebagai konverter termal, terutama dalam kasus di mana suhu permukaan tubuh bervariasi dalam rentang yang luas. Akhirnya, termografi inframerah digunakan, di mana gambar inframerah suatu objek diperoleh dalam warna bersyarat, di mana setiap warna sesuai dengan suhu tertentu. Metode pengukuran suhu ini menemukan aplikasi terluas dari diagnostik medis hingga pemeriksaan isolasi termal ruangan. Lihat juga FISIKA NEGARA PADAT; KRISTAL CAIR.
Pengukuran jumlah panas. Energi termal (jumlah panas) suatu benda dapat diukur secara langsung dengan apa yang disebut kalorimeter; Versi sederhana dari perangkat semacam itu ditunjukkan pada Gambar. 5. Ini adalah bejana tertutup yang diisolasi dengan hati-hati, dilengkapi dengan perangkat untuk mengukur suhu di dalamnya dan kadang-kadang diisi dengan fluida kerja dengan sifat yang diketahui, seperti air. Untuk mengukur jumlah panas dalam tubuh kecil yang dipanaskan, itu ditempatkan dalam kalorimeter dan menunggu sistem mencapai kesetimbangan termal. Jumlah panas yang ditransfer ke kalorimeter (lebih tepatnya, ke air yang mengisinya) ditentukan oleh peningkatan suhu air.Jumlah panas yang dilepaskan selama reaksi kimia, seperti pembakaran, dapat diukur dengan menempatkan "bom" kecil di kalorimeter. "Bom" berisi sampel, di mana kabel listrik dihubungkan untuk penyalaan, dan jumlah oksigen yang sesuai. Setelah sampel terbakar habis dan kesetimbangan termal tercapai, ditentukan berapa banyak suhu air dalam kalorimeter telah meningkat, dan karenanya jumlah panas yang dilepaskan. Lihat juga KALORIMETRI.
Satuan panas. Kalor adalah salah satu bentuk energi dan oleh karena itu harus diukur dalam satuan energi. Dalam sistem SI internasional, satuan energi adalah joule (J). Juga diperbolehkan untuk menggunakan unit non-sistemik dari jumlah kalori panas: kalori internasional adalah 4,1868 J, kalori termokimia adalah 4,1840 J. Di laboratorium asing, hasil penelitian sering dinyatakan menggunakan apa yang disebut. Kalori 15 derajat sama dengan 4,1855 J. British Thermal Unit (BTU) di luar sistem tidak digunakan lagi: BTU avg = 1,055 J. Sumber utama panas adalah reaksi kimia dan nuklir, serta berbagai proses konversi energi. Contoh reaksi kimia dengan pelepasan panas adalah pembakaran dan pemecahan komponen makanan. Hampir semua panas yang diterima oleh Bumi disediakan oleh reaksi nuklir yang terjadi di kedalaman Matahari. Umat manusia telah belajar bagaimana memperoleh panas dengan bantuan proses fisi nuklir terkontrol, dan sekarang mencoba menggunakan reaksi fusi termonuklir untuk tujuan yang sama. Jenis energi lain juga dapat diubah menjadi panas, seperti kerja mekanik dan energi listrik. Penting untuk diingat bahwa energi panas (seperti yang lain) hanya dapat diubah menjadi bentuk lain, tetapi tidak dapat diperoleh "dari ketiadaan" atau dihancurkan. Ini adalah salah satu prinsip dasar ilmu yang disebut termodinamika. TERMODINAMIKA Termodinamika adalah ilmu tentang hubungan antara panas, kerja, dan materi. Ide-ide modern tentang hubungan ini dibentuk atas dasar karya para ilmuwan besar di masa lalu seperti Carnot, Clausius, Gibbs, Joule, Kelvin, dan lain-lain.Termodinamika menjelaskan arti kapasitas panas dan konduktivitas termal suatu zat, ekspansi termal benda, dan panas transisi fase. Ilmu ini didasarkan pada beberapa prinsip hukum yang ditetapkan secara eksperimental.Awal Termodinamika. Hukum termodinamika ke-nol yang dirumuskan di atas memperkenalkan konsep kesetimbangan termal, suhu, dan termometri. Hukum pertama termodinamika adalah pernyataan kunci penting untuk semua ilmu pengetahuan secara keseluruhan: energi tidak dapat dihancurkan atau diperoleh "dari ketiadaan", sehingga energi total Semesta adalah nilai konstan. Dalam bentuknya yang paling sederhana, hukum pertama termodinamika dapat dinyatakan sebagai berikut: energi yang diterima sistem, dikurangi energi yang dilepaskannya, sama dengan energi yang tersisa dalam sistem. Sepintas, pernyataan ini tampak jelas, tetapi tidak demikian, misalnya, situasi seperti pembakaran bensin dalam silinder mesin mobil: di sini energi yang diterima adalah kimia, energi yang dilepaskan adalah mekanik (kerja), dan energi yang tersisa dalam sistem adalah termal.Jadi, jelas bahwa energi dapat berubah dari satu bentuk ke bentuk lain dan transformasi semacam itu terus terjadi di alam dan teknologi. Lebih dari seratus tahun yang lalu, J. Joule membuktikan ini untuk kasus konversi energi mekanik menjadi energi panas menggunakan perangkat yang ditunjukkan pada gambar. 6, sebuah. Dalam perangkat ini, beban turun dan naik memutar poros dengan bilah dalam kalorimeter yang diisi dengan air, sebagai akibatnya air dipanaskan. Pengukuran yang tepat memungkinkan Joule untuk menentukan bahwa satu kalori panas setara dengan 4,186 J kerja mekanis. Perangkat yang ditunjukkan pada gambar.
6, b, digunakan untuk menentukan ekivalen termal energi listrik.Hukum pertama termodinamika menjelaskan banyak fenomena umum. Misalnya, menjadi jelas mengapa tidak mungkin untuk mendinginkan dapur dengan lemari es terbuka. Mari kita asumsikan bahwa kita telah mengisolasi dapur secara termal dari lingkungan. Energi terus disuplai ke sistem melalui kabel daya lemari es, tetapi sistem tidak mengeluarkan energi apa pun. Dengan demikian, energi totalnya meningkat, dan dapur menjadi lebih hangat: cukup sentuh tabung penukar panas (kondensor) di bagian belakang lemari es, dan Anda akan memahami kegunaannya sebagai perangkat "pendingin". Tetapi jika pipa-pipa ini dikeluarkan dari sistem (misalnya, keluar dari jendela), maka dapur akan mengeluarkan lebih banyak energi daripada yang diterimanya, mis. akan didinginkan, dan kulkas bekerja sebagai AC jendela.
Hukum pertama termodinamika adalah hukum alam yang melarang penciptaan atau penghancuran energi. Namun, ia tidak mengatakan apa-apa tentang bagaimana proses transfer energi berlangsung di alam. Jadi, kita tahu bahwa benda yang panas akan memanaskan benda yang dingin jika benda-benda ini bersentuhan. Tetapi dapatkah benda dingin dengan sendirinya mentransfer cadangan panasnya ke benda panas? Kesempatan Terakhir pasti ditolak oleh hukum kedua termodinamika.
Hukum pertama juga mengecualikan kemungkinan membuat mesin dengan koefisien tindakan yang bermanfaat(efisiensi) lebih dari 100% (mirip
" abadi " mesin bisa mengeluarkan lebih banyak energi untuk waktu yang lama daripada yang dikonsumsi). Mustahil untuk membangun mesin bahkan dengan efisiensi yang sama dengan 100%, karena beberapa bagian dari energi yang disuplai ke dalamnya harus hilang olehnya dalam bentuk energi panas yang kurang berguna. Jadi, roda tidak akan berputar tanpa henti tanpa suplai energi, karena akibat gesekan pada bantalan, energi gerak mekanik lambat laun akan berubah menjadi panas hingga roda berhenti.Kecenderungan untuk mengubah pekerjaan yang "berguna" menjadi energi panas yang kurang berguna dapat dibandingkan dengan proses lain yang terjadi ketika dua bejana yang berisi gas yang berbeda dihubungkan. Setelah menunggu cukup lama, kami menemukan di kedua bejana campuran homogen gas alam bertindak sedemikian rupa sehingga urutan sistem menurun. Ukuran termodinamika gangguan ini disebut entropi, dan hukum kedua termodinamika dapat dirumuskan secara berbeda: proses di alam selalu berlangsung sedemikian rupa sehingga entropi sistem dan lingkungannya meningkat. Dengan demikian, energi Semesta tetap konstan, sementara entropinya terus bertambah.
Panas dan sifat zat. Zat yang berbeda memiliki kemampuan yang berbeda untuk menyimpan energi panas; itu tergantung pada struktur molekul dan kepadatannya. Banyaknya kalor yang diperlukan untuk menaikkan suhu satu satuan massa zat sebesar satu derajat disebut panas spesifik. Kapasitas panas tergantung pada kondisi di mana zat itu berada. Misalnya, untuk memanaskan satu gram udara dalam balon sebesar 1 K, lebih banyak panas diperlukan daripada memanaskannya dengan cara yang sama dalam bejana tertutup dengan dinding kaku, karena sebagian energi yang diberikan ke balon dihabiskan untuk memperluas udara, dan bukan dengan memanaskannya. Oleh karena itu, khususnya, kapasitas panas gas diukur secara terpisah pada tekanan konstan dan pada volume konstan.Dengan peningkatan suhu, intensitas pergerakan molekul yang kacau meningkat, sebagian besar zat memuai ketika dipanaskan. Derajat pemuaian suatu zat dengan kenaikan suhu sebesar 1 K disebut koefisien muai panas.
Agar suatu zat berpindah dari satu keadaan fase ke fase lainnya, misalnya, dari padat ke cair (dan kadang-kadang segera menjadi gas), ia harus menerima sejumlah panas. Jika benda padat dipanaskan, suhunya akan naik sampai mulai meleleh; sampai peleburan selesai, suhu tubuh akan tetap konstan, meskipun ada pasokan panas. Banyaknya kalor yang diperlukan untuk melebur satu satuan massa suatu zat disebut kalor peleburan. Jika Anda terus memasok panas, maka zat cair akan memanas hingga mendidih. Jumlah panas yang diperlukan untuk menguapkan satu satuan massa cairan pada suhu tertentu disebut panas penguapan.
teori kinetik-molekul. Teori kinetik molekuler menjelaskan sifat makroskopik suatu zat dengan mempertimbangkan pada tingkat mikroskopis perilaku atom dan molekul yang membentuk zat ini. Dalam hal ini, pendekatan statistik digunakan dan beberapa asumsi dibuat tentang partikel itu sendiri dan sifat gerakannya. Dengan demikian, molekul dianggap sebagai bola padat, yang dalam media gas bergerak kacau terus menerus dan menempuh jarak yang cukup jauh dari satu tumbukan ke tumbukan lainnya. Tumbukan dianggap elastis dan terjadi antara partikel yang ukurannya kecil dan jumlahnya sangat besar. Tak satu pun dari gas nyata sesuai persis dengan model ini, tetapi sebagian besar gas cukup dekat dengan itu, yang merupakan alasan nilai praktis dari teori kinetika molekuler.Berdasarkan ide-ide ini dan menggunakan pendekatan statistik, Maxwell menurunkan distribusi kecepatan molekul gas dalam volume terbatas, yang kemudian dinamai menurut namanya. Distribusi ini disajikan secara grafis pada gambar. 7 untuk massa hidrogen tertentu pada suhu 100 dan 1000
° C. Ordinat menyatakan jumlah molekul yang bergerak dengan kecepatan yang ditunjukkan pada absis. Jumlah total partikel sama dengan luas area di bawah setiap kurva dan sama dalam kedua kasus. Dapat dilihat dari grafik bahwa sebagian besar partikel memiliki kecepatan mendekati nilai rata-rata, dan hanya sebagian kecil yang memiliki kecepatan sangat tinggi atau rendah. Kecepatan rata-rata pada suhu ini terletak pada kisaran 2000-3000 m/s, yaitu sangat besar.Sejumlah besar molekul gas yang bergerak cepat seperti itu bekerja dengan gaya yang benar-benar terukur pada benda-benda di sekitarnya. Gaya mikroskopis yang dengannya banyak molekul gas menabrak dinding bejana menambah jumlah makroskopik yang disebut tekanan. Ketika energi disuplai ke gas (suhu naik), energi kinetik rata-rata molekulnya meningkat, partikel gas menabrak dinding lebih sering dan lebih keras, tekanan naik, dan jika dinding tidak sepenuhnya kaku, maka mereka meregang dan volume dari gas meningkat. Dengan demikian, pendekatan statistik mikroskopis yang mendasari teori kinetik molekuler memungkinkan untuk menjelaskan fenomena ekspansi termal yang telah kita diskusikan.
Hasil lain dari teori kinetik molekuler adalah hukum yang menjelaskan sifat-sifat gas yang memenuhi persyaratan yang tercantum di atas. Inilah yang disebut persamaan keadaan gas ideal menghubungkan tekanan, volume, dan suhu satu mol gas dan memiliki bentuk persamaan
PV = RT dimana P tekanan, volume V, T suhu, dan R konstanta gas universal sama dengan (8.31441± 0,00026) J/(mol H KE). Lihat juga TEORI MOLEKULER-KINETIK; TERMODINAMIKA. PERPINDAHAN PANAS Perpindahan panas adalah proses perpindahan panas di dalam suatu benda atau dari satu benda ke benda lainnya, karena adanya perbedaan suhu. Intensitas perpindahan panas tergantung pada sifat-sifat zat, perbedaan suhu dan mematuhi hukum alam yang ditetapkan secara eksperimental. Untuk membuat sistem pemanas atau pendingin yang efisien, berbagai mesin, pembangkit listrik, sistem isolasi termal, Anda perlu mengetahui prinsip-prinsip perpindahan panas. Dalam beberapa kasus, pertukaran panas tidak diinginkan (isolasi termal tungku peleburan, pesawat ruang angkasa, dll.), Sementara di lain itu harus sebesar mungkin (ketel uap, penukar panas, peralatan dapur).Ada tiga jenis utama perpindahan panas: konduksi, konveksi dan perpindahan panas radiasi.
Konduktivitas termal. Jika ada perbedaan suhu di dalam tubuh, maka energi panas berpindah dari bagian yang lebih panas ke bagian yang lebih dingin. Jenis perpindahan panas ini, karena gerakan termal dan tumbukan molekul, disebut konduktivitas termal; cukup suhu tinggi dalam padatan dapat diamati secara visual. Jadi, ketika batang baja dipanaskan dari satu ujung dalam nyala kompor gas, energi panas ditransfer melalui batang, dan cahaya menyebar pada jarak tertentu dari ujung yang dipanaskan (semakin berkurang intensitasnya dengan jarak dari tempat Pemanasan).Intensitas perpindahan panas karena konduktivitas termal tergantung pada gradien suhu, yaitu hubungan
D T/D x perbedaan suhu di ujung batang dengan jarak di antara mereka. Itu juga tergantung pada luas penampang batang (dalam m 2 ) dan konduktivitas termal material[ dalam unit yang sesuai W/(m Ch K)] . Hubungan antara besaran-besaran ini diturunkan oleh matematikawan Prancis J. Fourier dan memiliki bentuk sebagai berikut: di mana q aliran panas, k koefisien konduktivitas termal, dan SEBUAH luas penampang. Hubungan ini disebut hukum Fourier tentang konduksi panas; tanda minus di dalamnya menunjukkan bahwa panas ditransfer dalam arah yang berlawanan dengan gradien suhu.Ini mengikuti dari hukum Fourier bahwa aliran panas dapat dikurangi dengan mengurangi salah satu kuantitas koefisien konduktivitas termal, area atau gradien suhu. Untuk bangunan dalam kondisi musim dingin, nilai terakhir praktis konstan, dan oleh karena itu, untuk mempertahankan suhu yang diinginkan di dalam ruangan, tetap mengurangi konduktivitas termal dinding, mis. meningkatkan isolasi termal mereka.
Tabel menunjukkan koefisien konduktivitas termal dari beberapa zat dan bahan. Tabel menunjukkan bahwa beberapa logam menghantarkan panas jauh lebih baik daripada yang lain, tetapi semuanya adalah konduktor panas yang jauh lebih baik daripada udara dan bahan berpori.
|
KONDUKTIVITAS TERMAL DARI BEBERAPA BAHAN DAN BAHAN |
|
|
Zat dan bahan |
Konduktivitas termal, W / (m × K) |
| Aluminium | |
| Perunggu | |
| Bismut | |
| Tungsten | |
| Besi | |
| Emas | |
| Kadmium | |
| Magnesium | |
| Tembaga | |
| Arsenik | |
| Nikel | |
| Platinum | |
| Air raksa | |
| Memimpin | |
| Seng | |
|
bahan lainnya |
|
| Asbes | |
| Konkret | |
| Udara | |
| Eider turun (longgar) | |
| kacang pohon) | |
| Magnesia (MgO) | |
| Serbuk gergaji | |
| Karet (spons) | |
| Mika | |
| Kaca | |
| Karbon (grafit) | |
Tahanan termal dan listrik dari banyak zat menurun tajam ketika suhu turun di bawah suhu helium cair (1,8 K). Fenomena ini, yang disebut superkonduktivitas, digunakan untuk meningkatkan efisiensi banyak perangkat, mulai dari perangkat mikroelektronika hingga saluran listrik dan elektromagnet besar. Lihat juga SUPERKONDUKTIVITAS.
Konveksi. Seperti yang telah kami katakan, ketika panas disuplai ke cairan atau gas, intensitas pergerakan molekul meningkat, dan sebagai hasilnya, tekanan meningkat. Jika cairan atau gas tidak dibatasi volumenya, maka mereka memuai; kepadatan lokal cairan (gas) menjadi kurang, dan karena gaya apung (Archimedean), bagian media yang dipanaskan bergerak ke atas (itulah sebabnya udara hangat di dalam ruangan naik dari baterai ke langit-langit). Fenomena ini disebut konveksi. Agar tidak menyia-nyiakan panas sistem pemanas dengan sia-sia, Anda perlu menggunakan pemanas modern yang menyediakan sirkulasi udara paksa.Aliran panas konvektif dari pemanas ke media yang dipanaskan tergantung pada kecepatan awal molekul, kepadatan, viskositas, konduktivitas termal dan kapasitas panas, dan media; ukuran dan bentuk pemanas juga sangat penting. Rasio antara jumlah yang sesuai mematuhi hukum Newton
q = hA ( T W- TҐ ), dimana q aliran panas (diukur dalam watt), SEBUAH luas permukaan sumber panas (dalam m 2), T W dan T suhu sumber dan lingkungannya (dalam kelvin). Koefisien perpindahan panas konvektif h tergantung pada sifat medium, kecepatan awal molekulnya, dan juga pada bentuk sumber panas, dan diukur dalam satuan W/(m 2 jam KE).Nilai
h tidak sama untuk kasus-kasus ketika udara di sekitar pemanas tidak bergerak (konveksi bebas) dan ketika pemanas yang sama dalam aliran udara (konveksi paksa). Dalam kasus sederhana aliran fluida melalui pipa atau aliran di sekitar permukaan datar, koefisien h dapat dihitung secara teoritis. Namun, belum mungkin menemukan solusi analitik untuk masalah konveksi untuk aliran turbulen media. Turbulensi adalah gerakan kompleks cairan (gas), kacau dalam skala yang secara signifikan melebihi yang molekuler.Jika benda yang dipanaskan (atau, sebaliknya, dingin) ditempatkan di media stasioner atau dalam aliran, maka arus konvektif dan lapisan batas terbentuk di sekitarnya. Suhu, tekanan, dan kecepatan molekul pada lapisan ini berperan penting dalam menentukan koefisien perpindahan panas konveksi.
Konveksi harus dipertimbangkan dalam desain penukar panas, sistem pendingin udara, pesawat berkecepatan tinggi dan banyak aplikasi lainnya. Dalam semua sistem seperti itu, konduksi panas terjadi bersamaan dengan konveksi, baik antara padatan maupun di lingkungan mereka. Pada suhu tinggi Perpindahan panas radiasi juga dapat memainkan peran penting.
Perpindahan panas radiasi. Jenis ketiga perpindahan panas perpindahan panas radiasi berbeda dari konduksi panas dan konveksi dalam hal ini panas dapat ditransfer melalui ruang hampa. Kesamaannya dengan metode perpindahan panas lainnya adalah karena perbedaan suhu. Radiasi termal adalah salah satu jenisnya radiasi elektromagnetik. Jenis lain dari gelombang radio, ultraviolet dan radiasi gamma terjadi tanpa adanya perbedaan suhu.pada gambar. 8 menunjukkan ketergantungan energi radiasi termal (inframerah) pada panjang gelombang. Radiasi termal dapat disertai dengan emisi cahaya tampak, tetapi energinya kecil dibandingkan dengan energi radiasi dari bagian spektrum yang tidak terlihat.
Intensitas perpindahan panas dengan konduksi dan konveksi panas sebanding dengan suhu, dan fluks panas radiasi sebanding dengan pangkat empat suhu dan mematuhi hukum Stefan Boltzmann
Ruang perumahan dan kantor sering dipanaskan dengan pemancar panas listrik kecil; cahaya kemerahan dari spiral mereka terlihat radiasi termal dekat dengan tepi bagian inframerah dari spektrum. Ruangan dipanaskan oleh panas, yang dibawa terutama oleh bagian radiasi inframerah yang tidak terlihat. Di perangkat night vision
^ Kamera menggunakan sumber radiasi termal dan penerima peka IR yang memungkinkan Anda melihat dalam gelap.Matahari adalah pemancar energi panas yang kuat; itu memanaskan Bumi bahkan pada jarak 150 juta km. Intensitas radiasi matahari, yang tercatat dari tahun ke tahun oleh stasiun-stasiun yang terletak di banyak bagian dunia, kira-kira 1,37 W
/ m 2 . Energi matahari adalah sumber kehidupan di Bumi. Pencarian sedang dilakukan untuk mencari cara untuk menggunakannya dengan paling efektif. Panel surya telah diciptakan untuk memanaskan rumah dan menghasilkan listrik untuk kebutuhan rumah tangga. PERAN PANAS DAN PENGGUNAANNYA Proses perpindahan panas global tidak direduksi menjadi pemanasan Bumi oleh radiasi matahari. Arus konveksi besar-besaran di atmosfer menentukan perubahan harian dalam kondisi cuaca di seluruh dunia. Perbedaan suhu di atmosfer antara daerah khatulistiwa dan kutub, bersama dengan gaya Coriolis akibat rotasi Bumi, menyebabkan munculnya arus konveksi yang terus berubah, seperti angin pasat, aliran jet, dan front hangat dan dingin. Lihat juga IKLIM; METEOROLOGI DAN KLIMATOLOGI.Perpindahan panas (karena konduktivitas termal) dari inti cair Bumi ke permukaannya menyebabkan letusan gunung berapi dan munculnya geyser. Di beberapa daerah, energi panas bumi digunakan untuk pemanas ruangan dan pembangkit listrik.
Panas adalah peserta yang sangat diperlukan dalam hampir semua proses produksi. Kami akan menyebutkan yang paling penting di antaranya, seperti peleburan dan pemrosesan logam, pengoperasian mesin, produksi produk makanan, sintesis kimia, penyulingan minyak, pembuatan berbagai barang mulai dari batu bata dan piring hingga mobil dan elektronik. perangkat.
Banyak produksi dan transportasi industri, serta pembangkit listrik termal, tidak dapat bekerja tanpa mesin panas - perangkat yang mengubah panas menjadi pekerjaan yang bermanfaat. Contoh mesin tersebut adalah kompresor, turbin, uap, bensin dan mesin jet.
Salah satu mesin panas paling terkenal adalah turbin uap, yang mengimplementasikan bagian dari siklus Rankine yang digunakan di pembangkit listrik modern. Diagram yang disederhanakan dari siklus ini ditunjukkan pada gambar. 9. Air fluida kerja diubah menjadi uap superheated dalam ketel uap yang dipanaskan dengan membakar bahan bakar fosil (batubara, minyak atau gas alam). Uap tekanan tinggi memutar poros turbin uap, yang menggerakkan generator yang menghasilkan listrik. Uap buang mengembun ketika didinginkan dengan air mengalir, yang menyerap sebagian panas yang tidak digunakan dalam siklus Rankine. Selanjutnya, air diumpankan ke menara pendingin (cooling tower), dari mana sebagian panas dilepaskan ke atmosfer. Kondensat dikembalikan ke ketel uap melalui pompa, dan seluruh siklus diulang.
Semua proses dalam siklus Rankine menggambarkan prinsip-prinsip termodinamika yang dijelaskan di atas. Secara khusus, menurut hukum kedua, bagian dari energi yang dikonsumsi oleh pembangkit listrik harus dihamburkan ke lingkungan dalam bentuk panas. Ternyata sekitar 68% energi yang semula terkandung dalam bahan bakar fosil hilang dengan cara ini. Peningkatan efisiensi pembangkit listrik yang nyata dapat dicapai hanya dengan menaikkan suhu ketel uap (yang dibatasi oleh ketahanan panas bahan) atau dengan menurunkan suhu media tempat panas mengalir, yaitu. suasana.
Siklus termodinamika lain memiliki sangat penting di kami Kehidupan sehari-hari, adalah siklus pendinginan kompresor uap Rankin, skema yang ditunjukkan pada gambar. 10. Dalam lemari es dan AC rumah tangga, energi dipasok dari luar untuk menyediakannya. Kompresor meningkatkan suhu dan tekanan zat kerja freon kulkas, amonia atau karbon dioksida. Gas superheated diumpankan ke kondensor, di mana ia mendingin dan mengembun, melepaskan panas ke lingkungan. Cairan yang meninggalkan nozel kondensor melewati katup pelambatan ke evaporator, dan sebagian menguap, yang disertai dengan penurunan suhu yang tajam. Evaporator mengambil panas dari ruang kulkas, yang memanaskan fluida kerja di nozel; cairan ini disuplai oleh kompresor ke kondensor, dan siklus berulang lagi.
Siklus pendinginan ditunjukkan pada gambar. 10 juga dapat digunakan dalam pompa panas. Pompa panas seperti itu di musim panas mengeluarkan panas ke udara atmosfer yang panas dan mengkondisikan ruangan, dan di musim dingin, sebaliknya, mereka mengambil panas dari udara dingin dan memanaskan ruangan.
Reaksi nuklir merupakan sumber panas yang penting untuk tujuan seperti pembangkit listrik dan transportasi. Pada tahun 1905, A. Einstein menunjukkan bahwa massa dan energi dihubungkan oleh hubungan
E=mc2 , yaitu dapat saling masuk. kecepatan cahaya c sangat besar: 300 ribu km/ Dengan. Ini berarti bahwa bahkan sejumlah kecil materi dapat memberikan sejumlah besar energi. Jadi, dari 1 kg bahan fisil (misalnya, uranium), secara teoritis dimungkinkan untuk memperoleh energi, yang selama 1000 hari operasi terus menerus disediakan oleh pembangkit listrik dengan kapasitas 1 MW. Lihat juga STRUKTUR ATOM; Tungku DAN TEKNOLOGI Tungku; RADIASI ELEKTROMAGNETIK; PENUKAR PANAS; TURBIN; UNIT PENGUKURAN KUANTITAS FISIK.LITERATUR Zemansky M. Suhu sangat tinggi dan sangat rendah. M., 1968Paulus R. Mekanika, akustik, dan doktrin panas. M., 1971
Smorodinsky Ya.A. Suhu. M., 1981
Feng J. Mesin, energi, dan entropi. M., 1986
Atkins P.V. Keteraturan dan ketidakteraturan di alam. M., 1987
kalorimeter cair
Jenis kalorimeter ini, yang paling banyak digunakan dalam teknologi, desainnya sederhana dan perawatannya mudah. Jumlah panas yang dihasilkan oleh reaksi yang diinduksi secara eksternal pertama-tama dipindahkan ke bejana reaksi (di mana reaksi berlangsung) dan kemudian ke penangas cairan. Cairan dalam bak terus diaduk dengan menggunakan impeller, sekrup pengangkat atau pompa, yang mempercepat pemerataan suhu. Bak mandi diisolasi secara termal (terlindung) dari lingkungan sebanyak mungkin. Perubahan suhu penangas cairan adalah ukuran jumlah panas yang terdeteksi. Kapasitas panas massa yang akan dipanaskan tidak boleh terlalu tinggi untuk memastikan perubahan suhu yang cukup dan agar proses pengukuran tidak berlangsung terlalu lama (karena kehilangan panas meningkat).
Gambar Perangkat kalorimeter cair.
Dengan tuntutan tinggi pada keteguhan kondisi sekitar, dimungkinkan untuk menempatkan seluruh kalorimeter di bak lain dan menstabilkan suhu di dalamnya dengan akurasi tinggi menggunakan loop kontrol. Ini diperlukan di tempat pertama dalam kasus di mana diperlukan untuk melakukan percobaan pada suhu yang berbeda secara signifikan dari suhu lingkungan.
Untuk analisis pada suhu rendah (turun hingga sekitar -150°C), nitrogen cair digunakan sebagai media pendingin. Dalam hal ini, perlu memperhatikan fakta bahwa ketika mengubahnya, embun beku dari udara lembab di sekitarnya tidak mengendap pada sampel atau wadah sampel, karena lapisannya dapat mempengaruhi proses pengukuran. Untuk menghindari hal ini, ketika kalorimeter terbuka, sampel dan wadah sampel dibersihkan dengan gas nitrogen dingin.
Kalorimeter badan logam
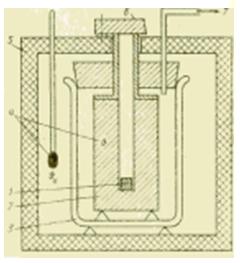
Gambar Skema perangkat kalorimeter logam.
Jika diperlukan untuk melakukan studi kalorimetri dalam rentang suhu yang lebih luas, maka kalorimeter cair tidak lagi cocok. Dalam kalorimeter benda logam yang sesuai untuk tujuan ini, jumlah panas yang dipindahkan diambil oleh balok logam (perak, tembaga, aluminium) yang biasanya pada suhu sekitar. Kalorimeter semacam itu terutama ditujukan untuk menentukan kapasitas panas spesifik c, J / (kg * K), zat cair dan padat.
Sampel didinginkan terlebih dahulu di luar kalorimeter dalam pabrik pendingin atau dipanaskan dalam tungku dan, setelah mencapai keadaan tunak, diturunkan (dijatuhkan) ke dalam lubang di balok logam. Menurut metode operasinya, alat semacam itu disebut kalorimeter jatuh bebas, dan menurut sifat proses termodinamika di dalamnya, kadang-kadang disebut kalorimeter perpindahan.
Jumlah panas yang dipindahkan selama pencampuran ini dari sampel (dengan parameter m1, c1, ) ke balok logam (m2, c2, ) menyebabkan perubahan suhu balok yang dapat diukur. Hal ini memungkinkan untuk menentukan nilai kapasitas panas spesifik sampel yang biasanya tidak diketahui untuk kondisi ideal(dengan tidak adanya pertukaran panas dengan lingkungan) dari ekspresi:
Blok logam itu sendiri terletak di bejana Dewar yang dievakuasi, dan kadang-kadang di bak cair. Dalam kasus terakhir, untuk mendapatkan kapasitas panas kalorimeter Ck, kapasitas panas penangas Cw harus ditambahkan ke kapasitas panas balok logam C2:
CK=C2+CW=c2m2+cWmW .
METODE PENGUKURAN KALORIMETRI
Paling sering, kalorimeter digunakan dalam mode kondisi lingkungan konstan. Ini berlaku terutama untuk sebagian besar kalorimeter pembakaran, di mana waktu reaksinya sangat singkat. Sementara suhu bagian dalam kalorimeter berubah karena reaksi, suhu udara sekitar tetap konstan. Dalam banyak kasus, penangas yang dikontrol suhu adalah digunakan sebagai lingkungan untuk menghindari pengaruh pada nilai terukur dari gangguan eksternal - fluktuasi suhu di dalam ruangan, radiasi, angin, dll.
Keuntungan dari skema pengukuran ini adalah biaya peralatan yang relatif rendah, yang dapat digunakan untuk melakukan bagian utama dari pengukuran kalorimetri. Kerugian utama harus dipertimbangkan pertukaran panas kalorimeter dengan lingkungan, yang memperumit interpretasi hasil. Metode pengukuran ini selalu disebut isoperibol (diatermik). Bagaimanapun, itu tidak dapat disebut isotermal, yang intinya terletak pada kenyataan bahwa suhu kalorimeter tetap konstan selama reaksi, seperti, misalnya, kalorimeter yang dirancang untuk mengukur transformasi fase.
metode adiabatik
Jika dimungkinkan untuk mengecualikan pertukaran panas dengan lingkungan, yaitu, untuk memastikan proses adiabatik, maka eksperimen dan interpretasi hasil disederhanakan, dan hasil pengukuran lebih akurat, karena tidak perlu terus merekam perubahan suhu dan menghitung koreksi. Selain itu, dalam hal ini, kenaikan suhu yang agak lebih besar dalam bejana kalorimeter dapat ditoleransi; untuk perangkat non-adiabatik, ini tidak dapat diterima karena peningkatan kehilangan panas.
Untuk menghindari pertukaran panas antara bejana kalorimeter dan sekitarnya (biasanya penangas cair), suhu penangas harus terus-menerus dikoreksi sesuai dengan perubahan suhu di dalam bejana. Dengan bantuan pengontrol elektronik (sirkuit pelacak), dimungkinkan untuk terus mempertahankan perbedaan suhu ini secara praktis sama dengan nol. Hal ini meningkatkan biaya peralatan pengukuran tergantung pada akurasi pengukuran yang dibutuhkan.
Elemen perangkat keras harus cepat dan stabil untuk waktu yang lama (memiliki penyimpangan minimal). Zona mati dari loop kontrol pelacakan harus dalam kisaran dari ±10-3 hingga ±10-5 K. Sebagai alat pengukur, Anda dapat menggunakan termometer kontak listrik respons cepat, yang, jika disertakan dalam rangkaian jembatan, memberikan impuls ke pengontrol untuk mengubah daya pemanas. Pemanasan dilakukan baik dengan menggunakan kumparan hambatan listrik atau langsung dalam bak cair, yang bertindak sebagai resistor pemanas karena disosiasi lemah (disebut pemanasan elektrolitik). Metode kedua ini praktis tanpa inersia. Hasilnya dapat diperoleh dengan menggunakan alat yang sudah ada untuk pengukuran suhu listrik atau menggunakan termometer cair tambahan (Beckmann).
Metode pengukuran adiabatik cocok untuk mempelajari proses lambat dan efek termal. Dengan perubahan cepat dalam jumlah panas (dalam kalorimeter pembakaran), inersia pemerataan suhu memiliki efek yang tidak menguntungkan bahkan akurasi metode non-adiabatik konvensional tidak tercapai. Namun, dengan menyediakan kapasitas panas yang rendah dari elemen pemanas dan sensor suhu dan dengan pencampuran intensif cairan mandi, dimungkinkan untuk memperoleh nilai kecil dari berbagai konstanta waktu (mengurangi inersia).
Metode kompensasi
Menggunakan kalorimeter diferensial atau ganda berdasarkan prinsip kompensasi, adalah mungkin untuk menghilangkan sebagian besar pengaruh eksternal pada proses pengukuran. Dua bejana kalorimetri identik dengan aksesori identik ditempatkan di lingkungan di bawah kondisi yang sama. Dalam satu bejana, proses yang diselidiki dengan efek termal terjadi, dan bejana lainnya dipanaskan dengan bantuan sistem kontrol servo sedemikian rupa sehingga kehilangan panas ke lingkungan untuk kedua bejana adalah sama. Oleh karena itu, daya pemanas input dapat ditempatkan dalam proporsi langsung dengan jumlah panas yang dilepaskan selama proses yang sedang dipelajari. Dalam hal ini, tugas eksperimental pengukuran masuk ke area lain dan direduksi menjadi penentuan yang sangat akurat dari daya pemanas listrik yang disediakan (W * s, J):
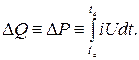
Kalorimeter diferensial digunakan, khususnya, di bawah kondisi sekitar adiabatik, terutama bila diharapkan perubahan yang sangat kecil atau sangat lambat dalam jumlah panas. Dalam proses endoterm, cukup memiliki satu bejana kalorimetri. Masukan panas dikendalikan sedemikian rupa sehingga suhu di dalam bejana tetap sama sepanjang waktu (metode isotermal). Kerugian dari kalorimeter diferensial adalah tingginya biaya peralatan dan alat ukur.
KALORIMETER PEMBAKARAN
Bahan bakar yang digunakan dalam fasilitas panas dan tenaga diperiksa untuk menentukan nilai kalornya H (J/kg). Indikator ini diperlukan untuk mengetahui faktor efisiensi, mempelajari efisiensi dan perhitungan energi yang dikonsumsi pada berbagai instalasi, serta untuk pengendalian proses pembakaran yang optimal. Fluktuasi yang signifikan dalam komposisi komponen yang mudah terbakar seringkali memerlukan penentuan nilai kalor secara terus menerus.
Ketika suatu zat benar-benar terbakar, sejumlah panas Q (panas pembakaran) dilepaskan. Jika kita membaginya dengan massa m (atau dengan volume dalam kondisi normal Vn), kita mendapatkan panas pembakaran (spesifik):
Tergantung pada keadaan produk pembakaran, dua jenis nilai kalor dibedakan: H0 lebih tinggi dan H lebih rendah, yang juga disebut panas pembakaran dan nilai kalor. Saat menentukan nilai kalor bersih Ni, air yang terbentuk selama reaksi kimia harus dalam keadaan uap. Selisih antara kedua kalor H0 - Ni sesuai dengan kalor penguapan air kental (indeks KO - kondensat) r, yaitu sebesar 2,441 MJ / kg.
Untuk bahan bakar padat dan cair, jumlah air yang dihasilkan dapat ditentukan berdasarkan analisis unsur, dan saat membakar bahan bakar gas, dengan mengukur jumlah kondensat.
Dalam tungku industri, suhu produk pembakaran selalu melebihi titik didih air. Oleh karena itu, hanya nilai kalor bersih Ni yang biasanya menarik, karena panas kondensasi air tidak dapat digunakan.
Kalorimeter Pembakaran untuk Padatan dan Cairan
Untuk proses pembakaran cepat, bentuk khusus kalorimeter cair telah dikembangkan - yang disebut bom kalorimetri Berthelot (Gbr. 3).
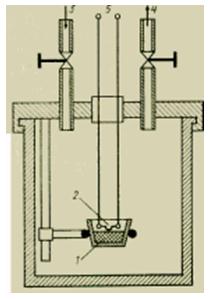
Gambar Perangkat bom kalorimetri.
Pembakaran sejumlah kecil zat yang diukur dengan tepat terjadi pada volume konstan dalam bom tertutup dalam atmosfer oksigen paling murni pada tekanan ~30 atm (3 MPa). Bom yang diisi ditempatkan di penangas cairan kalorimeter, yang menyerap panas pembakaran yang dilepaskan.
padatan biasanya ditekan menjadi briket kecil (tablet) dan ditimbang dengan sangat akurat. Dianjurkan untuk mencampur zat yang terbakar dengan buruk dengan cairan yang terbakar dengan baik dengan panas pembakaran yang diketahui (misalnya, asam benzoat). Zat cair ditempatkan dalam cangkir (perahu) yang terbuat dari platina atau kuarsa atau dalam kapsul plastik kecil. Di sampulnya, dibaut ke badan bom, ada semua perangkat yang diperlukan untuk penelitian: katup untuk memasok oksigen dan mengeluarkan produk pembakaran, pemegang sampel, dan penyala listrik. Pengapian dilakukan dengan mensuplai listrik ke kawat platina tipis. Panas yang diberikan untuk penyalaan harus diukur secara akurat sehingga dapat diperhitungkan saat menguraikan hasil percobaan. Dalam bom kalorimetri, nilai kalor H0 tertinggi ditentukan. Selama verifikasi, ekuivalen termal kalorimeter Ck ditentukan dengan membakar zat referensi (misalnya, asam benzoat) atau menggunakan alat pemanas listrik.
Kalorimeter pembakaran untuk zat gas
Untuk menentukan panas pembakaran media gas, ada berbagai metode. Semuanya, berbeda dengan bom kalorimetri untuk zat padat dan cair, didasarkan pada pengukuran berkelanjutan. Prinsip pengukuran yang digunakan cukup sederhana. Gas uji dibakar terus menerus dalam pembakar pada tekanan konstan. Semua panas yang dilepaskan selama pembakaran diserap baik oleh aliran media pendingin di penukar panas (kalorimeter basah atau penukar panas), atau dengan mencampur produk pembakaran dengan aliran udara pada laju aliran yang diketahui (kalorimeter kering atau pencampuran). Biasanya menentukan nilai kalor bersih Hu. Untuk menentukan nilai kalor kotor H0, perlu dilakukan kondensasi uap air (indeks KO) yang terkandung dalam gas buang. Mengetahui laju aliran massa dan perbedaan suhu pada saluran masuk (indeks e) dan saluran keluar (indeks a) kalorimeter, adalah mungkin untuk menghitung nilai kalor yang sesuai dengan menggunakan persamaan keseimbangan panas.
Perlakuan gas yang diperlukan pada dasarnya sama di semua kalorimeter gas. Sebelum pembakaran, gas (indeks G) terlebih dahulu dibersihkan dari kotoran mekanis padat (dalam filter) dan dibasahi (sampai jenuh dengan kelembaban, 100%), dan kemudian dibawa ke nilai tekanan awal yang ditentukan (menggunakan pengurangan tekanan katup) dan suhu media pendingin (indeks K). Udara yang dibutuhkan untuk pembakaran (indeks L) juga dilembabkan dan dibawa ke suhu media pendingin.
Tergantung pada akurasi yang diperlukan dan biaya instrumentasi yang diizinkan, beberapa kondisi ini mungkin tidak terpenuhi. Kalorimeter harus diverifikasi dengan gas referensi (misalnya hidrogen) untuk menentukan deviasi dari persamaan keadaan ideal kalorimeter. Untuk kalorimeter penukar panas (basah), persamaan di atas memiliki bentuk
dimana dan adalah laju aliran massa media pendingin dan bahan bakar, kg/s; sk - kapasitas panas spesifik media pendingin, J / (kg * K); - kenaikan suhu media pendingin, K.
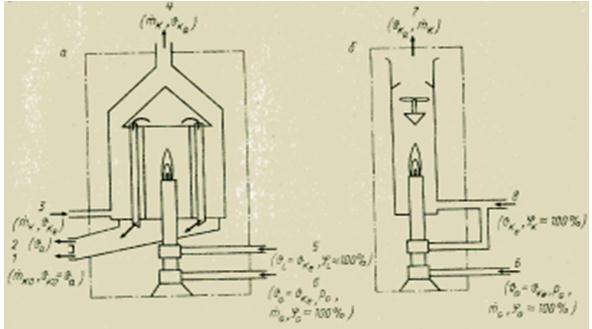
Gambar Perangkat kalorimeter basah (a) dan kering (b) untuk bahan bakar gas.
Kenaikan suhu biasanya 5-15 K. Karena massa termal yang besar, kalorimeter perpindahan panas memiliki konstanta waktu yang sangat lama, yang bisa sampai beberapa menit. Oleh karena itu, mereka kurang cocok untuk digunakan dalam loop kontrol tertutup sebagai sensor daripada kalorimeter kering (pencampuran), yang konstanta waktunya hanya beberapa detik. Di sisi lain, akurasi kalorimeter pertukaran panas yang dapat dicapai relatif tinggi. Kesalahannya tidak melebihi ±0,25-1%, sehingga dapat juga digunakan untuk pekerjaan laboratorium dan untuk verifikasi. Kalorimeter kering (pencampuran) memiliki kesalahan ±1 hingga ±2% dari batas atas rentang pengukuran.
Versi desain kalorimeter dari berbagai produsen berbeda terutama dalam perangkat tambahan dan keselamatan, elemen penginderaan, dan sirkuit komputasi yang memberikan kompensasi kesalahan. Jadi, dalam kalorimeter pertukaran panas, rasio laju aliran gas dan media pendingin dipertahankan dengan berbagai cara (lihat persamaan kalorimeter di atas), karena nilai kalor yang lebih tinggi H0 secara langsung hanya bergantung pada kenaikan suhu.
Dalam kalorimeter kering, kenaikan suhu diukur baik secara langsung menggunakan termometer kontak listrik atau secara tidak langsung menggunakan sensor dilatometrik, tabung ekspansi yang terletak di aliran gas buang. Dalam kalorimeter ADOS, pemanjangan termal tabung dilatometer berhubungan langsung dengan panas pembakaran dan dapat diubah menjadi sinyal apa pun menggunakan penghubung dan pengukur panjang. Dalam kalorimeter Reinecke, perpanjangan batang digunakan sebagai sinyal pengukur dalam rangkaian kontrol yang mengontrol aliran udara pendingin sehingga kenaikan suhunya tetap hampir konstan. Dalam hal ini, loop kontrol ternyata murni proporsional, tetapi beberapa penyimpangan residual tidak dapat dihindari di dalamnya. Dalam hal ini, konsumsi udara pendingin atau pemanjangan tabung dilatometrik (batang) adalah ukuran nilai kalor yang ditentukan. Prasyarat untuk mendapatkan akurasi yang cukup di semua kalorimeter kering adalah pencampuran yang baik antara udara pendingin dan produk pembakaran.
PENGUKURAN ALIRAN PANAS
Panas sebagai jenis energi ditransfer dalam tiga cara: melalui benda padat (konduksi termal), media cair atau gas (konveksi) dan tanpa partisipasi materi (radiasi). Dalam teknologi, ketiga komponen tersebut hampir selalu terlibat dalam perpindahan panas; namun, dalam banyak kasus adalah mungkin untuk mendapatkan hasil akurasi yang dapat diterima dengan mengukur hanya satu komponen.
Pengukuran aliran panas dengan konduktivitas termal
Perpindahan panas melalui dinding penghantar panas sangat penting di banyak bidang teknologi (penukar panas dari semua jenis, insulasi termal, dll.). Pada saat yang sama, bukan kontrol kuantitas produksi saat ini yang menarik, tetapi hasil pengukuran tunggal yang digunakan untuk menilai beban, memverifikasi pemenuhan indikator dan efisiensi yang dijamin.
Menurut hukum konduksi panas stasioner, fluks panas ditentukan oleh rumus berikut (J/s):
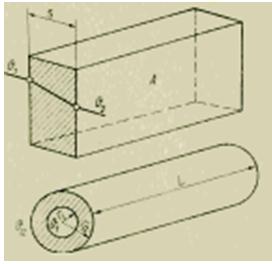
Karena konduktivitas termal dinding [J/(m*s*K)] dan dimensi geometrisnya diketahui, pengukuran fluks panas dikurangi untuk mengukur perbedaan suhu. Namun, teknik ini membutuhkan penentuan suhu permukaan yang sangat akurat. Kesalahan yang terkait dengan perubahan kondisi perpindahan panas saat memasang elemen sensitif suhu pada permukaan bisa sangat besar. Oleh karena itu, untuk pengukuran yang lebih akurat, metode di bawah ini direkomendasikan, di mana konduktivitas termal dan perpindahan panas digunakan secara bersamaan.
Pengukuran aliran panas dalam perpindahan panas (perpindahan panas dikombinasikan dengan konduksi panas)
Untuk dinding datar yang disebutkan pada bagian sebelumnya, hukum perpindahan panas (J/s) berikut ini berlaku:
![]() ,
,
dimana dalam koefisien perpindahan panas k 1J/(m2*s*K)], bersama dengan koefisien perpindahan panas [J/Dm*s*K)], koefisien perpindahan panas dan [J/(m2*s*K) ] dari kedua sisi dinding juga diperhitungkan.
Pada dinding datar yang dilalui oleh fluks panas yang diukur, pelat tipis kecil ditempatkan, suhu permukaannya ditentukan oleh termokopel film tipis built-in. Keuntungan pengukuran dengan cara ini adalah tidak memerlukan pengetahuan tentang sifat termal dinding, dan sifat pelat yang sesuai dapat dikurangi menjadi nilai konstan tunggal selama kalibrasi. Elemen sensitif semacam itu memiliki ukuran sekitar 30x30x0,5 mm; rentang pengukuran mencakup fluks panas dari 10 hingga 100.000 W/m2; kesalahannya adalah 2-5%.
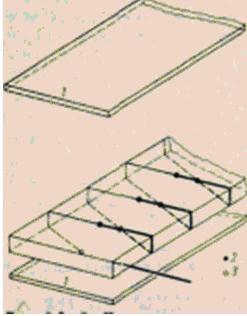
Gambar Prinsip pengoperasian meteran fluks panas.
Dengan peningkatan metode pengukuran ini, alas karet digunakan sebagai pengganti pelat yang dilapiskan. Dengan menempelkannya ke permukaan non-planar atau membungkusnya di sekitar permukaan melengkung, dimungkinkan untuk menentukan perpindahan panas dari permukaan dengan area yang relatif besar, misalnya, dari pipa, bejana, dll. Termokopel dibangun di kedua permukaan tikar sehingga persimpangan panas dan dinginnya terletak tepat satu sama lain (Gbr. 6). Dan dalam hal ini, kerapatan fluks panas sesuai dengan kalibrasi sebanding dengan perbedaan suhu. Namun, tikar yang diterapkan agak mengganggu perpindahan panas awal, yang menjadi terlihat dengan pengukuran yang akurat. Oleh karena itu, metode pengukuran ini terutama digunakan untuk menentukan konstanta termodinamika suatu zat, ketika pelanggaran aliran panas tidak mempengaruhi hasil pengukuran.
Pengukuran aliran panas di lingkungan saat ini.
Sebagian besar energi panas ditransfer oleh media cair atau gas (air, uap, dll.) yang bergerak dalam jaringan pipa tertutup. Namun, dibandingkan dengan transmisi energi listrik melalui kabel, jarak di mana energi panas dapat ditransmisikan terbatas. Untuk studi termoteknik dari semua jenis sistem pemanas dan pendingin, perlu untuk mengukur pelepasan dan konsumsi panas.
Fluks panas F (J/s), ditransmisikan oleh aliran medium - pembawa panas (kg/s) melalui bagian kontrol dengan luas A (m2) di zona tertentu, di mana neraca panas dikompilasi (dalam zona proses, Gambar. 7), sama dengan
Jumlah panas yang dilepaskan selama selang waktu t2 - t1 ditentukan sebagai integral (J):
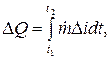
di mana perbedaan kandungan panas (entalpi, J/kg) pendingin di saluran masuk (indeks e) dan di saluran keluar (indeks a) dari zona keseimbangan panas.
Karena, dalam kasus umum, nilai entalpi hanya menarik dibandingkan dengan tingkat tertentu, misalnya, dengan entalpi pada suhu sekitar, semua pengukuran fluks panas pada dasarnya adalah pengukuran perbedaan.
Entalpi individu yang termasuk dalam persamaan umum dapat dinyatakan dalam suhu yang sesuai dan kapasitas panas spesifik;
Dengan demikian, pengukuran aliran panas secara langsung direduksi menjadi pengukuran suhu dan laju aliran massa. Dalam banyak kasus, bukan massa, tetapi aliran volume cairan pendingin diukur; dalam hal ini, hasil yang diperoleh hanya akan berbeda dengan nilai densitas cairan pendingin p. Kapasitas panas spesifik, ci, sendiri merupakan fungsi suhu. Namun, karena rentang pengukuran yang sempit dari banyak instrumen, mereka biasanya dapat dianggap sebagai nilai konstan tanpa banyak kehilangan akurasi. Kapasitas panas spesifik harus diketahui. Untuk cairan, persamaan aliran panas bahkan lebih disederhanakan, karena kapasitas panas spesifik independen dari tekanan:
![]() , J/s.
, J/s.
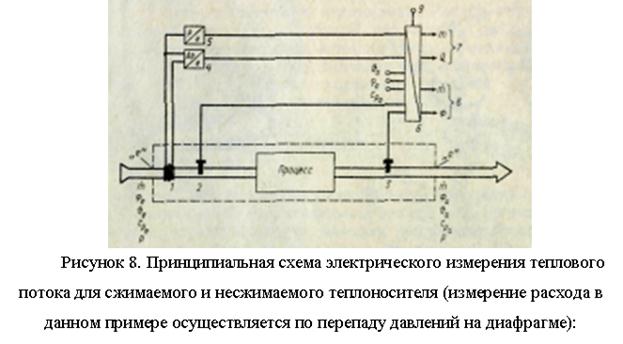
Dalam semua persamaan jenis ini, perlu untuk memperhitungkan tanda-tanda kuantitas tergantung pada apakah panas disuplai atau dihilangkan, apakah prosesnya endotermik atau eksotermik, apakah pendinginan atau pemanasan terjadi.
