Кількість теплоти в системі вимірюється. Методи та засоби вимірювання кількості тепла
Теплота- енергія, що передається від більш нагрітого тіла менш нагрітому при безпосередньому зіткненні або випромінюванні.
Мірою інтенсивності руху молекул є температура.
Кількість теплоти, яким володіє тіло за даної температури, залежить від його маси; наприклад, при одній і тій же температурі у великій чашці з водою полягає більше теплоти, ніж у маленькій, а у відрі з холодною водою його може бути більше, ніж у чашці з водою гарячою водою(хоча температура води у відрі та нижче).
Теплота відіграє у житті, зокрема й у функціонуванні його організму. Частина хімічної енергії, що міститься в їжі, перетворюється на теплоту, завдяки чому температура тіла підтримується близько 37°С. Тепловий баланс тіла людини також залежить від температури довкілля, і люди змушені витрачати багато енергії на обігрів житлових та виробничих приміщень взимку та на охолодження їх улітку. Більшу частину цієї енергії постачають теплові машини, наприклад котельні установки та парові турбіни електростанцій, що працюють на викопному паливі (вугілля, нафти) і виробляють електроенергію.
До кінця 18 ст. теплоту вважали матеріальною субстанцією, вважаючи, що температура тіла визначається кількістю міститься в ньому<калорической жидкости>, або<теплорода>. Пізніше Б.Румфорд, Дж.Джоуль та інші фізики того часу шляхом дотепних дослідів та міркувань спростували<калорическую>теорію, довівши, що теплота невагома і її можна отримувати у будь-яких кількостях просто за рахунок механічного руху. Теплота сама по собі не є речовиною - це лише енергія руху його атомів або молекул. Саме такого розуміння теплоти дотримується сучасна фізика.
У статті ми розглянемо, як пов'язані між собою теплота і температура і як вимірюють ці величини. Предметом нашого обговорення будуть також такі питання: передача теплоти від частини тіла до іншої; перенесення теплоти у вакуумі (просторі, що не містить речовини); роль теплоти у світі.
Теплота та температура
Кількість теплової енергії в речовині не можна визначити, спостерігаючи рух кожної його молекули окремо. Навпаки, лише вивчаючи макроскопічні властивості речовини, можна визначити усереднені протягом певного періоду показники мікроскопічного руху багатьох молекул. Температура речовини - це середній показник інтенсивності руху молекул, енергія якого і є теплова енергіяречовини.
Один з найзвичніших, але й найменш точних способів оцінки температури – на дотик. Торкаючись предмет, ми судимо про те, гарячий він чи холодний, орієнтуючись свої відчуття. Звичайно, ці відчуття залежать від температури нашого тіла, що підводить нас до поняття теплової рівноваги – одного з найважливіших при вимірі температури.
Теплова рівновага
Теплова рівновага між тілами А та В
Очевидно, що якщо два тіла A і B щільно притиснути один до одного, то, доторкнувшись їх досить довгий час, ми помітимо, що температура їх однакова. В цьому випадку говорять, що тіла A і B знаходяться в тепловій рівновазі один з одним. Однак тіла, взагалі кажучи, не обов'язково повинні стикатися, щоб між ними існувала теплова рівновага - достатньо, щоб їх температури були однаковими. У цьому можна переконатися за допомогою третього тіла C, привівши його спочатку теплову рівновагу з тілом A, а потім порівнявши температури тіл C і B. Тіло C тут грає роль термометра . У строгому формулюванні цей принцип називається нульовим початком термодинаміки: якщо тіла A і B знаходяться в тепловій рівновазі з третім тілом C, то ці тіла знаходяться також у тепловій рівновазі один з одним. Цей закон є основою всіх способів вимірювання температури.
Вимірювання температури

Температурні шкали

Термометри
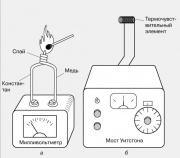
Термометри засновані на електричних ефектах
Якщо ми хочемо проводити точні експерименти та обчислення, то таких оцінок температури, як гарячий, теплий, холодний, холодний, недостатньо - нам потрібна проградуйована температурна шкала. Існує кілька таких шкал, і за точки відліку в них зазвичай взяті температури замерзання та кипіння води. Чотири найпоширеніші шкали представлені малюнку. Стоградусна шкала, за якою точці замерзання води відповідає 0 °, а точці кипіння 100 °, називається шкалою Цельсія на ім'я А. Цельсія, шведського астронома, який описав її в 1742. Вважають, що вперше застосував цю шкалу шведський натураліст К. Ліней. Зараз шкала Цельсія є найпоширенішою у світі. Температурна шкала Фаренгейта, в якій точкам замерзання і кипіння води відповідають вкрай незручні числа 32 і 212 °, була запропонована в 1724 р. Фаренгейтом. Шкала Фаренгейта широко поширена в англомовних країнах, але нею майже не користуються науковою літературою. Для переведення температури за Цельсієм (°С) у температуру за Фаренгейтом (°F) існує формула °F = (9/5)°C + 32, а для зворотного перекладу - формула °C = (5/9)(°F- 32).
Обидві шкали - як Фаренгейта, і Цельсія, - дуже незручні під час проведення експериментів за умов, коли температура опускається нижче точки замерзання води та виражається негативним числом. Для таких випадків були введені абсолютні шкали температур, в основі яких лежить екстраполяція до так званого абсолютного нуля - точки, в якій має припинитися молекулярний рух. Одна з них називається шкалою Ранкіна, а інша – абсолютною термодинамічною шкалою; температури за ними вимірюються у градусах Ранкіна (°R) та кельвінах (К). Обидві шкали починаються при температурі абсолютного нуля, а точка замерзання води відповідає 491,7°R і 273,16 K. Число градусів і кельвінів між точками замерзання та кипіння води за шкалою Цельсія та абсолютною термодинамічною шкалою дорівнює 100; для шкал Фаренгейта та Ранкіна воно теж однаково, але дорівнює 180. Градуси Цельсія переводяться в кельвіни за формулою K = ° C + 273,16, а градуси Фаренгейта - у градуси Ранкіна за формулою ° R = ° F + 459,7.
В основі дії приладів, призначених для вимірювання температури, лежать різні фізичні явища, пов'язані зі зміною теплової енергії речовини, - зміни електричного опору, об'єму, тиску, випромінювальних характеристик термоелектричних властивостей. Один з найпростіших і найзнайоміших інструментів для вимірювання температури – скляний термометр, зображений на малюнку. Кулю з нижньої частини термометра розташовують у середовищі або притискають до предмета, температуру якого хочуть виміряти, і в залежності від того, отримує кулька тепло або віддає, розширюється або стискається і її стовпчик піднімається або опускається в капілярі. Якщо термометр заздалегідь проградуйований і забезпечений шкалою, можна прямо дізнатися температуру тіла.
Інший прилад, дія якого ґрунтується на тепловому розширенні, - біметалічний термометр, зображений на малюнку. Основний його елемент - спіральна пластинка із двох спаяних металів із різними коефіцієнтами теплового розширення. При нагріванні один з металів розширюється сильніше за інший, спіраль закручується і повертає стрілку щодо шкали. Такі пристрої часто використовують для вимірювання температури повітря у приміщеннях та на вулиці, проте вони не підходять для визначення локальної температури.
Локальну температуру вимірюють зазвичай за допомогою термопари, що являє собою дві тяганини з різнорідних металів, спаяні з одного кінця. При нагріванні такого спаю на вільних кінцях тяганини виникає ЕРС, зазвичай складова кілька мілівольт. Термопари роблять із різних металевих пар: заліза та константану, міді та константану, хромелю та алюмелю. Їх термо-ЕРС практично лінійно змінюється з температурою у широкому температурному діапазоні.
Відомий і інший термоелектричний ефект - залежність опору провідного матеріалу від температури. Він лежить в основі роботи електричних термометрів опору, один із яких зображений на малюнку. Опір невеликого термочутливого елемента (термоперетворювача) - зазвичай котушки з тонкого дроту - порівнюють з опором змінного промінь резистора, використовуючи міст Уітстона. Вихідний пристрій може бути проградуйований безпосередньо в градусах.
Для вимірювання температури розпечених тіл, що випромінюють видиме світло, використовують оптичні пірометри . В одному з варіантів цього пристрою світло, що випромінюється тілом, порівнюють з випромінюванням нитки лампи розжарювання, поміщеної у фокальну площину бінокля, через який дивляться на тіло, що випромінює. Електричний струм, що нагріває нитку лампи, змінюють доти, доки при візуальному порівнянні свічення нитки і тіла не виявиться, що між ними встановилася теплова рівновага. Шкала приладу може бути проградуйована безпосередньо в одиницях температури.
Технічні досягнення останніх роківдозволили створити нові датчики температури. Наприклад, у випадках, коли потрібна особливо висока чутливість, замість термопари чи звичайного термометра опору використовують напівпровідниковий пристрій - термистор . В якості термоперетворювачів застосовують також барвники, що змінюють свій фазовий стан, і рідкі кристали, особливо в тих випадках, коли температура поверхні тіла змінюється в широкому діапазоні. Нарешті, використовується інфрачервона термографія, в якій отримують інфрачервоне зображення об'єкта в умовних кольорах, де кожен колір відповідає певній температурі. Цей спосіб вимірювання температури знаходить найширше застосування - від медичної діагностикидо перевірки теплоізоляції приміщень.
Вимірювання кількості теплоти
Водяний калориметр
Теплову енергію (кількість теплоти) тіла можна виміряти безпосередньо за допомогою так званого калориметра; простий варіант такого приладу зображено малюнку. Це ретельно теплоізольований закритий посуд, з пристроями для вимірювання температури всередині нього і іноді заповнюється робочою рідиною з відомими властивостями, наприклад водою . Щоб виміряти кількість теплоти у невеликому нагрітому тілі, його поміщають у калориметр і чекають, коли система прийде у теплову рівновагу. Кількість теплоти, передана калориметру (точніше, що наповнює його воді), визначають підвищення температури води.
Кількість теплоти, що виділяється в ході хімічної реакції, наприклад горіння, можна виміряти, помістивши в невелику калориметр<бомбу>. У<бомбе>знаходяться зразок, до якого підведені електричні дроти для підпалу, та відповідну кількість кисню. Після того як зразок повністю згоряє і встановлюється теплова рівновага, визначають, наскільки підвищилася температура води в калориметрі, а звідси - кількість теплоти, що виділилася.
Одиниці виміру теплоти
Теплота є однією з форм енергії, а тому повинна вимірюватися в одиницях енергії. У міжнародній системі СІ одиницею енергії є Джоуль (Дж). Допускається також застосування позасистемних одиниць кількості теплоти – калорій: міжнародна калорія дорівнює 4,1868 Дж, термохімічна калорія – 4,1840 Дж. У зарубіжних лабораторіях результати досліджень часто виражають за допомогою т.зв. 15-градусної калорії, що дорівнює 4,1855 Дж. Виходить із вживання позасистемна британська теплова одиниця (БТЕ): БТЕ середня = 1,055 Дж.
Джерела теплоти
Основними джерелами теплоти є хімічні та ядерні реакції, а також різні процеси перетворення енергії. Прикладами хімічних реакцій із теплоти є горіння і розщеплення компонентів їжі. Майже вся теплота, одержувана Землею, забезпечується ядерними реакціями, які у надрах Сонця. Людство навчилося отримувати теплоту за допомогою керованих процесів розподілу ядер, а тепер намагається використати з тією ж метою реакції термоядерного синтезу. На теплоту можна перетворювати й інші види енергії, наприклад механічну роботу та електричну енергію. Важливо пам'ятати, що теплову енергію (як і будь-яку іншу) можна лише перетворити на іншу форму, але не можна не отримати<из ничего>, не знищити. Це з основних принципів науки, званої термодинамікою .
Термодинаміка
Термодинаміка- це наука про зв'язок між теплотою, роботою та речовиною. Сучасні уявлення про ці взаємозв'язки сформувалися на основі праць таких великих учених минулого, як Карно, Клаузіус, Гіббс, Джоуль, Кельвін та ін. Термодинаміка пояснює сенс теплоємності та теплопровідності речовини, теплового розширення тіл, теплоти фазових переходів. Ця наука базується на кількох експериментально встановлених законах – засадах.
Теплота та властивості речовин
Різні речовинимають різну здатність накопичувати теплову енергію; це залежить від їхньої молекулярної структури і щільності. Кількість теплоти, необхідне підвищення температури одиниці маси речовини однією градус, називається його питомої теплоємністю . Теплоємність залежить від умов, у яких знаходиться речовина. Наприклад, щоб нагріти на 1 К один грам повітря в повітряній кулі, потрібно більше теплоти, ніж для такого ж його нагріву в герметичній посудині з жорсткими стінками, оскільки частина енергії, що повідомляється повітряній кулі, витрачається на розширення повітря, а не на його нагрівання. Тому, зокрема, теплоємність газів вимірюють окремо при постійному тиску і постійному обсязі.
У разі підвищення температури інтенсивність хаотичного руху молекул зростає - більшість речовин при нагріванні розширюється. Ступінь розширення речовини при підвищенні температури на 1 К називається коефіцієнтом теплового розширення.
Щоб речовина перейшла з одного фазового стану в інший, наприклад, з твердого в рідкий (а іноді відразу в газоподібний), воно має отримати певну кількість тепла. Якщо нагрівати тверде тіло, його температура буде підвищуватися до тих пір, поки воно не почне плавитися; до завершення плавлення температура тіла залишатиметься постійною, незважаючи на підведення тепла. Кількість теплоти, необхідне плавлення одиниці маси речовини, називається теплотою плавлення. Якщо підводити тепло і далі, то розплавлена речовина нагріється до кипіння. Кількість теплоти, необхідне випаровування одиниці маси рідини при цій температурі, називається теплотою пароутворення.
Роль теплоти та її використання
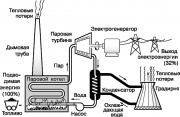
Схема роботи паротурбінної електростанції
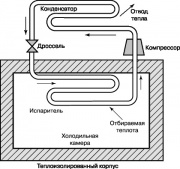
Схема холодильного циклу
Глобальні процеси теплообміну не зводяться до нагрівання Землі сонячним промінням. Масивними конвекційними потоками в атмосфері визначаються добові зміни погодних умов на всій земній кулі. Перепади температури в атмосфері між екваторіальними і полярними областями спільно з коріолісовими силами, зумовленими обертанням Землі, призводять до появи конвекційних потоків, що безперервно змінюються, таких, як пасати, струменеві течії, а також теплі і холодні фронти.
Перенесення тепла (за рахунок теплопровідності) від розплавленого ядра Землі до її поверхні призводить до виверження вулканів та появи гейзерів. У деяких регіонах геотермальна енергія використовується для обігріву приміщень та вироблення електроенергії.
Теплота - неодмінний учасник багатьох виробничих процесів. Згадаємо такі найважливіші з них, як виплавка та обробка металів, робота двигунів, виробництво харчових продуктів, хімічний синтез, переробка нафти, виготовлення найрізноманітніших предметів - від цегли та посуду до автомобілів та електронних пристроїв.
Багато промислові виробництва та транспорт, і навіть теплоелектростанції було неможливо працювати без теплових машин - пристроїв, які перетворюють теплоту на корисну работу. Прикладами таких машин можуть бути компресори, турбіни, парові, бензинові і реактивні двигуни.
Однією з найвідоміших теплових машин є парова турбіна, в якій реалізується частина циклу Ранкіна, що використовується на сучасних електростанціях. Спрощена схема цього циклу представлена малюнку. Робочу рідину - воду - перетворюють на перегріту пару в паровому казані, що нагрівається за рахунок спалювання викопного палива (вугілля, нафти або природного газу). Пар високого
Газовик - промислове газове обладнання Довідник ДЕРЖСТАНДАРТ, СНиП, ПБ
Одиниці вимірювання температури та кількості тепла
Основною одиницею вимірювання температури був градус Міжнародної температурної шкали, що практично відповідає градусу Цельсія. Ця величина дорівнює 1/100 температурного інтервалу між 0 і 100 ° С, тобто між температурами плавлення льоду та кипіння води при тиску 760 мм рт. ст.
Абсолютною температурою називається температура, яка відраховується від абсолютного нуля, тобто від -273,16 ° С, і вимірювана в градусах Кельвіна (° К). Градус Кельвіна за величиною відрізняється від градуса Цельсія. Тому абсолютна температура виражається у градусах стоградусної шкали наступним чином:
Т, ° К = t, ° С + 273,16
У системі СІ одиницею вимірювання температури встановлено градус Кельвіна. Допускається для вираження практичних результатів вимірювання температури застосування градуса Цельсія поряд із градусом Кельвіна, залежно від початку відліку (положення нуля) за шкалою.
Приклад: 250 ±5 °С = 523,16 ±5 °К.
У системі СІ робота, енергія та кількість теплоти вимірюються у джоулях (Дж). Іноді застосовують більшу і зручну для практичних цілей одиницю — кілоджоуль (кДж), рівний 1000 Дж. фізична величина, що показує, яку роботу може зробити тіло.
Як позасистемні теплові одиниці допускається застосування калорії та кілокалорії. Калорія - це кількість тепла, необхідного для нагрівання 1 г води на 1 ° С (від 195 до 205 С).
1 кал (калорія) = 4,1868 Дж;
1 ккал (кілокалорія) = 1000 кал = 4186,8 Дж = 4,187 кДж;
1 Мкал (мегакалорія) = 106 кал = 4,1868 МДж;
1 Гкал (гігакалорія) = 109 кал = 4186,8 МДж.
Для порівняння в оцінці палива застосовується так зване умовне тепло, теплота згоряння якого до розрахунку приймається умовно дорівнює 7 Мкал/кг чи 7 Гкал/т. У разі говорять відповідно про 1 кг чи 1 т умовного палива (т. в. т.).
Теплота відіграє у житті, зокрема й у функціонуванні його організму. Частина хімічної енергії, що міститься в їжі, перетворюється на теплоту, завдяки чому температура тіла підтримується поблизу 37
° С. Тепловий баланс тіла людини залежить також від температури навколишнього середовища, і люди змушені витрачати багато енергії на обігрів житлових та виробничих приміщень узимку та на охолодження їх улітку. Більшу частину цієї енергії постачають теплові машини, наприклад котельні установки та парові турбіни електростанцій, що працюють на викопному паливі (вугілля, нафти) і виробляють електроенергію.До кінця 18 ст. теплоту вважали матеріальною субстанцією, вважаючи, що температура тіла визначається кількістю «калоричної рідини», що міститься в ньому, або «теплороду». Пізніше Б.Румфорд, Дж.Джоуль та інші фізики того часу шляхом дотепних дослідів та міркувань спростували «калоричну» теорію, довівши, що теплота невагома і її можна отримувати у будь-яких кількостях просто за рахунок механічного руху. Теплота сама по собі не є речовиною - це лише енергія руху його атомів або молекул. Саме такого розуміння теплоти дотримується сучасна фізика. Див. такожФізика.
У статті ми розглянемо, як пов'язані між собою теплота і температура і як вимірюють ці величини. Предметом нашого обговорення будуть також такі питання: передача теплоти від частини тіла до іншої; перенесення теплоти у вакуумі (просторі, що не містить речовини); роль теплоти у світі.
ТЕПЛОТА ТА ТЕМПЕРАТУРА Кількість теплової енергії в речовині не можна визначити, спостерігаючи рух кожної його молекули окремо. Навпаки, лише вивчаючи макроскопічні властивості речовини, можна визначити усереднені протягом певного періоду показники мікроскопічного руху багатьох молекул. Температура речовини це середній показник інтенсивності руху молекул, енергія якого і є теплова енергія речовини.Один з найзвичніших, але й найменш точних способів оцінки температури на дотик. Торкаючись предмет, ми судимо про те, гарячий він чи холодний, орієнтуючись свої відчуття. Звичайно, ці відчуття залежать від температури нашого тіла, що підводить нас до поняття теплової рівноваги - одному з найважливіших при вимірі температури.
Теплова рівновага. Очевидно, що якщо два тіла A і B (Рис. 1) щільно притиснути один до одного, то, доторкнувшись їх через досить довгий час, ми помітимо, що температура їх однакова. У цьому випадку кажуть, що тіла A і B перебувають у тепловому рівновазі друг з одним. Однак тіла, взагалі кажучи, не обов'язково повинні стикатися, щоб між ними існувала теплова рівновага, достатньо, щоб їх температури були однаковими. У цьому можна переконатися за допомогою третього тіла C , привівши його спочатку в теплову рівновагу з тілом A , а потім порівнявши температури тіл C і B. Тіло C тут грає роль термометра. У строгому формулюванні цей принцип називається нульовим початком термодинаміки: якщо тіла A і B перебувають у тепловому рівновазі з третім тілом C, ці тіла перебувають у тепловому рівновазі друг з одним.Цей закон є основою всіх способів вимірювання температури.Вимірювання температури. Якщо ми хочемо проводити точні експерименти та обчислення, то таких оцінок температури, як гарячий, теплий, прохолодний, холодний, недостатньо нам потрібна проградуйована температурна шкала. Існує кілька таких шкал, і за точки відліку в них зазвичай взяті температури замерзання та кипіння води. Чотири найпоширеніші шкали представлені на рис. 2. Стоградусна шкала, за якою точці замерзання води відповідає 0° , а точці кипіння 100° , називається шкалою Цельсія на ім'я А.Цельсія, шведського астронома, який описав її в 1742. Вважають, що вперше застосував цю шкалу шведський натураліст К.Лінней. Зараз шкала Цельсія є найпоширенішою у світі. Температурна шкала Фаренгейта, в якій точкам замерзання та кипіння води відповідають вкрай незручні числа 32 та 212° , була запропонована в 1724 р. Фаренгейтом. Шкала Фаренгейта широко поширена в англомовних країнах, але нею майже не користуються науковою літературою. Для переведення температури за Цельсієм (° С) в температуру за Фаренгейтом (° F) існує формула° F = (9/5) ° C + 32, а для зворотного перекладу формула° C = (5/9) (° F - 32). Обидві шкали як Фаренгейта, так і Цельсія, дуже незручні при проведенні експериментів в умовах, коли температура опускається нижче точки замерзання води і виражається негативним числом. Для таких випадків були введені абсолютні шкали температур, в основі яких лежить екстраполяція до так званого абсолютного нуля точки, в якій має припинитися молекулярний рух. Одна з них називається шкалою Ранкіна, а інша - абсолютною термодинамічною шкалою; температури за ними вимірюються в градусах Ранкіна (° R) та кельвінах (К). Обидві шкали починаються при температурі абсолютного нуля, а точка замерзання води відповідає 491,7° R і 273,16 K. Число градусів і кельвінів між точками замерзання та кипіння води за шкалою Цельсія та абсолютною термодинамічною шкалою однаково і дорівнює 100; для шкал Фаренгейта та Ранкіна воно теж однаково, але дорівнює 180. Градуси Цельсія переводяться в кельвіни за формулою K =° C + 273,16, а градуси Фаренгейта в градуси Ранкіна за формулою° R = ° F + 459,7. В основі дії приладів, призначених для вимірювання температури, лежать різні фізичні явища, пов'язані зі зміною теплової енергії речовини, зміни електричного опору, обсягу, тиску, випромінювальних характеристик, термоелектричних властивостей. Один з найпростіших і знайомих інструментів для вимірювання температури - ртутний скляний термометр, зображений на рис. 3, а. Кульку з ртуттю в нижній частині термометра розташовують у середовищі або притискають до предмета, температуру якого хочуть виміряти, і в залежності від того, отримує кулька тепло або віддає, ртуть розширюється або стискається і її стовпчик піднімається або опускається в капілярі. Якщо термометр заздалегідь проградуйований і забезпечений шкалою, можна прямо дізнатися температуру тіла.Інший прилад, дія якого заснована на тепловому розширенні, біметалічний термометр, зображений на рис.
3, б. Основний його елемент спіральна пластинка із двох спаяних металів з різними коефіцієнтами теплового розширення. При нагріванні один з металів розширюється сильніше за інший, спіраль закручується і повертає стрілку щодо шкали. Такі пристрої часто використовують для вимірювання температури повітря у приміщеннях та на вулиці, проте вони не підходять для визначення локальної температури.Локальну температуру вимірюють зазвичай за допомогою термопари, що являє собою дві зволікання з різнорідних металів, спаяні з одного кінця (рис.
4, а). При нагріванні такого спаю на вільних кінцях тяганини виникає ЕРС, що зазвичай становить кілька мілівольт. Термопари роблять із різних металевих пар: заліза та константану, міді та константану, хромелю та алюмелю. Їх термо-ЕРС практично лінійно змінюється з температурою у широкому температурному діапазоні.Відомий і інший термоелектричний ефект залежність опору провідного матеріалу від температури. Він лежить в основі роботи електричних термометрів опору, один із яких зображений на рис.
4, б. Опір невеликого термочутливого елемента (термоперетворювача) зазвичай котушки з тонкого дроту порівнюють з опором проградуйованого змінного резистора, використовуючи міст Уітстона. Вихідний пристрій може бути проградуйований безпосередньо в градусах.Для вимірювання температури розпечених тіл, що випромінюють видиме світло, використовують оптичні пірометри. В одному з варіантів цього пристрою світло, що випромінюється тілом, порівнюють з випромінюванням нитки лампи розжарювання, поміщеної у фокальну площину бінокля, через який дивляться на тіло, що випромінює. Електричний струм, що нагріває нитку лампи, змінюють доти, доки при візуальному порівнянні світіння нитки та тіла не виявиться, що між ними встановилася теплова рівновага. Шкала приладу може бути проградуйована безпосередньо в одиницях температури.
Технічні здобутки останніх років дозволили створити нові датчики температури. Наприклад, у тих випадках, коли потрібна особливо висока чутливість, замість термопари або звичайного термометра опору використовують напівпровідниковий пристрій термістор. В якості термоперетворювачів застосовують також барвники, що змінюють свій фазовий стан, і рідкі кристали, особливо в тих випадках, коли температура поверхні тіла змінюється в широкому діапазоні. Нарешті, використовується інфрачервона термографія, в якій отримують інфрачервоне зображення об'єкта в умовних кольорах, де кожен колір відповідає певній температурі. Цей спосіб вимірювання температури знаходить найширше застосування від медичної діагностики до перевірки теплоізоляції приміщень. Див. такожФІЗИКА ТВЕРДОГО ТІЛА; РІДКИЙ КРИСТАЛ.
Вимірювання кількості теплоти. Теплову енергію (кількість теплоти) тіла можна виміряти за допомогою так званого калориметра; простий варіант такого приладу зображено на рис. 5. Це ретельно теплоізольований закритий посуд, з пристроями для вимірювання температури всередині нього і іноді заповнюється робочою рідиною з відомими властивостями, наприклад водою. Щоб виміряти кількість теплоти у невеликому нагрітому тілі, його поміщають у калориметр і чекають, коли система прийде у теплову рівновагу. Кількість теплоти, передана калориметру (точніше, що наповнює його воді), визначають підвищення температури води.Кількість теплоти, що виділяється в ході хімічної реакції, наприклад, горіння, можна виміряти, помістивши в калориметр невелику «бомбу». У «бомбі» знаходяться зразок, до якого підведено електричні дроти для підпалу, та відповідну кількість кисню. Після того як зразок повністю згоряє і встановлюється теплова рівновага, визначають, наскільки підвищилася температура води в калориметрі, а звідси - кількість теплоти, що виділилася. Див. такожКАЛОРИМЕТРІЯ.
Одиниці виміру теплоти. Теплота є однією з форм енергії, а тому повинна вимірюватися в одиницях енергії. У міжнародній системі СІ одиницею енергії є Джоуль (Дж). Допускається також застосування позасистемних одиниць кількості теплоти калорій: міжнародна калорія дорівнює 4,1868 Дж, термохімічна калорія 4,1840 Дж. У зарубіжних лабораторіях результати досліджень часто виражають за допомогою т.зв. 15-градусної калорії, що дорівнює 4,1855 Дж. Виходить із вживання позасистемна британська теплова одиниця (БТЕ): БТЕ середня = 1,055 Дж. Основними джерелами теплоти є хімічні та ядерні реакції, а також різні процеси перетворення енергії. Прикладами хімічних реакцій із теплоти є горіння і розщеплення компонентів їжі. Майже вся теплота, одержувана Землею, забезпечується ядерними реакціями, які у надрах Сонця. Людство навчилося отримувати теплоту за допомогою керованих процесів розподілу ядер, а тепер намагається використати з тією ж метою реакції термоядерного синтезу. На теплоту можна перетворювати й інші види енергії, наприклад механічну роботу та електричну енергію. Важливо пам'ятати, що теплову енергію (як і будь-яку іншу) можна лише перетворити на іншу форму, але не можна отримати «з нічого», ні знищити. Це з основних принципів науки, званої термодинамікою. ТЕРМОДИНАМІКА Термодинаміка - це наука про зв'язок між теплотою, роботою і речовиною. Сучасні уявлення про ці взаємозв'язки сформувалися на основі праць таких великих учених минулого, як Карно, Клаузіус, Гіббс, Джоуль, Кельвін та ін. Термодинаміка пояснює сенс теплоємності та теплопровідності речовини, теплового розширення тіл, теплоти фазових переходів. Ця наука базується на кількох експериментально встановлених законах, засадах.Почала термодинаміки. Сформульований вище нульовий початок термодинаміки вводить поняття теплової рівноваги, температури та термометрії. Перший початок термодинаміки є твердженням, що має ключове значення для всієї науки в цілому: енергію не можна ні знищити, ні отримати «з нічого», так що повна енергія Всесвіту є постійна величина. У найпростішій формі перший початок термодинаміки можна сформулювати так: енергія, яку отримує система, мінус енергія, яку вона віддає, дорівнює енергії, що залишається в системі. На перший погляд це твердження здається очевидним, але не таким, наприклад, ситуації, як згоряння бензину в циліндрах автомобільного двигуна: тут одержувана енергія є хімічною, що віддається механічною (роботою), а енергія, що залишається в системі, теплової.Отже, ясно, що енергія може переходити з однієї форми в іншу і такі перетворення постійно відбуваються в природі і техніці. Понад сто років тому Дж.Джоуль довів це для випадку перетворення механічної енергії на теплову за допомогою пристрою, показаного на рис. 6, а. У цьому пристрої вантажі, що опускаються і піднімаються, обертали вал з лопатями в заповненому водою калориметрі, в результаті чого вода нагрівалася. Точні вимірювання дозволили Джоулю визначити, що одна калорія теплоти еквівалентна 4,186 Дж механічної роботи. Пристрій, зображений на рис.
6, б, використовувалося визначення теплового еквівалента електричної енергії.Перше початок термодинаміки пояснює багато звичайних явищ. Наприклад, стає зрозумілим, чому не можна охолодити кухню за допомогою відкритого холодильника. Припустимо, що ми теплоізолювали кухню від навколишнього середовища. По дроту живлення холодильника в систему безперервно підводиться енергія, але ніякої енергії система не віддає. Таким чином, її повна енергія зростає, і в кухні стає все тепліше: досить доторкнутися до трубки теплообмінника (конденсатора) на задній стінці холодильника, і ви зрозумієте марність його як «охолоджуючого» пристрою. Але якби ці трубки було виведено межі системи (наприклад, за вікно), то кухня віддавала більше енергії, ніж отримувала, тобто. охолоджувалась би, а холодильник працював як віконний кондиціонер.
Перший початок термодинаміки - закон природи, що виключає створення заново або знищення енергії. Однак воно нічого не говорить про те, як протікають у природі процеси передачі енергії. Так, ми знаємо, що гаряче тіло нагріє холодне, якщо ці тіла привести до зіткнення. Але чи зможе холодне тіло саме собою передати запас своєї теплоти гарячому? Остання можливістькатегорично відкидається другим початком термодинаміки.
Перший початок виключає можливість створення двигуна з коефіцієнтом корисної дії(ККД) більше 100% (подібний
«Вічний» двигун міг би скільки завгодно довго віддавати більше енергії, ніж сам споживає). Не можна побудувати двигун навіть з ККД, рівним 100%, так як деяка частина енергії, що підводиться до нього, обов'язково повинна бути втрачена ним у вигляді менш корисної теплової енергії. Так, колесо не буде крутитися скільки завгодно довго без підведення енергії, оскільки внаслідок тертя в підшипниках енергія механічного руху поступово переходитиме в теплоту, поки колесо не зупиниться.Тенденцію до перетворення «корисної» роботи на менш корисну енергію «теплоту» можна зіставити з іншим процесом, який відбувається, якщо з'єднати дві судини, що містять різні гази. Почекавши досить довго, ми виявляємо в обох судинах однорідну суміш газів природа діє так, що впорядкованість системи зменшується. Термодинамічна міра цієї невпорядкованості називається ентропією, і другий початок термодинаміки можна сформулювати інакше: процеси у природі завжди протікають отже ентропія системи та її оточення збільшується. Таким чином, енергія Всесвіту залишається постійною, а її ентропія безперервно зростає.
Теплота та властивості речовин. Різні речовини мають різну здатність накопичувати теплову енергію; це залежить від їхньої молекулярної структури і щільності. Кількість теплоти, необхідне підвищення температури одиниці маси речовини однією градус, називається його питомою теплоємністю. Теплоємність залежить від умов, у яких знаходиться речовина. Наприклад, щоб нагріти на 1 К один грам повітря в повітряній кулі, потрібно більше теплоти, ніж для такого ж його нагріву в герметичній посудині з жорсткими стінками, оскільки частина енергії, що повідомляється повітряній кулі, витрачається на розширення повітря, а не на його нагрівання. Тому, зокрема, теплоємність газів вимірюють окремо при постійному тиску та при постійному обсязі.При підвищенні температури інтенсивність хаотичного руху молекул зростає, більшість речовин при нагріванні розширюється. Ступінь розширення речовини у разі підвищення температури на 1 К називається коефіцієнтом теплового розширення.
Щоб речовина перейшла з одного фазового стану в інший, наприклад, з твердого в рідке (а іноді відразу в газоподібне), воно має отримати певну кількість тепла. Якщо нагрівати тверде тіло, його температура буде підвищуватися до того часу, поки воно почне плавитися; до завершення плавлення температура тіла залишатиметься постійною, незважаючи на підведення тепла. Кількість теплоти, необхідне плавлення одиниці маси речовини, називається теплотою плавлення. Якщо підводити тепло і далі, то розплавлена речовина нагріється до кипіння. Кількість теплоти, необхідне випаровування одиниці маси рідини при цій температурі, називається теплотою пароутворення.
Молекулярно-кінетична теорія. Молекулярно-кінетична теорія пояснює макроскопічні властивості речовини, розглядаючи на мікроскопічному рівні поведінку атомів і молекул, що становлять цю речовину. При цьому використовується статистичний підхід і робляться деякі припущення щодо самих частинок та характеру їхнього руху. Так, молекули вважаються твердими кульками, які у газових середовищах перебувають у безперервному хаотичному русі і пробігають значні відстані від одного зіткнення до іншого. Зіткнення вважаються пружними та відбуваються між частинками, розмір яких малий, а число дуже велике. Жоден з реальних газів не відповідає точності цієї моделі, проте більшість газів досить близькі до неї, чим і зумовлена практична цінність молекулярно-кінетичної теорії.Виходячи з цих уявлень та використовуючи статистичний підхід, Максвелл вивів розподіл швидкостей молекул газу в обмеженому обсязі, названий згодом його ім'ям. Цей розподіл представлений графічно на рис. 7 для певної маси водню при температурах 100 і 1000
° C. По осі ординат відкладається число молекул, що рухаються зі швидкістю, вказаною на осі абсцис. Повне число частинок дорівнює площі під кожною кривою та в обох випадках однаково. З графіка видно, що більшість частинок має швидкості, близькі до деякого середнього значення, і лише мале їх число має дуже високі або низькі швидкості. Середні швидкості при зазначених температурах лежать в інтервалі 20003000 м / с, тобто. дуже великі.Велика кількість молекул газу, що настільки швидко рухаються, діє з цілком вимірною силою на навколишні тіла. Мікроскопічні сили, з якими численні молекули газу вдаряють стінки судини, складаються в макроскопічну величину, звану тиском. При підведенні енергії до газу (підвищення температури) середня кінетична енергія його молекул зростає, частки газу частіше і сильніше ударяють об стінки, тиск підвищується, і якщо стінки не цілком жорсткі, то вони розтягуються і обсяг газу збільшується. Так, мікроскопічний статистичний підхід, що лежить в основі молекулярно-кінетичної теорії, дозволяє пояснити явище теплового розширення, про яке ми говорили.
Ще один результат молекулярно-кінетичної теорії - закон, що описує властивості газу, який задовольняє переліченим вище вимогам. Це так зване рівняння стану ідеального газупов'язує тиск, об'єм і температуру одного моля газу і має вигляд рівності
PV = RT, де P тиск, V обсяг, T температура, а R універсальна газова постійна, рівна (8,31441± 0,00026) Дж/(моль Ч До). Див. такожМОЛЕКУЛЯРНО-КІНЕТИЧНА ТЕОРІЯ;Термодинаміка. ТЕПЛОПЕРЕДАЧА Теплопередача - це процес перенесення теплоти всередині тіла або від одного тіла до іншого, обумовлений різницею температур. Інтенсивність перенесення теплоти залежить від властивостей речовини, різниці температур та підпорядковується експериментально встановленим законам природи. Щоб створювати ефективно працюючі системи нагрівання чи охолодження, різноманітні двигуни, енергоустановки, системи теплоізоляції, потрібно знати принципи теплопередачі. В одних випадках теплообмін небажаний (теплоізоляція плавильних печей, космічних кораблів тощо), а в інших він має бути якнайбільше (парові котли, теплообмінники, кухонний посуд).Існують три основні види теплопередачі: теплопровідність, конвекція та променистий теплообмін.
Теплопровідність. Якщо всередині тіла є різниця температур, то теплова енергія переходить від гарячішої його частини до холоднішої. Такий вид теплопередачі, зумовлений тепловими рухами та зіткненнями молекул, називається теплопровідністю; при достатньо високих температураху твердих тілах його можна спостерігати візуально. Так, при нагріванні сталевого стрижня з одного кінця в полум'ї газового пальника теплова енергія передається по стрижню, і на деяку відстань від кінця, що нагрівається, поширюється світіння (з видаленням від місця нагріву все менш інтенсивне).Інтенсивність теплопередачі з допомогою теплопровідності залежить від градієнта температури, тобто. відносини
D Т/D x різниці температур на кінцях стрижня на відстані між ними. Вона також залежить від площі поперечного перерізу стрижня (в м 2 ) та коефіцієнта теплопровідності матеріалу[ у відповідних одиницях Вт/(мЧ К)] . Співвідношення між цими величинами було виведено французьким математиком Ж. Фур'є і має такий вигляд:де q тепловий потік, k коефіцієнт теплопровідності, а A площа поперечного перерізу. Це співвідношення називається законом теплопровідності Фур'є; знак «мінус» у ньому свідчить про те, що теплота передається у напрямку, зворотному градієнту температури.З закону Фур'є випливає, що тепловий потік можна знизити, зменшивши одну з величин коефіцієнт теплопровідності, площу або градієнт температури. Для будівлі в зимових умовах останні величини практично постійні, а тому підтримки в приміщенні потрібної температури залишається зменшувати теплопровідність стін, тобто. покращувати їхню теплоізоляцію.
У таблиці представлені коефіцієнти теплопровідності деяких речовин та матеріалів. З таблиці видно, що одні метали проводять тепло набагато краще за інших, але вони є значно кращими провідниками тепла, ніж повітря і пористі матеріали.
|
ТЕПЛОПРОВІДНІСТЬ ДЕЯКИХ РЕЧОВИН І МАТЕРІАЛІВ |
|
|
Речовини та матеріали |
Теплопровідність, Вт/(м×К) |
| Алюміній | |
| Бронза | |
| Вісмут | |
| Вольфрам | |
| Залізо | |
| Золото | |
| Кадмій | |
| Магній | |
| Мідь | |
| Миш'як | |
| Нікель | |
| Платина | |
| Ртуть | |
| Свинець | |
| Цинк | |
|
Інші матеріали |
|
| Азбест | |
| Бетон | |
| Повітря | |
| Гагачий пух (нещільний) | |
| Дерево (горіх) | |
| Магнезія (MgO) | |
| Тирса | |
| Гума (губчаста) | |
| Слюда | |
| Скло | |
| Вуглець (графіт) | |
Тепловий та електричний опір багатьох речовин різко зменшується при зниженні температури нижче температури рідкого гелію (1,8 K). Це явище, зване надпровідністю, використовується для підвищення ефективності роботи багатьох пристроїв від приладів мікроелектроніки до ліній електропередачі і великих електромагнітів. Див. такожСВЕРХПРОВІДНІСТЬ.
Конвекція. Як ми вже говорили, при підведенні тепла до рідини або газу збільшується інтенсивність руху молекул, а внаслідок цього підвищується тиск. Якщо рідина чи газ не обмежені обсягом, всі вони розширюються; локальна щільність рідини (газу) стає меншою, і завдяки виштовхуючим (архімедовим) силам нагріта частина середовища рухається вгору (саме тому тепле повітря в кімнаті піднімається від батарей до стелі). Це явище називається конвекцією. Щоб не витрачати тепло опалювальної системи, потрібно користуватися сучасними обігрівачами, що забезпечують примусову циркуляцію повітря.Конвективний тепловий потік від нагрівача до середовища, що нагрівається, залежить від початкової швидкості руху молекул, щільності, в'язкості, теплопровідності і теплоємності і середовища; дуже важливі також розмір та форма нагрівача. Співвідношення між відповідними величинами підпорядковується закону Ньютона
q = hA ( T W- T Ґ ), де q тепловий потік (вимірюваний у ватах), A Площа поверхні джерела тепла (в м 2), T Wі T Ґ ¦ температури джерела та його оточення (у кельвінах). Коефіцієнт конвективного теплоперенесення h залежить від властивостей середовища, початкової швидкості її молекул, а також від форми джерела тепла і вимірюється в одиницях Вт/(м 2 год До).Величина
h неоднакова для випадків, коли повітря навколо нагрівача нерухоме (вільна конвекція) і коли той же нагрівач знаходиться в повітряному потоці (вимушена конвекція). У простих випадках течії рідини по трубі або обтікання плоскої поверхні коефіцієнт h можна розрахувати теоретично. Однак знайти аналітичне рішення задачі про конвекцію для турбулентного перебігу середовища поки що не вдається. Турбулентність - це складний рух рідини (газу), хаотичний в масштабах, що істотно перевищують молекулярні.Якщо нагріте (або, навпаки, холодне) тіло помістити в нерухоме середовище або потік, то навколо нього утворюються конвективні струми і прикордонний шар. Температура, тиск та швидкість руху молекул у цьому шарі відіграють важливу роль при визначенні коефіцієнта конвективного теплоперенесення.
Конвекцію необхідно враховувати під час проектування теплообмінників, систем кондиціювання повітря, високошвидкісних літальних апаратів та багатьох інших пристроїв. У всіх подібних системах одночасно з конвекцією має місце теплопровідність, причому як між твердими тілами, так і в навколишньому середовищі. При підвищених температурахСуттєву роль може грати і променистий теплообмін.
Променистий теплообмін. Третій вид теплопередачі променистий теплообмін відрізняється від теплопровідності та конвекції тим, що теплота в цьому випадку може передаватися через вакуум. Подібність його з іншими способами передачі тепла в тому, що він теж обумовлений різницею температур. Теплове випромінювання - це один з видів електромагнітного випромінювання. Інші його види радіохвильове, ультрафіолетове і гамма-випромінювання виникають у відсутності різниці температур.На рис. 8 представлено залежність енергії теплового (інфрачервоного) випромінювання від довжини хвилі. Теплове випромінювання може супроводжуватися випромінюванням видимого світла, але його енергія мала в порівнянні з енергією випромінювання невидимої частини спектра.
Інтенсивність теплопередачі шляхом теплопровідності та конвекції пропорційна температурі, а променистий тепловий потік пропорційний четвертому ступеню температури і підпорядковується закону Стефана Больцмана.
Житлові та офісні приміщення часто обігрівають невеликими електричними тепловипромінювачами; червоне свічення їх спіралей - це видиме теплове випромінювання, близьке до межі інфрачервоної частини спектра. Приміщення ж обігрівається теплотою, яку несе переважно невидима, інфрачервона частина випромінювання. У приладах нічного ви
^ ня застосовуються джерело теплового випромінювання і приймач, чутливий до ІЧ-випромінювання, що дозволяє бачити в темряві.Потужним випромінювачем теплової енергії є Сонце; воно нагріває Землю навіть з відривом 150 млн. км. Інтенсивність сонячного випромінювання, реєстрована рік у рік станціями, розташованими у багатьох точках земної кулі, становить приблизно 1,37 Вт
/ м 2 . Сонячна енергія - джерело життя на Землі. Ведуться пошуки способів найефективнішого її використання. Створено сонячні батареї, що дозволяють обігрівати будинки та отримувати електроенергію для побутових потреб. РОЛЬ ТЕПЛОТИ ТА ЇЇ ВИКОРИСТАННЯ Глобальні процеси теплообміну не зводяться до нагрівання Землі сонячним промінням. Масивними конвекційними потоками в атмосфері визначаються добові зміни погодних умов на всій земній кулі. Перепади температури в атмосфері між екваторіальними і полярними областями спільно з коріолісовими силами, зумовленими обертанням Землі, призводять до появи конвекційних потоків, що безперервно змінюються, таких, як пасати, струменеві течії, а також теплі і холодні фронти. Див. такожКЛІМАТ; МЕТЕОРОЛОГІЯ І КЛІМАТОЛОГІЯ.Перенесення тепла (за рахунок теплопровідності) від розплавленого ядра Землі до її поверхні призводить до виверження вулканів та появи гейзерів. У деяких регіонах геотермальна енергія використовується для обігріву приміщень та вироблення електроенергії.
Теплота - неодмінний учасник багатьох виробничих процесів. Згадаємо такі найважливіші з них, як виплавка та обробка металів, робота двигунів, виробництво харчових продуктів, хімічний синтез, переробка нафти, виготовлення найрізноманітніших предметів від цегли та посуду до автомобілів та електронних пристроїв.
Багато промислових виробництва та транспорту, а також теплоелектростанції не могли б працювати без теплових машин, пристроїв, що перетворюють теплоту на корисну роботу. Прикладами таких машин можуть бути компресори, турбіни, парові, бензинові і реактивні двигуни.
Однією з найвідоміших теплових машин є парова турбіна, в якій реалізується частина циклу Ранкіна, що використовується на сучасних електростанціях. Спрощена схема цього циклу представлена на рис. 9. Робочу рідину - воду - перетворюють на перегріту пару в паровому котлі, що нагрівається за рахунок спалювання викопного палива (вугілля, нафти або природного газу). Пар високого тискуобертає вал парової турбіни, що приводить у дію генератор, що виробляє електроенергію. Відпрацьована пара конденсується при охолодженні проточною водою, яка поглинає частину теплоти, яка не використана в циклі Ранкіна. Далі вода подається в вежу (градирню), що охолоджує, звідки частина тепла йде в атмосферу. Конденсат за допомогою насоса повертають у паровий котел і весь цикл повторюється.
Всі процеси в циклі Ранкіна ілюструють описані вище за початок термодинаміки. Зокрема, згідно з другим початком, частина енергії, що споживається електростанцією, повинна розсіюватися у навколишньому середовищі у вигляді теплоти. Виявляється, що таким чином втрачається приблизно 68% енергії, що спочатку містилася у викопному паливі. Помітного підвищення ККД електростанції можна було досягти, лише підвищивши температуру парового котла (яка лімітується жароміцністю матеріалів) чи знизивши температуру середовища, куди йде тепло, тобто. атмосфери.
Інший термодинамічний цикл, що має велике значенняв нашої повсякденному житті, ¦ це парокомпресорний холодильний цикл Ранкіна, схема якого представлена на рис. 10. У холодильниках та побутових кондиціонерах енергія для його забезпечення підводиться ззовні. Компресор підвищує температуру та тиск робочої речовини холодильника фреону, аміаку або вуглекислого газу. Перегрітий газ подається в конденсатор, де охолоджується та конденсується, віддаючи тепло навколишньому середовищу. Рідина, що виходить з патрубків конденсатора, проходить через клапан, що дроселює, у випарник, і частина її випаровується, що супроводжується різким зниженням температури. Випарник відбирає у камери холодильника тепло, яке нагріває робочу рідину в патрубках; ця рідина подається компресором у конденсатор, і цикл знову повторюється.
Холодильний цикл представлений на рис. 10 можна використовувати і в тепловому насосі. Такі теплові насоси влітку віддають тепло гарячому атмосферному повітрі та кондиціонують приміщення, а взимку, навпаки, відбирають тепло у холодного повітря та обігрівають приміщення.
Важливим джерелом теплоти для таких цілей, як виробництво електроенергії та транспортні перевезення, є ядерні реакції. У 1905 А. Ейнштейн показав, що маса та енергія пов'язані співвідношенням
E = mc 2 , тобто. можуть переходити один одного. Швидкість світла c дуже велика: 300 тис. км/ с. Це означає, що навіть мала кількість речовини може дати величезну кількість енергії. Так, з 1 кг речовини, що ділиться (наприклад, урану) теоретично можна отримати енергію, яку за 1000 діб безперервної роботи дає електростанція потужністю 1 МВт. Див. такожАТОМА БУДОВА; ПЕЧЕЙ ТА ТОПОК ТЕХНОЛОГІЯ; ЕЛЕКТРОМАГНІТНЕ ВИПРОМІНЮВАННЯ;ТЕПЛООБМІННИК; ТУРБІНА; ОДИНИЦІ ВИМІРЮВАННЯ ФІЗИЧНИХ ВЕЛИЧИН.ЛІТЕРАТУРА Земанський М. Температури дуже високі та дуже низькі. М., 1968Поль Р. Механіка, акустика та вчення про теплоту. М., 1971
Смородинський Я.А. Температура. М., 1981
Фен Дж. Машини, енергія та ентропія. М., 1986
Еткінс П.В. Порядок і безладдя у природі.М., 1987
Рідинні калориметри
Цей тип калориметра, що найбільш широко вживається в техніці, простий за конструкцією та зручний в обслуговуванні. Кількість тепла, одержуване в результаті реакції, викликаної ззовні, спочатку передається реакційній судині (в якій протікала реакція), а потім рідинній ванні. Рідина у ванні безперервно перемішується за допомогою крильчатки, гвинта або насосів, що прискорює вирівнювання температур. Ванна максимально можливою мірою теплоізольована (екранована) від навколишнього середовища. Зміна температури рідинної ванни є мірою кількості тепла, що визначається. Теплоємність мас, що нагріваються, повинна бути не дуже великою, щоб забезпечити достатню зміну температури і щоб процес вимірювання тривав не дуже довго (через це зростають втрати тепла).
Малюнок Влаштування рідинного калориметра.
За високих вимог до постійної навколишніх умов можна весь калориметр помістити в ще одну ванну і стабілізувати температуру в ній про високу точність, використовуючи контур регулювання. Це необхідно в першу чергу в тих випадках, коли потрібно провести досвід при температурах, які значно відрізняються від температури навколишнього середовища.
Для проведення аналізів при низьких температурах (приблизно до -150°С) як охолодне середовище застосовують рідкий азот. При цьому необхідно звертати увагу на те, щоб на проби або судини з пробами при їх зміні не осаджувався іній з навколишнього вологого повітря, оскільки його шар може вплинути на процес вимірювання. Щоб уникнути цього, коли калориметр відкритий, пробу та посудину з пробами обдувають холодним газоподібним азотом.
Калориметри з металевим тілом
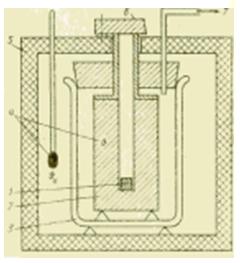
Малюнок Схема пристрою металевого калориметра.
Якщо потрібно провести калориметричні дослідження у ширшому діапазоні температур, то рідинні калориметри вже непридатні. У придатних для цієї мети калориметрах з металевим тілом кількість тепла, що передається, сприймається металевим блоком (зі срібла, міді, алюмінію), який зазвичай має температуру навколишнього середовища. Такий калориметр призначений головним чином для визначення питомої теплоємності, Дж/(кг*К), рідких і твердих речовин.
Пробу спочатку охолоджують поза калориметром холодильної установкиабо нагрівають в печі і після досягнення стану, що встановився, опускають (роняють) в отвір металевого блоку. За способом роботи такий прилад називають калориметром вільного падіння, а характером термодинамічних процесів у ньому його іноді називають калориметром усунення.
Кількість тепла, що передається при такому змішуванні від проби (з параметрами m1, c1,) металевому блоку (m2, c2, ), викликає зміну температури блоку, що піддається виміру. Це дозволяє визначити зазвичай невідоме значення питомої теплоємності проби для ідеальних умов(за відсутності теплообміну навколишнім середовищем) з виразу:
Сам металевий блок розташовується у вакуумованій посудині Дьюара, а іноді в рідинній ванні. В останньому випадку для отримання теплоємності калориметра Ск до теплоємності металевого блоку С2 потрібно додати теплоємність ванни Cw:
CK = C2 + CW = c2m2 + cWmW.
КАЛОРИМЕТРИЧНІ МЕТОДИ ВИМІРЮВАННЯ
Найчастіше калориметри використовують у режимі незмінності умов довкілля. Це відноситься в першу чергу до більшості калориметрів горіння, час реакції в яких дуже мало. У той час як температура внутрішніх частин калориметра змінюється внаслідок протікання реакції, температура навколишнього повітря залишається постійною. впливу на вимірювану величину зовнішніх перешкод - коливань температури у приміщенні, випромінювання, проказника тощо.
Перевагою цієї вимірювальної схеми є порівняно малі витрати на апаратуру, за допомогою якої можна виконати переважну частину калориметричних вимірів. Основним недоліком слід вважати теплообмін калориметра з довкіллям, що ускладнює розшифровку результатів. Цей спосіб вимірювання завжди називають ізоперибольним (діатермічним). У жодному разі його не можна називати ізотермічним, сутність якого полягає в тому, що температура калориметра під час протікання реакції залишається постійною, як, наприклад, калориметрів, призначених для вимірювання фазових перетворень.
Адіабатичний метод
Якщо вдається виключити теплообмін з навколишнім середовищем, тобто забезпечити адіабатичне перебіг процесу, проведення експерименту і розшифровка результатів спрощується, а результат вимірювання виходить більш точним, так як відпадає необхідність у безперервному запису зміни температури і в обчисленні поправок. Крім того, у цьому випадку можна допустити трохи більший підйом температури в калориметричній посудині; у неадіабатичних приладів це неприйнятно через збільшення теплових втрат.
Щоб виключити теплообмін між калориметричною судиною та її безпосереднім оточенням (зазвичай рідинною ванною), температуру ванни необхідно весь час коригувати відповідно до змін температури всередині посудини. За допомогою електронного регулятора (схеми стеження) можна постійно підтримувати різницю цих температур, що дорівнює нулю. Це підвищує вартість вимірювальної апаратури залежно від необхідної точності вимірів.
Елементи апаратури повинні бути швидкодіючими та зберігати стабільність протягом тривалого часу (мати мінімальний дрейф). Зона нечутливості контуру слідкуючого регулювання повинна бути в межах від ±10-3 до ±10-5 К. Як вимірювальні пристрої можна використовувати будь-які малоінерційні електричні контактні термометри, які при включенні в мостову схему дають імпульс регулятору на зміну потужності нагріву. Нагрів здійснюється або за допомогою електричної спіралі опору, або прямим способом у рідинній ванні, яка завдяки слабкій дисоціації діє як нагрівальний опір (так зване електролітичне нагрівання). Цей другий спосіб практично безінерційний. Результат можна отримувати за допомогою вже наявних засобів для електричного вимірювання температури або за додатково встановлюваним рідинним термометром (Бекмана).
Адіабатичний метод вимірювання придатний для вивчення головним чином повільних процесів е тепловими ефектами. При швидких змін кількості тепла (в калориметрах горіння) інерційність вирівнювання температур надає такий несприятливий вплив, що не досягається навіть точність звичайних неадіабатичних методів. Однак, забезпечуючи малу теплоємність нагрівальних елементів та датчиків температури та здійснюючи інтенсивне перемішування рідини ванни, можна отримати малі значення різних постійних часу (зменшити інерційність).
Компенсаційний метод
Використовуючи диференціальні або здвоєні калориметри, що базуються на принципі компенсації, вдається значною мірою виключити зовнішні впливи на процес вимірювання. Два ідентичні калориметричні судини з ідентичними допоміжними пристроями поміщені в навколишнє середовище про однакові умови. В одній посудині протікає досліджуваний процес з тепловим ефектом, а інший посуд за допомогою системи регулювання, що стежить, нагрівається таким чином, що втрати тепла в навколишнє середовище для обох судин однакові. Тому потужність нагріву, що підводиться, можна поставити в пряму залежність від кількості тепла, що вивільняється при досліджуваному процесі. При цьому експериментальне завдання вимірювання переходить в іншу область і зводиться до дуже точного визначення електричної потужності нагрівання, що підводиться (Вт*с, Дж):
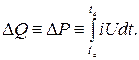
Диференціальний калориметр застосовується, зокрема, за адіабатичних умов навколишнього середовища, насамперед тоді, коли слід очікувати дуже малих або дуже повільних змін кількості тепла. При ендотермічних процесах достатньо мати одну калориметричну судину. Підведення тепла контролюється з таким розрахунком, щоб температура в посудині постійно залишалася однією і тією ж (ізотермічний метод). Недоліком диференціальних калориметрів є великі витрати на апаратуру та кошти техніки вимірювань.
Калориметри горіння
Паливо, що застосовується в теплосиловому господарстві, досліджують з метою визначення його теплоти згоряння Н (Дж/кг). Цей показник необхідний визначення коефіцієнтів корисної дії, дослідження економічності і розрахунків за витрачену енергію у різних установках, і навіть оптимального управління процесом горіння. Значні коливання у складі горючих компонентів нерідко зумовлюють необхідність безперервного визначення теплоти згоряння.
При повному згорянні речовини виділяється кілька тепла Q (тепло згоряння). Якщо поділити його на масу т (або на об'єм за нормальних умов Vn), то вийде (питома) теплота згоряння:
Залежно від стану продуктів згоряння розрізняють два види теплоти згоряння: високу Н0 і нижчу Ні, які називають теплотою горіння і теплотворною здатністю. При визначенні нижчої теплоти згоряння Ні вода, що утворюється при хімічних реакціях, повинна перебувати у пароподібному стані. Різниця обох теплот Н0 - Не відповідає теплоті пароутворення води, що конденсується (індекс КО - конденсату) r, яка дорівнює 2,441 МДж/кг.
Для твердих і рідких палив кількість води, що виходить, можна визначити на основі елементарного аналізу, а при спалюванні газоподібних палив - вимірюванням кількості конденсату.
У промислових топках температура продуктів згоряння перевищує точку кипіння води. Тому зазвичай цікавий лише нижча теплота згоряння Ні, оскільки теплота конденсації води може бути використана.
Калориметри горіння для твердих та рідких речовин
Для процесів горіння, що швидко протікають, розроблена спеціальна форма рідинного калориметра - так звана калориметрична бомба Бертло (рис. 3).
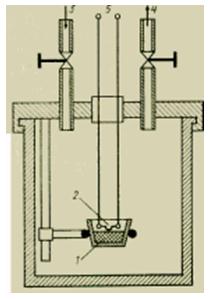
Малюнок Пристрій калориметричної бомби.
Спалювання малої, точно відміреної кількості речовини відбувається при постійному обсязі в герметичній бомбі в атмосфері можливо чистішого кисню під тиском ~30 ат (3 МПа). Заповнена бомба поміщається в рідинну ванну калориметра, яка і сприймає тепло горіння, що виділяється.
Тверді речовинизазвичай пресують брикети (таблетки) малих розмірів і дуже точно зважують. Погано палаючі речовини доцільно перемішувати з рідинами, що добре горять, з відомою теплотою згоряння (наприклад, бензойною кислотою). Рідкі речовини поміщають у чашки (човники) із платини чи кварцу чи малі пластмасові капсули. На кришці, що закріплюється до корпусу бомби болтами, розташовані всі пристрої, необхідні для дослідження: клапани для подачі кисню та відведення продуктів згоряння, тримачі для проб та електричний запальник. Запалювання здійснюють підведенням електрики до тонкого платинового дроту. Тепло, що підводиться для запалювання, повинно бути точно виміряне, щоб його можна було врахувати при розшифровці результатів експерименту. У калориметричній бомбі визначають найвищу теплоту згоряння Н0. При перевірці визначають тепловий еквівалент калориметра Ск спалюванням еталонної речовини (наприклад, бензойної кислоти) або за допомогою електричного нагрівального пристрою.
Калориметр горіння для газоподібних речовин
Для визначення теплоти згоряння газоподібних середовищ є різні способи. Усі вони на відміну калориметричної бомби для твердих і рідких речовин засновані на безперервному вимірі. Застосовуваний принцип виміру дуже простий. Досліджуваний газ безперервно спалюють у пальнику при постійному тиску. Все тепло, що виділяється при згорянні, поглинається або потоком охолоджуючого середовища в теплообміннику (вологий або теплообмінний калориметр), або за допомогою змішування продуктів згоряння з потоком повітря з відомою витратою (сухий або змішуючий калориметр). Зазвичай визначають нижчу теплоту згоряння Нu. Щоб визначити вищу теплоту згоряння Н0, необхідно сконденсувати водяну пару (індекс КО), що міститься в газах, що відходять. Знаючи масові витрати потоків та різницю температур на вході (індекс е) та виході (індекс а) калориметра, можна за рівнянням теплового балансу обчислити відповідну теплоту згоряння.
Необхідна підготовка газу в усіх газових калориметрах, в принципі, однакова. Перед спалюванням газ (індекс G) спочатку очищають від твердих механічних домішок (у фільтрі) і зволожують (до насичення вологою, 100 %), а потім доводять до заданих значень попереднього тиску (за допомогою редукційного клапана) та температури охолоджуючого середовища (індекс К) . Необхідне для горіння повітря (індекс L) теж зволожують і доводять до температури охолоджуючого середовища.
Залежно від необхідної точності та допустимих витрат на вимірювальну апаратуру, деякі з цих умов можуть не виконуватися. Калориметри слід повірити на еталонному газі (наприклад, водні), щоб встановити відхилення від рівняння для ідеального стану калориметра. Для теплообмінного (вологого) калориметра згадане рівняння має вигляд
де і - масові витрати охолоджуючого середовища та палива, кг/с; ск - питома теплоємність охолодного середовища, Дж/(кг*К); - приріст температури охолоджуючого середовища, К.
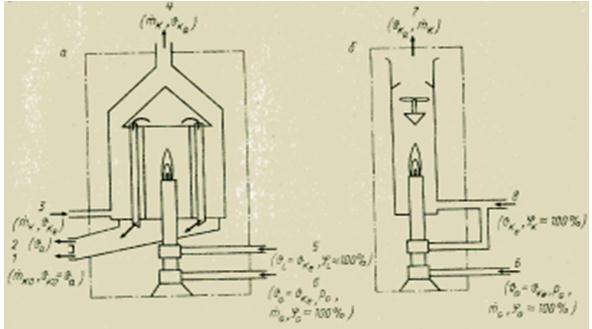
Малюнок Влаштування вологого (а) та сухого (б) калориметрів для газоподібного палива.
Підвищення температури зазвичай становить 5-15 К. Через велику термічну масу теплообмінні калориметри мають дуже велику постійну часу, яка може сягати кількох хвилин. Тому вони менш зручні для використання в замкнутому ланцюзі регулювання як датчик, ніж сухі (змішують) калориметри, постійна часу яких складає всього кілька секунд. Натомість досяжна точність теплообмінних калориметрів порівняно висока. Їхня похибка не перевищує ±0,25-1%, так що їх можна використовувати також для лабораторних робіт і для перевірок. Сухі калориметри (змішують) мають похибку від ±1 до ±2 % верхньої межі діапазону вимірювань.
Конструктивні виконання калориметрів різних виробників відрізняються насамперед допоміжними та запобіжними пристроями, чутливими елементами та обчислювальними схемами, що забезпечують компенсацію похибок. Так, у теплообмінних калориметрах різними способами підтримується сталість відношення витрат газу та охолоджуючого середовища (див. наведене вище рівняння калориметра), завдяки чому найвища теплота згоряння Н0 безпосередньо залежить тільки від підвищення температури.
У сухих калориметрах підвищення температури вимірюють або безпосередньо за допомогою електричних контактних термометрів, або побічно за допомогою дилатометричного датчика - труби, що розширюється, розташованої в потоці відхідних газів. У калориметрі фірми ADOS термічне подовження дилатометричної труби безпосередньо відповідає теплоті згоряння і може бути перетворено на будь-який сигнал за допомогою важеля передачі та вимірювача довжини. У калориметрі фірми Reinecke подовження стрижня використовується як вимірювальний сигнал у ланцюзі регулювання, яка керує витратою охолоджуючого повітря з таким розрахунком, щоб підвищення температури залишалося практично постійним. Контур регулювання у своїй виходить суто пропорційним, проте у ньому неминуче деяке залишкове відхилення. При цьому витрата охолоджуючого повітря або подовження дилатометричної труби (стрижня) є мірою теплоти згоряння, що визначається. Необхідною передумовою для отримання достатньої точності у всіх сухих калориметрах є хороше перемішування повітря і продуктів згорання, що охолоджує.
ВИМІРЮВАННЯ ТЕПЛОВИХ ПОТОКІВ
Тепло як вид енергії передається трьома способами: через тверде тіло (теплопровідністю), рідкими мулом газоподібними середовищами (конвекцією) та без участі матерії (випромінюванням). У техніці майже завжди у передачі тепла беруть участь усі три складові; проте у багатьох випадках можна отримати результати прийнятної точності, вимірюючи лише одну складову.
Вимірювання теплового потокупри теплопровідності
Передача тепла через теплопровідні стіни має важливе значення у багатьох галузях техніки (теплообмінники всіх видів, теплоізоляція тощо). При цьому становлять інтерес не стільки поточний контроль виробничих величин, скільки результати одноразових вимірювань, що використовуються для оцінки навантаження, перевірки виконання показників, що гарантуються, і економічності.
Відповідно до законів стаціонарної теплопровідності, тепловий потік визначається за такими формулами (Дж/с):
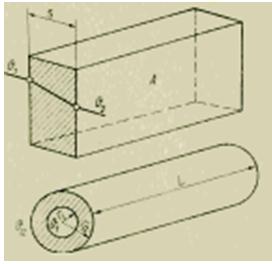
Оскільки коефіцієнт теплопровідності стінки [Дж/(м*с*К)] та її геометричні розміри відомі, вимірювання теплового потоку зводиться до вимірювання різниці температур. Однак ця методика вимагає дуже точного визначення температури поверхонь. Похибки, пов'язані зі зміною умов теплопередачі при встановленні чутливих температурних елементів на поверхнях, можуть бути досить великими. Тому для більш точних вимірів рекомендуються методи, що наводяться нижче, при яких одночасно використовуються і теплопровідність, і тепловіддача.
Вимірювання теплових потоків при теплопередачі (тепловіддачі у поєднанні з теплопровідністю)
Для згаданої у попередньому розділі плоскої стінки справедливий наступний закон теплопередачі (Дж/с):
![]() ,
,
де у коефіцієнті теплопередачі k 1Дж/(м2*с*К)] поряд з коефіцієнтом теплопровідності [Дж/Дм*с*К)] враховані також і коефіцієнти тепловіддачі та [Дж/(м2*c*К)] обох сторін стінки.
На плоску стінку, через яку проходить тепловий потік, що вимірюється, накладають невелику тонку пластинку, температуру поверхні якої визначають вбудованими тонкоплівковими термопарами. Перевага вимірювання у такий спосіб полягає в тому, що при цьому не потрібно знати термічні властивості стінки, а відповідні властивості пластинки можуть бути зведені при градуювання до однієї постійної величини. Такі чутливі елементи мають розмір приблизно 30×30×0,5 мм; діапазон вимірювання охоплює теплові потоки від 10 до 100000 Вт/м2; похибка становить 2-5%.
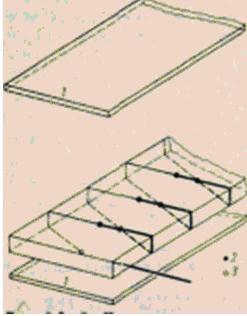
Принцип роботи вимірювача теплового потоку.
При вдосконаленні цього методу вимірювань замість пластинки, що накладається, застосовують гумові мати. Приклеюючи їх до неплоських поверхонь або обгортаючи ними криволінійну поверхню, можна визначити тепловіддачу і від поверхні порівняно великої площі, наприклад від труби, судини і т.п. проти іншого (рис. 6). І в цьому випадку щільність теплового потоку відповідно до градуювання пропорційна різниці температур. Однак мати, що накладаються, кілька порушують початковий теплообмін, що стає помітним при точних вимірюваннях. Тому такий спосіб вимірювання застосовують головним чином визначення термодинамічних констант речовини, коли порушення теплового потоку не впливає на результат вимірювання.
Вимірювання теплових потоків у поточних середовищах.
Значна частина теплової енергії передається рідким або газоподібним середовищами (водою, парою тощо), що рухаються в замкнутій трубопровідній мережі. Однак порівняно з передачею електричної енергії по проводах відстань, на яку може бути передана теплова енергія, обмежена. Для теплотехнічних досліджень всіх видів нагрівальних та холодильних систем потрібно вимірювати виділення та споживання тепла.
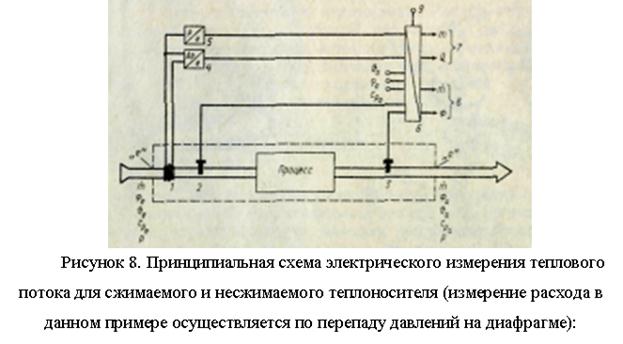
Тепловий потік Ф (Дж/с), переданий потокомсередовища - теплоносія (кг/с) через контрольний переріз площею А (м2) у певній зоні, для якої складений тепловий баланс (у зоні процесу, рис. 7), дорівнює
Кількість тепла, відданого за час t2 - t1 визначиться як інтеграл (Дж):
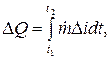
де - Різниця тепломісткості (ентальпій, Дж/кг) теплоносія на вході (індекс е) і на виході (індекс а) зони теплового балансу.
Оскільки в загальному випадку величина ентальпії цікавить тільки в порівнянні з певним рівнем, наприклад з ентальпією при температурі навколишнього середовища, всі вимірювання теплових потоків є по суті різницевими вимірюваннями.
Окремі ентальпії, що входять до загального рівняння, можна виразити через відповідні температури та питомі теплоємності;
Таким чином, вимірювання теплового потоку безпосередньо зводиться до вимірювання температур та масових витрат. У багатьох випадках вимірюють не масову, а об'ємну витрату теплоносія; при цьому отриманий результат буде відрізнятися тільки на величину щільності теплоносія р. Питомі теплоємності сi, є функціями температури . Однак через вузькість діапазону вимірювання багатьох приладів їх зазвичай можна вважати постійними величинами без великої шкоди для точності. Питома теплоємність має бути відома. Для рідин рівняння теплового потоку ще спрощується, тому що їх питомі теплоємності не залежать від тиску:
![]() , Дж/с.
, Дж/с.
У всіх рівняннях такого виду необхідно брати до уваги знаки величин залежно від того, чи підводиться чи відводиться тепло, чи є процес ендотермічним чи екзотермічним, чи відбувається охолодження чи нагрівання.
