Vodorod sulfidining turli haroratlarda issiqlik sig'imi. Tabiiy gazning solishtirma issiqlik sig'imi
O'ziga xos emas, balki umumiy issiqlik quvvati, umumiy qabul qilingan jismoniy ma'noda, moddaning qizib ketish qobiliyatidir. Hech bo'lmaganda termal fizika bo'yicha har qanday darslik bizga shunday deydi - bu klassik ta'rif issiqlik sig'imi(to'g'ri so'z). Aslida, bu qiziqarli jismoniy xususiyatdir. Kundalik hayotda bizga kam ma'lum "tanganing tomoni". Ma'lum bo'lishicha, issiqlik tashqi tomondan berilganda (isitish, isinish) barcha moddalar issiqlikka bir xil ta'sir ko'rsatmaydi ( issiqlik energiyasi) va boshqacha isitiladi. Qobiliyat Yoqilg'i sifatida ishlatiladigan tabiiy gaz issiqlik energiyasini qabul qilish, qabul qilish, saqlash va to'plash (to'plash). TABIY yonuvchi gazning issiqlik sig'imi deyiladi. Va o'zi metanning issiqlik sig'imi, gaz yoqilg'isining termofizik xususiyatlarini tavsiflovchi fizik xususiyatdir. Shu bilan birga, har xil qo'llaniladigan jihatlarda, muayyan amaliy holatga qarab, biz uchun bir narsa muhim bo'lib chiqishi mumkin. Masalan: moddaning qabul qilish qobiliyati issiq yoki to'plash qobiliyati issiqlik energiyasi yoki uni saqlab qolish uchun "talant". Biroq, ba'zi farqlarga qaramay, jismoniy ma'noda bizga kerak bo'lgan xususiyatlar tasvirlanadi metanning issiqlik sig'imi.
Fundamental xarakterga ega bo'lgan kichik, ammo juda "yomon illat" - bu isitish qobiliyati - metanning issiqlik sig'imi, nafaqat bilan bevosita bog'liq kimyoviy tarkibi, moddaning molekulyar tuzilishi, balki uning miqdori (vazn, massa, hajm) bilan ham. Bunday "yoqimsiz" aloqa tufayli, general metanning issiqlik sig'imi moddaning juda noqulay jismoniy xususiyatiga aylanadi. Chunki bitta o'lchangan parametr bir vaqtning o'zida "ikki xil narsani" tasvirlaydi. Ya'ni: haqiqatan ham xarakterlaydi TABIY GAZning termofizik xususiyatlari, ammo "o'tishda" uning miqdorini ham hisobga oladi. "Yuqori" issiqlik fizikasi va materiyaning "banal" miqdori (bizning holatlarimizda: gaz yoqilg'isi) avtomatik ravishda bog'langan bir turdagi integral xarakteristikani shakllantirish.
Xo'sh, nima uchun bizga "adekvat psixika" aniq ko'rinadigan bunday termofizik xususiyatlar kerak? Fizika nuqtai nazaridan, jami metanning issiqlik sig'imi(eng qo'pol tarzda) nafaqat gaz yoqilg'ida to'planishi mumkin bo'lgan issiqlik energiyasini tasvirlashga harakat qiladi, balki uning miqdori haqida "bizni xabardor qiladi". TABIY YONGILGAN GAZ. Bu aniq, tushunarli, barqaror, to'g'ri emas, balki bema'nilik bo'lib chiqadi metanning termofizik xarakteristikasi. Amaliy uchun mos foydali doimiy o'rniga termofizik hisoblar, bizga suzuvchi parametr berilgan, bu olingan issiqlik miqdorining yig'indisi (integral) TABIY GAZ va uning massasi yoki metan hajmi.
Albatta, bunday "ishtiyoq" uchun rahmat, lekin miqdor TABIY YONIG'ILIGI GAZ Men o'zimni o'lchay olaman. Natijalarni ancha qulayroq, "inson" shaklida olish. Miqdori TABIY YONGILGAN GAZ Men umumiydan murakkab formuladan foydalanib, matematik usullar va hisob-kitoblar bilan "chiqarishni" xohlamayman metanning issiqlik sig'imi, har xil haroratlarda, lekin vaznini (massasini) gramm (g, g), kilogramm (kg), tonna (tonna), kublar (kub metr, kub metr, m3), litr (l) yoki millilitr (ml) bilan aniqlang. ). Ayniqsa bu aqlli odamlar uzoq vaqt oldin ushbu maqsadlar uchun juda mos keladigan o'lchash asboblari paydo bo'ldi. Masalan: tarozi yoki boshqa qurilmalar.
Ayniqsa, parametrning "zerikarli suzuvchi tabiati": umumiy tabiiy gazning issiqlik sig'imi. Uning beqaror, o'zgaruvchan "kayfiyati". "Xizmat hajmi yoki dozasini" o'zgartirganda, TABIY GAZning turli haroratlarda issiqlik sig'imi darhol o'zgaradi. Ko'proq yonuvchan gaz aralashmasi, jismoniy miqdor, mutlaq qiymat metanning issiqlik sig'imi- ortadi. Yonuvchan gaz aralashmasining kamroq miqdori, qiymati metanning issiqlik sig'imi kamayadi. "Sharmandalik" ba'zilari chiqadi! Boshqacha qilib aytadigan bo'lsak, bizda "bo'lgan" narsani hech qanday tarzda doimiy tavsiflovchi deb hisoblash mumkin emas TABIY GAZning turli haroratlarda termofizik xususiyatlari. Va biz uchun tushunarli, doimiy koeffitsient, tavsiflovchi mos yozuvlar parametri "bo'lishi" maqsadga muvofiqdir. termal xususiyatlar gaz yoqilg'isi, metan miqdori (og'irligi, massasi, hajmi) bo'yicha "ma'lumotnomalar"siz. Nima qilish kerak?
Bu erda bizni qutqarish uchun juda oddiy, ammo "juda ilmiy" usul keladi. Bu nafaqat sud ijrochisiga tegishli "ud. - o'ziga xos", old jismoniy miqdor, lekin ko'rib chiqilayotgan materiya miqdorini istisno qilishni o'z ichiga olgan oqlangan yechimga. Tabiiyki, "noqulay, ortiqcha" parametrlar: massa yoki hajm TABIY YONGILGAN GAZ istisno qilish mutlaqo mumkin emas. Hech bo'lmaganda, agar metan miqdori bo'lmasa, unda "muhokama mavzusi" bo'lmaydi. Va modda bo'lishi kerak. Shuning uchun biz ba'zi bir shartli massa yoki hajm standartini tanlaymiz, bu bizga kerak bo'lgan "C" koeffitsientining qiymatini aniqlash uchun mos bo'lgan birlik deb hisoblanishi mumkin. Uchun TABIY GAZ yoqilg'isining og'irligi, amaliy foydalanishda qulay bo'lgan metan massasining bunday birligi 1 kilogramm (kg) bo'lib chiqdi.
Endi biz biz bir kilogramm TABIY GAZni 1 darajaga qizdiramiz va issiqlik miqdori (issiqlik energiyasi) isitishimiz kerak gaz aralashmasi bir daraja - bu bizning to'g'ri jismoniy parametrimiz, koeffitsient "C", yaxshi, juda to'liq va aniq birini tasvirlab TABIY GAZning turli haroratlarda termofizik xususiyatlari. E'tibor bering, endi biz xarakteristikani tavsiflash bilan shug'ullanamiz jismoniy mulk modda, lekin uning miqdori haqida "bizni qo'shimcha ravishda ma'lumot berishga" harakat qilmaydi. Qulaymi? Til ojiz. Bu butunlay boshqa masala. Aytgancha, endi biz general haqida gapirmayapmiz metanning issiqlik quvvati. Hammasi o'zgardi. BU TABIY GAZNING XUSUSIY ISITIGI, bu ba'zan boshqa nom bilan ataladi. Qanaqasiga? Shunchaki MASSIVE TABIY YONGILGAN GAZNING ISSIQLIK QUVVATLARI. Maxsus (ud.) Va massa (m.) - bu holda: sinonimlar, ular bu erda bizga kerak bo'lgan narsani anglatadi. koeffitsient "C".
Jadval 1. Koeffitsient: TABIY GAZning solishtirma issiqlik sig'imi (sp.). TABIY yonuvchi GAZning massa issiqlik sig'imi. Malumot ma'lumotlari.
Oddiy qilib aytganda, issiqlik quvvati FROM tanaga sarflanishi kerak bo'lgan issiqlik miqdori deyiladi bu jarayon tanani bir daraja qizdirish uchun: .
Odatda, issiqlik sig'imi moddaning miqdori birligiga aytiladi va tanlangan birlikka qarab ular quyidagilardan ajralib turadi:
o'ziga xos massa issiqlik sig'imi Bilan, 1 kg gazga taalluqli, J/(kgK);
o'ziga xos hajmli issiqlik sig'imi Bilan´, normal jismoniy sharoitda 1 m 3 hajmdagi gaz miqdori, J / (m 3 K);
solishtirma molyar issiqlik sig'imi m Bilan, bir kilomolga ishora qilinadi, J / (kmolK).
Maxsus issiqlik sig'imlari o'rtasidagi bog'liqlik aniq munosabatlar bilan belgilanadi:
Bilan= μ Bilan/μ; Bilan´= Bilan r n. (2.13)
Bu yerda r n - normal sharoitdagi gaz zichligi.
Tana haroratining bir xil miqdordagi issiqlik bilan o'zgarishi sodir bo'layotgan jarayonning tabiatiga bog'liq issiqlik sig'imi jarayonning funktsiyasidir. Bu shuni anglatadiki, bir xil ishchi suyuqlik, jarayonga qarab, uni 1 K ga qizdirish uchun har xil miqdordagi issiqlikni talab qiladi. Raqamli kattalik Bilan+ ∞ dan – ∞ gacha oʻzgaradi.
Termodinamik hisoblarda katta ahamiyatga ega ega:
doimiy bosimdagi issiqlik sig'imi
Bilan p = d q p/ dT, (2.14)
q p , jarayonda tanaga doimiy bosim ostida, tana haroratining o'zgarishiga keltiriladi dT;
doimiy hajmdagi issiqlik sig'imi
Bilan v = δ q v /dT, (2.15)
issiqlik miqdori d nisbatiga teng q v, jarayonda tanaga doimiy hajmda, tana haroratining o'zgarishiga keltiriladi dT.
Yopiq tizimlar uchun termodinamikaning birinchi qonuniga muvofiq d q = du + pdf.
Shuni hisobga olgan holda 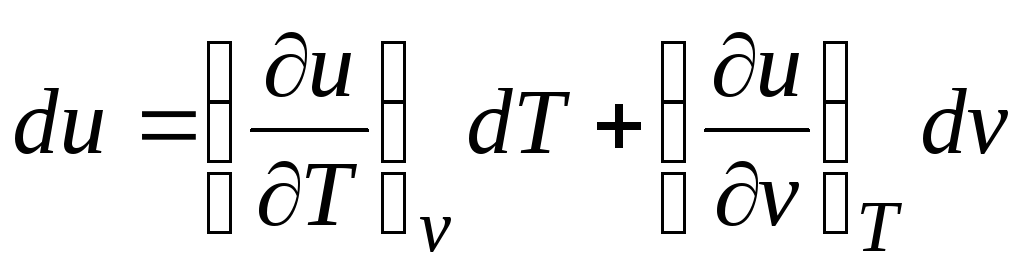 (munosabatlar (2.1))
(munosabatlar (2.1))
Δ q = (∂u/∂T) v dT + [(∂u/∂v) T + p]dv. (2.16)
Izokorik jarayon uchun ( v=const) bu tenglama shaklni oladi 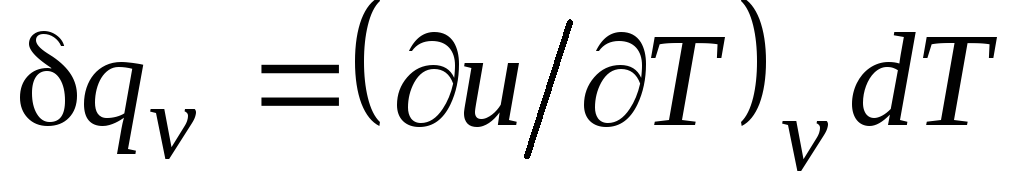 , va (2.15) ni hisobga olgan holda, biz buni olamiz
, va (2.15) ni hisobga olgan holda, biz buni olamiz
c v = (∂u/∂T) v . (2.17)
Ideal gaz uchun
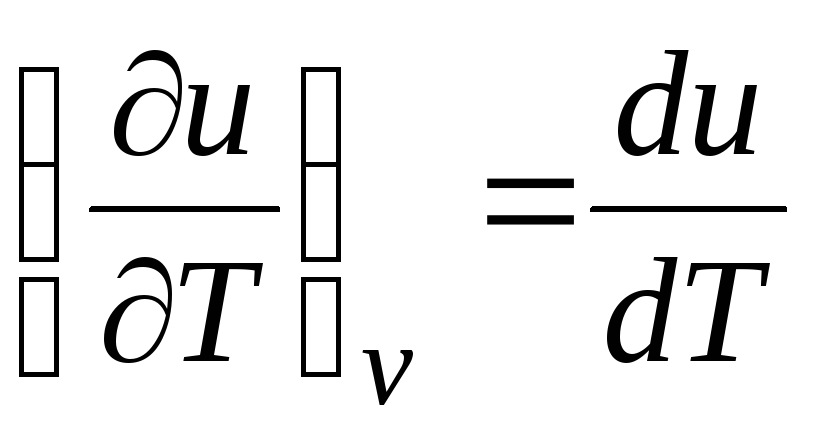 (2.2 tenglama), shuning uchun
(2.2 tenglama), shuning uchun
c v = du/dT. (2.18)
Izobar jarayon uchun ( R=const) (2.16) va (2.14) tenglamalardan olamiz
c p = (∂ u/∂T) v + [(∂u/∂v) T + p](dv/dT) p
Chunki ichki energiya ideal gaz faqat uning harorati bilan belgilanadi va o'ziga xos hajmga bog'liq emas, keyin
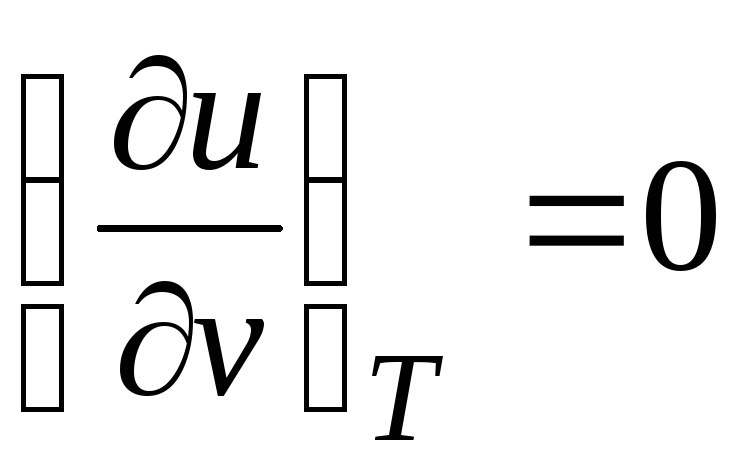 .
(2.19)
.
(2.19)
Klapeyron tenglamasidan (1.4) pv
= RT(1.3) quyidagicha 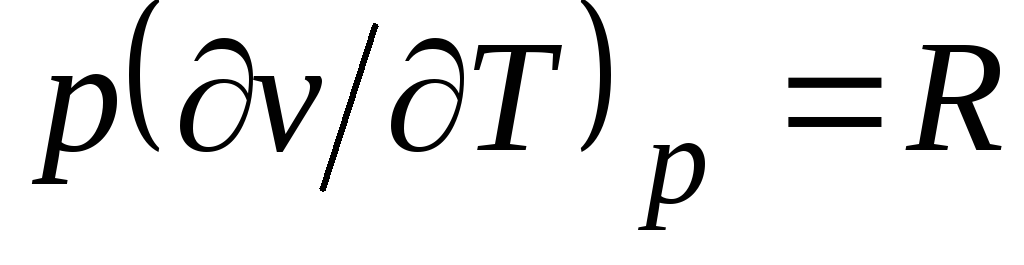 , qayerda
, qayerda
c p= Bilan v + R. (2.20)
Munosabat (2.20) Mayer tenglamasi deb ataladi va ideal gazlarning texnik termodinamikasida asosiylaridan biridir.
Jarayonda v\u003d const, gazga berilgan issiqlik faqat uning ichki energiyasini o'zgartirish uchun ketadi, p \u003d const jarayonida esa issiqlik ichki energiyani oshirish va kengaytirish ishini bajarish uchun sarflanadi. shuning uchun c p ko'proq Bilan v ushbu ishning miqdori bo'yicha.
Formula ![]() haqiqiy issiqlik sig'imi deb ataladigan narsani, ya'ni ma'lum bir haroratda issiqlik sig'imi qiymatini aniqlaydi. Amalda issiqlik miqdorini hisoblash uchun issiqlik sig'imi keng qo'llaniladi q 12, bu tanani bir haroratdan isitish uchun sarflanishi kerak ( t 1) boshqasiga ( t 2) (yoki sovutilganda chiqariladi t 2 gacha t 1).
haqiqiy issiqlik sig'imi deb ataladigan narsani, ya'ni ma'lum bir haroratda issiqlik sig'imi qiymatini aniqlaydi. Amalda issiqlik miqdorini hisoblash uchun issiqlik sig'imi keng qo'llaniladi q 12, bu tanani bir haroratdan isitish uchun sarflanishi kerak ( t 1) boshqasiga ( t 2) (yoki sovutilganda chiqariladi t 2 gacha t 1).
Agar issiqlik quvvati ko'rsatilgan harorat oralig'ida o'zgarmasa, u holda
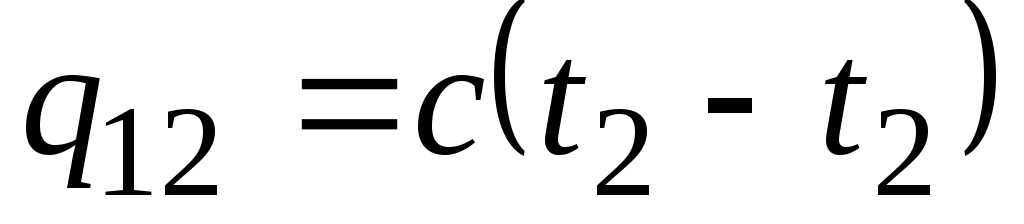 , kJ/kg va
, kJ/kg va 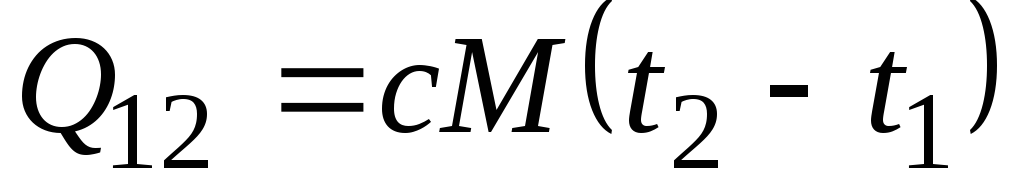 , kJ. (2.21)
, kJ. (2.21)
Ushbu formuladan taxminiy (juda ham aniq bo'lmagan) hisoblar uchun ham foydalanish mumkin. Masalan, xona haroratida suvning solishtirma issiqlik sig'imi 4,187 kJ/(kgC), havoniki esa 1 kJ/(kgC) ga teng. Deyarli barcha moddalarning issiqlik sig'imi harorat oshishi bilan o'zgarganligi sababli (ko'pincha ortadi), aniqrog'i, formuladan foydalanish kerak.
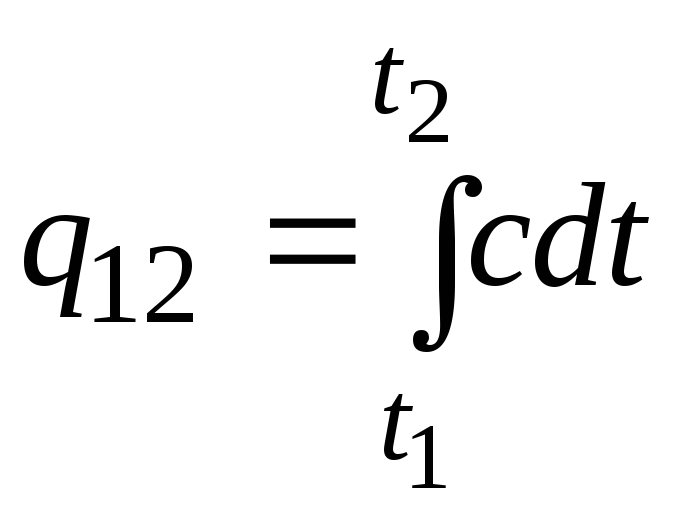 .
(2.21a)
.
(2.21a)
Shaklda. 2,2 magnitudali q 12 soyali maydon sifatida ko'rsatilgan. O'rtacha qiymat teoremasini qo'llash orqali yozishning eng oson yo'li ko'rinadi
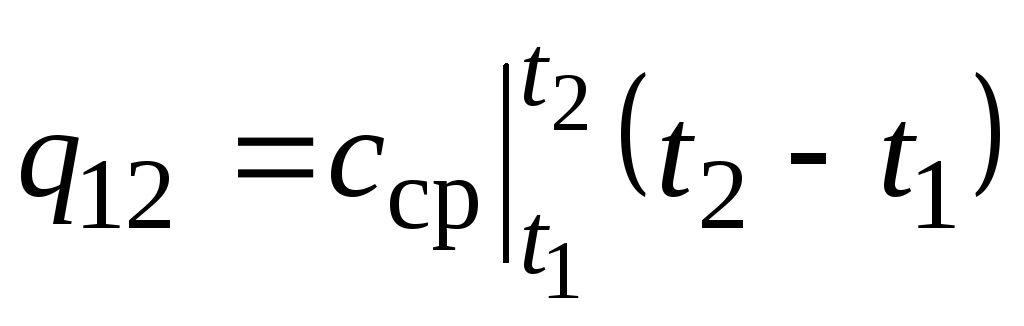 ,
(2.22)
,
(2.22)
qayerda 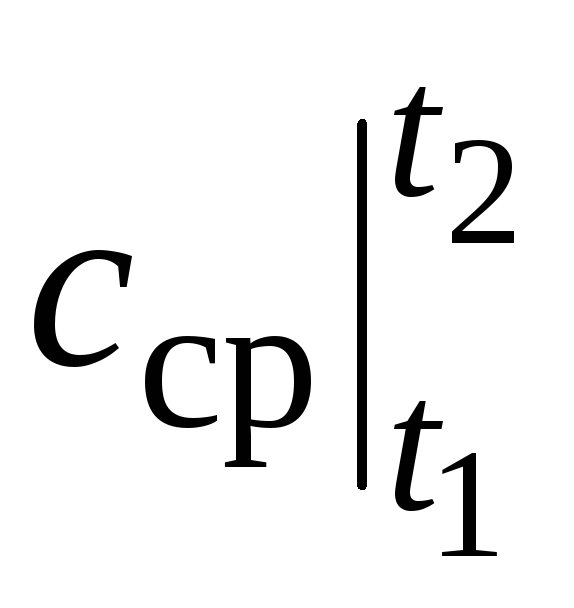 harorat oralig'idagi o'rtacha issiqlik sig'imi t 1 …t 2 .
harorat oralig'idagi o'rtacha issiqlik sig'imi t 1 …t 2 .
Guruch. 2.2. Haqiqiy issiqlik sig'imining haroratga bog'liqligi
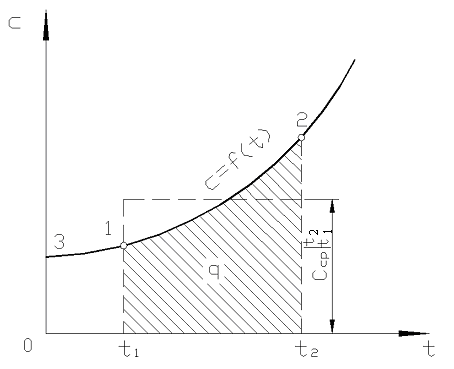
Biroq, haqiqiy hisob-kitoblar uchun bunday belgi juda noqulay, chunki issiqlik quvvati jadvallardan tanlanadi va 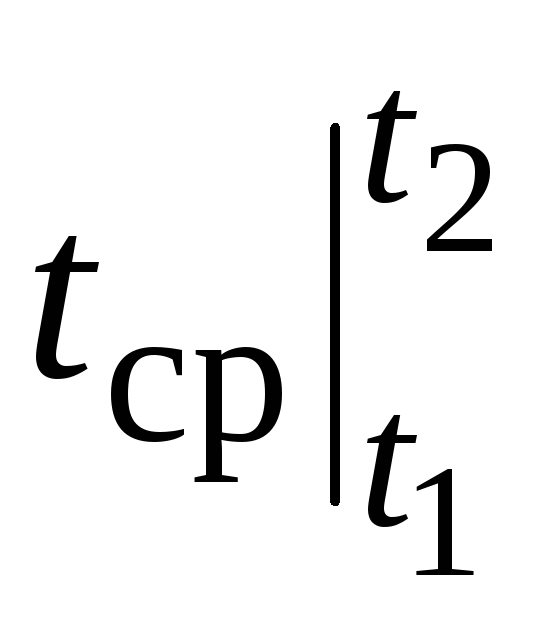 qandayligiga bog'liq t 1 va dan t 2. Ikki argumentdan iborat funktsiya jadvali juda og'ir bo'ladi.
qandayligiga bog'liq t 1 va dan t 2. Ikki argumentdan iborat funktsiya jadvali juda og'ir bo'ladi.
Amalda, quyidagicha davom eting. Istalgan issiqlik miqdori tanani 0 S dan haroratgacha qizdirish uchun zarur bo'lgan issiqlik miqdori o'rtasidagi farq sifatida taqdim etiladi. t 2 va t 1 mos ravishda (2.2-rasm)
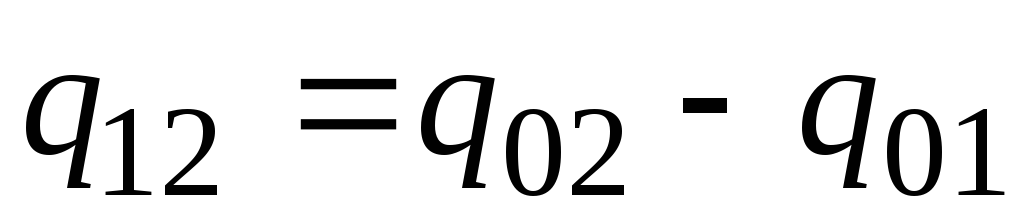 . (2.23)
. (2.23)
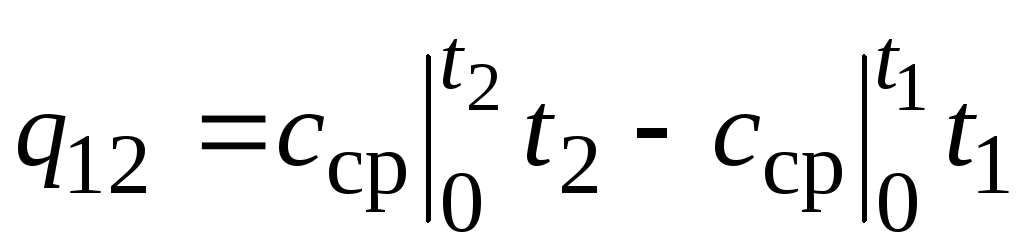 ,
(2.24)
,
(2.24)
qayerda 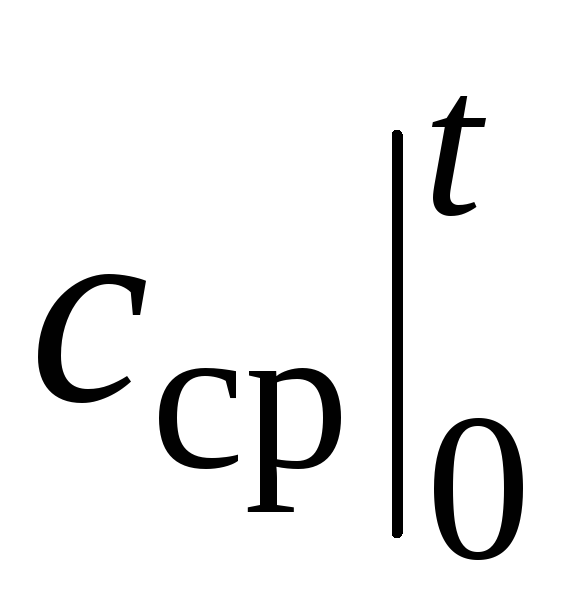 - harorat oralig'ida o'rtacha issiqlik sig'imi 0 ... tC.
- harorat oralig'ida o'rtacha issiqlik sig'imi 0 ... tC.
O'rtacha issiqlik quvvatining qiymati 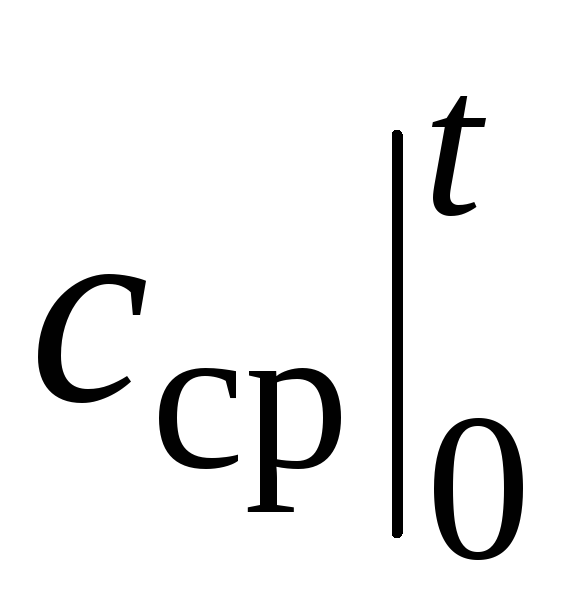 ma'lum bir modda uchun (va ma'lum bir jarayon, ya'ni. Bilan R yoki c v) faqat bitta haroratga bog'liq t. Aynan shu issiqlik sig'imlari barcha jadvallarda "o'rtacha" nomi ostida berilgan. Aytilgan narsa haqiqatdir Bilan
(Bilan R va c v), shuningdek uchun Bilan va Bilan. Misol tariqasida, quyidagi jadvalda ba'zi eng keng tarqalgan gazlar uchun issiqlik sig'imi haroratga nisbatan ko'rsatilgan. Shuni ta'kidlash kerakki, (2.24) formulada harorat Selsiy gradusiga almashtiriladi.
ma'lum bir modda uchun (va ma'lum bir jarayon, ya'ni. Bilan R yoki c v) faqat bitta haroratga bog'liq t. Aynan shu issiqlik sig'imlari barcha jadvallarda "o'rtacha" nomi ostida berilgan. Aytilgan narsa haqiqatdir Bilan
(Bilan R va c v), shuningdek uchun Bilan va Bilan. Misol tariqasida, quyidagi jadvalda ba'zi eng keng tarqalgan gazlar uchun issiqlik sig'imi haroratga nisbatan ko'rsatilgan. Shuni ta'kidlash kerakki, (2.24) formulada harorat Selsiy gradusiga almashtiriladi.
At turli gazlarning o'rtacha molyar issiqlik sig'imi R=const
(M.P. Vukalovich, V.A. Kirillin, V.N. Timofeevga ko'ra)
|
t, C |
Bilan R, kJ/(kmolK) |
|||||||
|
N 2 atmosfera | ||||||||
Ushbu jadvalda qiymatlar Bilan p 100 S orqali beriladi. Ular harorat bilan unchalik o'zgarmasligi sababli, oraliq qiymatlarni chiziqli ekstrapolyatsiya orqali topish mumkin. Bu qanday amalga oshirilganini eslang. Jadvalli funksiya qiymatlari mavjud y
= f(x) da 1 (qachon X= X 1) va da 2 (qachon X= X 2). Funktsiya qiymati da(X) da X 1 <X<X 2 teng 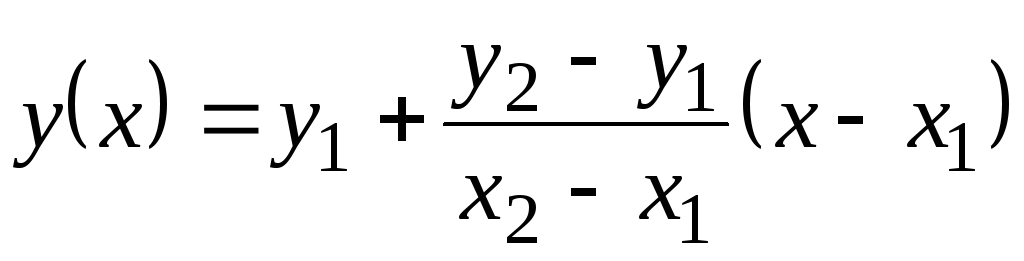 . Bu formula monoton ortib borayotgan funktsiya uchun ham to'g'ri keladi (qachon da 2 >da 1) va monoton kamayish uchun ( da 2 <da 1); Bunday holda, kasr salbiy bo'ladi, chunki X 2 > X 1 har doim.
. Bu formula monoton ortib borayotgan funktsiya uchun ham to'g'ri keladi (qachon da 2 >da 1) va monoton kamayish uchun ( da 2 <da 1); Bunday holda, kasr salbiy bo'ladi, chunki X 2 > X 1 har doim.
Jadvalda harorat va bosimga qarab gazlarning issiqlik o'tkazuvchanligi qiymatlari ko'rsatilgan.
Issiqlik o'tkazuvchanligi qiymatlari 20 K (-253 ° C) dan 1500 K (1227 ° C) gacha bo'lgan haroratlar va 1 dan 1000 atmosferagacha bo'lgan bosim uchun ko'rsatilgan.
Jadval quyidagi gazlarning issiqlik o'tkazuvchanligini hisobga olgan holda:,, freon-14 CF 4, etilen C 2 H 4. Issiqlik o'tkazuvchanligining birligi Vt / (m deg).
Shuni ta'kidlash kerak gazlarning issiqlik o'tkazuvchanligi harorat va bosimning oshishi bilan ortadi. Masalan, ammiak gazining issiqlik o'tkazuvchanligi xona haroratida va normal atmosfera bosimida 0,024 Vt / (m deg) ni tashkil qiladi va 300 daraja qizdirilganda issiqlik o'tkazuvchanligi 0,067 Vt / (m deg) qiymatiga oshadi. Agar bu gazning bosimi 300 atmosferaga oshirilsa, u holda issiqlik o'tkazuvchanlik qiymati yanada yuqori bo'ladi va 0,108 Vt / (m deg) qiymatga ega bo'ladi.
Eslatma: Ehtiyot bo'ling! Jadvaldagi issiqlik o'tkazuvchanligi 10 3 faktor bilan ko'rsatilgan. 1000 ga bo'lishni unutmang!
Noorganik gazlarning haroratga bog'liq issiqlik o'tkazuvchanligi
Jadvalda normal atmosfera bosimidagi haroratga qarab noorganik gazlarning issiqlik o'tkazuvchanligi qiymatlari berilgan. Gazlarning issiqlik o'tkazuvchanligi qiymatlari 80 dan 1500 K gacha (-193 ... 1227 ° S) haroratlarda ko'rsatilgan.
Jadvalda quyidagi gazlarning issiqlik o'tkazuvchanligi ko'rsatilgan: azot oksidi N 2 O, oltingugurt geksaflorid SF 6, azot oksidi NO, vodorod sulfidi H 2 S, ammiak NH 3, oltingugurt dioksidi SO 2, bug 'H 2 O, karbonat angidrid CO 2 , og'ir suv bug'i D 2 O, havo.
Shuni ta'kidlash kerak noorganik gazlarning issiqlik o'tkazuvchanligi gaz harorati oshishi bilan ortadi.
Eslatma: Jadvaldagi gazlarning issiqlik o'tkazuvchanligi 10 3 faktor bilan ko'rsatilgan. 1000 ga bo'lishni unutmang!
Organik gazlarning issiqlik o'tkazuvchanligi haroratga bog'liq
Jadvalda normal atmosfera bosimidagi haroratga qarab organik gazlar va ba'zi suyuqliklarning bug'larining issiqlik o'tkazuvchanlik qiymatlari ko'rsatilgan. Gazlarning issiqlik o'tkazuvchanligi qiymatlari jadvalda 120 dan 800 K gacha bo'lgan harorat oralig'ida keltirilgan.
Quyidagi organik gazlar va suyuqliklarning issiqlik o'tkazuvchanligi berilgan: aseton CH 3 COCH 3, oktan C 8 H 18, pentan C 5 H 12, butan C 4 H 10, geksan C 6 H 14, propilen C 3 H 6, geptan C 7 H 16, amil spirti C 5 H 11 OH, ksilen C 8 H 10, izopropil spirti C 2 H 7 OH, metan CH 4, metil spirti CH 3 OH, uglerod tetraklorid CCl 4, siklogeksan C 6 H 12, etan C 2 H 6, uglerod tetraflorid CF 4, freon-11 3, etilxlorid C 2 H 5 Cl, freon-12 CF 2 Cl 2, etilen C 2 H 4, freon-13 CF 3 Cl, etil format HCOOC 2 H 5, freon-21 CHFCl 2, dietil efir (C 2 H 5 ) 2O.
Jadvaldan ko'rinib turibdiki, organik gazlarning issiqlik o'tkazuvchanligi qiymati ham gaz harorati oshishi bilan ortadi.
Diqqatli bo'ling! Jadvaldagi issiqlik o'tkazuvchanligi 10 3 faktor bilan ko'rsatilgan. 1000 ga bo'lishni unutmang! Masalan, 400 K (127 ° S) haroratda aseton bug'ining issiqlik o'tkazuvchanligi 0,0204 Vt / (m deg) ni tashkil qiladi.
