Tiek mērīts siltuma daudzums sistēmā. Siltuma daudzuma mērīšanas metodes un līdzekļi
Siltums- enerģija, kas tiek pārnesta no vairāk uzkarsēta ķermeņa uz mazāk sakarsētu, izmantojot tiešu kontaktu vai starojumu.
Temperatūra ir molekulu kustības intensitātes mērs.
Siltuma daudzums, kas piemīt ķermenim noteiktā temperatūrā, ir atkarīgs no tā masas; piemēram, tajā pašā temperatūrā liela ūdens krūze satur vairāk siltuma nekā maza, un spainis auksta ūdens var saturēt vairāk siltuma nekā tase ūdens. karsts ūdens(lai gan ūdens temperatūra spainī ir zemāka).
Siltumam ir svarīga loma cilvēka dzīvē, tostarp viņa ķermeņa darbībā. Daļa pārtikā esošās ķīmiskās enerģijas tiek pārvērsta siltumā, tādējādi uzturot ķermeņa temperatūru ap 37°C. Cilvēka ķermeņa siltuma bilance ir atkarīga arī no temperatūras vidi, un cilvēki ir spiesti tērēt daudz enerģijas dzīvojamo un ražošanas telpu apsildīšanai ziemā un dzesēšanai vasarā. Lielāko daļu šīs enerģijas piegādā siltumdzinēji, piemēram, katli un tvaika turbīnas spēkstacijās, kas sadedzina fosilo kurināmo (ogles, naftu) un ražo elektroenerģiju.
Līdz 18. gadsimta beigām. siltumu uzskatīja par materiālu vielu, uzskatot, ka ķermeņa temperatūru nosaka tā saturs<калорической жидкости>, vai<теплорода>. Vēlāk B. Ramfords, Dž. Džouls un citi tā laika fiziķi ar ģeniālu eksperimentu un spriešanas palīdzību atspēkoja<калорическую>teoriju, kas pierāda, ka siltums ir bezsvara un to var iegūt jebkurā daudzumā, vienkārši ar mehānisku kustību. Siltums pats par sevi nav viela – tā ir tikai tā atomu vai molekulu kustības enerģija. Tieši šādai siltuma izpratnei pieturas mūsdienu fizika.
Šajā rakstā mēs aplūkosim, kā siltums un temperatūra ir saistīti un kā šie lielumi tiek mērīti. Mūsu diskusijas tēma būs arī šādi jautājumi: siltuma pārnešana no vienas ķermeņa daļas uz otru; siltuma pārnese vakuumā (telpā, kurā nav vielas); siltuma loma mūsdienu pasaulē.
Siltums un temperatūra
Siltumenerģijas daudzumu vielā nevar noteikt, novērojot katras tās molekulas kustību atsevišķi. Gluži pretēji, tikai pētot vielas makroskopiskās īpašības, var atrast daudzu molekulu mikroskopiskās kustības raksturlielumus, kas aprēķināti vidēji noteiktā laika periodā. Vielas temperatūra ir vidējais molekulārās kustības intensitātes rādītājs, kuras enerģija ir siltumenerģija vielas.
Viens no visizplatītākajiem, bet arī neprecīzākajiem veidiem, kā novērtēt temperatūru, ir pieskāriens. Pieskaroties objektam, mēs vērtējam, vai tas ir karsts vai auksts, koncentrējoties uz savām sajūtām. Protams, šīs sajūtas ir atkarīgas no mūsu ķermeņa temperatūras, kas mūs noved pie termiskā līdzsvara jēdziena - viena no vissvarīgākajām temperatūras mērīšanas laikā.
Termiskais līdzsvars
Termiskais līdzsvars starp ķermeņiem A un B
Acīmredzot, ja divi ķermeņi A un B ir cieši piespiesti viens otram, tad, pieskaroties tiem pēc pietiekami ilga laika, mēs pamanīsim, ka to temperatūra ir vienāda. Šajā gadījumā tiek uzskatīts, ka ķermeņi A un B atrodas termiskā līdzsvarā viens ar otru. Tomēr, vispārīgi runājot, ķermeņiem nav obligāti jāsaskaras, lai starp tiem pastāvētu termiskais līdzsvars - pietiek ar to, ka to temperatūra ir vienāda. To var pārbaudīt, izmantojot trešo ķermeni C, vispirms nogādājot to termiskā līdzsvarā ar ķermeni A un pēc tam salīdzinot ķermeņa C un B temperatūru. Ķermenis C šeit spēlē termometra lomu. Stingrā formulējumā šo principu sauc par termodinamikas nulles likumu: ja ķermeņi A un B atrodas termiskā līdzsvarā ar trešo ķermeni C, tad arī šie ķermeņi atrodas termiskā līdzsvarā viens ar otru. Šis likums ir visu temperatūras mērīšanas metožu pamatā.
Temperatūras mērīšana

Temperatūras skalas

Termometri
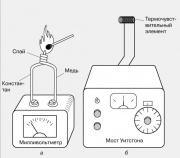
Termometri, kuru pamatā ir elektriskie efekti
Ja mēs vēlamies veikt precīzus eksperimentus un aprēķinus, tad nepietiek ar tādiem temperatūras rādītājiem kā karsts, silts, vēss, auksts - mums ir vajadzīga graduēta temperatūras skala. Ir vairākas šādas skalas, un par atskaites punktiem parasti tiek ņemtas ūdens sasalšanas un viršanas temperatūras. Četri visizplatītākie svari ir parādīti attēlā. Celsija skalu, pēc kuras ūdens sasalšanas temperatūra atbilst 0° un viršanas temperatūrai 100°, sauc par Celsija skalu, kas nosaukta zviedru astronoma A. Celsija vārdā, kurš to aprakstīja 1742. gadā. Tiek uzskatīts, ka zviedru dabaszinātnieks C. Linnejs pirmo reizi izmantoja šo skalu. Tagad Celsija skala ir visizplatītākā pasaulē. Fārenheita temperatūras skalu, kurā ūdens sasalšanas un viršanas temperatūra atbilst ārkārtīgi neērtiem skaitļiem 32 un 212 °, 1724. gadā ierosināja Fārenheits. Fārenheita skala ir plaši izplatīta angliski runājošajās valstīs, taču zinātniskajā literatūrā to gandrīz neizmanto. Lai pārvērstu Celsija temperatūru (°C) uz Fārenheita temperatūru (°F), ir formula °F = (9/5)°C + 32, un apgrieztajai pārvēršanai ir formula °C = (5/9)( °F-32).
Abas skalas – gan Fārenheita, gan Celsija – ir ļoti neērti, veicot eksperimentus apstākļos, kad temperatūra nokrītas zem ūdens sasalšanas punkta un tiek izteikta kā negatīvs skaitlis. Šādos gadījumos tika ieviestas absolūtās temperatūras skalas, kuru pamatā ir ekstrapolācija uz tā saukto absolūto nulli - punktu, kurā molekulārajai kustībai vajadzētu apstāties. Vienu no tām sauc par Rankine skalu, bet otru par absolūto termodinamisko skalu; Temperatūra tiek mērīta Rankine grādos (°R) un kelvinos (K). Abas skalas sākas pie absolūtās nulles temperatūras, un ūdens sasalšanas punkts atbilst 491,7°R un 273,16 K. Gādu un kelvinu skaits starp ūdens sasalšanas un viršanas punktiem pēc Celsija skalas un absolūtās termodinamiskās skalas ir vienāds un vienāds ar 100; Fārenheita un Rankina skalām arī tas ir vienāds, bet vienāds ar 180. Celsija grādus pārvērš kelvinos, izmantojot formulu K = °C + 273,16, un Fārenheita grādus pārvērš Rankīna grādos, izmantojot formulu °R = °F + 459.7.
Temperatūras mērīšanai paredzēto instrumentu darbība balstās uz dažādām fizikālām parādībām, kas saistītas ar vielas siltumenerģijas izmaiņām - elektriskās pretestības, tilpuma, spiediena, emisijas raksturlielumu un termoelektrisko īpašību izmaiņām. Viens no vienkāršākajiem un pazīstamākajiem temperatūras mērīšanas instrumentiem ir stikla termometrs, kas parādīts attēlā. Bumbiņu termometra apakšā ievieto vidē vai piespiež pret objektu, kura temperatūra ir jāmēra, un atkarībā no tā, vai bumbiņa saņem vai izdala siltumu, tā izplešas vai saraujas, un tās kolonna kapilārā paceļas vai nokrīt. . Ja termometrs ir iepriekš kalibrēts un aprīkots ar skalu, tad jūs varat tieši uzzināt ķermeņa temperatūru.
Vēl viena ierīce, kuras darbības pamatā ir termiskā izplešanās, ir bimetāla termometrs, kas parādīts attēlā. Tās galvenais elements ir spirālveida plāksne, kas izgatavota no diviem metinātiem metāliem ar dažādiem termiskās izplešanās koeficientiem. Sildot, viens no metāliem izplešas vairāk nekā otrs, spirāle pagriežas un pagriež bultiņu attiecībā pret skalu. Šādas ierīces bieži izmanto iekštelpu un āra gaisa temperatūras mērīšanai, taču tās nav piemērotas vietējās temperatūras noteikšanai.
Vietējo temperatūru parasti mēra, izmantojot termopāri, kas ir divi atšķirīgu metālu vadi, kas pielodēti vienā galā. Sildot šādu savienojumu, vadu brīvajos galos rodas emf, kas parasti ir vairāki milivolti. Termopāri ir izgatavoti no dažādiem metālu pāriem: dzelzs un konstantāna, vara un konstantāna, hromela un alumela. Viņu termo-emf mainās gandrīz lineāri ar temperatūru plašā temperatūras diapazonā.
Ir zināms arī cits termoelektrisks efekts - vadoša materiāla pretestības atkarība no temperatūras. Tas ir elektriskās pretestības termometru darbības pamatā, no kuriem viens ir parādīts attēlā. Maza temperatūras jutīga elementa (termiskā devēja) - parasti smalkas stieples spoles - pretestību salīdzina ar kalibrēta mainīga rezistora pretestību, izmantojot Vitstona tiltu. Izvades ierīci var kalibrēt tieši grādos.
Optiskos pirometrus izmanto, lai mērītu karstu ķermeņu temperatūru, kas izstaro redzamo gaismu. Vienā šīs ierīces iemiesojumā korpusa izstarotā gaisma tiek salīdzināta ar kvēlspuldzes kvēldiega emisiju, kas novietota binokļa fokusa plaknē, caur kuru tiek skatīts izstarojošais ķermenis. Elektriskā strāva, kas silda lampas kvēldiegu, tiek mainīta, līdz vizuāli salīdzinot kvēldiega un korpusa mirdzumu, atklājas, ka starp tiem ir izveidots termiskais līdzsvars. Instrumenta skalu var kalibrēt tieši temperatūras vienībās.
Tehniskie sasniegumi pēdējos gadosļāva izveidot jaunus temperatūras sensorus. Piemēram, gadījumos, kad nepieciešama īpaši augsta jutība, termopāra vai parastā pretestības termometra vietā izmanto pusvadītāju ierīci - termistoru. Krāsvielas un šķidrie kristāli, kas maina savu fāzes stāvokli, tiek izmantoti arī kā termiskie pārveidotāji, īpaši gadījumos, kad ķermeņa virsmas temperatūra svārstās plašā diapazonā. Visbeidzot tiek izmantota infrasarkanā termogrāfija, kas rada objekta infrasarkano attēlu nepatiesās krāsās, kur katra krāsa atbilst noteiktai temperatūrai. Šī temperatūras mērīšanas metode atrod visplašāko pielietojumu - no medicīniskā diagnostika pirms telpu siltumizolācijas pārbaudes.
Siltuma mērīšana
Ūdens kalorimetrs
Ķermeņa siltumenerģiju (siltuma daudzumu) var izmērīt tieši, izmantojot tā saukto kalorimetru; vienkārša šādas ierīces versija ir parādīta attēlā. Tas ir rūpīgi izolēts slēgts trauks, kas aprīkots ar ierīcēm temperatūras mērīšanai tajā un dažreiz piepildīts ar darba šķidrumu ar zināmām īpašībām, piemēram, ūdeni. Lai izmērītu siltuma daudzumu nelielā apsildāmā korpusā, to ievieto kalorimetrā un gaida, līdz sistēma sasniedz termisko līdzsvaru. Siltuma daudzumu, kas tiek nodots kalorimetram (precīzāk, ūdenim, kas to piepilda), nosaka ūdens temperatūras paaugstināšanās.
Siltuma daudzumu, kas izdalās ķīmiskās reakcijas, piemēram, sadegšanas laikā, var izmērīt, novietojot nelielu<бомбу>. IN<бомбе>ir paraugs, kuram pieslēgti aizdedzes elektrības vadi, un atbilstošs skābekļa daudzums. Pēc tam, kad paraugs pilnībā izdeg un ir izveidojies termiskais līdzsvars, nosaka, cik daudz ir palielinājusies ūdens temperatūra kalorimetrā un līdz ar to arī izdalītā siltuma daudzums.
Siltuma vienības
Siltums ir enerģijas veids, un tāpēc tas jāmēra enerģijas vienībās. Enerģijas SI mērvienība ir džouls (J). Var izmantot arī nesistēmiskās siltuma daudzuma mērvienības - kalorijas: starptautiskā kalorija ir 4,1868 J, termoķīmiskā kalorija - 4,1840 J. Ārvalstu laboratorijās pētījumu rezultāti bieži tiek izteikti, izmantojot t.s. 15 grādu kalorija ir vienāda ar 4,1855 J. Ārpussistēmas britu termiskā iekārta (BTU) tiek pakāpeniski pārtraukta: BTU vid. = 1,055 J.
Siltuma avoti
Galvenie siltuma avoti ir ķīmiskās un kodolreakcijas, kā arī dažādi enerģijas pārveidošanas procesi. Ķīmisko reakciju, kas izdala siltumu, piemēri ir sadegšana un pārtikas sastāvdaļu sadalīšanās. Gandrīz visu siltumu, ko saņem Zeme, nodrošina kodolreakcija, kas notiek Saules dziļumos. Cilvēce ir iemācījusies iegūt siltumu, izmantojot kontrolētus kodola skaldīšanas procesus, un tagad šim pašam mērķim mēģina izmantot kodolsintēzes reakcijas. Cita veida enerģiju, piemēram, mehānisko darbu un elektrisko enerģiju, var pārvērst siltumā. Ir svarīgi atcerēties, ka siltumenerģiju (tāpat kā jebkuru citu) var tikai pārvērst citā formā, bet to nevar saņemt<из ничего>, ne iznīcināt. Tas ir viens no zinātnes, ko sauc par termodinamiku, pamatprincipiem.
Termodinamika
Termodinamika ir zinātne par siltuma, darba un matērijas attiecībām. Mūsdienu priekšstati par šīm attiecībām veidojās, balstoties uz tādu izcilu pagātnes zinātnieku kā Kārno, Klausiusa, Gibsa, Džoula, Kelvina uc darbiem. Termodinamika izskaidro vielas siltumietilpības un siltumvadītspējas, ķermeņu termiskās izplešanās nozīmi. , un fāzu pāreju siltumu. Šīs zinātnes pamatā ir vairāki eksperimentāli izveidoti likumi – principi.
Vielu siltums un īpašības
Dažādas vielas ir dažādas spējas uzkrāt siltumenerģiju; tas ir atkarīgs no to molekulārās struktūras un blīvuma. Siltuma daudzumu, kas nepieciešams, lai vielas masas vienības temperatūru palielinātu par vienu grādu, sauc par tās īpatnējo siltumietilpību. Siltuma jauda ir atkarīga no apstākļiem, kādos viela atrodas. Piemēram, lai uzsildītu vienu gramu gaisa balonā par 1 K, ir nepieciešams vairāk siltuma nekā tādai pašai karsēšanai noslēgtā traukā ar stingrām sienām, jo daļa no balonam piešķirtās enerģijas tiek tērēta gaisa paplašināšanai, un nevis sildot to. Tāpēc jo īpaši gāzu siltumietilpību mēra atsevišķi nemainīgā spiedienā un nemainīgā tilpumā.
Paaugstinoties temperatūrai, palielinās molekulu haotiskās kustības intensitāte – vairums vielu karsējot izplešas. Tiek saukta vielas izplešanās pakāpe, kad temperatūra paaugstinās par 1 K termiskās izplešanās koeficients.
Lai viela pārietu no vienas fāzes stāvokļa uz otru, piemēram, no cietas uz šķidrumu (un dažreiz tieši uz gāzveida), tai jāsaņem noteikts siltuma daudzums. Ja silda ciets, tad tā temperatūra paaugstināsies, līdz tā sāks kust; līdz kušana ir pabeigta, ķermeņa temperatūra saglabāsies nemainīga, neskatoties uz siltuma pievienošanu. Siltuma daudzumu, kas nepieciešams, lai izkausētu vielas masas vienību, sauc par saplūšanas siltumu. Ja karsēsiet tālāk, izkausētā viela uzkarsēs līdz vārīšanās temperatūrai. Siltuma daudzumu, kas nepieciešams šķidruma masas vienības iztvaicēšanai noteiktā temperatūrā, sauc par iztvaikošanas siltumu.
Siltuma loma un tā izmantošana
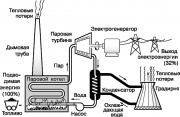
Tvaika turbīnu spēkstacijas darbības shēma
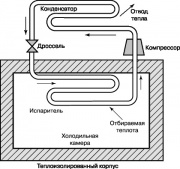
Saldēšanas cikla diagramma
Globālie siltuma apmaiņas procesi neaprobežojas tikai ar Zemes sildīšanu ar saules starojumu. Masīvas konvekcijas straumes atmosfērā nosaka ikdienas laika apstākļu izmaiņas visā pasaulē. Temperatūras izmaiņas atmosfērā starp ekvatoriālo un polāro reģionu kopā ar Koriolisa spēkiem, ko izraisa Zemes rotācija, izraisa nepārtraukti mainīgu konvekcijas straumju parādīšanos, piemēram, pasātiem, strūklu straumēm un siltajām un aukstajām frontēm.
Siltuma pārnešana (sakarā ar siltumvadītspēju) no izkausētā Zemes kodola uz tās virsmu izraisa vulkāna izvirdumus un geizeru parādīšanos. Dažos reģionos ģeotermālo enerģiju izmanto telpu apkurei un elektroenerģijas ražošanai.
Siltums ir gandrīz katra cilvēka neatņemama sastāvdaļa ražošanas procesi. Minēsim svarīgākos no tiem, piemēram, metālu kausēšanu un pārstrādi, dzinēju darbību, pārtikas ražošanu, ķīmisko sintēzi, naftas pārstrādi un visdažādāko priekšmetu izgatavošanu – no ķieģeļiem un traukiem līdz automašīnām un elektroniskām ierīcēm.
Daudzas rūpnieciskās ražošanas un transporta, kā arī termoelektrostacijas nevarētu darboties bez siltumdzinējiem – ierīcēm, kas pārvērš siltumu lietderīgā darbā. Šādu mašīnu piemēri ir kompresori, turbīnas, tvaika, benzīna un reaktīvie dzinēji.
Viens no pazīstamākajiem siltumdzinējiem ir tvaika turbīna, kas īsteno daļu no mūsdienu spēkstacijās izmantotā Rankine cikla. Šī cikla vienkāršota diagramma ir parādīta attēlā. Darba šķidrumu - ūdeni - tvaika katlā pārvērš pārkarsētā tvaikā, ko silda, dedzinot fosilo kurināmo (ogles, naftu vai dabasgāzi). Augsts tvaiks
Gazovik - rūpnieciskās gāzes iekārtas rokasgrāmata GOST, SNiP, PB Fizikālo daudzumu vienības, fizikāli ķīmiskie jēdzieni, attiecības, gāzu sastāvs un īpašības
Mērvienības temperatūras un siltuma daudzuma mērīšanai
Temperatūras mērīšanas pamatvienība bija starptautiskās temperatūras skalas grāds, kas ir gandrīz līdzvērtīgs Celsija grādam. Šī vērtība ir vienāda ar 1/100 no temperatūras intervāla starp 0 un 100 °C, t.i., starp ledus kušanas temperatūru un ūdens viršanas temperatūru 760 mm Hg spiedienā. Art.
Absolūtā temperatūra ir temperatūra, ko mēra no absolūtās nulles, t.i. –273,16 °C, un mēra Kelvina grādos (°K). Kelvina grāds pēc izmēra neatšķiras no Celsija grāda. Tāpēc absolūtā temperatūra tiek izteikta grādu skalā šādi:
T, °K = t, °C + 273,16
Temperatūras mērvienība SI ir Kelvina grāds. Temperatūras mērījumu praktisko rezultātu izteikšanai ir atļauts izmantot Celsija grādus kopā ar Kelvina grādu atkarībā no skalas izcelsmes (nulles pozīcijas).
Piemērs: 250 ±5 °C = 523,16 ±5 °K.
SI sistēmā darbu, enerģiju un siltumu mēra džoulos (J). Dažreiz tiek izmantota lielāka un praktiskām vajadzībām ērtāka mērvienība - kilodžouls (kJ), kas vienāds ar 1000 J. Par darba vienību SI tiek uzskatīts darbs, kas veikts ar 1 N spēku, lai pārvietotos 1 m. Enerģija - fiziskais daudzums, parādot, cik daudz darba ķermenis spēj paveikt.
Kalorijas un kilokalorijas var izmantot kā nesistēmas siltuma vienības. Kalorija ir siltuma daudzums, kas nepieciešams, lai 1 g ūdens uzsildītu par 1 °C (no 19,5 līdz 20,5 °C).
1 cal (kalorija) = 4,1868 J;
1 kcal (kilokalorija) = 1000 cal = 4186,8 J = 4,187 kJ;
1 Mcal (megakalorija) = 10 6 cal = 4,1868 MJ;
1 Gcal (gigakalorija) = 10 9 cal = 4186,8 MJ.
Salīdzinājumam, novērtējot degvielu, tiek izmantots tā sauktais konvencionālais siltums, kura siltumspēja aprēķinam tiek pieņemta nosacīti vienāda ar 7 Mcal/kg vai 7 Gcal/t. Šādos gadījumos mēs runājam attiecīgi par 1 kg vai 1 tonnu standarta degvielas (t.e.f.).
Siltumam ir svarīga loma cilvēka dzīvē, tostarp viņa ķermeņa darbībā. Daļa pārtikā esošās ķīmiskās enerģijas tiek pārvērsta siltumā, tādējādi uzturot ķermeņa temperatūru ap 37
° C. Cilvēka ķermeņa siltuma bilance ir atkarīga arī no apkārtējās vides temperatūras, un cilvēki ir spiesti tērēt daudz enerģijas dzīvojamo un ražošanas telpu apsildīšanai ziemā un dzesēšanai vasarā. Lielāko daļu šīs enerģijas piegādā siltumdzinēji, piemēram, katli un tvaika turbīnas spēkstacijās, kas sadedzina fosilo kurināmo (ogles, naftu) un ražo elektroenerģiju.Līdz 18. gadsimta beigām. siltumu uzskatīja par materiālu vielu, uzskatot, ka ķermeņa temperatūru nosaka tajā esošā “kaloriju šķidruma” vai “kaloriju” daudzums. Vēlāk B.Rumfords, Dž.Džouls un citi tā laika fiziķi ar ģeniāliem eksperimentiem un spriešanu atspēkoja “kaloriju” teoriju, pierādot, ka siltums ir bezsvara un to var iegūt jebkurā daudzumā, vienkārši ar mehānisku kustību. Siltums pats par sevi nav viela; tā ir tikai tā atomu vai molekulu kustības enerģija. Tieši šādai siltuma izpratnei pieturas mūsdienu fizika. Skatīt arī FIZIKA.
Šajā rakstā mēs aplūkosim, kā siltums un temperatūra ir saistīti un kā šie lielumi tiek mērīti. Mūsu diskusijas tēma būs arī šādi jautājumi: siltuma pārnešana no vienas ķermeņa daļas uz otru; siltuma pārnese vakuumā (telpā, kurā nav vielas); siltuma loma mūsdienu pasaulē.
SILTUMS UN TEMPERATŪRA Siltumenerģijas daudzumu vielā nevar noteikt, novērojot katras tās molekulas kustību atsevišķi. Gluži pretēji, tikai pētot vielas makroskopiskās īpašības, var atrast daudzu molekulu mikroskopiskās kustības raksturlielumus, kas aprēķināti vidēji noteiktā laika periodā. Vielas temperatūra ir vidējais molekulārās kustības intensitātes rādītājs, kuras enerģija ir vielas siltumenerģija.Viens no visizplatītākajiem, bet arī neprecīzākajiem veidiem, kā novērtēt temperatūru, ir pieskāriens. Pieskaroties objektam, mēs vērtējam, vai tas ir karsts vai auksts, koncentrējoties uz savām sajūtām. Protams, šīs sajūtas ir atkarīgas no mūsu ķermeņa temperatūras, kas mūs noved pie termiskā līdzsvara jēdziena, kas ir viens no vissvarīgākajiem temperatūras mērīšanas laikā.
Termiskais līdzsvars. Acīmredzot, ja divi ķermeņi A un B (1. att.) cieši piespiediet viens pret otru, tad, pieskaroties tiem pēc pietiekami ilga laika, pamanīsim, ka to temperatūra ir vienāda. Šajā gadījumā viņi saka, ka ķermeņi A un B atrodas termiskā līdzsvarā viens ar otru. Tomēr, vispārīgi runājot, ķermeņiem nav obligāti jāsaskaras, lai starp tiem pastāvētu termiskais līdzsvars; pietiek ar to, ka to temperatūra ir vienāda. To var pārbaudīt, izmantojot trešo ķermeni C , vispirms novedot to termiskā līdzsvarā ar ķermeni A , un pēc tam salīdzinot ķermeņa temperatūru C un B. Ķermenis C šeit spēlē termometra lomu. Stingrā formulējumā šo principu sauc par termodinamikas nulles likumu: ja ķermeņi A un B atrodas termiskā līdzsvarā ar trešo ķermeni C, tad arī šie ķermeņi ir termiskā līdzsvarā viens ar otru.Šis likums ir visu temperatūras mērīšanas metožu pamatā.Temperatūras mērīšana. Ja mēs vēlamies veikt precīzus eksperimentus un aprēķinus, tad nepietiek ar tādiem temperatūras rādītājiem kā karsts, silts, vēss, auksts, mums ir vajadzīga graduēta temperatūras skala. Ir vairākas šādas skalas, un par atskaites punktiem parasti tiek ņemtas ūdens sasalšanas un viršanas temperatūras. Četras visbiežāk sastopamās skalas ir parādītas attēlā. 2. Celtniecības grādu skala, kurā ūdens sasalšanas punkts atbilst 0° , un viršanas temperatūra ir 100° , sauc par Celsija skalu pēc zviedru astronoma A. Celsija vārdā, kurš to aprakstīja 1742. gadā. Tiek uzskatīts, ka zviedru dabaszinātnieks K. Linnejs pirmo reizi izmantoja šo skalu. Tagad Celsija skala ir visizplatītākā pasaulē. Fārenheita temperatūras skala, kurā ūdens sasalšanas un viršanas temperatūra atbilst ārkārtīgi neērtajiem cipariem 32 un 212° , 1724. gadā ierosināja G. Fārenheits. Fārenheita skala ir plaši izplatīta angliski runājošajās valstīs, taču zinātniskajā literatūrā to gandrīz neizmanto. Lai pārvērstu temperatūru uz Celsija (° C) līdz Fārenheita temperatūrai (° F) ir formula°F = (9/5) ° C + 32 un reversās tulkošanas formulai°C = (5/9) (°F - 32). Abas skalas, Fārenheita un Celsija skalas, ir ļoti neērtas, veicot eksperimentus apstākļos, kad temperatūra nokrītas zem ūdens sasalšanas punkta un tiek izteikta kā negatīvs skaitlis. Šādos gadījumos tika ieviestas absolūtās temperatūras skalas, kuru pamatā ir ekstrapolācija uz tā saukto absolūto nulli, punktu, kurā molekulārajai kustībai vajadzētu beigties. Vienu no tām sauc par Rankine skalu, bet otru par absolūto termodinamisko skalu; to temperatūru mēra Rankine grādos (° R) un kelvins (K). Abas skalas sākas no absolūtās nulles, un ūdens sasalšanas punkts atbilst 491,7° R un 273,16 K. Grādu un kelvinu skaits starp ūdens sasalšanas un viršanas temperatūru pēc Celsija skalas un absolūtās termodinamiskās skalas ir vienāds un vienāds ar 100; Fārenheita un Rankine skalām arī tas ir vienāds, bet vienāds ar 180. Celsija grādus pārvērš kelvinos, izmantojot formulu K =° C + 273,16 un no Fārenheita grādiem līdz Rankine grādiem saskaņā ar formulu°R = °F + 459,7. Temperatūras mērīšanai paredzēto instrumentu darbība balstās uz dažādām fizikālām parādībām, kas saistītas ar vielas siltumenerģijas izmaiņām, elektriskās pretestības, tilpuma, spiediena, emisijas raksturlielumu un termoelektrisko īpašību izmaiņām. Viens no vienkāršākajiem un pazīstamākajiem temperatūras mērīšanas instrumentiem ir dzīvsudraba stikla termometrs, kas parādīts attēlā. 3, A. Dzīvsudraba bumbiņu termometra apakšējā daļā ievieto vidē vai piespiež pret objektu, kura temperatūra ir jāmēra, un atkarībā no tā, vai bumbiņa saņem vai izdala siltumu, dzīvsudrabs izplešas vai saraujas un tā kolonna paceļas vai iekrīt kapilārā. Ja termometrs ir iepriekš kalibrēts un aprīkots ar skalu, tad jūs varat tieši uzzināt ķermeņa temperatūru.Vēl viena ierīce, kuras darbības pamatā ir termiskā izplešanās, ir bimetāla termometrs, kas parādīts attēlā.
3, b. Tās galvenais elements spirālveida plāksne no diviem metinātiem metāliem ar dažādiem termiskās izplešanās koeficientiem. Sildot, viens no metāliem izplešas vairāk nekā otrs, spirāle pagriežas un pagriež bultiņu attiecībā pret skalu. Šādas ierīces bieži izmanto iekštelpu un āra gaisa temperatūras mērīšanai, taču tās nav piemērotas vietējās temperatūras noteikšanai.Vietējo temperatūru parasti mēra, izmantojot termopāri, kas ir divi atšķirīgu metālu vadi, kas pielodēti vienā galā (att.
4, A). Sildot šādu savienojumu, vadu brīvajos galos rodas emf, kas parasti ir vairāki milivolti. Termopāri ir izgatavoti no dažādiem metālu pāriem: dzelzs un konstantāna, vara un konstantāna, hromela un alumela. Viņu termo-emf mainās gandrīz lineāri ar temperatūru plašā temperatūras diapazonā.Ir zināms arī cits termoelektrisks efekts: vadoša materiāla pretestības atkarība no temperatūras. Tas ir elektriskās pretestības termometru darbības pamatā, no kuriem viens ir parādīts attēlā.
4, b. Maza temperatūras jutīga elementa (termiskā pārveidotāja) pretestību parasti salīdzina ar plānas stieples spoles pretestību ar kalibrēta mainīga rezistora pretestību, izmantojot Vitstonas tiltu. Izvades ierīci var kalibrēt tieši grādos.Optiskos pirometrus izmanto, lai mērītu karstu ķermeņu temperatūru, kas izstaro redzamo gaismu. Vienā šīs ierīces iemiesojumā korpusa izstarotā gaisma tiek salīdzināta ar kvēlspuldzes kvēldiega emisiju, kas novietota binokļa fokusa plaknē, caur kuru tiek skatīts izstarojošais ķermenis. Elektriskā strāva, kas silda lampas kvēldiegu, tiek mainīta, līdz vizuāli salīdzinot kvēldiega un korpusa mirdzumu, atklājas, ka starp tiem ir izveidots termiskais līdzsvars. Instrumenta skalu var kalibrēt tieši temperatūras vienībās.
Tehniskie sasniegumi pēdējos gados ir ļāvuši izveidot jaunus temperatūras sensorus. Piemēram, gadījumos, kad nepieciešama īpaši augsta jutība, termopāra vai parastā pretestības termometra vietā tiek izmantota pusvadītāju ierīce, termistors. Krāsvielas un šķidrie kristāli, kas maina savu fāzes stāvokli, tiek izmantoti arī kā termiskie pārveidotāji, īpaši gadījumos, kad ķermeņa virsmas temperatūra svārstās plašā diapazonā. Visbeidzot tiek izmantota infrasarkanā termogrāfija, kas rada objekta infrasarkano attēlu nepatiesās krāsās, kur katra krāsa atbilst noteiktai temperatūrai. Šai temperatūras mērīšanas metodei ir visplašākais pielietojums no medicīniskās diagnostikas līdz telpu siltumizolācijas pārbaudei. Skatīt arī CIETVIELAS FIZIKA; ŠĶIDRAIS KRISTĀLS.
Siltuma daudzuma mērīšana. Ķermeņa siltumenerģiju (siltuma daudzumu) var izmērīt tieši, izmantojot tā saukto kalorimetru; vienkārša šādas ierīces versija ir parādīta attēlā. 5. Šis ir rūpīgi izolēts slēgts trauks, kas aprīkots ar ierīcēm temperatūras mērīšanai tajā un dažreiz piepildīts ar darba šķidrumu ar zināmām īpašībām, piemēram, ūdeni. Lai izmērītu siltuma daudzumu nelielā apsildāmā korpusā, to ievieto kalorimetrā un gaida, līdz sistēma sasniedz termisko līdzsvaru. Siltuma daudzumu, kas tiek nodots kalorimetram (precīzāk, ūdenim, kas to piepilda), nosaka ūdens temperatūras paaugstināšanās.Siltuma daudzumu, kas izdalās ķīmiskās reakcijas, piemēram, sadegšanas laikā, var izmērīt, ievietojot kalorimetrā nelielu “bumbu”. “Bumbā” ir paraugs, kuram aizdedzināšanai pieslēgti elektrības vadi, un atbilstošs skābekļa daudzums. Pēc tam, kad paraugs ir pilnībā sadedzināts un ir izveidots termiskais līdzsvars, nosaka, cik daudz ir palielinājusies ūdens temperatūra kalorimetrā un līdz ar to izdalītā siltuma daudzums. Skatīt arī KALORIMETRIJA.
Siltuma mērvienības. Siltums ir enerģijas veids, un tāpēc tas jāmēra enerģijas vienībās. Enerģijas SI mērvienība ir džouls (J). Var izmantot arī nesistēmiskas siltuma daudzuma kaloriju vienības: starptautiskā kalorija ir 4,1868 J, termoķīmiskā kalorija 4,1840 J. Ārvalstu laboratorijās pētījumu rezultāti bieži tiek izteikti, izmantojot t.s. 15 grādu kalorija ir vienāda ar 4,1855 J. Ārpussistēmas britu termiskā iekārta (BTU) tiek pakāpeniski pārtraukta: BTU vid. = 1,055 J. Galvenie siltuma avoti ir ķīmiskās un kodolreakcijas, kā arī dažādi enerģijas pārveidošanas procesi. Ķīmisko reakciju, kas izdala siltumu, piemēri ir sadegšana un pārtikas sastāvdaļu sadalīšanās. Gandrīz visu siltumu, ko saņem Zeme, nodrošina kodolreakcija, kas notiek Saules dziļumos. Cilvēce ir iemācījusies iegūt siltumu, izmantojot kontrolētus kodola skaldīšanas procesus, un tagad šim pašam mērķim mēģina izmantot kodolsintēzes reakcijas. Cita veida enerģiju, piemēram, mehānisko darbu un elektrisko enerģiju, var pārvērst siltumā. Ir svarīgi atcerēties, ka siltumenerģiju (tāpat kā jebkuru citu) var pārvērst tikai citā formā, bet nevar iegūt “no nekā” vai iznīcināt. Tas ir viens no zinātnes, ko sauc par termodinamiku, pamatprincipiem. TERMODINAMIKA Termodinamika ir zinātne par siltuma, darba un matērijas attiecībām. Mūsdienu priekšstati par šīm attiecībām veidojās, balstoties uz tādu izcilu pagātnes zinātnieku kā Kārno, Klausiusa, Gibsa, Džoula, Kelvina uc darbiem. Termodinamika izskaidro vielas siltumietilpības un siltumvadītspējas, ķermeņu termiskās izplešanās nozīmi. , un fāzu pāreju siltumu. Šīs zinātnes pamatā ir vairāki eksperimentāli izveidoti likumi un principi.Termodinamikas pirmsākumi. Iepriekš formulētais termodinamikas nulles likums ievieš termiskā līdzsvara, temperatūras un termometrijas jēdzienus. Pirmais termodinamikas likums ir apgalvojums, kas ir ļoti svarīgs visai zinātnei kopumā: enerģiju nevar ne iznīcināt, ne iegūt “no nekā”, tāpēc Visuma kopējā enerģija ir nemainīgs lielums. Vienkāršākajā formā pirmo termodinamikas likumu var formulēt šādi: enerģija, ko sistēma saņem, mīnus enerģija, ko tā izdala, ir vienāda ar enerģiju, kas paliek sistēmā. No pirmā acu uzmetiena šis apgalvojums šķiet acīmredzams, bet, piemēram, ne, situācijas, piemēram, benzīna sadegšana automašīnas dzinēja cilindros: šeit saņemtā enerģija ir ķīmiska, izdalītā enerģija ir mehāniska (darba), bet sistēmā paliekošā enerģija ir termiska.Tātad ir skaidrs, ka enerģija var pārveidoties no viena veida citā un ka šādas pārvērtības pastāvīgi notiek dabā un tehnoloģijās. Vairāk nekā pirms simts gadiem J. Džouls to pierādīja gadījumam, kad mehāniskā enerģija tika pārveidota siltumenerģijā, izmantojot ierīci, kas parādīta attēlā. 6, A. Šajā ierīcē lejupejoši un augoši svari grieza vārpstu ar asmeņiem ar ūdeni pildītā kalorimetrā, izraisot ūdens uzsilšanu. Precīzi mērījumi ļāva Džoulam noteikt, ka viena siltuma kalorija ir līdzvērtīga 4,186 J mehāniskā darba. Attēlā redzamā ierīce.
6, b, tika izmantots, lai noteiktu elektriskās enerģijas termisko ekvivalentu.Pirmais termodinamikas likums izskaidro daudzas ikdienas parādības. Piemēram, kļūst skaidrs, kāpēc virtuvi nevar atdzesēt ar atvērtu ledusskapi. Pieņemsim, ka esam izolējuši virtuvi no apkārtējās vides. Enerģija tiek nepārtraukti piegādāta sistēmai caur ledusskapja barošanas vadu, bet sistēma neizdala enerģiju. Tādējādi tā kopējā enerģija palielinās, un virtuve kļūst arvien siltāka: vienkārši pieskarieties siltummaiņa (kondensatora) caurulēm ledusskapja aizmugurējā sienā, un jūs sapratīsit tās kā “dzesēšanas” ierīces nederīgumu. Bet, ja šīs caurules tiktu izņemtas ārpus sistēmas (piemēram, ārpus loga), tad virtuve izdalītu vairāk enerģijas nekā saņemta, t.i. atdzesētu, un ledusskapis darbotos kā logu gaisa kondicionieris.
Pirmais termodinamikas likums ir dabas likums, kas izslēdz enerģijas radīšanu vai iznīcināšanu. Tomēr tas neko nesaka par to, kā dabā notiek enerģijas pārneses procesi. Tātad, mēs zinām, ka karsts ķermenis uzsildīs aukstu, ja šie ķermeņi nonāks saskarē. Bet vai auksts ķermenis pats var nodot savu siltuma rezervi karstajam? Pēdējā iespēja To kategoriski noraida termodinamikas otrais likums.
Pirmais likums arī izslēdz iespēju izveidot dzinēju ar koeficientu noderīga darbība(efektivitāte) vairāk nekā 100% (līdzīgs
"mūžīgs" dzinējs patvaļīgi ilgu laiku varētu piegādāt vairāk enerģijas, nekā pats patērē). Nav iespējams uzbūvēt dzinēju pat ar 100% efektivitāti, jo tam noteikti jāzaudē daļa no tam piegādātās enerģijas mazāk noderīgas siltumenerģijas veidā. Tādējādi ritenis bez enerģijas padeves negriezīsies ilgu laiku, jo gultņu berzes dēļ mehāniskās kustības enerģija pakāpeniski pārvērtīsies siltumā, līdz ritenis apstāsies.Tendenci pārvērst "noderīgo" darbu mazāk lietderīgā siltumenerģijā var salīdzināt ar citu procesu, kas notiek, savienojot divus traukus, kas satur dažādas gāzes. Pietiekami ilgi gaidot, abos traukos atrodam viendabīgu gāzu maisījumu, daba darbojas tā, ka sistēmas kārtība samazinās. Šo traucējumu termodinamisko mēru sauc par entropiju, un otro termodinamikas likumu var formulēt dažādi: procesi dabā vienmēr norisinās tā, ka palielinās sistēmas un tās vides entropija. Tādējādi Visuma enerģija paliek nemainīga, bet tā entropija nepārtraukti palielinās.
Vielu siltums un īpašības. Dažādām vielām ir dažādas spējas uzkrāt siltumenerģiju; tas ir atkarīgs no to molekulārās struktūras un blīvuma. Siltuma daudzumu, kas nepieciešams, lai paaugstinātu vielas masas vienības temperatūru par vienu grādu, sauc par to īpatnējā siltuma jauda. Siltuma jauda ir atkarīga no apstākļiem, kādos viela atrodas. Piemēram, lai uzsildītu vienu gramu gaisa balonā par 1 K, ir nepieciešams vairāk siltuma nekā tādai pašai karsēšanai noslēgtā traukā ar stingrām sienām, jo daļa no balonam piešķirtās enerģijas tiek tērēta gaisa paplašināšanai, un nevis sildot to. Tāpēc jo īpaši gāzu siltumietilpību mēra atsevišķi nemainīgā spiedienā un nemainīgā tilpumā.Paaugstinoties temperatūrai, palielinās molekulu haotiskās kustības intensitāte, lielākā daļa vielu karsējot izplešas. Vielas izplešanās pakāpi, kad temperatūra paaugstinās par 1 K, sauc par termiskās izplešanās koeficientu.
Lai viela pārietu no vienas fāzes stāvokļa uz otru, piemēram, no cietas uz šķidrumu (un dažreiz tieši uz gāzveida), tai jāsaņem noteikts siltuma daudzums. Ja karsējat cietu vielu, tās temperatūra paaugstināsies, līdz tā sāks kust; līdz kušana ir pabeigta, ķermeņa temperatūra saglabāsies nemainīga, neskatoties uz siltuma pievienošanu. Siltuma daudzumu, kas nepieciešams, lai izkausētu vielas masas vienību, sauc par saplūšanas siltumu. Ja karsēsiet tālāk, izkausētā viela uzkarsēs līdz vārīšanās temperatūrai. Siltuma daudzumu, kas nepieciešams šķidruma masas vienības iztvaicēšanai noteiktā temperatūrā, sauc par iztvaikošanas siltumu.
Molekulārā kinētiskā teorija. Molekulārā kinētiskā teorija izskaidro vielas makroskopiskās īpašības, mikroskopiskā līmenī ņemot vērā šo vielu veidojošo atomu un molekulu uzvedību. Šajā gadījumā tiek izmantota statistiskā pieeja un izdarīti daži pieņēmumi par pašām daļiņām un to kustības raksturu. Tādējādi molekulas tiek uzskatītas par cietām bumbiņām, kuras gāzveida vidē atrodas nepārtrauktā haotiskā kustībā un veic ievērojamus attālumus no vienas sadursmes līdz otrai. Sadursmes tiek uzskatītas par elastīgām un notiek starp daļiņām, kuru izmērs ir mazs, bet to skaits ir ļoti liels. Neviena no reālajām gāzēm precīzi neatbilst šim modelim, taču lielākā daļa gāzu ir diezgan tuvu tam, kas nosaka molekulārās kinētiskās teorijas praktisko vērtību.Pamatojoties uz šīm idejām un izmantojot statistisko pieeju, Maksvels atvasināja gāzes molekulu ātrumu sadalījumu ierobežotā tilpumā, kas vēlāk tika nosaukts viņa vārdā. Šis sadalījums ir grafiski parādīts attēlā. 7 noteiktai ūdeņraža masai 100 un 1000 temperatūrā
° C. Ordinātu ass attēlo molekulu skaitu, kas pārvietojas ar ātrumu, kas norādīts uz abscisu ass. Kopējais daļiņu skaits ir vienāds ar laukumu zem katras līknes un ir vienāds abos gadījumos. Diagramma parāda, ka lielākajai daļai daļiņu ātrums ir tuvu kādai vidējai vērtībai, un tikai nelielai daļai ir ļoti liels vai mazs ātrums. Vidējais ātrums norādītajās temperatūrās ir robežās no 20003000 m/s, t.i. ļoti liels.Liels skaits šādu ātri kustīgu gāzes molekulu iedarbojas ar diezgan izmērāmu spēku uz apkārtējiem ķermeņiem. Mikroskopiskie spēki, ar kuriem daudzas gāzes molekulas ietriecas tvertnes sieniņās, kopā veido makroskopisku daudzumu, ko sauc par spiedienu. Kad gāzei tiek piegādāta enerģija (paaugstinās temperatūra), palielinās tās molekulu vidējā kinētiskā enerģija, gāzes daļiņas biežāk un stiprāk skar sienas, palielinās spiediens, un, ja sienas nav pilnībā stingras, tad tās stiepjas un tilpums. gāzes daudzums palielinās. Tādējādi mikroskopiskā statistiskā pieeja, kas ir molekulārās kinētiskās teorijas pamatā, ļauj mums izskaidrot mūsu apspriesto termiskās izplešanās fenomenu.
Vēl viens molekulārās kinētiskās teorijas rezultāts ir likums, kas apraksta tādas gāzes īpašības, kas atbilst iepriekš uzskaitītajām prasībām. Šis ir tā sauktais stāvokļa vienādojums ideāla gāze savieno viena mola gāzes spiedienu, tilpumu un temperatūru, un tam ir vienādības forma
PV = RT, kur P spiediens, V apjoms, T temperatūra, un R universālā gāzes konstante, kas vienāda ar (8.31441± 0,00026) J/(mol H UZ). Skatīt arī MOLEKULĀRĀ KINĒTISKĀ TEORIJA; TERMODINAMIKA. SILTUMA NODOŠANA Siltuma pārnese ir siltuma pārneses process ķermeņa iekšienē vai no viena ķermeņa uz otru temperatūras atšķirību dēļ. Siltuma pārneses intensitāte ir atkarīga no vielas īpašībām, temperatūras starpības un pakļaujas eksperimentāli noteiktajiem dabas likumiem. Lai izveidotu efektīvi strādājošas apkures vai dzesēšanas sistēmas, dažādus dzinējus, spēkstacijas, siltumizolācijas sistēmas, ir jāzina siltuma pārneses principi. Dažos gadījumos siltuma apmaiņa ir nevēlama (kausēšanas krāšņu, kosmosa kuģu uc siltumizolācija), savukārt citos tai jābūt pēc iespējas lielākai (tvaika katli, siltummaiņi, virtuves piederumi).Ir trīs galvenie siltuma pārneses veidi: vadītspēja, konvekcija un starojuma siltuma pārnese.
Siltumvadītspēja. Ja ķermeņa iekšienē ir temperatūras starpība, tad siltumenerģija pārvietojas no karstākās ķermeņa daļas uz aukstāko. Šo siltuma pārneses veidu, ko izraisa termiskās kustības un molekulu sadursmes, sauc par siltumvadītspēju; ar pietiekami daudz augstas temperatūras cietās vielās to var novērot vizuāli. Tādējādi, karsējot tērauda stieni no viena gala gāzes degļa liesmā, pa stieni tiek pārnesta siltumenerģija, un noteiktā attālumā no uzkarsētā gala izplatās spīdums (ar attālumu no sildīšanas vietas arvien mazāk intensīvs). ).Siltuma pārneses intensitāte siltumvadītspējas dēļ ir atkarīga no temperatūras gradienta, t.i. attiecības
D T/D x temperatūras starpība stieņa galos līdz attālumam starp tiem. Tas ir atkarīgs arī no stieņa šķērsgriezuma laukuma (m 2 ) un materiāla siltumvadītspējas koeficientu[ attiecīgajās vienībās W/(m CH K) ] . Sakarību starp šiem lielumiem atvasināja franču matemātiķis J. Furjē, un tai ir šāda forma: Kur q siltuma plūsma, k siltumvadītspējas koeficients, un A šķērsgriezuma laukums. Šo attiecību sauc par Furjē siltumvadītspējas likumu; mīnusa zīme tajā norāda, ka siltums tiek pārnests virzienā, kas ir pretējs temperatūras gradientam.No Furjē likuma izriet, ka siltuma plūsmu var samazināt, samazinot vienu no lielumiem: siltumvadītspējas koeficientu, laukumu vai temperatūras gradientu. Ēkai ziemas apstākļos pēdējās vērtības ir praktiski nemainīgas, un tāpēc, lai telpā uzturētu vēlamo temperatūru, atliek samazināt sienu siltumvadītspēju, t.i. uzlabot to siltumizolāciju.
Tabulā parādīti dažu vielu un materiālu siltumvadītspējas koeficienti. Tabulā redzams, ka daži metāli vada siltumu daudz labāk nekā citi, taču tie visi ir ievērojami labāki siltuma vadītāji nekā gaiss un poraini materiāli.
|
DAŽU VIELU UN MATERIĀLU SILTUMU VADĪTĪBA |
|
|
Vielas un materiāli |
Siltumvadītspēja, W/(m × K) |
| Alumīnijs | |
| Bronza | |
| Bismuts | |
| Volframs | |
| Dzelzs | |
| Zelts | |
| Kadmijs | |
| Magnijs | |
| Varš | |
| Arsēns | |
| Niķelis | |
| Platīns | |
| Merkurs | |
| Svins | |
| Cinks | |
|
Citi materiāli |
|
| Azbests | |
| Betons | |
| Gaiss | |
| Eider uz leju (brīva) | |
| Koka rieksts) | |
| Magnēzijs (MgO) | |
| Zāģu skaidas | |
| Gumija (sūklis) | |
| Vizla | |
| Stikls | |
| Ogleklis (grafīts) | |
Daudzu vielu termiskā un elektriskā pretestība strauji samazinās, temperatūrai nokrītot zem šķidrā hēlija temperatūras (1,8 K). Šo fenomenu, ko sauc par supravadītspēju, izmanto, lai uzlabotu daudzu ierīču efektivitāti, sākot no mikroelektronikas ierīcēm līdz elektropārvades līnijām un lieliem elektromagnētiem. Skatīt arī SUPERVADĪTĪBA.
Konvekcija. Kā jau teicām, kad šķidrumam vai gāzei tiek piegādāts siltums, palielinās molekulu kustības intensitāte, kā rezultātā palielinās spiediens. Ja šķidrumam vai gāzei nav ierobežots tilpums, tas izplešas; šķidruma (gāzes) lokālais blīvums kļūst mazāks, un, pateicoties peldspējas (Arhimēda) spēkiem, uzkarsētā vides daļa virzās uz augšu (tādēļ siltais gaiss telpā paceļas no radiatoriem līdz griestiem). Šo parādību sauc par konvekciju. Lai netērētu apkures sistēmas siltumu, jāizmanto mūsdienīgi sildītāji, kas nodrošina piespiedu gaisa cirkulāciju.Konvektīvā siltuma plūsma no sildītāja uz apsildāmo vidi ir atkarīga no molekulu sākotnējā kustības ātruma, blīvuma, viskozitātes, siltumvadītspējas un siltumietilpības un vides; Ļoti svarīgi ir arī sildītāja izmērs un forma. Attiecības starp attiecīgajiem lielumiem pakļaujas Ņūtona likumam
q = hA ( T W- TҐ), kur q siltuma plūsma (mēra vatos), A siltuma avota virsmas laukums (m 2), T W Un TҐ avota un tā vides temperatūra (kelvinos). Konvektīvās siltuma pārneses koeficients h ir atkarīgs no vides īpašībām, tās molekulu sākotnējā ātruma, kā arī no siltuma avota formas, un to mēra vienībās W/(m 2 H UZ).Lielums
h nav vienāds gadījumos, kad gaiss ap sildītāju ir stacionārs (brīvā konvekcija) un kad tas pats sildītājs atrodas gaisa plūsmā (piespiedu konvekcija). Vienkāršos gadījumos, kad šķidrums plūst pa cauruli vai plūst ap līdzenu virsmu, koeficients h var aprēķināt teorētiski. Tomēr vēl nav izdevies atrast analītisku risinājumu konvekcijas problēmai vides turbulentai plūsmai. Turbulence ir sarežģīta šķidruma (gāzes) kustība, kas ir haotiska mērogā, kas ir ievērojami lielāks par molekulāro.Ja apsildāmu (vai, gluži otrādi, aukstu) ķermeni ievieto stacionārā vidē vai plūsmā, tad ap to veidojas konvekcijas strāvas un robežslānis. Temperatūrai, spiedienam un molekulu kustības ātrumam šajā slānī ir liela nozīme konvektīvās siltuma pārneses koeficienta noteikšanā.
Konvekcija ir jāņem vērā siltummaiņu, gaisa kondicionēšanas sistēmu, ātrgaitas lidmašīnu un daudzu citu lietojumu projektēšanā. Visās šādās sistēmās siltumvadītspēja notiek vienlaikus ar konvekciju gan starp cietiem ķermeņiem, gan to vidē. Plkst paaugstinātas temperatūras Nozīmīga loma var būt arī starojuma siltuma pārnesei.
Starojuma siltuma pārnese. Trešais siltuma pārneses veids, starojuma siltuma pārnese, atšķiras no vadīšanas un konvekcijas ar to, ka siltumu šajā gadījumā var pārnest caur vakuumu. Tā līdzība ar citām siltuma pārneses metodēm ir tāda, ka to izraisa arī temperatūras atšķirības. Termiskais starojums ir viens no veidiem elektromagnētiskā radiācija. Cita veida radioviļņi, ultravioletais un gamma starojums rodas, ja nav temperatūras starpības.Attēlā 8. attēlā parādīta termiskā (infrasarkanā) starojuma enerģijas atkarība no viļņa garuma. Siltuma starojumu var pavadīt redzamās gaismas emisija, taču tā enerģija ir maza, salīdzinot ar starojuma enerģiju no neredzamās spektra daļas.
Siltuma pārneses intensitāte vadīšanas un konvekcijas ceļā ir proporcionāla temperatūrai, un starojuma siltuma plūsma ir proporcionāla temperatūras ceturtajai pakāpei un atbilst Stefana Bolcmaņa likumam
Dzīvojamās un biroju telpas bieži tiek apsildītas ar maziem elektriskiem siltuma izstarotājiem; to spirāļu sarkanais mirdzums ir redzams termiskais starojums, kas atrodas tuvu spektra infrasarkanās daļas malai. Telpu silda siltums, ko galvenokārt nes starojuma neredzamā, infrasarkanā daļa. Nakts redzamības ierīcēs
^ Šīs ierīces izmanto termiskā starojuma avotu un uztvērēju, kas ir jutīgs pret infrasarkano starojumu, ļaujot redzēt tumsā.Saule ir spēcīga siltumenerģijas izstarotāja; tas silda Zemi pat 150 miljonu km attālumā. Saules starojuma intensitāte, ko gadu no gada reģistrē stacijas, kas atrodas daudzviet pasaulē, ir aptuveni 1,37 W
/ m 2 . Saules enerģija ir dzīvības avots uz Zemes. Šobrīd tiek meklēti veidi, kā to visefektīvāk izmantot. Saules paneļi ir radīti māju apsildīšanai un elektroenerģijas ražošanai sadzīves vajadzībām. SILTUMA LOMA UN TĀ IZMANTOŠANA Globālie siltuma apmaiņas procesi neaprobežojas tikai ar Zemes sildīšanu ar saules starojumu. Masīvas konvekcijas straumes atmosfērā nosaka ikdienas laika apstākļu izmaiņas visā pasaulē. Temperatūras izmaiņas atmosfērā starp ekvatoriālo un polāro reģionu kopā ar Koriolisa spēkiem, ko izraisa Zemes rotācija, izraisa nepārtraukti mainīgu konvekcijas straumju parādīšanos, piemēram, pasātiem, strūklu straumēm un siltajām un aukstajām frontēm. Skatīt arī KLIMATS; METEOROLOĢIJA UN KLIMATOLOĢIJA.Siltuma pārnešana (sakarā ar siltumvadītspēju) no izkausētā Zemes kodola uz tās virsmu izraisa vulkāna izvirdumus un geizeru parādīšanos. Dažos reģionos ģeotermālo enerģiju izmanto telpu apkurei un elektroenerģijas ražošanai.
Siltums ir neaizstājams gandrīz visu ražošanas procesu dalībnieks. Minēsim svarīgākos no tiem, piemēram, metālu kausēšanu un pārstrādi, dzinēju darbību, pārtikas ražošanu, ķīmisko sintēzi, naftas pārstrādi un visdažādāko priekšmetu izgatavošanu – no ķieģeļiem un traukiem līdz automašīnām un elektroniskām ierīcēm.
Daudzas rūpnieciskās ražošanas un transporta, kā arī termoelektrostacijas nevarētu darboties bez siltumdzinējiem – ierīcēm, kas pārvērš siltumu lietderīgā darbā. Šādu mašīnu piemēri ir kompresori, turbīnas, tvaika, benzīna un reaktīvie dzinēji.
Viens no slavenākajiem siltumdzinējiem ir tvaika turbīna, kas īsteno daļu no Rankine cikla, ko izmanto mūsdienu spēkstacijās. Šī cikla vienkāršota diagramma ir parādīta attēlā. 9. Darba šķidruma ūdeni pārvērš pārkarsētā tvaikā tvaika katlā, ko silda, dedzinot fosilo kurināmo (ogles, naftu vai dabasgāzi). Tvaiks augstspiediena griež tvaika turbīnas vārpstu, kas darbina ģeneratoru, kas ražo elektrību. Izplūdes tvaiks kondensējas, ja to atdzesē tekoša ūdens, kas absorbē daļu siltuma, kas netiek izmantots Rankine ciklā. Tālāk ūdens tiek piegādāts dzesēšanas tornim, no kurienes daļa siltuma tiek izvadīta atmosfērā. Kondensāts tiek atgriezts tvaika katlā, izmantojot sūkni, un viss cikls tiek atkārtots.
Visi Rankine cikla procesi ilustrē iepriekš aprakstītos termodinamikas principus. Jo īpaši saskaņā ar otro likumu daļa no elektrostacijas patērētās enerģijas ir jāizkliedē vidē siltuma veidā. Izrādās, ka šādā veidā tiek zaudēti aptuveni 68% no sākotnēji fosilā kurināmā ietvertās enerģijas. Ievērojamu spēkstacijas efektivitātes pieaugumu varētu panākt, tikai paaugstinot tvaika katla temperatūru (ko ierobežo materiālu siltumnoturība) vai pazeminot vides temperatūru, kurp aiziet siltums, t.i. atmosfēra.
Vēl viens termodinamiskais cikls liela nozīme mūsu Ikdiena, tas ir tvaika kompresora dzesēšanas Rankine cikls, kura diagramma ir parādīta attēlā. 10. Ledusskapjos un sadzīves gaisa kondicionieros enerģija tās nodrošināšanai tiek piegādāta no ārpuses. Kompresors palielina ledusskapja darba vielas temperatūru un spiedienu: freonu, amonjaku vai oglekļa dioksīdu. Pārkarsētā gāze tiek piegādāta kondensatoram, kur tā atdziest un kondensējas, izdalot siltumu vidē. Šķidrums, kas iziet no kondensatora caurulēm, caur droseļvārstu nonāk iztvaicētājā, un daļa no tā iztvaiko, ko pavada strauja temperatūras pazemināšanās. Iztvaicētājs ņem siltumu no ledusskapja kameras, kas silda darba šķidrumu caurulēs; šo šķidrumu kompresors piegādā kondensatoram, un cikls atkārtojas vēlreiz.
Attēlā parādītais saldēšanas cikls. 10, var izmantot arī siltumsūknī. Šādi siltumsūkņi vasarā atdod siltumu karstajam atmosfēras gaisam un kondicionē telpu, savukārt ziemā, gluži pretēji, ņem siltumu no aukstā gaisa un silda telpu.
Kodolreakcijas ir svarīgs siltuma avots, piemēram, enerģijas ražošanai un transportēšanai. 1905. gadā A. Einšteins parādīja, ka masa un enerģija ir saistītas ar attiecību
E = mc 2 , t.i. var pārveidoties viens par otru. Gaismas ātrums c ļoti liels: 300 tūkstoši km/ Ar. Tas nozīmē, ka pat neliels daudzums vielas var nodrošināt milzīgu enerģijas daudzumu. Tādējādi no 1 kg skaldāmā materiāla (piemēram, urāna) teorētiski ir iespējams iegūt enerģiju, ko 1 MW elektrostacija nodrošina 1000 nepārtrauktas darbības dienu laikā. Skatīt arī ATOMA UZBŪVE; KRĀSNS UN UZKURŠKAS TEHNOLOĢIJA; ELEKTROMAGNĒTISKĀ RADIĀCIJA; SILUMMAINIS; TURBĪNA; FIZISKO DAUDZUMU MĒRVIENĪBAS.LITERATŪRA Zemanskis M. Temperatūra ir ļoti augsta un ļoti zema. M., 1968. gadsPols R. Mehānika, akustika un siltuma izpēte. M., 1971. gads
Smorodinsky Ya.A. Temperatūra. M., 1981. gads
Fens Dž. Mašīnas, enerģija un entropija. M., 1986. gads
Atkins P.V. Kārtība un nekārtība dabā. M., 1987. gads
Šķidrie kalorimetri
Šāda veida kalorimetri, kas visplašāk tiek izmantoti tehnoloģijās, ir vienkāršas konstrukcijas un viegli kopjami. Ārēji izraisītas reakcijas radītais siltuma daudzums vispirms tiek pārnests uz reakcijas trauku (kurā notika reakcija) un pēc tam uz šķidruma vannu. Šķidrums vannā tiek nepārtraukti sajaukts, izmantojot lāpstiņriteni, pacelšanas skrūvi vai sūkņus, kas paātrina temperatūras izlīdzināšanu. Vanna ir maksimāli termiski izolēta (ekranēta) no apkārtējās vides. Šķidruma vannas temperatūras izmaiņas ir konstatētā siltuma daudzuma mērs. Sildāmo masu siltumietilpība nedrīkst būt pārāk liela, lai nodrošinātu pietiekamu temperatūras maiņu un lai mērīšanas process neieilgst pārāk ilgi (kas palielina siltuma zudumus).
Attēls Šķidruma kalorimetra ierīce.
Ja pastāv augstas prasības pastāvīgiem vides apstākļiem, visu kalorimetru var ievietot citā vannā un ar vadības cilpas palīdzību tajā ar augstu precizitāti stabilizēt temperatūru. Tas ir nepieciešams galvenokārt gadījumos, kad ir nepieciešams veikt eksperimentus temperatūrā, kas ievērojami atšķiras no apkārtējās vides temperatūras.
Lai veiktu analīzes zemā temperatūrā (līdz aptuveni -150°C), kā dzesēšanas vidi izmanto šķidro slāpekli. Šajā gadījumā ir jāpievērš uzmanība tam, lai uz paraugiem vai traukiem ar paraugiem, mainot tos, nenogulsnējas sals no apkārtējā mitrā gaisa, jo tā slānis var ietekmēt mērīšanas procesu. Lai no tā izvairītos, kad kalorimetrs ir atvērts, paraugu un parauga tvertni iztīra ar aukstu slāpekļa gāzi.
Kalorimetri ar metāla korpusu
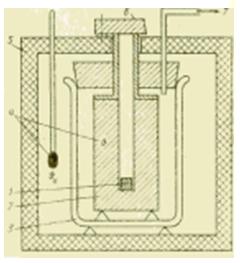
Attēls Metāla kalorimetra konstrukcijas diagramma.
Ja nepieciešams veikt kalorimetriskos pētījumus plašākā temperatūras diapazonā, tad šķidrie kalorimetri vairs nav piemēroti. Piemērotos kalorimetros ar metāla korpusu pārnesto siltuma daudzumu uztver metāla bloks (sudrabs, varš, alumīnijs), kas parasti atrodas apkārtējās vides temperatūrā. Šis kalorimetrs galvenokārt paredzēts šķidru un cietu vielu īpatnējās siltumietilpības c, J/(kg*K) noteikšanai.
Paraugu vispirms atdzesē ārpus kalorimetra saldēšanas iekārta vai uzkarsē cepeškrāsnī un pēc līdzsvara stāvokļa sasniegšanas nolaiž (iemet) metāla bloka atverē. Pamatojoties uz darbības metodi, šādu ierīci sauc par brīvā kritiena kalorimetru, un, pamatojoties uz tajā esošo termodinamisko procesu raksturu, to dažreiz sauc par nobīdes kalorimetru.
Siltuma daudzums, kas tiek nodots šādas sajaukšanas laikā no parauga (ar parametriem m1, c1, ) uz metāla bloku (m2, c2, ) rada izmērāmas bloka temperatūras izmaiņas. Tas ļauj noteikt parauga parasti nezināmo īpatnējo siltuma jaudu ideāli apstākļi(ja nav siltuma apmaiņas ar vidi) no izteiksmes:
Pats metāla bloks atrodas evakuētā Djūāra kolbā un dažreiz arī šķidruma vannā. Pēdējā gadījumā, lai iegūtu kalorimetra Ck siltumietilpību, metāla bloka C2 siltumietilpībai jāpievieno vannas siltumietilpība Cw:
CK=C2+CW=c2m2+cWmW .
KALORIMETRISKĀS MĒRĪŠANAS METODES
Visbiežāk kalorimetri tiek izmantoti nemainīgu vides apstākļu režīmā. Tas galvenokārt attiecas uz lielāko daļu degšanas kalorimetru, kuros reakcijas laiks ir ļoti īss. Kamēr reakcijas rezultātā mainās kalorimetra iekšējo daļu temperatūra, apkārtējā temperatūra paliek nemainīga. Daudzos gadījumos kā termostata vanna tiek izmantota. vidi, lai izvairītos no ietekmes uz ārējo traucējumu izmērīto vērtību - temperatūras svārstībām telpā, starojumu, caurvējiem utt.
Šīs mērīšanas shēmas priekšrocība ir salīdzinoši zemās aprīkojuma izmaksas, ar kurām var veikt lielāko daļu kalorimetrisko mērījumu. Par galveno trūkumu jāuzskata kalorimetra siltuma apmaiņa ar vidi, kas apgrūtina rezultātu interpretāciju. Šo mērīšanas metodi vienmēr sauc par izoperibolu (diatermisko). Jebkurā gadījumā to nevar saukt par izotermisku, kura būtība ir tāda, ka reakcijas laikā kalorimetra temperatūra paliek nemainīga, piemēram, kalorimetri, kas paredzēti fāzu pārvērtību mērīšanai.
Adiabātiskā metode
Ja ir iespējams novērst siltuma apmaiņu ar vidi, t.i., nodrošināt procesa adiabātisko gaitu, tad eksperimenta veikšana un rezultātu interpretācija tiek vienkāršota, un mērījumu rezultāts ir precīzāks, jo nav nepieciešams nepārtraukti reģistrēt temperatūru izmaiņas un aprēķināt labojumus. Turklāt šajā gadījumā var pieļaut nedaudz lielāku temperatūras paaugstināšanos kalorimetriskā traukā; Ierīcēm, kas nav adiabātiskas, tas ir nepieņemami palielinātu siltuma zudumu dēļ.
Lai novērstu siltuma apmaiņu starp kalorimetrisko trauku un tā tuvāko vidi (parasti šķidruma vannu), vannas temperatūra pastāvīgi jāpielāgo atbilstoši temperatūras izmaiņām trauka iekšpusē. Izmantojot elektronisko regulatoru (monitoringa ķēdi), jūs varat pastāvīgi uzturēt starpību starp šīm temperatūrām gandrīz vienādu ar nulli. Tas palielina mērīšanas iekārtu izmaksas atkarībā no nepieciešamās mērījumu precizitātes.
Aprīkojuma elementiem jābūt ātri iedarbīgiem un ilgstoši stabiliem (ar minimālu dreifēšanu). Servo vadības cilpas mirušajai zonai jābūt diapazonā no ±10-3 līdz ±10-5 K. Kā mērierīces var izmantot jebkurus zemas inerces elektriskos kontakttermometrus, kas, pieslēgti pie tilta ķēdes, dod impulss regulatoram, lai mainītu apkures jaudu. Sildīšanu veic vai nu izmantojot elektriskās pretestības spoli, vai tieši šķidruma vannā, kas, pateicoties vājai disociācijai, darbojas kā sildīšanas pretestība (tā sauktā elektrolītiskā sildīšana). Šī otrā metode ir praktiski bez inerces. Rezultātu var iegūt, izmantojot esošos elektriskās temperatūras mērīšanas līdzekļus vai izmantojot papildus uzstādītu šķidruma termometru (Beckman).
Adiabātiskā mērīšanas metode ir piemērota, lai pētītu galvenokārt lēnus procesus, kas saistīti ar termisko ietekmi. Strauji mainoties siltuma daudzumam (degšanas kalorimetros), temperatūras izlīdzināšanas inercei ir tik nelabvēlīga ietekme, ka netiek sasniegta pat parasto neadiabātisko metožu precizitāte. Taču, nodrošinot zemu sildelementu un temperatūras sensoru siltumietilpību un intensīvi maisot vannas šķidrumu, iespējams iegūt nelielas dažādu laika konstantu vērtības (samazināt inerci).
Kompensācijas metode
Izmantojot diferenciālos vai duālos kalorimetrus, kas balstīti uz kompensācijas principu, ir iespējams būtiski novērst ārējās ietekmes uz mērīšanas procesu. Divi identiski kalorimetrijas trauki ar identiskām palīgierīcēm tiek novietoti vidē ar vienādiem apstākļiem. Vienā traukā pētāmais process notiek ar termisko efektu, bet otrs trauks, izmantojot izsekošanas kontroles sistēmu, tiek uzkarsēts tā, lai siltuma zudumi apkārtējai videi abiem traukiem būtu vienādi. Tāpēc piegādāto apkures jaudu var tieši atkarīgi no pētāmā procesa laikā izdalītā siltuma daudzuma. Šajā gadījumā eksperimentālā mērīšanas uzdevums tiek pārvietots uz citu apgabalu un tiek samazināts līdz ļoti precīzai piegādātās elektriskās sildīšanas jaudas (W*s, J) noteikšanai:
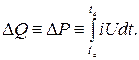
Diferenciālais kalorimetrs tiek izmantots īpaši adiabātiskajos vides apstākļos, it īpaši, ja ir sagaidāmas ļoti nelielas vai ļoti lēnas siltuma daudzuma izmaiņas. Endotermiskajiem procesiem pietiek ar vienu kalorimetrisko trauku. Siltuma padeve tiek kontrolēta tā, lai temperatūra traukā visu laiku paliktu nemainīga (izotermiskā metode). Diferenciālo kalorimetru trūkums ir augstās aprīkojuma un mērīšanas tehnoloģijas izmaksas.
DEDEGŠANAS KALORIMETRI
Termoelektrostacijās izmantotā kurināmā tiek pārbaudīta, lai noteiktu tās siltumspēju H (J/kg). Šis rādītājs ir nepieciešams, lai noteiktu efektivitātes faktorus, pētītu efektivitāti un aprēķinātu patērēto enerģiju dažādās iekārtās, kā arī optimālai sadegšanas procesa kontrolei. Būtiskas degošu komponentu sastāva svārstības bieži vien liek pastāvīgi noteikt siltumspēju.
Kad viela ir pilnībā sadegusi, izdalās noteikts siltuma daudzums Q (sadegšanas siltums). Ja to sadala ar masu t (vai ar tilpumu normālos apstākļos Vn), iegūst (īpatnējo) sadegšanas siltumu:
Atkarībā no sadegšanas produktu stāvokļa izšķir divus sadegšanas siltuma veidus: augstāku H0 un zemāku H0, ko sauc arī par degšanas siltumu un siltumspēju. Nosakot zemāko degšanas siltumu Ne ūdens veidojās laikā ķīmiskās reakcijas, jābūt tvaika stāvoklī. Atšķirība starp abiem siltumiem H0 - Ni atbilst kondensētā ūdens iztvaikošanas siltumam (CO - kondensāta indekss) r, kas ir vienāds ar 2,441 MJ/kg.
Cietajam un šķidrajam kurināmajam iegūto ūdens daudzumu var noteikt, pamatojoties uz elementu analīzi, bet, sadedzinot gāzveida kurināmo, mērot kondensāta daudzumu.
Rūpnieciskajās krāsnīs sadegšanas produktu temperatūra vienmēr pārsniedz ūdens viršanas temperatūru. Tāpēc parasti interesē tikai zemākā Ni sildīšanas vērtība, jo nevar izmantot ūdens kondensācijas siltumu.
Degšanas kalorimetri cietām vielām un šķidrumiem
Ātriem sadegšanas procesiem ir izstrādāta īpaša šķidruma kalorimetra forma - tā sauktais Bertelo bumbas kalorimetrs (3. att.).
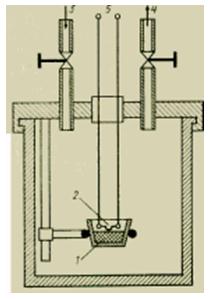
Zīmējums Kalorimetriskās bumbas dizains.
Neliela, precīzi izmērīta vielas daudzuma sadegšana notiek konstantā tilpumā noslēgtā bumbā iespējami tīrākā skābekļa atmosfērā ~30 atm (3 MPa) spiedienā. Piepildīto bumbu ievieto kalorimetra šķidruma vannā, kas absorbē izdalīto sadegšanas siltumu.
Cietās vielas parasti saspiež mazās briketēs (tabletēs) un ļoti precīzi nosver. Slikti degošas vielas vēlams sajaukt ar labi degošiem šķidrumiem ar zināmu siltumspēju (piemēram, benzoskābi). Šķidrās vielas ievieto krūzītēs (laiviņās), kas izgatavotas no platīna vai kvarca vai mazās plastmasas kapsulās. Uz vāka, kas ir pieskrūvēts pie bumbas korpusa, atrodas visas izpētei nepieciešamās ierīces: vārsti skābekļa padevei un sadegšanas produktu noņemšanai, paraugu turētāji un elektriskā aizdedze. Aizdedzi veic, piegādājot elektroenerģiju plānai platīna stieplei. Aizdedzināšanai piegādātais siltums ir precīzi jāmēra, lai to varētu ņemt vērā, interpretējot eksperimenta rezultātus. Bumbas kalorimetrā nosaka augstāko sadegšanas siltumu H0. Verifikācijas laikā kalorimetra C termisko ekvivalentu nosaka, sadedzinot standartvielu (piemēram, benzoskābi) vai izmantojot elektrisko sildīšanas ierīci.
Degšanas kalorimetrs gāzveida vielām
Gāzveida vides sadegšanas siltuma noteikšanai ir dažādas metodes. Visi tie, atšķirībā no bumbas kalorimetra cietām un šķidrām vielām, ir balstīti uz nepārtrauktu mērījumu. Izmantotais mērīšanas princips ir ļoti vienkāršs. Testa gāzi nepārtraukti sadedzina deglī pie nemainīga spiediena. Viss sadegšanas radītais siltums tiek absorbēts vai nu ar dzesēšanas šķidruma plūsmu siltummainī (slapjā vai siltuma apmaiņas kalorimetrs), vai arī sajaucot sadegšanas produktus ar gaisa plūsmu ar zināmu plūsmas ātrumu (sausais vai jaukšanas kalorimetrs). Parasti nosaka zemāko siltumspēju Нu. Lai noteiktu augstāku siltumspēju H0, nepieciešams kondensēt izplūdes gāzēs esošos ūdens tvaikus (CO indeksu). Zinot masas plūsmas ātrumus un temperatūras starpību kalorimetra ieejā (indekss e) un izejā (indekss a), ir iespējams aprēķināt atbilstošo sadegšanas siltumu, izmantojot siltuma bilances vienādojumu.
Nepieciešamā gāzes sagatavošana visos gāzes kalorimetros būtībā ir vienāda. Pirms sadegšanas gāzi (indekss G) vispirms attīra no cietajiem mehāniskajiem piemaisījumiem (filtrā) un samitrina (līdz piesātināšanai ar mitrumu, 100%), un pēc tam noregulē līdz norādītajām sākotnējā spiediena vērtībām (izmantojot spiediena samazināšanas vārstu ) un dzesēšanas līdzekļa temperatūra (indekss K) . Degšanai nepieciešamais gaiss (indekss L) arī tiek mitrināts un sasildīts līdz dzesēšanas vides temperatūrai.
Atkarībā no nepieciešamās precizitātes un mērīšanas iekārtas pieņemamām izmaksām daži no šiem nosacījumiem var nebūt izpildīti. Kalorimetri jātestē ar standartgāzi (piemēram, ūdeņradi), lai noteiktu novirzi no kalorimetra ideālā stāvokļa vienādojuma. Siltuma apmaiņas (mitrā) kalorimetram minētajam vienādojumam ir forma
kur un ir dzesēšanas līdzekļa un degvielas masas plūsmas ātrumi, kg/s; ск - dzesēšanas līdzekļa īpatnējā siltumietilpība, J/(kg*K); - dzesēšanas vides temperatūras paaugstināšanās, K.
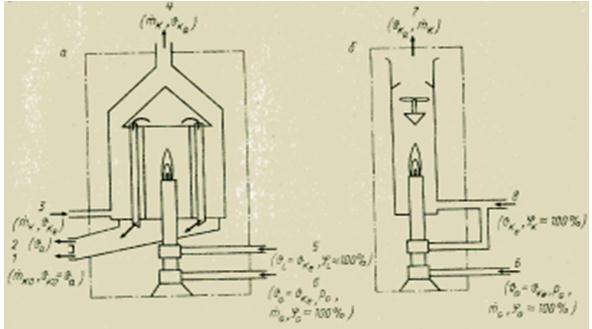
Attēls Slapjo (a) un sauso (b) kalorimetru konstrukcija gāzveida degvielai.
Temperatūras paaugstināšanās parasti ir 5-15 K. Lielās termiskās masas dēļ siltuma apmaiņas kalorimetriem ir ļoti ilga laika konstante, kas var sasniegt vairākas minūtes. Tāpēc tie ir mazāk ērti lietošanai slēgtā vadības cilpā kā sensors nekā sausie (jaukšanas) kalorimetri, kuru laika konstante ir tikai dažas sekundes. Bet siltuma apmaiņas kalorimetru sasniedzamā precizitāte ir salīdzinoši augsta. To kļūda nepārsniedz ±0,25-1%, tāpēc tos var izmantot arī laboratorijas darbiem un verifikācijai. Sausajiem kalorimetriem (sajaukšanas) kļūda ir ±1 līdz ±2% no mērījumu diapazona augšējās robežas.
Dažādu ražotāju kalorimetru konstrukcijas galvenokārt atšķiras ar palīgierīcēm un drošības ierīcēm, jutīgiem elementiem un skaitļošanas shēmām, kas nodrošina kļūdu kompensāciju. Tādējādi siltuma apmaiņas kalorimetros dažādos veidos tiek uzturēta nemainīga gāzes un dzesēšanas līdzekļa plūsmas ātruma attiecība (sk. iepriekš doto kalorimetra vienādojumu), kā rezultātā augstākā siltumspēja H0 tieši atkarīga tikai no temperatūras pieauguma.
Sausajos kalorimetros temperatūras paaugstināšanos mēra vai nu tieši, izmantojot elektriskos kontakttermometrus, vai netieši, izmantojot dilatometrisko sensoru - izplešanās cauruli, kas atrodas dūmgāzu plūsmā. ADOS kalorimetrā dilatometriskās caurules termiskais pagarinājums tieši atbilst sadegšanas siltumam, un to var pārveidot par jebkuru signālu, izmantojot sviras transmisiju un garuma mērītāju. Reinecke kalorimetrā stieņa pagarinājums tiek izmantots kā mērīšanas signāls vadības ķēdē, kas kontrolē dzesēšanas gaisa plūsmu tā, lai temperatūras pieaugums paliktu praktiski nemainīgs. Šajā gadījumā vadības cilpa izrādās tīri proporcionāla, taču tajā ir neizbēgama zināma atlikušā novirze. Šajā gadījumā dzesēšanas gaisa plūsmas ātrums vai dilatometriskās caurules (stieņa) pagarinājums ir noteiktās siltumspējas mērs. Nepieciešams priekšnoteikums pietiekamas precizitātes iegūšanai visos sausos kalorimetrijos ir laba dzesēšanas gaisa un sadegšanas produktu sajaukšana.
SILTUMA PLŪSMAS MĒRĪJUMI
Siltums kā enerģijas veids tiek pārnests trīs veidos: caur cietu ķermeni (siltuma vadītspēja), šķidru vai gāzveida vidi (konvekcija) un bez matērijas līdzdalības (starojums). Tehnoloģijā siltuma pārnese gandrīz vienmēr ietver visas trīs sastāvdaļas; tomēr daudzos gadījumos ir iespējams iegūt pieņemamas precizitātes rezultātus, mērot tikai vienu komponentu.
Mērīšana siltuma plūsma ar siltumvadītspēju
Siltuma pārnese caur siltumvadošām sienām ir svarīga daudzās tehnoloģiju jomās (visu veidu siltummaiņi, siltumizolācija utt.). Šajā gadījumā interesē ne tik daudz pašreizējā ražošanas vērtību uzraudzība, cik atsevišķu mērījumu rezultāti, ko izmanto, lai novērtētu slodzi, pārbaudītu garantēto rādītāju izpildi un efektivitāti.
Saskaņā ar stacionārās siltumvadītspējas likumiem siltuma plūsmu nosaka pēc šādām formulām (J/s):
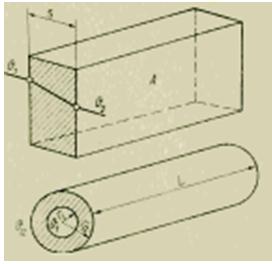
Tā kā sienas siltumvadītspējas koeficients [J/(m*s*K)] un tās ģeometriskie izmēri ir zināmi, siltuma plūsmas mērīšana tiek samazināta līdz temperatūras starpības mērīšanai. Tomēr šis paņēmiens prasa ļoti precīzu virsmas temperatūras noteikšanu. Kļūdas, kas saistītas ar siltuma pārneses apstākļu izmaiņām, uzstādot uz virsmām temperatūras jutīgus elementus, var būt diezgan lielas. Tāpēc precīzākiem mērījumiem ir ieteicamas tālāk norādītās metodes, kas vienlaikus izmanto gan siltumvadītspēju, gan siltuma pārnesi.
Siltuma plūsmu mērīšana siltuma pārneses laikā (siltuma pārnese apvienojumā ar siltumvadītspēju)
Iepriekšējā sadaļā minētajai plakanajai sienai ir spēkā šāds siltuma pārneses likums (J/s):
![]() ,
,
kur siltuma pārneses koeficientā k 1J/(m2*s*K)], kopā ar siltumvadītspējas koeficientu [J/Dm*s*K)], siltuma pārneses koeficienti un [J/(m2*s*K) ] no abām sienas pusēm.
Uz plakanas sienas, caur kuru iziet izmērītā siltuma plūsma, tiek uzlikta neliela plāna plāksne, kuras virsmas temperatūru nosaka ar iebūvētiem plānslāņa termopāriem. Šādas mērīšanas priekšrocība ir tāda, ka nav nepieciešams zināt sienas siltuma īpašības, un atbilstošās plāksnes īpašības kalibrēšanas laikā var samazināt līdz vienai nemainīgai vērtībai. Šādu jutīgu elementu izmērs ir aptuveni 30x30x0,5 mm; mērījumu diapazons aptver siltuma plūsmas no 10 līdz 100 000 W/m2; kļūda ir 2-5%.
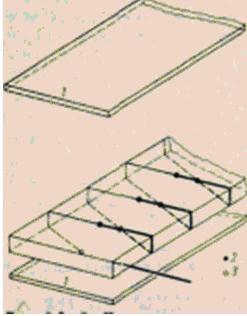
Attēls Siltuma plūsmas mērītāja darbības princips.
Uzlabojot šo mērīšanas metodi, uzklātās plāksnes vietā tiek izmantoti gumijas paklājiņi. Līmējot tos uz nelīdzenām virsmām vai aptinot ap izliektu virsmu, iespējams noteikt siltuma pārnesi no relatīvi lielas virsmas, piemēram, no caurules, trauka u.c. Termopāri ir iebūvēti abās virsmās. paklāju tā, lai to karstā un aukstā savienojuma vietas atrastos tieši viens pret otru (6. att.). Un šajā gadījumā siltuma plūsmas blīvums saskaņā ar kalibrēšanu ir proporcionāls temperatūras starpībai. Tomēr uzklātie paklāji nedaudz traucē sākotnējo siltuma pārnesi, kas kļūst pamanāma ar precīziem mērījumiem. Tāpēc šī mērīšanas metode galvenokārt tiek izmantota vielas termodinamisko konstantu noteikšanai, kad siltuma plūsmas traucējumi neietekmē mērījuma rezultātu.
Siltuma plūsmu mērīšana plūstošajā vidē.
Ievērojamu siltumenerģijas daļu pārnes šķidrās vai gāzveida vielas (ūdens, tvaiks u.c.), kas pārvietojas slēgtā cauruļvadu tīklā. Tomēr, salīdzinot ar elektriskās enerģijas pārvadi pa vadiem, attālums, kādā siltumenerģiju var pārraidīt, ir ierobežots. Visu veidu apkures un saldēšanas sistēmu siltumtehnikas pētījumiem nepieciešams veikt siltuma ražošanas un patēriņa mērījumus.
Siltuma plūsma F (J/s), straumēts dzesēšanas šķidruma (kg/s) caur vadības sekciju ar laukumu A (m2) noteiktā zonā, kurai tiek apkopots siltuma bilance (procesa zonā, 7. att.) ir vienāds ar
Siltuma daudzumu, kas dots laika intervālā t2 - t1, nosaka kā integrāli (J):
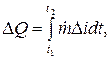
kur ir dzesēšanas šķidruma siltuma satura (entalpija, J/kg) starpība pie ieplūdes (indekss e) un pie izejas (indekss a) siltuma bilances zonā.
Tā kā entalpija parasti ir svarīga tikai saistībā ar noteiktu līmeni, piemēram, entalpiju apkārtējās vides temperatūrā, visi siltuma plūsmas mērījumi būtībā ir atšķirības mērījumi.
Atsevišķās entalpijas, kas iekļautas vispārējā vienādojumā, var izteikt ar atbilstošām temperatūrām un īpatnējām siltumietilpībām;
Tādējādi siltuma plūsmas mērīšana tiek tieši samazināta līdz temperatūras un masas plūsmas ātruma mērīšanai. Daudzos gadījumos mēra nevis masas plūsmas ātrumu, bet gan dzesēšanas šķidruma tilpuma plūsmas ātrumu; šajā gadījumā iegūtais rezultāts atšķirsies tikai ar dzesēšanas šķidruma blīvuma vērtību p. Īpatnējās siltuma jaudas ci pašas ir temperatūras funkcijas. Tomēr daudzu instrumentu šaurā mērījumu diapazona dēļ tos parasti var uzskatīt par nemainīgām vērtībām, nezaudējot precizitāti. Ir jāzina īpatnējā siltumietilpība. Šķidrumiem siltuma plūsmas vienādojums ir vēl vairāk vienkāršots, jo tie īpatnējās siltuma jaudas nav atkarīgi no spiediena:
![]() , J/s.
, J/s.
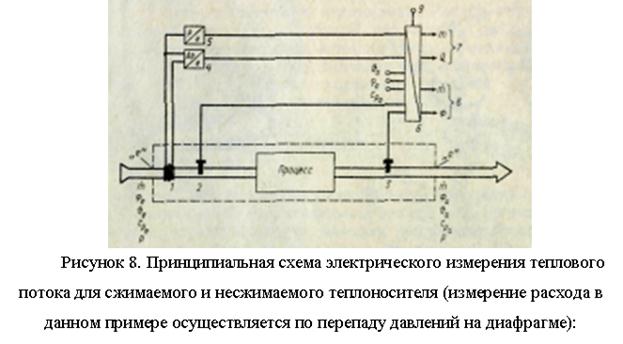
Visos šāda veida vienādojumos ir jāņem vērā lielumu pazīmes atkarībā no tā, vai siltums tiek piegādāts vai noņemts, vai process ir endotermisks vai eksotermisks, vai notiek dzesēšana vai karsēšana.
