燃料、ガス混合物および熱容量
熱機関(機械)では、作動油はさまざまなガスの混合物です。 混合物の成分が入らない場合 化学反応それらの間で、各成分がクライペロンの状態方程式に従う場合、そのような混合物は理想気体と見なされます。
混合物を計算するには、μcm(平均モル質量)とR cm(混合物の比気体定数)を決定する必要があります。 それらを決定するには、混合物の組成、つまり、この混合物を形成する成分と量、混合物に含まれる各成分が持つパラメーターを知る必要があります。
混合物の各成分は、混合物に他のガスがないかのように動作し、混合物が配置されている利用可能なボリューム全体を占め、独自の状態方程式に従い、壁にいわゆる分圧を加えます。混合物のすべての成分のは同じであり、混合物の温度に等しい。
ドルトンの法則によれば、混合物Pの圧力は、混合物に含まれる個々の成分の分圧の合計に等しくなります。
ここで、nは混合成分の数です。
アマグの法則によれば、混合物の体積Vは、混合物の温度と圧力での混合物に含まれる個々の成分の部分体積の合計に等しくなります。
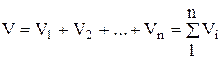 , (1.21)
, (1.21)
ここで-部分体積、m 3; 混合物のV-体積、m 3
混合物の組成は、体積(モル)または質量分率で示されます。
i番目の成分の体積分率は、混合物の体積に対する成分の部分体積の比率です。つまり、混合物の成分の体積分率の合計は1です。 値が%で指定されている場合、それらの合計= 100%です。
i番目の成分のモル分率niは、成分N iのキロモル数と混合物Nのキロモル数の比率です。つまり、ここで、 ![]() 、、すなわち、各成分および混合物全体のキロモル数は、対応する成分および混合物全体の、1キロモルが占める体積に対する比率に等しい。
、、すなわち、各成分および混合物全体のキロモル数は、対応する成分および混合物全体の、1キロモルが占める体積に対する比率に等しい。
同じ条件下の理想気体が同じ体積のキロモルを持っていることを考えると、置換後、次のようになります。 理想気体モル分数と体積分率は数値的に等しい。
i番目の成分の質量分率は、混合物の質量に対する成分の質量の比率です。したがって、混合物の質量は、成分の質量の合計に等しく、成分の質量分率の合計も等しくなります。 1(または100%)に。
体積分率から質量分率への変換、およびその逆の変換は、次の比率に基づいています。
![]() ,
,
ここで、ρ=μ/ 22.4、kg /m3です。
したがって、i番目の成分の質量分率は次の関係から決定されます。
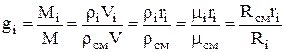 ,
,
ここで、は混合物の密度、kg / m 3は、i番目の成分の体積分率です。
将来的には、体積分率で決定できるようになります。
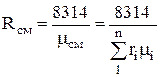 .
.
密度体積分率の混合物は、比率から決定されます
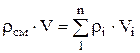 、 どこ
、 どこ 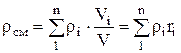 , (1.22)
, (1.22)
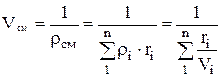 .
.
分圧は次の式で決定されます。
![]() また
また 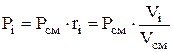 (1.23)
(1.23)
コンポーネントと混合物の状態方程式は、全体として次の形式になります。
![]() ;
;
![]() ,
,
ここで、変換後、次のように取得します。 大規模株式
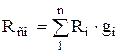 ,
, 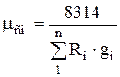 . (1.24)
. (1.24)
の混合物の密度と比容積 大規模シェア:
; 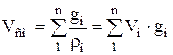 . (1.25)
. (1.25)
分圧を計算するには、次の式を使用します。
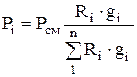 . (1.26)
. (1.26)
質量分率から体積分率への変換は、次の式に従って実行されます。
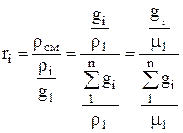 .
.
ガスの混合物の熱容量を決定するとき、ガス混合物を加熱(冷却)するために、混合物の各成分を加熱(冷却)する必要があると想定される。
ここで、Q i = M i c i ∆tは、混合物のi番目の成分の温度を変化させるために費やされる熱です。ciは、混合物のi番目の成分の質量熱容量です。
混合物の熱容量は、比率から決定されます(混合物が質量分率で与えられる場合)
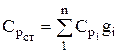 、同様に
、同様に 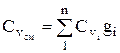 . (1.28)
. (1.28)
体積分率で与えられる混合物のモルおよび体積熱容量は、次の式で決定されます。
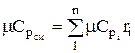 ;
; 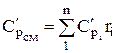 ;
;
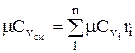 ;
; 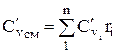
例1.5乾燥空気の質量は、g O2 \ u003d 23.3%の酸素とg N 2 \ u003d 76.6%の窒素で構成されています。 体積による空気の組成(rO2とrN 2)と混合物の気体定数を決定します。
解決.
1.表1から、kg/kmolとkg/kmolがわかります。
2.酸素と窒素の体積分率を決定します。
1.空気(混合物)のガス定数は、次の式で決定されます。
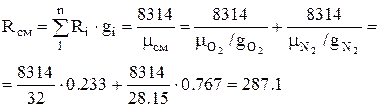 、J / kg K
、J / kg K
例1.6。 温度がt1=900°Cからt2= 1200に変化したときに、質量がM =2kgのガス混合物をP=constで加熱するのに必要な熱量を決定します。これは重量%で構成されます。 °C。
解決:
1. P=constおよびt1= 900 o C(P2から)でのガス混合物を構成するコンポーネントの平均質量熱容量を決定します。
1.0258 kJ / kg K; = 1.1045 kJ / kg K;
1.1078 kJ / kg K; = 2.1097 kJ / kg K;
2. P=constおよびt1= 1200 o C(P2から)でのガス混合物を構成するコンポーネントの平均質量熱容量を決定します。
1.0509 kJ / kg K; = 1.153 kJ / kg K;
1.1359 kJ / kg K; = 2.2106 kJ / kg K;
3.温度範囲の混合物の平均質量熱容量を決定します:t 2 \u003d1200°Cおよびt1\ u003d 900°C:
4. P =constで混合物2kgを加熱するための熱量:
熱力学の第一法則システムの内部エネルギーの変化と、作動流体への熱供給の結果として環境の外圧の力に対して実行される機械的仕事との間に定量的な関係を確立します。
閉じた熱力学系の場合、第1法則の方程式は次の形式になります。
作動油(またはシステム)に与えられた熱は、体温の上昇によって内部エネルギー(dU)を増加させ、作動油の膨張とその増加によって外部仕事(dL)を実行するために使用されます。音量。
最初の法則は、dH = dq + VdP =dq-dL0と書くことができます。
ここで、dL 0 \ u003d VdP-圧力変化の基本的な作業は、有用な外部(技術的)作業と呼ばれます。
dUは、作動油(システム)の内部エネルギーの変化であり、分子の熱運動(並進、回転、振動)のエネルギーと分子の相互作用の位置エネルギーが含まれます。
ある状態から別の状態へのシステムの遷移は熱供給の結果として発生するため、作動油は加熱され、その温度はdTだけ上昇し、体積はdVだけ増加します。
体温の上昇はその粒子の運動エネルギーの増加を引き起こし、体の体積の増加は粒子の位置エネルギーの変化につながります。 その結果、物体の内部エネルギーはdUだけ増加するため、内部エネルギーUは物体の状態の関数であり、2つの独立したパラメーターU = f 1(P、V)の関数として表すことができます。 U = f 2(P、T)、U = f 3(υ、T)。 熱力学的プロセスにおける内部エネルギーの変化は、初期(U 1)状態と最終(U 2)状態によってのみ決定されます。
微分形式では、内部エネルギーの変化が書かれています
a)比容積と温度の関数として
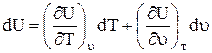
b)温度の関数として、 、 それから
温度によるCvの変化を考慮する必要がある実際の計算では、実験式と特定の内部エネルギー(多くの場合モル)の表があります。 理想気体の場合、混合物のモル内部エネルギーUmは次の式で決定されます。
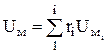 、J / kmol
、J / kmol
質量分率で与えられる混合物の場合。 この上 内部エネルギーがある システムのプロパティとシステムの状態を特徴づける.
エンタルピー Kamerling-Onnesによって導入された熱状態関数です(勝者 ノーベル賞、1913)、これはシステムUの内部エネルギーと、システムPの圧力とその体積Vの積の合計です。
それに含まれる量は状態関数であるため、Hも状態関数です。つまりH \ u003d f 1(P、V); H = f 2(V、T); H = f 3(P、T)。
熱力学的プロセスにおけるエンタルピーdHの変化は、初期のH1と最終のH2の状態によって決定され、プロセスの性質には依存しません。 システムに1kgの物質が含まれている場合、特定のエンタルピーJ/kgが適用されます。
理想気体の場合、微分方程式は次の形式になります。
したがって、特定のエンタルピーは次の式で決定されます。
熱力学の第1法則の方程式は、dq = dU +Pdυであり、唯一のタイプの仕事が拡張仕事Pdυ= d(Pυ)-υdPである場合、dq = d(U +Pυ)-υdP、ここで
工学の実践では、均質なガスではなく、化学的に無関係なガスの混合物を扱わなければならないことがよくあります。 混合ガスの例としては、大気、天然ガス、燃料の燃焼生成物などがあります。
混合ガスの場合、以下の規定が有効です。
1.混合物に入る各ガスには、温度があります。 温度に等しい混合物。
2.混合物に含まれるガスはいずれも混合物の体積全体に分散しているため、各ガスの体積は混合物全体の体積に等しくなります。
3.混合物に含まれる各ガスは、独自の状態方程式に従います。
4.混合物は全体として新しいガスのようであり、独自の状態方程式に従います。
ガス混合物の研究は、一定の温度で、混合物の圧力が混合物に含まれるガスの分圧の合計に等しいというドルトンの法則に基づいています。
ここで、pcmは混合物の圧力です。
pi-混合物に含まれるi番目のガスの分圧。
nは混合物に含まれるガスの数です。
分圧は、混合物に入るガスが、同じ温度で混合物の全体積を単独で占める場合にかかる圧力です。
混合ガスの設定方法
ガス混合物の組成は、質量、体積、モル分率で指定できます。
質量分率。 混合物に含まれるガスの質量分率は、混合物の質量に対するこのガスの質量の比率です。
m 1 \ u003d M 1 / M cm; m 2 \ u003d M 2 / M cm; ..........; m n \ u003d M n / M cm、
ここで、m 1、m 2、...、mn- 質量分率ガス;
M 1、M 2、...、Mn-個々のガスの質量;
Mcmは混合物の質量です。
それは簡単にわかります 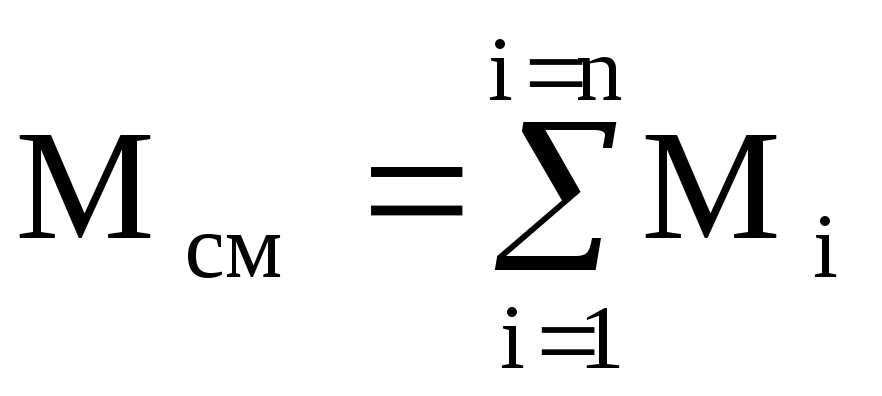 と
と 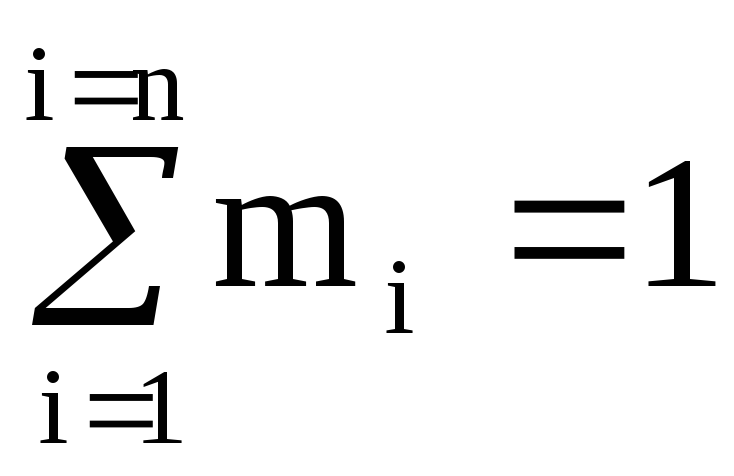 (100%).
(100%).
ボリュームシェア。混合物に含まれるガスの体積分率は、混合物の体積に対するこのガスの減少した(部分的な)体積の比率です。
r 1 \ u003d V 1 / V cm; r 2 \ u003d V 2 / V cm; .........、r n = V n / V cm;
ここで、V 1、V 2、...、Vn-ガスの量を減らします。
Vcmは混合物の体積です。
r 1、r 2、...、rn-ガスの体積分率。
減少した体積は、混合物の条件下(混合物の温度と圧力で)のガスの体積です。
減少した体積は次のように表すことができます。1つを除くすべてのガスが混合物を含む容器から除去され、残りのガスが温度を維持しながら混合物の圧力に圧縮されると、その体積は減少または部分的になります。
混合物の体積は、減少したガスの体積の合計に等しくなることが証明できます。
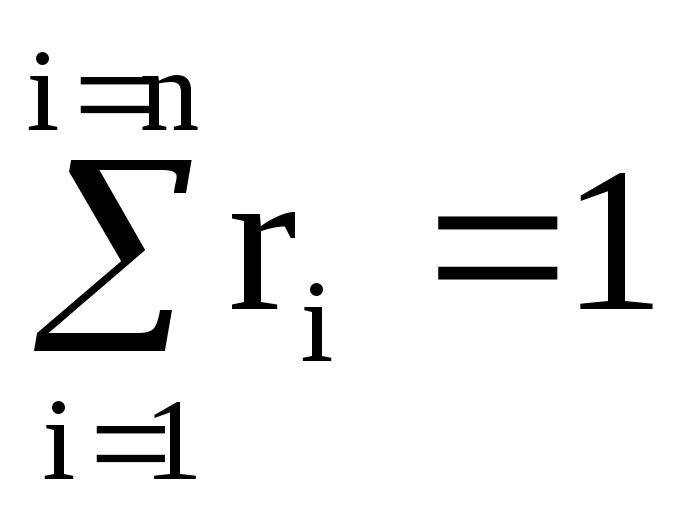 (100%).
(100%).
モル分率。混合物に含まれるガスのモル分率は、混合物のキロモル数に対するこのガスのキロモル数の比率です。
r 1 \ u003d n 1 / n cm; r 2 \ u003d n 2 / n cm; .........、r n \ u003d n n / n cm、
ここで、r 1、r 2、...、rn-ガスのモル分率。
n cmは、混合物のキロモル数です。
n 1、n 2、...、nnはガスのキロモル数です。
モル分率で混合物を指定することは、体積分率で混合物を指定することと同じです。 モルと体積分率は、混合物に含まれる各ガスに対して同じ数値を持っています。
混合物のガス定数と見かけの(平均)分子量。質量分率で与えられるガス混合定数を計算するために、状態方程式を記述します。
混合用
pcm×Vcm= M cm R cm T; (1.9)
ガス用
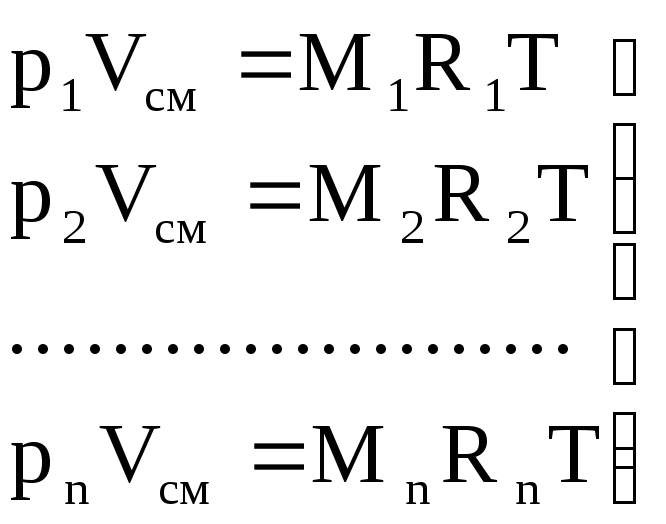 .
(1.10)
.
(1.10)
方程式の左と右の部分を合計します(1.10)
(p 1 + p 2 + .... + p n)V cm =(M 1 R 1 + M 2 R 2 + ..... + M n R n)T。
なぜなら 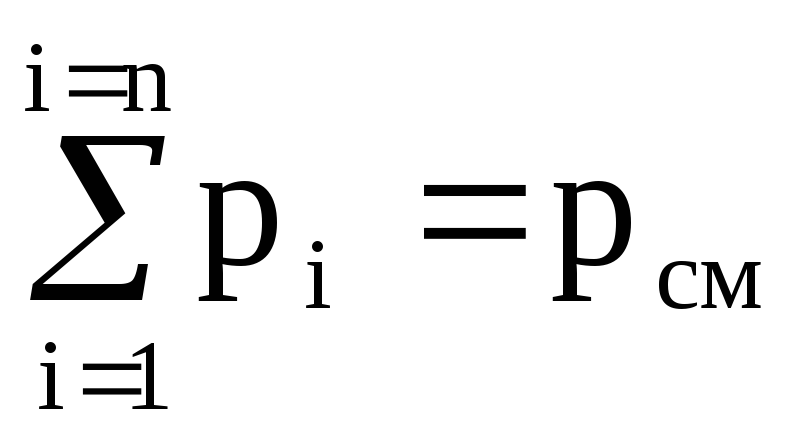 ,
,
次にpcmV cm =(M 1 R 1 + M 2 R 2 + ..... + M n R n)T.(1.11)
式(1.9)および(1.11)は、次のことを意味します。
M cm R cm T \ u003d(M 1 R 1 + M 2 R 2 + ..... + M n R n)T。
R cm \ u003d M 1 / M cm R 1 + M 2 / M cm R 2 + ...... + M n / M cm R n \ u003d
M 1 R 1 + m 2 R 2 + ...... + m n R n
また 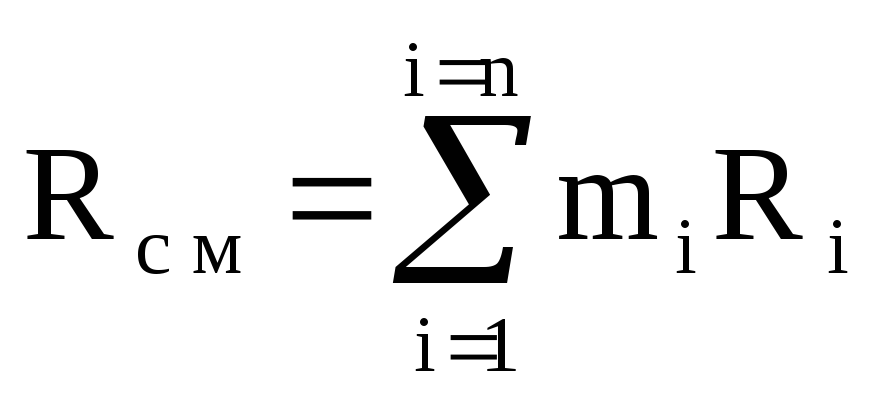 ,
(1.12)
,
(1.12)
ここで、Rcmは混合物の気体定数です。
i番目のガスの気体定数から
R i = 8314 / m i、
次に、式(1.12)は次のように書き直されます。
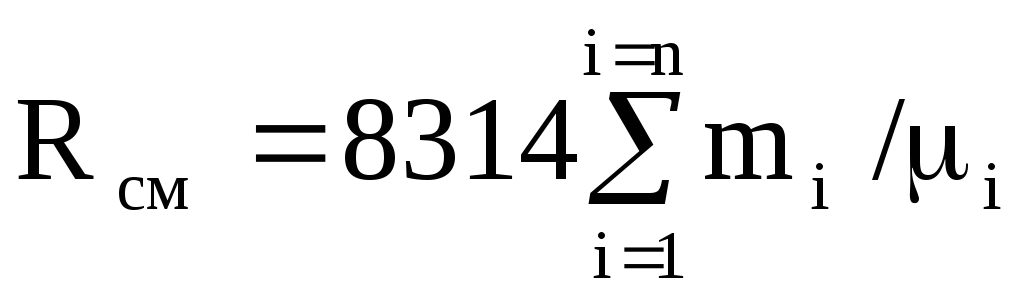 .
(1.13)
.
(1.13)
ガス混合物のパラメータを決定するときは、ガス混合物の見かけの(平均)分子量と呼ばれる特定の条件値を使用すると便利です。 混合物の見かけの分子量の概念により、従来、混合物を均質なガスと見なすことができ、計算が大幅に簡素化されます。
別のガスの場合、式
類推すると、混合物の場合、次のように書くことができます
m cm R cm = 8314、(1.14)
ここで、mcmは混合物の見かけの分子量です。
式(1.14)から、式(1.12)と(1.13)を使用して、次のようになります。
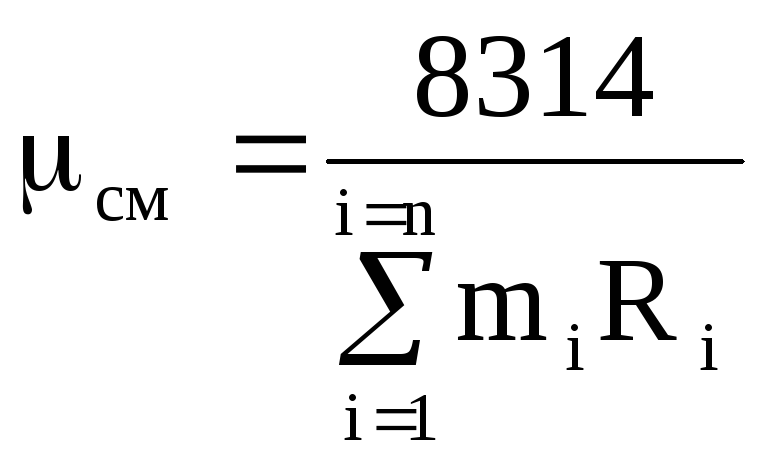 ,
(1.15)
,
(1.15)
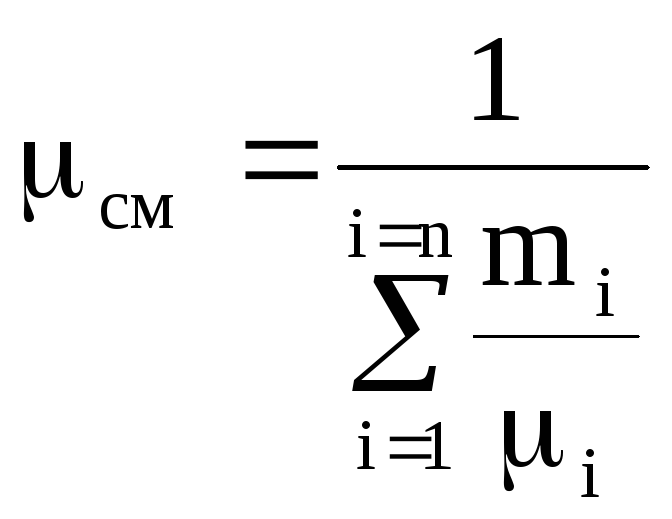 .
(1.16)
.
(1.16)
このように議論すると、体積分率からRcmとmcmを計算するための式、質量分率を体積分率に変換するための式、逆に、体積分率を質量分率に変換するための式、混合物の比体積ucmとを計算するための式を得ることができます。質量と体積の割合による混合密度rcm、そして最後に、体積と質量の割合による混合物に含まれるガスの分圧を計算するための式。 表には、これらの式を導出せずに示しています。
ガス混合物の計算式
|
混合物の組成を設定する |
ある構成から別の構成に転送する |
混合物の密度と比容積 |
混合物の見かけの分子量 |
ガス混合定数 |
分圧 |
|
質量分率 |
|
|
|
|
|
|
体積分率 |
|
|
|
|
|
ガスの熱容量
物体の熱容量は、物体を1 K加熱または冷却するために必要な熱量です。単位量の物質の熱容量は、比熱容量と呼ばれます。
したがって、物質の比熱容量は、このプロセスで温度を1 K変化させるために、報告するか、物質の単位から差し引く必要がある熱量です。
以下では比熱容量のみを考慮しているため、比熱容量を単に熱容量と呼びます。
ガスの量は、質量、体積、キロモル数で表すことができます。 ガス量を設定する場合、この量は通常の状態になり、通常の立方メートル(nm 3)で測定されることに注意してください。
ガスの量を設定する方法に応じて、次の熱容量が区別されます。
c-質量熱容量、J /(kg×K);
c¢-体積熱容量、J /(nm 3×K);
cm-モル熱容量、J /(kmol×K)。
これらの熱容量の間には、次の関係があります。
c = c m / m; withm=with×m;
с¢=сm/22.4; m = s¢×22.4の場合、
ここから 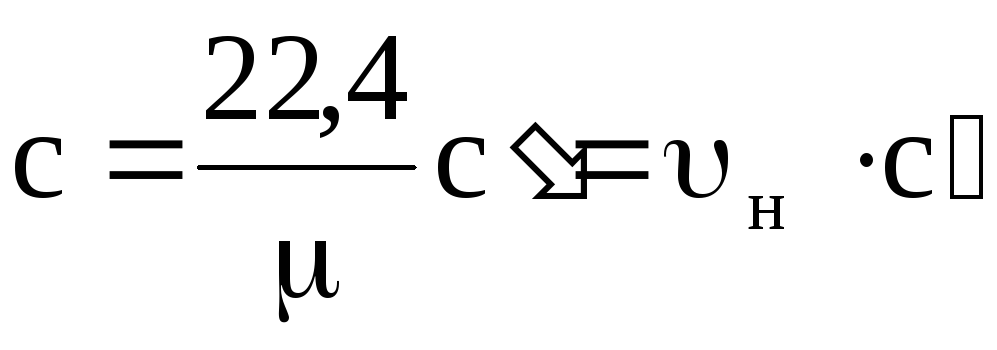 ; s¢=s×rn、
; s¢=s×rn、
ここで、unおよびrn-通常の条件下での比容積および密度。
等圧および等圧の熱容量
作動油に与えられる熱の量は、熱力学的プロセスの特徴に依存します。 熱力学的プロセスに応じて、2種類の熱容量が実用上重要です。等圧と等圧です。
u=constでの熱容量は等積です。
c u-質量定積熱容量、
c¢ uは体積定積熱容量であり、
cm uはモル定積熱容量です。
p=constでの熱容量は等圧です。
c p-質量等圧熱容量、
c¢р-体積等圧熱容量、
cmp-モル等圧熱容量。
p = constで実行されるプロセスで同じ温度変化がある場合、u=constで実行されるプロセスよりも多くの熱が消費されます。 これは、u = constでは、体に与えられる熱はその内部エネルギーの変化にのみ費やされ、p = constでは、熱は内部エネルギーの増加と膨張の仕事の実行の両方に費やされるという事実によって説明されます。 Mayer方程式による質量等圧熱容量と質量等圧熱容量の差
c p-c u=R。 (1.17)
式(1.17)の左辺と右辺にキロモル質量mを掛けると、次のようになります。
c m p-c m u= 8314 J /(kmol×K)(1.18)
熱力学とその応用では、等圧と等圧の熱容量の比率が非常に重要です。
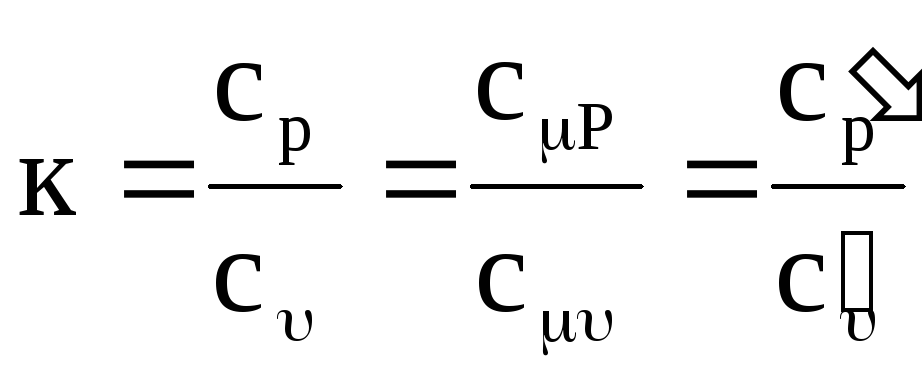 ,
(1.19)
,
(1.19)
ここで、kは断熱指数です。
計算によると、単原子ガスk»1.67、二原子ガスk»1.4、および三原子ガスk»1.29です。
値がわかりやすい に温度に依存します。 実際、式(1.17)と(1.19)から次のようになります。
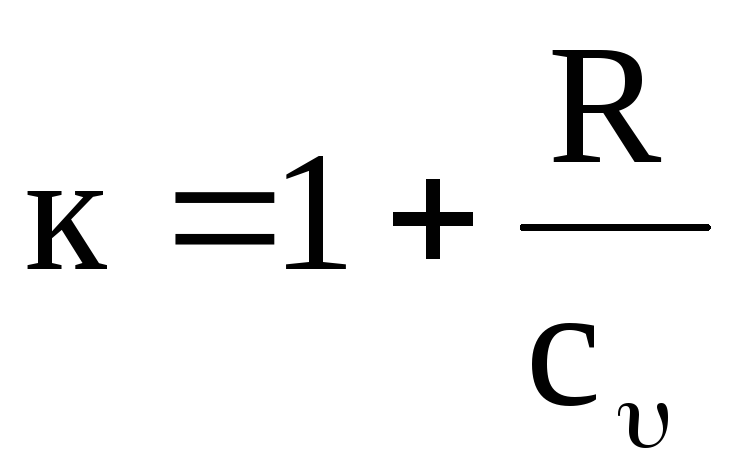 ,
(1.20)
,
(1.20)
および式(1.18)および(1.19)から
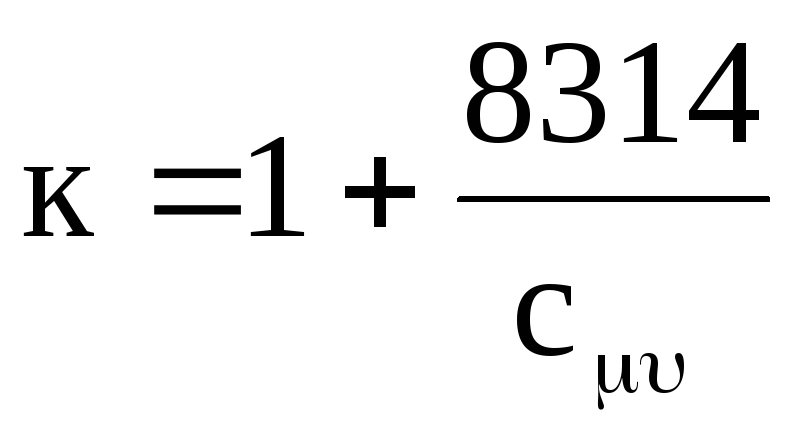 .
(1.21)
.
(1.21)
ガス温度の上昇に伴って熱容量が増加するため、kの値は減少し、1に近づきますが、常にそれよりも大きいままです。
kの値がわかれば、対応する熱容量の値を決定できます。 したがって、たとえば、式(1.20)から次のようになります。
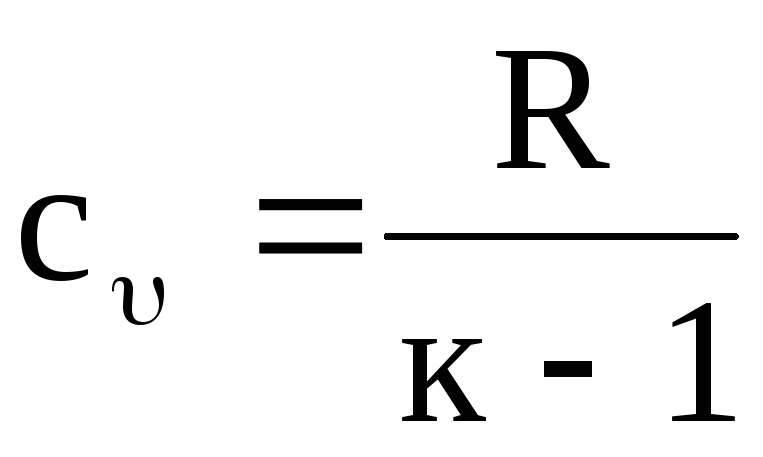 ,
(1.22)
,
(1.22)
それ以来 p=k×sの場合 u、それから私達は得る
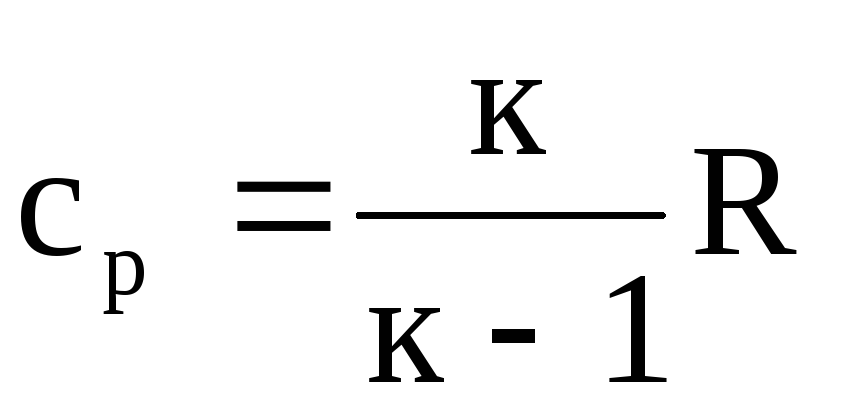 .
(1.23)
.
(1.23)
同様に、モル熱容量については、式(1.21)から次のようになります。
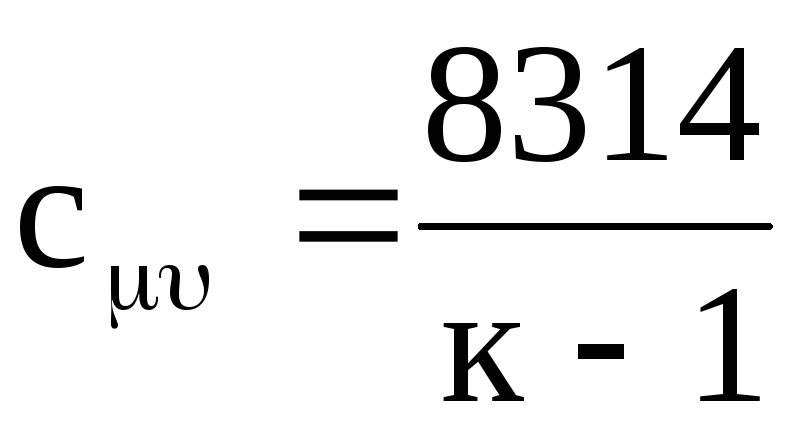 .
(1.24)
.
(1.24)
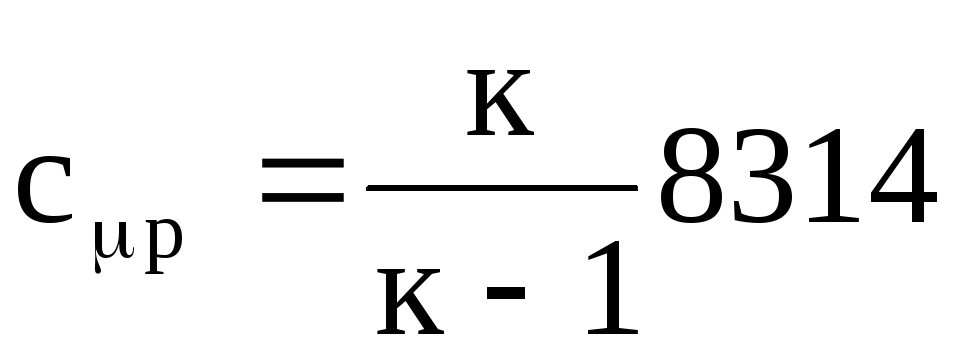 .
(1.25)
.
(1.25)
平均および真の熱容量
ガスの熱容量は、温度と、ある程度は圧力に依存します。 熱容量の圧力への依存性は小さく、ほとんどの計算では無視されます。 熱容量の温度依存性は重要であり、考慮に入れる必要があります。 この依存関係は、次の式で非常に正確に表されます。
c = a + の t + et 2、(1.26)
ここで、 のおよびeは、特定のガスに対して一定の値です。
多くの場合、熱工学の計算では、非線形依存性(1.26)は線形依存性に置き換えられます。
c = a + の t。 (1.27)
|
式(1.26)に従って熱容量の温度依存性をグラフで作成すると、これは曲線依存性になります(図1.4)。 図に示すように、各温度値には独自の熱容量値があり、これは一般に真の熱容量と呼ばれます。 数学的には、真の熱容量の式は次のように記述されます。
|
|
|
|
したがって、真の熱容量は、温度dtの微小変化に対する微小量の熱dqの比率です。 言い換えれば、真の熱容量は、特定の温度でのガスの熱容量です。 イチジクに 1.4では、温度t 1での真の熱容量はt1で示され、セグメント1-4として示され、温度t 2-でt2として示され、セグメント2-3として示されます。 式(1.28)から次のようになります dq=cdt。 (1.29) 実際の計算では、常に決定します 最終変更時の熱量 |
温度。 物質がt1からt2に加熱されたときに単位量に報告される熱量qは、(1.29)をt1からt2に積分することによって求めることができることは明らかです。
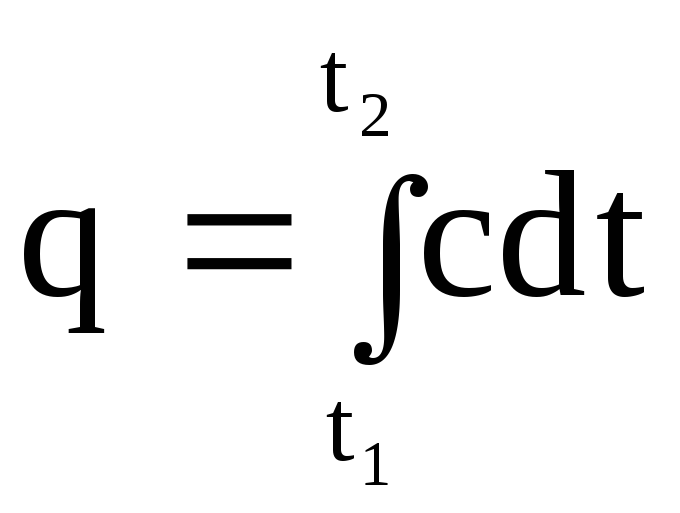 .
(1.30)
.
(1.30)
グラフィカルに、積分(1.30)は領域4-1-2-3で表されます。 式(1.30)で、線形依存性(1.27)に従って真の熱容量の値を代入すると、次のようになります。
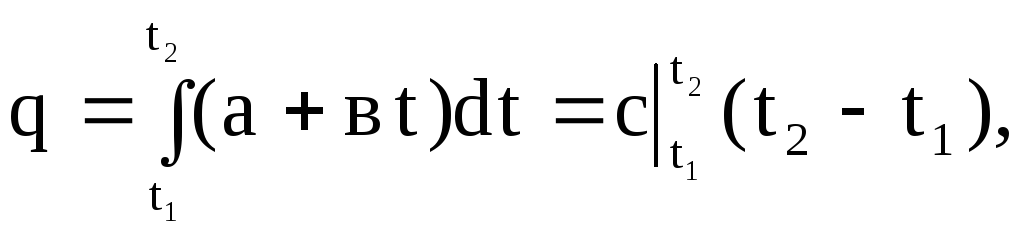 (1.31)
(1.31)
どこ 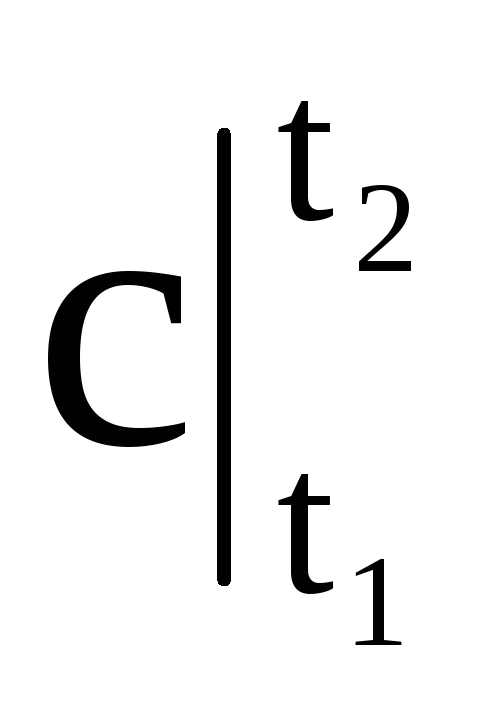 -t1からt2までの温度範囲での平均熱容量。
-t1からt2までの温度範囲での平均熱容量。
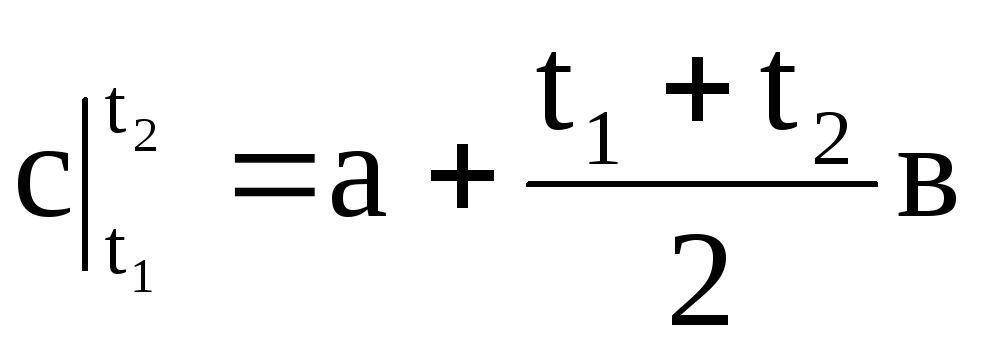 ,
(1.32)
,
(1.32)
したがって、平均熱容量は、最終的な熱量qと最終的な温度変化の比率t 2-t 1:です。
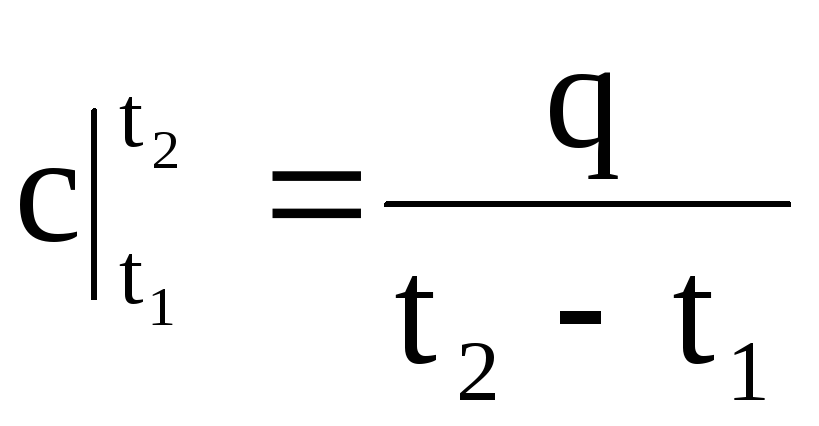 .
(1.33)
.
(1.33)
4-3(図1.4)に基づいて、図4-1-2-3と同じサイズの長方形4-1¢-2¢-3を作成すると、この長方形の高さは次のようになります。平均熱容量に等しくなります。ここで 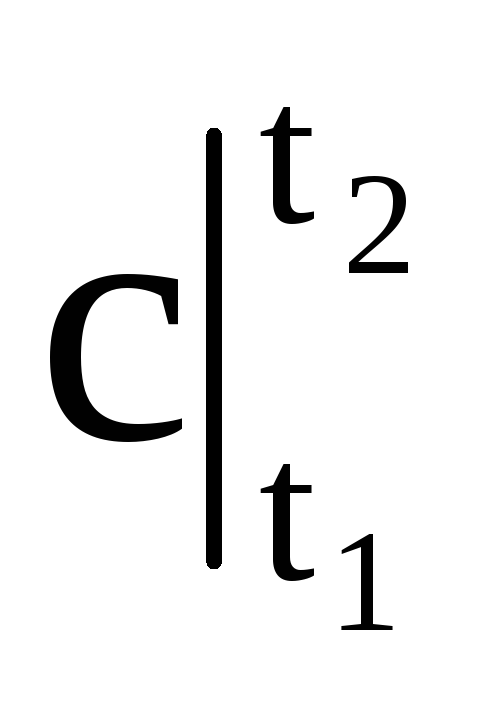 は温度範囲t1〜t2にあります。
は温度範囲t1〜t2にあります。
通常、平均熱容量の値は、物質の熱力学的特性の表に示されています。 ただし、これらのテーブルのボリュームを減らすために、0°Cからt°Cの温度範囲で決定された平均熱容量の値を提供します。
与えられた温度範囲t1〜t 2での平均熱容量の値を計算する必要がある場合、これは次のように実行できます。
曲線c\u003d f(t)(図1.4)の下の面積0a14は、ガス温度を0°Cからt1°Cに上げるために必要な熱量q1に対応します。
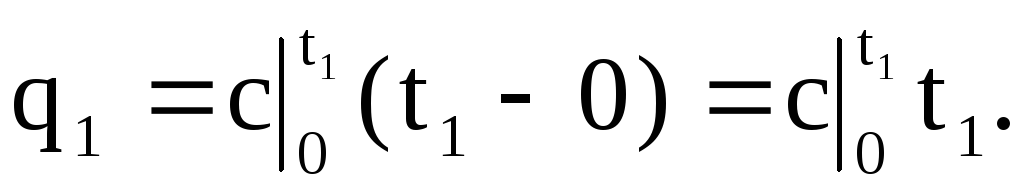
同様に、領域0a23は、温度が0oCからt2oCに上昇するときのq2に対応します。
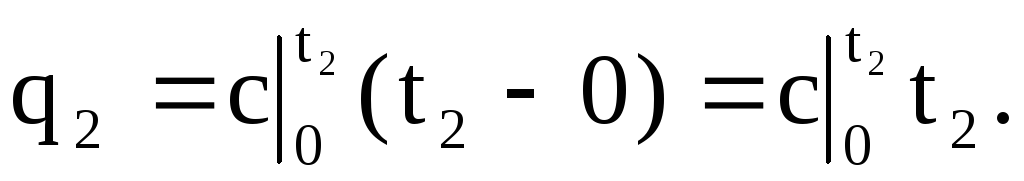
したがって、q \ u003d q 2-q 1(領域4123)は次のように表すことができます。
![]() (1.34)
(1.34)
(1.34)によるqの値を式(1.33)に代入すると、任意の温度範囲での平均熱容量の式が得られます。
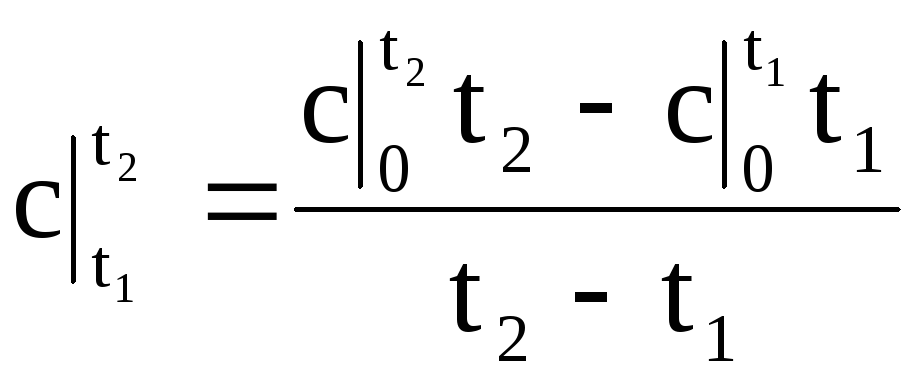 .
(1.35)
.
(1.35)
したがって、平均熱容量は、式(1.35)を使用して表形式の平均熱容量から計算できます。 さらに、非線形依存性c = f(t)を取得します。 また、線形関係を使用した式(1.32)を使用して、平均熱容量を求めることもできます。 値aと のさまざまなガスの式(1.32)は、文献に記載されています。
作動油に供給または除去される熱量は、次の式のいずれかを使用して計算できます。
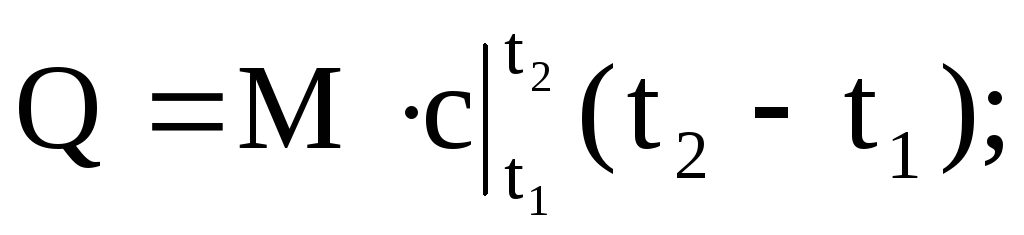 (1.36)
(1.36)
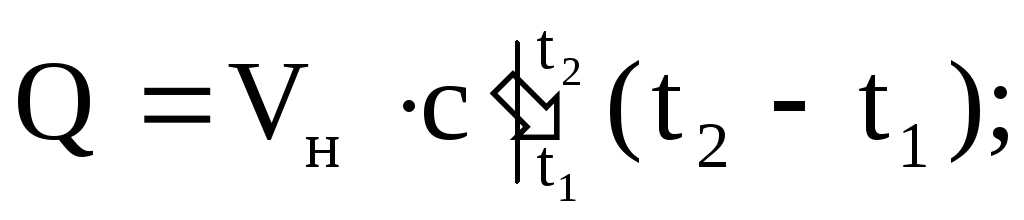 (1.37)
(1.37)
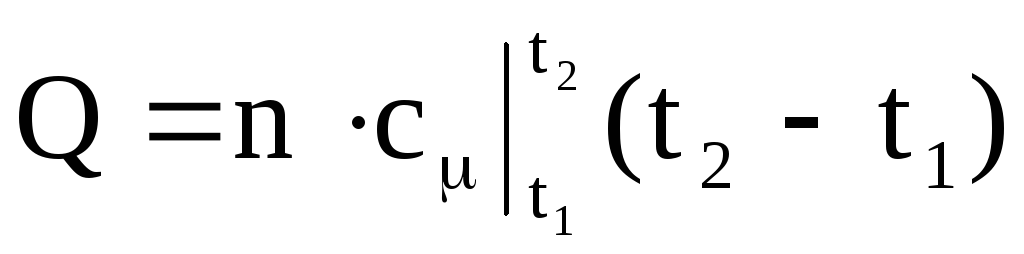 ,
(1.38)
,
(1.38)
どこ 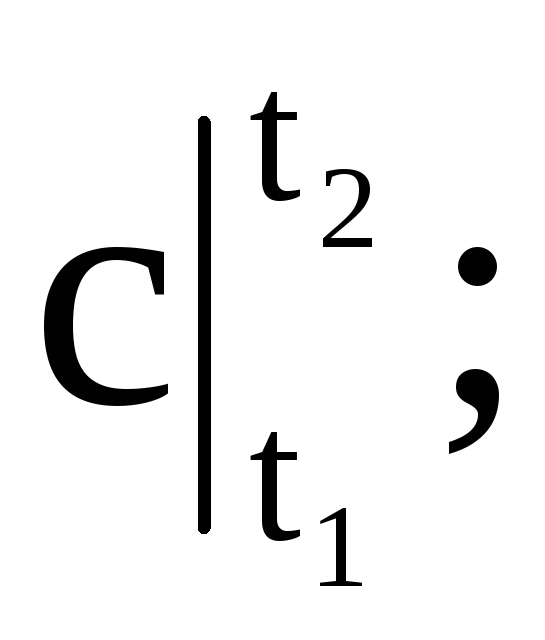
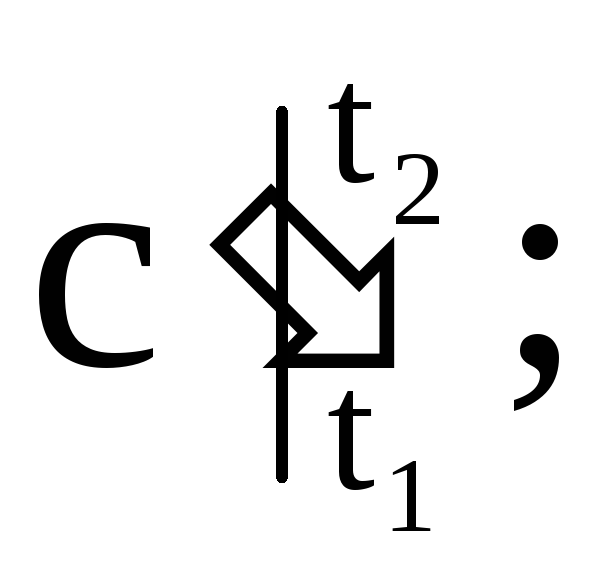
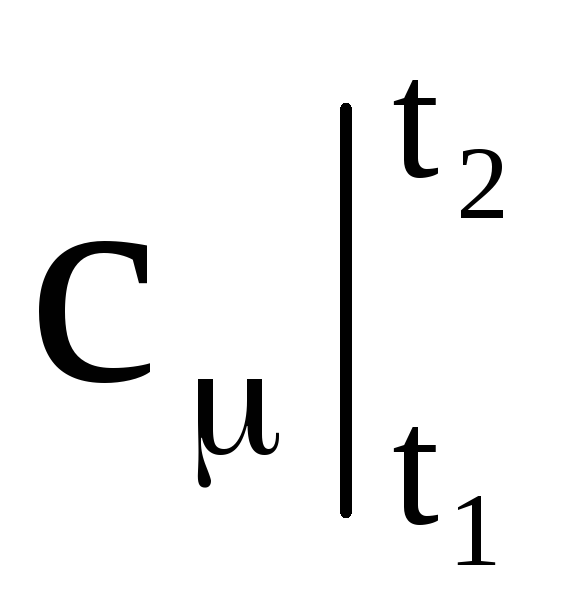 -それぞれ、平均質量、体積、モル熱容量。 Mはガスの質量です。 nはガスのキロモル数です。 Vn-通常の状態でのガスの量。
-それぞれ、平均質量、体積、モル熱容量。 Mはガスの質量です。 nはガスのキロモル数です。 Vn-通常の状態でのガスの量。
ガスの体積Vnは次のように求めることができます。 与えられた条件:pV = MRTおよび通常の条件:p n V n = MRT nの状態方程式を記述したら、2番目の方程式を最初の方程式に帰します。
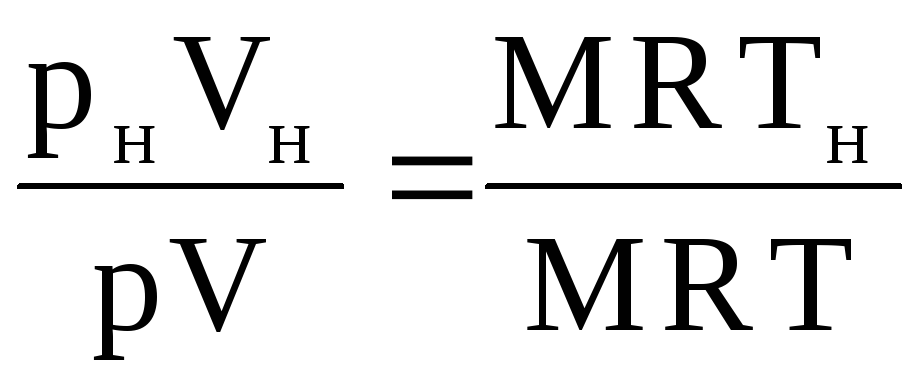 ,
,
ここから 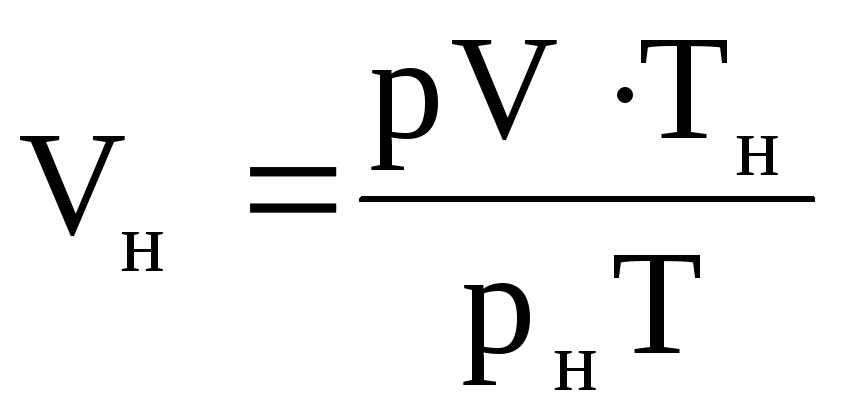 .
(1.39)
.
(1.39)
ガス混合物の熱容量
ガス混合物の熱容量は、混合物の組成が与えられ、混合物に含まれる成分の熱容量がわかっている場合に計算できます。
質量Mcmの混合物を1K加熱するには、各コンポーネントの温度も1K上昇させる必要があります。 同時に、c i M iに等しい量の熱が、質量Мiの混合物のi番目の成分の加熱に費やされます。 混合物全体について、熱量 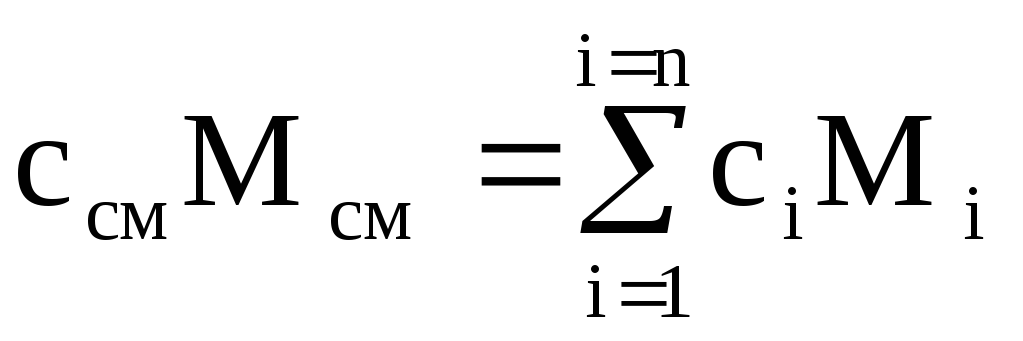 ,
,
ここで、ciとccmは、i番目の成分と混合物の質量熱容量です。
最後の式をMcmで割ると、混合物の質量熱容量の計算式が得られます。
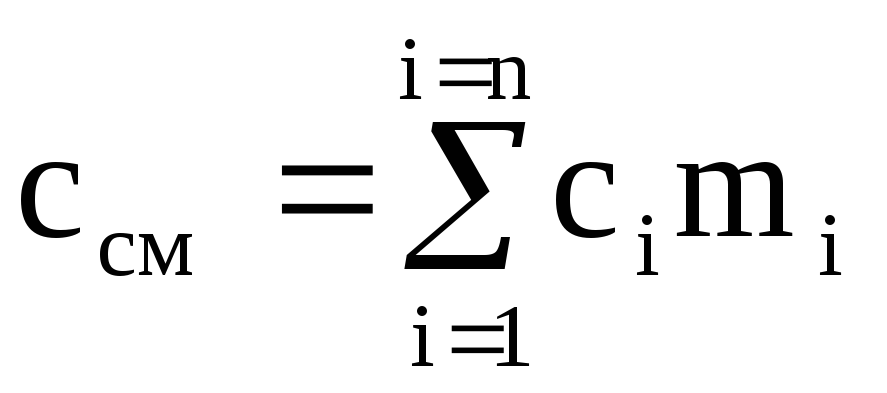 ,
(1.40)
,
(1.40)
ここで、m iは、i番目の成分の質量分率です。
同様に議論すると、混合物の体積熱容量c¢cmとモル熱容量cmcmがわかります。
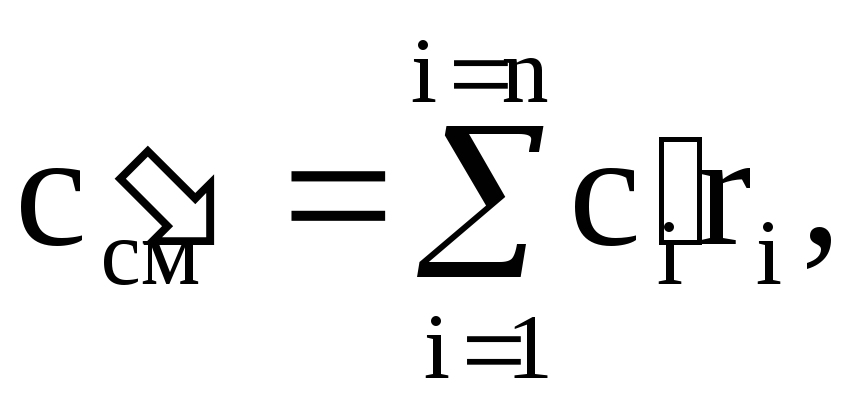 (1.41)
(1.41)
ここで、c¢i-i番目のコンポーネントの体積分率、ri-i番目のコンポーネントの体積分率、
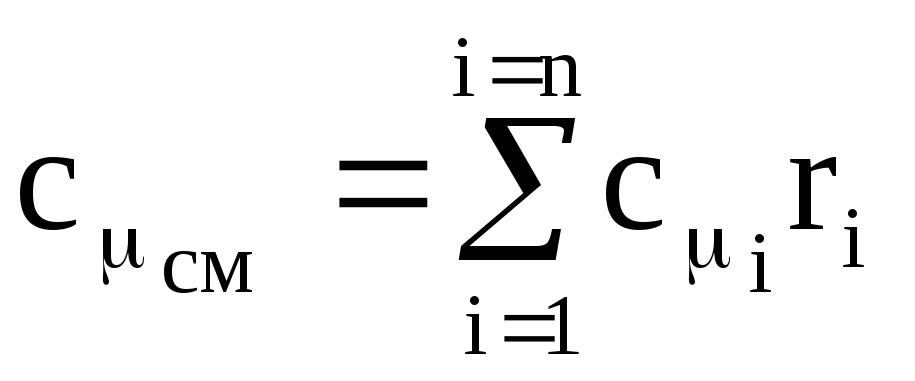 ,
(1.42)
,
(1.42)
ここで、cmiはi番目の成分のモル熱容量です。
r i-i番目の成分のモル(体積分率)分数。
実用的な仕事№ 2
トピック:熱容量、エンタルピー、理想気体の混合、内部エネルギー、仕事、熱力学的プロセス。
作業の目的:理論的なトレーニング中に得られた知識の統合、熱工学計算の実装におけるスキルの習得。
私。基本的な定義、式、方程式
1.理想気体の混合物
ガス混合物は、互いに化学的に相互作用しないいくつかのガスの機械的混合物です。 混合物中の各ガスはガス成分と呼ばれます。 混合物に他のガスがないかのように動作します。 混合物全体に均一に分布します。 混合物の各ガスが容器の壁に及ぼす圧力は、分圧と呼ばれます。 理想気体の混合物の基本法則はドルトンの法則であり、それによれば、混合物の圧力は、混合物を形成する気体の分圧の合計に等しくなります。
2.内部エネルギー
体の内部エネルギーは、体を構成する微粒子の運動の運動エネルギーとそれらの位置エネルギーの組み合わせです。 相互作用が定義されています。 相互引力または反発力。 内部エネルギーの絶対値を決定することは不可能であるため、熱力学的計算では、計算されるのは内部エネルギーの絶対値ではなく、その変化です。
![]() また
また ![]()
ここで、U1およびU2-作動流体(ガス)の初期状態と最終状態の内部エネルギー。
u1および2-ビート。 作動油の初期状態と最終状態の内部エネルギー。
このことから、内部エネルギーの変化はプロセスの性質や経路に依存せず、変化のプロセスの開始時と終了時の作動油の状態によって決定されます。
理想気体の特徴は、その中に分子相互作用の力がないこと、したがって内部ポテンシャルエネルギーがないことです。 U n \ u003d 0およびU„ \ u003d0。したがって、理想気体の内部エネルギーは次のようになります。
U = U k = f(T)unu u = uk = f(T)。
H.ガス作業。
熱力学において、エネルギーの交換の結果としての作動流体の状態の変化。 環境プロセスと呼ばれます。 この場合、作業体の主なパラメータが変更されます。
熱の機械的仕事への変換は、作動流体の状態を変化させるプロセスに関連しています。 ガスの状態を変化させるプロセスは、膨張および収縮プロセスである可能性があります。 ガスの任意の質量M(kg)の場合、仕事は次のようになります。
L \ u003d M l \ u003d Mp(v 2-v 1)\ u003d、J
ここで、l \ u003d p(v 2 -v 1)J / kgは、1kgのガスの仕事または特定の仕事です。
4.ガスエンタルピー、
エンタルピーは、作動流体(ガス)と環境との接続の位置エネルギーを特徴付けるパラメーターです。 エンタルピーと特定のエンタルピー:
I \ u003d U + pV、Jおよびi i \u003dおよび+pv、J/kg。
5.熱容量。
比熱容量は、特定の温度範囲で1°Cだけガスを加熱するために1kgのガスに供給しなければならない熱量です。
比熱容量は、質量、体積、キロモルです。 質量C、体積C、およびキロモルCの熱容量の間には関連性があります。
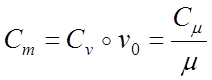 ;
; 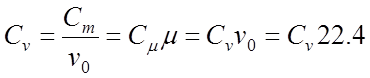
ここで、Vo 22.4 m 3/kmol-ビート。 通常の状態でのガスの量。
質量ud。 混合ガスの熱容量:
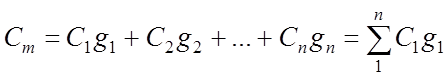
ガス混合物の体積比熱:
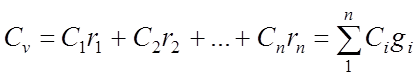
ガス混合物のキロモル比熱:
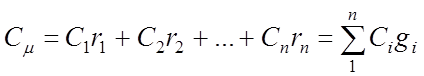
6.熱量を決定するための方程式
作動流体(ガス)によって放出または取り込まれる熱の量は、次の式で決定できます。
Q \ u003d M C m(t 2 -t 1)、JまたはQ \ u003d VC(t-t)、J、ここで、MおよびVはガスの重量または体積量、kgまたはm 3;
tut-プロセスの終了時と開始時のガス温度°С;
CおよびC-質量および体積の平均ビート。 ガスの熱容量
t cp \ u003d J/kgKまたはJ/m 3 K
7.熱力学の第一法則
この法則は、熱と機械的仕事の相互変換を考慮しています。 この法則によれば、熱は機械的仕事に変換され、逆もまた同様であり、機械的仕事は厳密に同等の量の熱に変換されます。 熱と仕事の等価方程式は次の形式になります。
熱と仕事の等価原理を考慮に入れると、任意の質量のガスの熱収支方程式は次のようになります。
Q \ u003d U+Lおよびq\u003d u + l \ u003d u -u + l
問題解決II
タスク#1(#1)
大気乾燥空気の質量組成はおおよそ次のとおりです。g02=23.2%、g N 2 = 76.8%。
気圧計を使用して空気がP=101325 Paの場合、空気の体積組成、そのガス定数、見かけの分子量、酸素と窒素の分圧を決定します。
私は空気の体積組成を決定します:
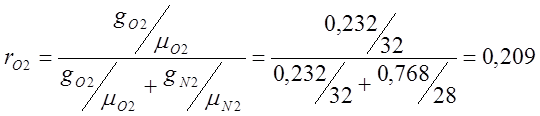 ;
;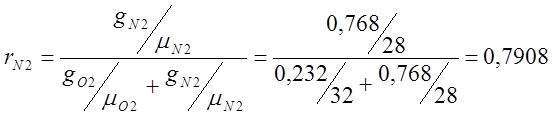 ;
;
ここで、rは質量分率です。
mは相対分子量です。
gは体積分率です。
m空気。 = m O2 r O2 + m N2 r N2 = 32 0.209 + 28 0.7908 = 6.668 + 22.14 = 28.83;
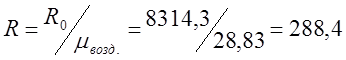
 ;
;
ここで、R0はガス定数です。
さまざまなガスの分圧を決定します。
P O 2 \ u003d P cm r O2 \ u003d 101325 0.209 \ u003d 21176.9(Pa);
P N 2 \ u003d P cm r N 2 \ u003d 101325 0.7908 \ u003d 80127.81(Pa);
ここで、P O 2、PN2-分圧。
Pcmは混合物の圧力です。
タスク#2(#2)
容器は仕切りによって2つの部分に分割され、その容積はV 1 = 1.5m3およびV2= 1.0m3です。 ボリュームV1の最初の部分には、P 1 =0.5MPaおよびt1=30°CでCO2が含まれています。 ボリュームV2の2番目の部分には、P 2 =0.2MPaおよびt2=57°CでO2が含まれています。 CO2とO2の質量と体積分率、混合物の見かけの分子量、およびパーティションが削除されて混合プロセスが完了した後のガス定数を決定します。
私は個々のガス定数を決定します:
これを行うために、相対分子量を決定します。m(CO 2)\ u003d 32 + 12 \ u003d 44; m(O 2)= 32;
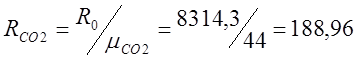
 ;
;
![]()
 ;
;
Klaiperonの特性方程式に従って、ガスの質量を決定します。
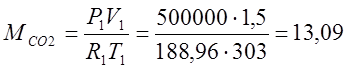 (kg);
(kg);
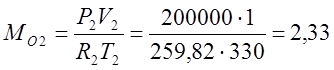 (kg);
(kg);
質量分率を決定します:
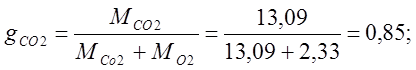
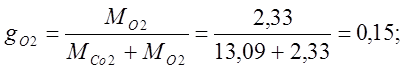
体積分率を決定します:
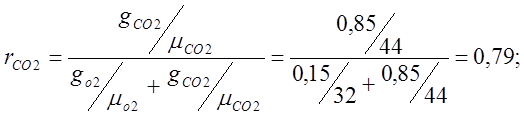
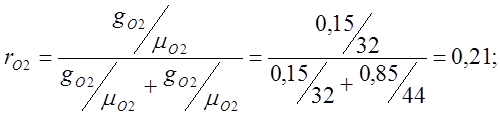
空気の見かけの分子量を決定します。
m空気。 \ u003d m O2 r O 2 + m CO2 r CO2 \ u003d 32 0.21 + 44 0.79 \ u003d 6.72 + 34.74 \ u003d 41.48;
空気(R)の個々の気体定数を決定します。
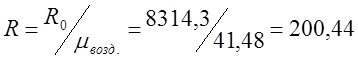
 ;
;
タスク#3(#6)
容量300lの容器には、圧力P 1 \ u003d0.2MPaおよびt1\ u003d 200Cの酸素があります。酸素の温度がt2\ u003d 300 0に上昇するために、どのくらいの熱を供給する必要がありますか。 C? 容器内にどのような圧力が確立されますか? 計算には、n.oでの酸素の平均体積比熱を取ります。 C 02 \ u003d 0.935 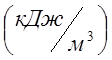
シャルルの法則に従って、私はプロセスの最終的な圧力を決定します。
; 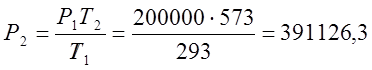 (Pa);
(Pa);
ここで、P、Tはガスパラメータです。
酸素(R)の個々の気体定数を決定します。
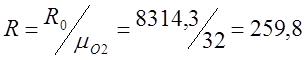
 ;
;
プロセスは定積であるため、適切な式に従って供給する必要のある熱量を決定します。Q v \ u003d M C cv(T 2 -T 1)このために、Claiperon特性方程式に従って、質量を決定します。ガスの
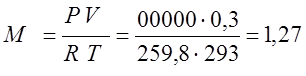 (kg); Q v \ u003d M C cv(T 2 -T 1)\ u003d 1.27 935280 \ u003d 332486(J)。
(kg); Q v \ u003d M C cv(T 2 -T 1)\ u003d 1.27 935280 \ u003d 332486(J)。
タスク#4(#7)
一定の過圧Pexで2m3の空気を加熱するためにどれだけの熱を消費する必要があるか。 \ u003d 100°Cの温度から500°Cの温度まで0.2MPa。この場合、空気はどのような働きをしますか? 計算には、大気圧Patを取ります。 \ u003d 0.1 MPa、空気の平均質量等圧熱容量C pm \ u003d 1.022 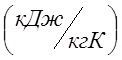 ; 空気の見かけの分子量M空気を念頭に置いてガス定数を計算します。 =29。
; 空気の見かけの分子量M空気を念頭に置いてガス定数を計算します。 =29。
空気の個々のガス定数を決定します。
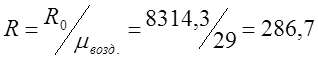
 ;
;
絶対圧力は、超過圧力と大気圧P =Pestの合計に等しくなります。 +Pat。 = 0.1 + 0.2 = 0.3 MPa
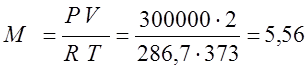 (kg);
(kg);
プロセスは等圧であるため、対応する式に従ってQとLを決定します。
ゲイ・リュサックの法則に従って、私は最終的なボリュームを決定します:
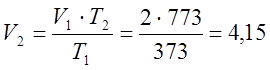 m 3;
m 3;
Q \ u003d M C pm(T 2 -T 1)\ u003d 5.56 1022 400 \ u003d 2272928(J);
L \ u003d P(V 2 -V 1)\ u003d 300000 2.15 \ u003d 645000(J)
タスク#5(#8)
シリンダー内には、圧力P = 0.5 MPa、温度t 1 =400°Cの空気があります。プロセスの最後に温度t2= 0 0 Cになるように、P=constで空気から熱が除去されます。セット。空気V1\u003d400lが入っているシリンダーの体積。
除去される熱の量、最終的な体積、内部エネルギーの変化、および圧縮の完全な仕事を決定しますC pm = 1.028 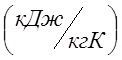 .
.
プロセスは等圧であるため、ゲイ・リュサックの法則に従って、最終的なボリュームを決定します。
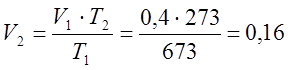 m 3;
m 3;
Klaiperonの特性方程式に従って、ガスの質量を決定します。
前の問題からR=286.7 
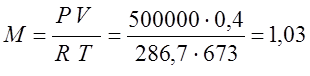 (kg);
(kg);
私は放出される熱の量を決定します:
Q = M C pm(T 2 -T 1)= 1.03 1028(273-673)=-423536(J);
私は費やした仕事の量を決定します:
L = P(V 2 -V 1)= 500,000(0.16-0.4)=-120,000(J);
総量を決定する式から、内部エネルギー量の変化を決定します。
![]() ; (J)
; (J)
問題#6(#9)
圧力P1=1.1MPaおよびt1=25sで体積V1= 0.02 m3の空気は、可動ピストンを備えたシリンダー内で圧力P 2 =0.11MPaまで膨張します。 シリンダー内で膨張が発生した場合、最終体積V 2、最終温度t 2、空気によって行われる仕事、および供給される熱を求めます。
a)等温
b)断熱指数k=1.4で断熱的に
c)ポリトロープ指数n=1.3のポリトロープ
等温プロセス:
P 1 / P 2 \ u003d V 2 / V 1
V 2 \ u003d 0.02 1.1 / 0.11 \ u003d 0.2M 3
Q = L = RMT 1 Ln(V 2 / V 1)= P 1 V 1 Ln(V 2 / V 1)= 1.1 10 6 0.02Ln(0.2 / 0.02)= 22000 J
断熱プロセス:
V 1 / V 2 \ u003d(P 2 / P 1)1 / k
V 2 \ u003d V 1 /(P 2 / P 1)1 / k \ u003d 0.02 /(0.11 / 1.1)1 / 1.4 \ u003d 0.1036M 3
T 2 / T 1 \ u003d(P 2 / P 1)k-1 / k
T 2 \ u003d(P 2 / P 1)k-1 / k T 1 \ u003d(0.11 / 1.1)1.4-1 / 1.4 298 \ u003d 20.32k
C v \ u003d 727.4 J / kg k
L \ u003d 1 / k-1(P 1 V 1 -P 2 V 2)\ u003d(1 / 1.4-1)(1.1 10 6 0.02 -0.11 10 6 0、1)= 2.0275 10 6 J
ポリトロープ過程:
V 1 / V 2 \ u003d(P 2 / P 1)1 / n
V 2 \ u003d V 1 /(P 2 / P 1)1 / n \ u003d 0.02 /(0.11 / 1.1)1 / 1.3 \ u003d 0.118M 3
T 2 / T 1 \ u003d(P 2 / P 1)n-1 / n
T 2 \ u003d(P 2 / P 1)n-1 / n T 1 \ u003d(0.11 / 1.1)1.3-1 / 1.3 298 \ u003d 175k
L \ u003d 1 / n-1(P 1 V 1 -P 2 V 2)\ u003d(1 /(1.3-1))(1.1 10 6 0.02 -0.11 10 6 0.118)= 30000J
Q =(k-n / k-1)l M =((1.4-1.3)/(1.4-1))30000 = 7500J
文学:
1.エネルギー、モスクワ、1975年。
2.リトヴィンA.M. 「熱工学の理論的基礎」、出版社「エネルギー」、モスクワ、1969年。
3. Tugunov P.I.、Samsonov A.A.、「熱工学、熱機関、および蒸気動力設備の基礎」、Nedra出版社、モスクワ、1970年。
4. Krutov V.I.、「熱工学」、出版社「工学」、モスクワ、1986年。
実習No.1
目標: 学生に理想気体と気体混合物の概念、および気体の熱容量を与えます。
簡単な理論情報
理想気体と気体混合物、および気体の熱容量を計算するときは、次の式を知って使用する必要があります。
理想気体の状態方程式:
–1kgのガスの場合
, (1.1)
- 為に mガスのkg
, (1.2)
–1モルのガスの場合
, (1.3)
ここで、はモル体積mです。 3 / mol; は普遍的な(モル)気体定数、J /(mol K)です。
ユニバーサルガス定数=8.314J /(mol。 に)。
比気体定数、J /(kg K)、
, (1.4)
ここで、はモル質量、kg/molです。
、(1.4a)
ここで、は物質の相対分子量です。
熱力学的温度、K、
, (1.5)
摂氏での温度はどこですか、 0C。
ガスの体積をいわゆる通常の状態にするのが通例です。この状態では、ガスの圧力は\ u003d 101.3 kPa、温度は\ u003d 0 0C。
ガス混合圧力
, (1.6)
ここで、はコンポーネントの分圧です。
混合ガス用
, (1.7)
ここで、はコンポーネントの質量です。
、(1.7a)
ここで、はコンポーネントの部分的な(縮小された)体積、mです。 3 .
ガス混合密度
, (1.8)
ここで、はコンポーネントの体積分率です。 このコンポーネントの密度、kg / m 3 ;
、(1.8a)
ここで、はコンポーネントの質量分率です。
理想気体の混合物の見かけのモル質量
, (1.9)
ここで、はコンポーネントのモル質量です。
。 (1.9a)
質量と体積分率の比率
. (1.10)
コンポーネントの分圧
. (1.11)
熱容量は、温度を1上昇させるために、体(システム)に供給しなければならない熱量を決定します。 0 C(1 Kあたり)。
これらの熱容量の間には機能的な関係があります
. (1.12)
熱計算で特に重要なのは、一定の圧力と一定の体積でのプロセスにおけるガスの熱容量です。それぞれ、等圧および等圧の熱容量です。 それらはメイヤー方程式によって接続されています:
–1kgのガスの場合
, (1.13)
ここで、は等圧および等圧の比熱容量です。
– ガス1モルに対して
、(1.13a)
ここで、は等圧および等圧のモル熱容量です。
これらの熱容量の比率は、断熱指数と呼ばれます
. (1.14)
からまでの温度範囲での平均熱容量は、通常、次のように計算されます。
, (1.15)
ここで、は0から0までの温度範囲での平均熱容量です。 0Сおよび0から0С。
ガスの混合物の熱容量:
- 明確な
, (1.16)
どこ –比熱容量成分;
–容積測定
、(1.16a)
どこ コンポーネントの体積熱容量です。
–臼歯
、(1.16b)
ここで、はコンポーネントのモル熱容量です。
ガイドライン問題解決へ
タスク番号1。
コンプレッサーは4mの量の空気を送り出します 3 /分17時 0 Cおよび10mの容積のタンクへの100kPaの圧力 3 。 タンク内の圧力が0.1から0.9MPaに上昇するのにどのくらい時間がかかりますか? 計算するときは、タンク内の気温は変化せず、17に等しいと仮定します。 0C。
解決
式(1.2)によるコンプレッサー運転開始時のタンク内の空気の質量
kg、
受け入れられた場合:
287 kJ /(kg。 K)-空気の比ガス定数(付録B);
17 + 273.15 = 290.15 K-式(1.5)による。
式(1.2)によると、最終圧力に達したときのタンク内の空気の質量= 0.9 MPa
kg。
依存性に応じた初期パラメータでの空気密度(1.1)
kg /m3。
問題の状態に応じて、コンプレッサーの体積流量は4mに設定されます。 3 / min、マスフィードを決定する必要があります
kg/分
空気がタンクに押し込まれたときのコンプレッサーの稼働時間
分。
答え: 20分で、タンク内の圧力は0.1から0.9MPaに増加します。
タスク番号2。
熱容量が一定であると仮定して、一定の圧力と体積でのプロセスにおける空気の比熱容量と体積熱容量を決定します。 通常の状態での空気密度=1.29kg / m 3 .
解決
空気の場合、相対分子量= 28.96(付録B)と、二原子ガスの場合のモル熱容量の値= 29.1 J /(mol。 K)および\ u003d 20.8 J /(mol。 K)(付録B)。
式(1.4a)に従って、次のように決定します。
– 空気のモル質量
kg / mol
式(1.12)で計算します。
– 等圧比熱
J /(kg。K)\ u003d 1.005 kJ /(kg。K)、
– 等圧体積熱容量
kJ /(m 3. K)、
– 定積比熱
J /(kg K)\ u003d 0.718 kJ /(kg。 に)、
– 定積体積熱容量
kJ /(m 3. K)。
答え: 比熱容量は0.718kJ/(kg . K)、および体積熱容量は0.926 kJ /(m 3. K)。
のタスク 独立したソリューション
タスク番号1。
通常の状態での二酸化炭素の密度を求めます。
タスク番号2。
70での窒素100kgの体積はどれくらいですか 0 Cと0.2MPaの圧力?
タスク番号3。
面積120mの講堂の空気の質量を決定します 2 高さ3.5m。観客の気温は18度です。 0 C、気圧は100kPaです。
タスク番号4。
30の温度で10リットルの体積の場合、酸素分子の原子数を決定します 0 Cおよび0.5MPaの圧力は63.5gの酸素です。
タスク番号5。
容量8mのタンク内 3 圧力10MPa、温度27の空気があります 0 C.空気の一部が使い果たされた後、圧力は5 MPaに下がり、温度は20に下がりました。 0 C.使用する空気の質量を決定します。
タスク#6
コンプレッサーはガスを10mのタンクに送り込みます 3 。 この場合、リザーバー内の圧力は、20の一定のガス温度で0.2から0.7MPaに増加します。 0 C.供給が180mの場合、コンプレッサーの動作時間を決定します 3 / h フィードは通常の状態で決定されます。
タスク番号7。
コンプレッサーは7mのタンクに空気を送り込みます 3 、タンク内の圧力が0.1から0.6MPaに増加します。 温度も15から50に上昇します 0 C.流量が30mの場合、コンプレッサーの稼働時間を決定します 3 / h、通常の状態に関連:0.1MPaおよび0 0C。
タスク番号8。
燃料の燃焼熱を測定するために、酸素で満たされた0.4リットルの熱量測定爆弾が使用されます。 充電中、爆弾内の酸素圧は2.2MPaに達します。 酸素は6リットルのシリンダーから供給されます。 初期圧力が12MPaの場合、シリンダーには何回のチャージで十分な酸素がありますか? 計算するときは、シリンダー内と爆弾を充電するときの両方で20に等しい酸素の温度を取ります 0C。
タスク番号9。
定置式エンジンの始動は、40リットルのシリンダーからの圧縮空気で行われます。 1回の始動で0.1m3の空気が消費されます 3 通常の条件下で決定されます。 シリンダー内の圧力が2.5から1MPaに低下した場合のエンジン始動回数を決定します。 気温を10度にします 0C。
タスク番号10。
燃料燃焼のガス状生成物は、等圧プロセスで温度から温度へと冷却されます。 ガスの組成は体積分率で与えられます:、、。 1mで放出される熱量を求めます 3 燃焼生成物。 体積は通常の状態で決定されます。
表に従って初期データを取得します。 1.1暗号(オプション番号)によって異なります。 計算は、平均熱容量を使用して実行されます。
表1.1。 初期データ
テストの質問
1.理想気体の定義を示し、実在気体との違いを示します。
2.ガス定数とユニバーサルガス定数の違いは何ですか?
3.混合物中のガスの分圧とは何ですか?それは物理的に存在し、どのように決定されますか?
4.混合物中のガスの部分体積とは何ですか、それは物理的に存在し、どのように決定されますか?
5.質量分率がわかっている場合、混合物中のガスの体積分率を決定するにはどうすればよいですか?
6.理想気体のどの特性が、それらの特定のモル等圧および等圧熱容量の数値を決定します。
ナレッジベースで優れた作業を送信するのは簡単です。 以下のフォームを使用してください
学生、大学院生、研究や仕事で知識ベースを使用する若い科学者はあなたに非常に感謝するでしょう。
http://www.allbest.ru/でホスト
ロシア連邦教育科学省
連邦州予算教育機関
高等教育
ヴォルゴグラード州立工科大学
キーロフイブニングファカルティ
規律に関する学期の作業:
熱工学
話題になっている:
燃料、ガス混合物および熱容量
完成者:学生gr.TVB-385
シェルチェンコB.D.
チェック:Assoc。 ゴリュノフV.A.
ヴォルゴグラード2015
調子
燃料燃焼温度酸化剤
工業炉では、燃料(エタノール)を一定の圧力で燃焼させます。 空気はある温度で酸化剤として使用されます T 1 =660K。 過剰空気の係数は次のように与えられます:a=1.0および燃料燃焼の完全係数w=0.9。 最大燃焼温度Tgの理論値を決定します。 燃料によって導入される熱は無視してください。
タブ。 No.1。 燃料の組成と発熱量
タブ。 2番。 平均等積質量熱容量(c v)の式
|
熱容量kJ/kg * K |
|||
|
0.691 + 7.1 * 10-5 T |
|||
|
0.775 + 11.7 * 10 -5 T |
|||
|
1.328 + 28.07 * 10 -5 T |
|||
|
0.716 + 7.54 * 10 -5 T |
|||
|
0.628 + 6.75 * 10 -5 T |
タブ。 番号3。 計算結果
最大理論燃焼温度は、熱収支方程式を使用して求められます :
zhQ H + Q o \ u003d Q p.sg.
ここで、Qo-酸化剤によって導入された熱。
Qh-燃料の正味発熱量。
g-燃料燃焼の完全性係数。
Qn。 Cr-燃焼生成物が受ける熱;
燃料の燃焼中に放出される熱(lQ h)を見つけます。
表2から、Qhの値が取得されます。
Q h \ u003d 27100 kJ / kg
表1から、wの値が取得されます(私のバージョンでは、w = 0.9)
と* Q H \ u003d 0.9 * 27100 \ u003d 24390 kJ / kg
酸化剤によってもたらされる熱を見つけます:
Q o \ u003dCp。 空気 *m空気*T1
表2の式に従って、空気の平均等積質量熱容量を決定します。
cv空気\u003d0.691 + 7.1 * 10 -5 * 660 \ u003d 0.73786 kJ / kg * K
Mayerの式を使用して、平均等圧質量熱容量を計算します。
Av air \ u003d c v air + R \ u003d 0.73786 + 0.287 \ u003d 1.02486 kJ / kg * K
理論的に必要な空気の質量を決定します。
m o air \ u003d 2.67 * C p + 8H p --O p / 0.23 \ u003d(2.67 * 0.52 + 8 * 0.13-0.35)/ 0.23 \ u003d(1.3884 + 1.04-0.35)/0.23=2.0784/0.23=9.0365 Kg / Kg
空気の実際の質量を決定します。
m air \ u003d a * m o air \ u003d 1.0 * 9.0365 \ u003d 9.0365 Kg / Kg
Q oを定義します:
Q o \ u003dCp。 空気 *m空気*T1 \ u003d 1.02486 * 9.0365 * 660 \ u003d 6112.36 kJ / kg
酸化剤と燃焼燃料によって導入される熱を計算します。
zhQ H + Q o \ u003d 24390 + 6112.36 \ u003d 30502.36 kJ / kg
燃焼生成物の熱を見つけます(Qn.Сг):
Qn。 Cr \ u003d C R、p。sg * m p、sg *T2。
a)燃焼生成物の質量を決定します。
m p、sg \ u003d 1 + m air \ u003d 1 + 9.0365 \ u003d 10.0365
b)燃焼生成物の成分の質量分率を計算します。
g co 2 \ u003d m co 2 / m p、sg \ u003d 3.67 * C P / m p、sg \ u003d 3.67 * 0.52 / 10.0365 \ u003d 0.1901
g H 2 o \ u003d m H 2 o / m p、sg \ u003d 9 * H p / m p、sg \ u003d 9 * 0.13 / 10.0365 \ u003d 0.1166
g o2 \ u003d m o2 / m p、sg \ u003d 0.23 *(a-1)* m o air / m p、sg \ u003d 0.23 *(1.0-1)* 9.0365 / 10.0365 \ u003d 0
g N2 \ u003d m N2 / m p、sg \ u003d 0.77 * a * m o air / m p、sg \ u003d 0.77 * 1.0 * 9.0365 / 10.0365 \ u003d \ u003d 0.693
c)次の式を使用して、燃焼生成物の平均等圧質量熱容量を求めます。
C P、p。sg \ u003d g(co 2)* C p(co 2)+ g(H 2 o)* C p(H 2 O)+ g(o 2)* C p(O 2)+ g( N 2)* C p(N 2)\ u003d
燃焼生成物のコンポーネントの等圧熱容量を見つけます。
a) c v(co 2)\ u003d 0.775 + 11.7 * 10 -5 * T 2
b) c v(H2 o)\ u003d 1.328 + 28.07 * 10 -5 * T 2
c) c v(O 2)\ u003d 0.628 + 6.75 * 10 -5 * T 2
d) c v(N 2)\ u003d 0.716 + 7.54 * 10 -5 * T 2
マイヤーの公式を使用して、pで見つけます。 :
1. C p(co 2)\ u003d c v(co 2)+ R \ u003d 0.775 + 11.7 * 10 -5 * T 2 +0.189 \ u003d 0.964 + 11.7 * 10 -5 * T 2
2. C p(H2O)\ u003d c v(H2 o)+ R \ u003d 1.328 + 28.07 * 10 -5 * T 2 +0.462 \ u003d 1.79 + 28.07 * 10 -5 * T 2
3. C p(O 2)\ u003d c v(O 2)+ R \ u003d 0.628 + 6.75 * 10 -5 * T 2 + 0.260 \ u003d 0.888 + 6.75 * 10 -5 * T 2
4. C p(N 2)\ u003d c v(N 2)+ R \ u003d 0.716 + 7.54 * 10 -5 * T 2 + 0.297 \ u003d 1.013 + 7.54 * 10 -5 * T 2
したがって、次の式に従って、燃焼生成物の平均等圧質量熱容量を求めます。
C P、p。sg \ u003d g(co 2)* C p(co 2)+ g(H 2 o)* C p(H 2 O)+ g(o 2)* C p(O 2)+ g( N 2)* C p(N 2)\ u003d 0.1901 *(0.964 + 11.7 * 10 -5 * T 2)+ 0.1166 *(1.79 + 28.07 * 10 -5 * T 2)+ 0 *(0.888 + 6.75 * 10 -5 * T 2)+ 0.693 *(1.013 + 7.54 * 10 -5 * T 2)\ u003d 0.1832 + 2.2242 * 10 -5 * T 2 + 0.2087 + 3.2729 * 10 -5 * T 2 +0 + 0.702 + 5.2252 * 10 -5 * T 2 = 1.0939 + 10.7223 * 10 -5 * T 2 = 1.0939 + 10.7223 * 10 -5 * 3934.89 = = 1.516
燃焼生成物の熱Qnを求めます。 SG:
Qn。 Cr \ u003d C R、p.sg * m p、sg * T 2 \ u003d(1.0939 + 10.7223 * 10 -5 * T 2)* 10.0365 * T 2
熱収支方程式を使用して、最大理論燃焼温度(T 2)を決定します。
とQ h= Q n . SG
24390 =(1.0939 + 10.7223 * 10 -5 * T 2)* 10.0365 * T 2両側を10.0365カットします:
10.7223 * 10 -5 *(T 2)2 + 1.09369 * T 2-2430.13 = 0
1.09369 + 1.495 / 0.000214 = 1875 K
Allbest.ruでホスト
同様の文書
ガス混合物の質量、体積、およびモル熱容量の決定。 対流熱伝達係数と対流の計算 熱の流れパイプからガレージの空気まで。 式D.I.による計算 燃料の最低発熱量と最高発熱量のメンデレーエフ。
テスト、2015年1月11日追加
ガス混合物、熱容量。 平均モルと比熱容量の計算。 基本的なエンジンサイクル 内燃機関。 熱係数 便利なアクションディーゼルサイクル。 水蒸気、蒸気発電所。 ランキンサイクルの一般的な概念。
タームペーパー、2012年11月1日追加
比熱-温度変化に対する物質の単位量が受ける熱の比率。 熱量のプロセスの性質への依存性、および熱容量-そのコースの条件への依存性。 理想気体による熱力学的プロセス。
要約、2009年1月25日追加
可燃性ガスの成分の熱効果の積とその量の積の合計としてのガス燃料の発熱量の決定。 天然ガスを燃焼させるために理論的に必要な空気の流れ。 燃焼生成物の量の決定。
テスト、2010年11月17日追加
ガス混合物のモル質量と質量熱容量。 断熱状態プロセス。 サイクルのポイントでの作業体のパラメータ。 サイクルの熱効率に対する圧縮比、圧力上昇、等圧膨張の影響。 等積線に沿った熱除去のプロセス。
タームペーパー、2010年3月7日追加
空気の流れと燃焼生成物の量の決定。 ロータリーキルンでのボーキサイトの焼結中の炭塵の組成と過剰空気の係数の計算。 メンデレーエフの半実験式を使用して、燃料の燃焼熱を計算します。
テスト、2014年2月20日追加
空気中の燃料の燃焼を計算する方法:空気中の酸素量、燃焼生成物、 発熱量燃料、熱量測定および実際の燃焼温度。 酸素が豊富な空気中での燃料の燃焼。
タームペーパー、2011年12月8日追加
熱を仕事や他の種類のエネルギーに変換するプロセスを研究する物理学の一分野としての熱力学。 ガス温度計回路の主な機能の特性評価。 理想気体の基本的な性質の考察。 「熱容量」の概念の本質。
プレゼンテーション、2014年4月15日追加
別の種類の燃料に切り替える前のボイラーユニットの説明。 設置が認められているバーナーの特性。 排気ガス温度の正当化。 2種類の燃料の燃焼中の空気と燃焼生成物の量の計算。 熱収支と燃料消費量。
論文、2015年6月13日追加
トンネルドライヤーの目的。 燃料の組成と燃焼用空気の計算。 燃料燃焼中の燃焼生成物の総量と理論温度の決定。 乾燥トンネルの技術計算。 乾燥プロセスの熱技術計算。

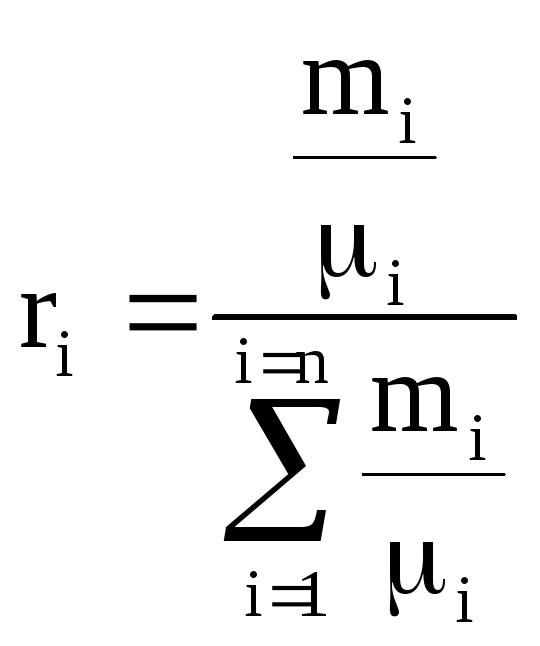
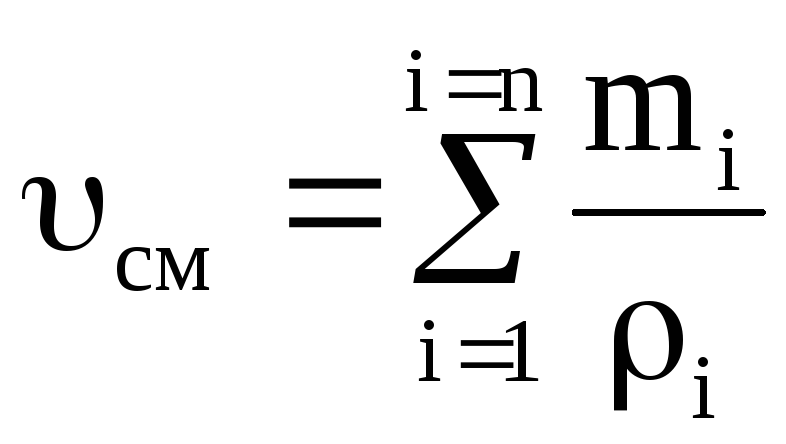
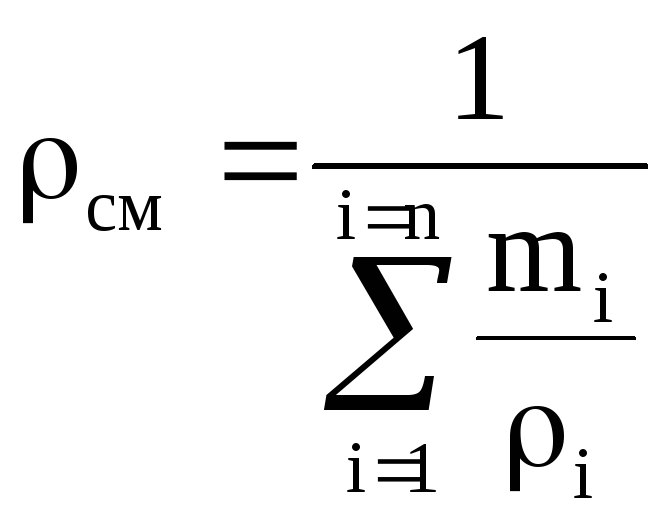
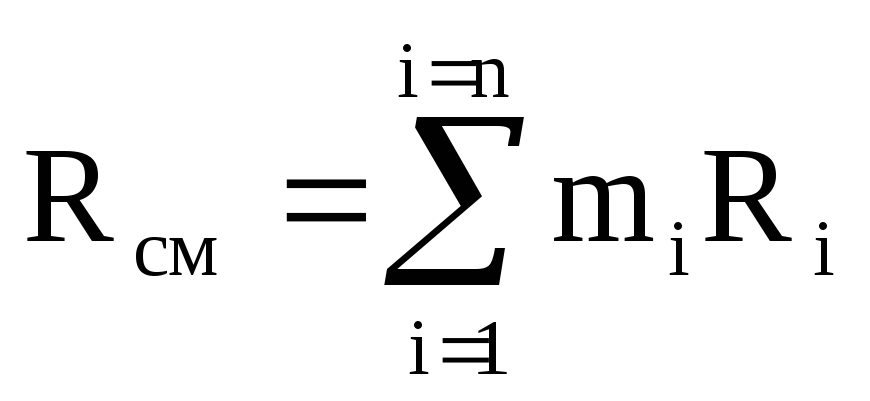

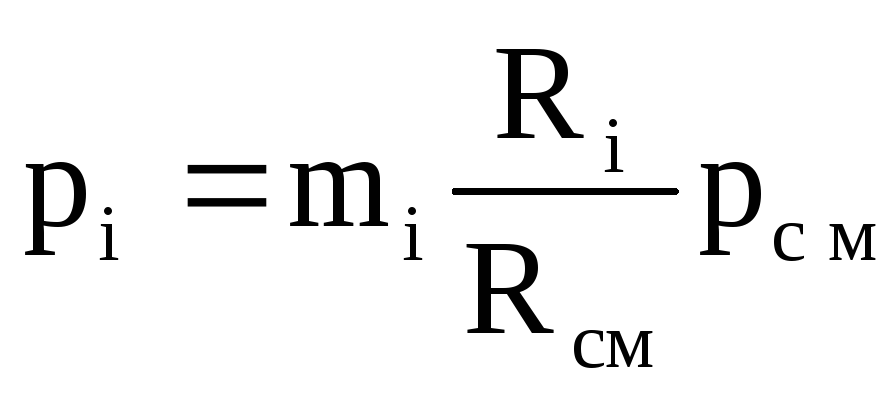
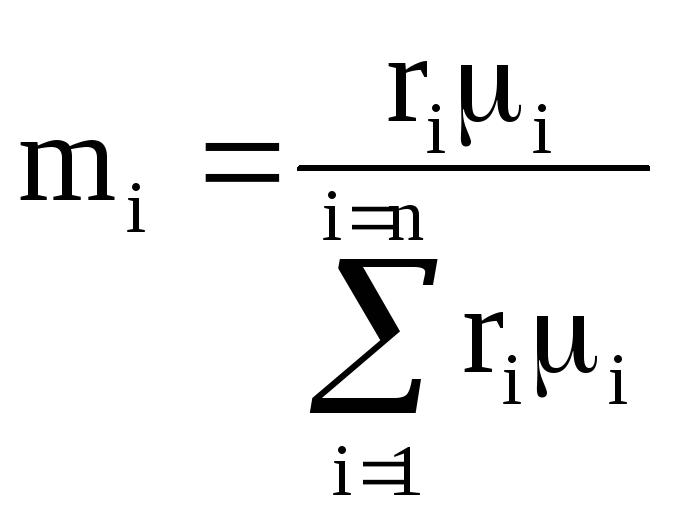
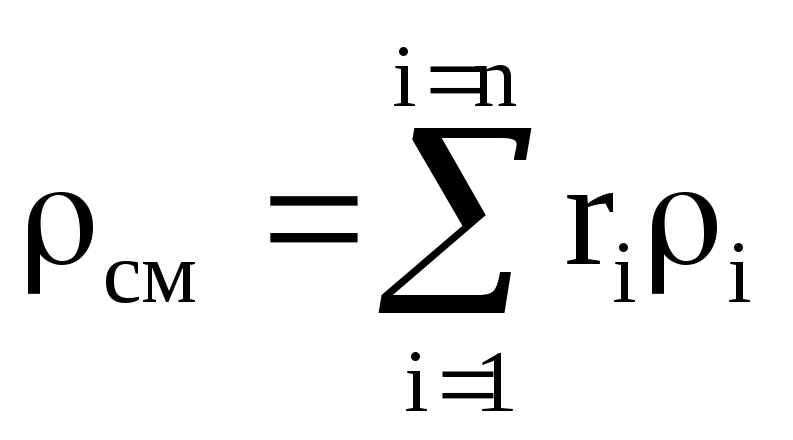
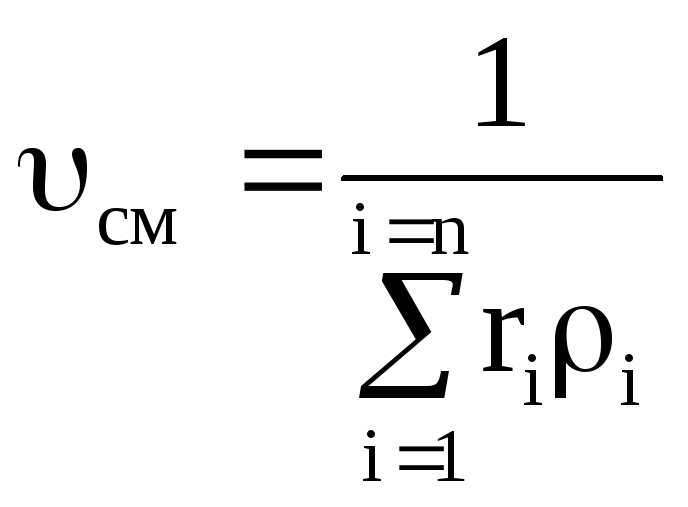
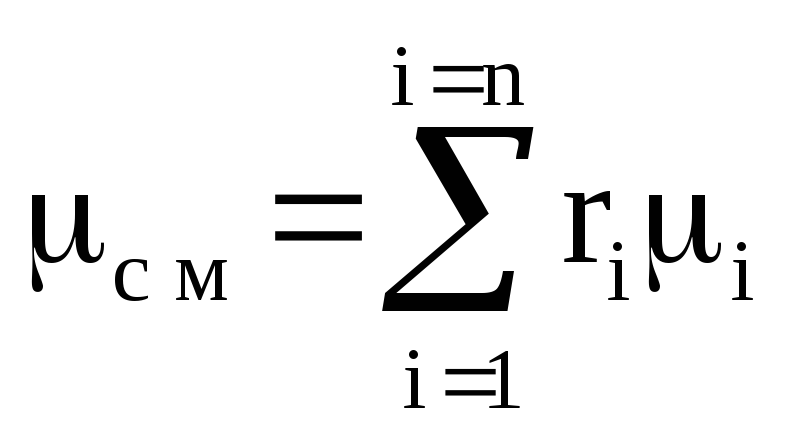
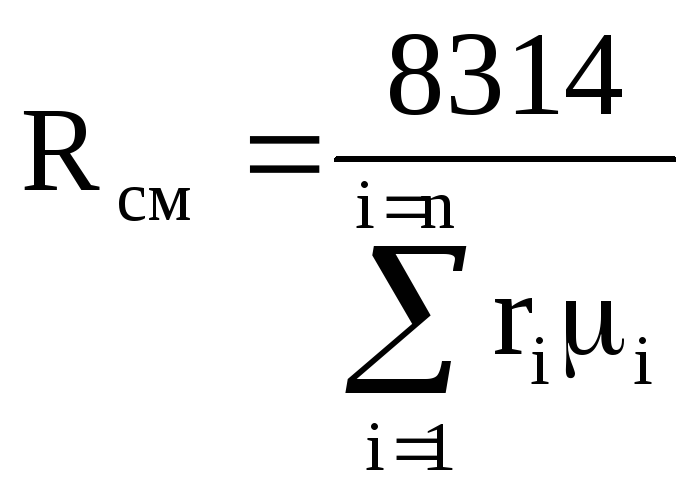
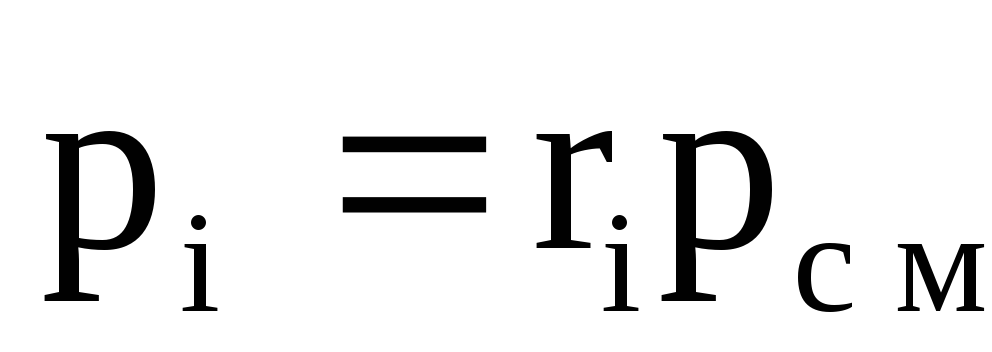
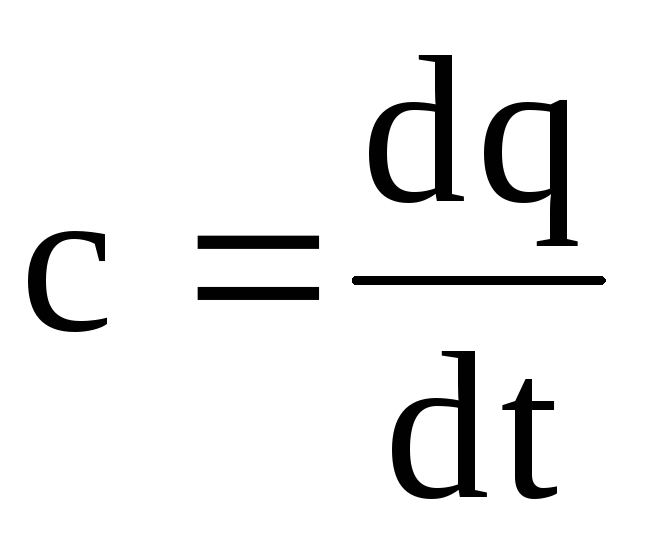 .
(1.28)
.
(1.28)