Як визначити питому теплоємність води. Велика енциклопедія нафти та газу
ПРИЛАДИ ТА ПРИЛАДДЯ: калориметр, термометр, ваги, випробувані тіла, мензурка (проградуйована в грамах), електронагрівальний прилад.
- Підтвердити експериментально справедливість рівняння теплового балансу;
- Обчислити питомі теплоємності твердих тіл;
– оформити у вигляді таблиці результати вимірів та обчислень;
– записати свої пропозиції щодо покращення техніки вимірювань та обчислень у даній роботі.
КОРОТКА ТЕОРІЯ ДОСВІДУ
Одним із основних фізичних понять термодинаміки є теплоємність.
Теплоємністю тіланазивається фізична величина, чисельно рівна теплоті, яку треба повідомити тілу для зміни її температури на 1 К у аналізованому термодинамічному процесі. З іншого боку, теплоємність тіла дорівнює відношенню теплоти dQ, що повідомляється тілу, до зміни dT температури тіла в даному термодинамічному процесі:
Теплоємність тіла залежить від його хімічного складу, маси тіла та його термодинамічного стану, а також, як видно з визначення, від виду процесу зміни стану тіла, в якому надходить теплота dQ.
Теплові властивостіоднорідних тіл характеризуються значеннями питомої та мольної (молярної) теплоємності. Питомою теплоємністю речовининазивається фізична величина з, чисельно рівна теплоті, яку треба повідомити одному кілограму речовини для зміни його температури на 1 К у аналізованому термодинамічному процесі. Теплоємність однорідного тіла можна визначити як добуток маси тіла mна питому теплоємність зйого речовини:
![]() або (2.2).
або (2.2).
Таким чином, зв'язок між dQ і dT для однорідного тіла має вигляд:
Молярною теплоємністюназивається фізична величина С, чисельно рівна теплоті, яку потрібно повідомити одному молю речовини для зміни його температури на 1 К в аналізованому термодинамічному процесі:
З = Мс = (2.4),
де М - молярна маса речовини; З– його питома теплоємність у тому процесі.
Вираз (2.4) можна записати тепер у формі:
де = n – кількість речовини.
Одиницею вимірювання теплоємності тіла є 1 Дж/К, питомої теплоємності- 1 Дж/кг. К, молярної – 1 Дж/моль. До.
Якщо нагрівання відбувається в умовах коли обсяг залишається постійним, то відповідна молярна теплоємність називається теплоємністю при постійному обсязі, або ізохоричною теплоємністю, і позначається З v:
Якщо при нагріванні постійним залишається тиск, то теплоємність називається теплоємністю при постійному тискуЗ р (її можна також назвати ізобаричною теплоємністю):
Зазначимо, що для твердих тіл безпосередньому виміру доступна лише теплоємність при постійному тиску, а не при постійному обсязі, оскільки через теплове розширення не можна забезпечити сталість об'єму тіла. Однак внаслідок малості зміни об'єму при нагріванні різницю між теплоємностями С р і С мало.
Експериментально теплоємність тіла визначають, застосовуючи рівняння теплового балансу. Нехай тіло нагріте до температури, яка вище температури довкілля. Тоді, остигаючи, тіло віддає кілька тепла. За законом збереження енергії в замкнутій системі кількість тепла, отримана середовищем, повинна бути точно дорівнює кількості тепла, відданого тілом. У цьому роботі, остигаючи, випробуване тіло віддає тепло воді, що у калориметрі, і самому калориметру.
Нехай це випробуване тіло масою m, нагріте до температури t 0, опущено в калориметр із водою, температура якої t 1. Внаслідок теплообміну Температура водиі калориметра підвищується до t 2, а Температура тілазнижується до t 2. Кількість теплоти, віддане тілом, дорівнює:
Q відд = cm(t 0 - t 2) (2.6),
де с – питома теплоємність випробуваного тіла,
t 0- Початкова температура тіла,
t 2- Кінцева температура тіла,
m- маса тіла.
Кількість теплоти, отримана калориметром та водою дорівнює:
де і – маса та питома теплоємність калориметра,
І – маса та питома теплоємність води,
t 1- Початкова температура води,
t 2- Кінцева температура води.
За законом збереження енергії у замкнутій системі:
Q отд = Q підлогу (2.8).
Тоді, підставляючи формули 2.6 та 2.7 до рівняння 2.8 та виражаючи шукану величину З , Отримаємо:
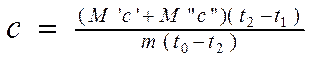 (2.9).
(2.9).
Визначити питомі теплоємності трьох циліндричних тіл з різних металів
1. Визначити значення мас тіл – m i, маси калориметра – , питомої теплоємності води – , питомої теплоємності калориметра – .
2. Налити в калориметр відважену кількість холодної води масою кімнатної температури (приблизно 150 г).
3. Виміряти початкову температуру холодної води t1.
4. Нагріти воду в посудині до кипіння.
5. Помістити одне з випробуваних тіл у киплячу воду на деякий час. Температуру нагрітого тіла t 0 прийняти рівної температурикипіння води за нормальних умов – 100 °С.
6. Помістити нагріте тіло до калориметра з водою. Дочекатися закінчення теплообміну та виміряти кінцеву температуру в калориметрі – t 2 .
8. Визначити аналогічно питомі теплоємності двох інших тіл.
9. Результати вимірювань та обчислень занести до таблиці 3.
10. За значеннями питомих теплоємностей визначити речовини, з яких виготовлені тіла.
12. Вимірявши лінійні розміри тіл, визначити їх густини.
13. Провести розрахунок похибок та записати результат відповідно до ГОСТу.
14. Записати висновки щодо лабораторної роботи.
Таблиця 3
| № п/п | М", кг | М", кг | m, кг | C", Дж/кг. | C", Дж/кг. | t 0 , 0 C | t 1 , 0 C | t 2 , 0 C | C, Дж/кг. До |
Сторінка 2
Точність визначення питомої теплоємності за Сайкс дуже висока. Однак цей метод пов'язаний з більшими експериментальними труднощами, ніж метод Сміта, і також дає точні результати тільки для кривих нагріву, хоча може бути застосований для отримання кривих охолодження. Спосіб Сміта дозволяє легше досліджувати вузькі температурні інтервали, але, ймовірно, менш точний.
Отже, для визначення питомої теплоємності сг речовини потрібно виміряти роботу А, досконалу зовнішніми силами, що діють на тіло, і виміряти зміну температури тіла, що спостерігається в результаті здійснення роботи, в умовах відсутності теплообміну його з іншими тілами.
Найбільш уживаний спосіб визначення питомої теплоємності; званий способом змішування. Калориметр (Реньо) складається з посудини червоної міді, поставленої на дерев'яних ніжках на дно іншої мідної судини, від якої він відділений шаром повітря, теплопровідність і теплоємність якого, віднесена до одиниці об'єму, незначні. Перший посуд наповнюється водою.
Розглянемо тепер способи визначення питомої теплоємності газової суміші.
Безпосереднє (пряме) визначення питомої теплоємності Су та вивчення ходу її зміни залежно від температури та питомого обсягу є одним із ефективних засобіввивчення критичного стану речовин Тому експериментальні визначення теплоємності представляють великий теоретичний та практичний інтерес щодо критичних явищ.
Яка є формула визначення питомої теплоємності розчинів.
При проведенні дослідів з визначення питомої теплоємності методом змішування необхідно досліджуваний зразок нагрівати до точно фіксованої температури. Для цього застосовують переносні нагрівачі, які встановлюють над калориметром на короткий час, необхідне швидкого перенесення нагрітого зразка в калориметр.
| Схема устрою. |
Сутність найпростішого абсолютного стаціонарного способу визначення питомої теплоємності зводиться до наступного: зразок випробуваного матеріалу товщиною і площею поперечного перерізу 5 поміщається між нагрівачем і охолоджувачем. Нагрівачем може служити посудина з гарячою водоюабо електронагрівальний елемент так, щоб його потужність могла за бажанням регулюватися зміною напруги. Охолоджувачем є порожнисте металеве тіло, через яке пропускається холодна вода. Температури на поверхні, що нагрівається і охолоджується, зразка (tj і, відповідно, / 2) вимірюються термопарами.
Нижче наведено приклад обробки дослідних даних щодо питомої теплоємності зразка пісковика. Порожнистий циліндр, заповнений порошком зразка породи, що досліджується, підігрівався до 40 С і охолоджувався в камері спокійного повітря до температури 18 - 20 С.
На рис. 3 - 6 наведено номограми для визначення питомої теплоємності рідких індивідуальних вуглеводнів та нафтових сумішей, а також водних розчинів метанолу та етанолу.
Наприклад складемо рівняння теплового балансу, що використовується щодо питомої теплоємності речовини з допомогою калориметра. Приблизно вважатимуться, що у разі у теплообміні беруть участь три тіла: калориметр, рідина і тіло, питому теплоємність речовини якого визначають.
6.4. Теплообмін між тілами
6.4.1. Тепломісткість тіла, питома теплоємність речовини, молярна теплоємність речовини
Для того, щоб підвищити температуру тіла, йому необхідно повідомити деяку кількість теплоти.
1 кг даної речовини на 1 К, називається питомою теплоємністюречовинита обчислюється за формулою
c уд = Q m Δ T ,
де Q - кількість теплоти, необхідне нагрівання деякої маси речовини; m – маса речовини; ΔT – зміна температури речовини при нагріванні.
У Міжнародній системі одиниць питома теплоємність речовини вимірюється в джоулях, поділених на кілограм-кельвін (1 Дж/(кг К)).
Кількість теплоти, необхідна для нагрівання деякої маси речовини, визначається твором
Q = c уд m ∆T.
Кількість теплоти, необхідне нагрівання даного тіла на 1 К, називається теплоємністю тілата обчислюється за формулою
C = Q Δ T ,
де Q - кількість теплоти, необхідне нагрівання даного тіла; ΔT – зміна температури тіла при нагріванні.
У Міжнародній системі одиниць теплоємність тіла вимірюється у джоулях, поділених на кельвін (1 Дж/К).
Кількість теплоти, необхідне нагрівання деякого тіла , визначається добутком
Q = C ΔT ,
де C – теплоємність тіла.
Теплоємність тіла та теплоємність речовини, з якої складається дане тіло, зв'язані між собоювиразом
C = mc уд,
де C – теплоємність тіла; m – маса тіла; c уд - Питома теплоємність речовини, з якої виготовлено це тіло.
Кількість теплоти, необхідне нагрівання 1 моль даної речовини на 1 До, називається молярною теплоємністю речовинита обчислюється за формулою
c μ = Q ν Δ T ,
де Q - кількість теплоти, необхідне нагрівання деякої кількості речовини; ν - кількість речовини; ΔT – зміна температури зазначеної кількості речовини при нагріванні.
У Міжнародній системі одиниць молярна теплоємність речовини вимірюється у джоулях на моль-кельвін (1 Дж/(моль ⋅ К)).
Кількість теплоти, необхідна для нагрівання деякої кількості речовини, визначається твором
Q = c µ νΔT.
Молярна та питома теплоємності речовини зв'язані між собоювиразом
c µ = Mс уд,
де c µ - молярна теплоємність речовини; M – молярна маса речовини; з уд - питома теплоємність речовини.
Приклад 14. Залізна та свинцева кульки мають однакові діаметри. У скільки разів теплоємність залізної кульки більша за теплоємність свинцевої? Питомі теплоємності заліза та свинцю дорівнюють 0,46 та 0,13 кДж/(кг ⋅ К), а щільності – 7,80 та 11,5 г/см 3 відповідно.
Рішення . Теплоємності кульок визначаються такими формулами:
- залізної кульки -
C 1 = m 1 c уд1
де m 1 - маса залізної кульки; c уд1 - питома теплоємність заліза;
- свинцевої кульки -
C 2 = m 2 c уд2
де m 2 - маса свинцевої кульки; c уд2 - питома теплоємність свинцю.
Шуканим є відношення теплоємностей:
C 1 C 2 = m 1 c уд 1 m 2 c уд 2
яке визначається ставленням мас залізної та свинцевої кульок та ставленням питомих теплоємностей заліза та свинцю.
Маси кульок визначаються їх розмірами та щільністю:
- залізної кульки -
m 1 = ρ 1 V 1 ,
де 1 - щільність заліза; V 1 - обсяг залізної кульки;
- свинцевої кульки -
m 2 = ρ 2 V 2 ,
де 2 - щільність свинцю; V 2 - обсяг свинцевої кульки.
Кульки мають однакові діаметри, тому їх обсяги однакові:
V 1 = V 2 = V = π d 2 6 ,
де d - діаметри залізної та свинцевої кульок.
З урахуванням останньої обставини відношення мас одно:
m 1 m 2 = ρ 1 V 1 ρ 2 V 2 = ρ 1 ρ 2 .
Підставимо m 1 /m 2 у формулу для відношення теплоємностей залізної та свинцевої кульок:
C 1 C 2 = ρ 1 c уд 1 ρ 2 c уд 2 .
Проведемо обчислення:
C 1 C 2 = 7,80 ⋅ 10 3 ⋅ 0,46 ⋅ 10 3 11,5 ⋅ 10 3 ⋅ 0,13 ⋅ 10 3 = 2,4 .
Теплоємність залізної кульки перевищує в 2,4 рази теплоємність свинцевої кульки.
Приклад 15. При виготовленні суміші бункер засипали деяку масу піску і вчетверо велику масу цементу. Питома теплоємність цементу та піску дорівнює 810 і 960 Дж/(кг ⋅ К) відповідно. Визначити питому теплоємність суміші.
Рішення . Питома теплоємність суміші визначається формулою
c уд = Q m Δ T ,
де Q - кількість теплоти, необхідне для того, щоб підвищити температуру суміші на T ; m – маса суміші.
Кількість теплоти, необхідне для нагрівання суміші, -
Q = Q 1 + Q 2
де Q 1 - кількість теплоти, необхідне для нагрівання піску, що входить до складу суміші, на T ; Q 2 - кількість теплоти, необхідне нагрівання цементу, що входить до складу суміші, на ΔT .
Кількість теплоти, необхідне нагрівання:
- піску -
Q 1 = c уд1 m 1 ∆T ,
де c уд1 – питома теплоємність піску; m 1 – маса піску;
- цементу -
Q 2 = c уд2 m 2 ∆T ,
де c уд2 - Питома теплоємність цементу; m 2 – маса цементу.
Кількість теплоти, необхідне нагрівання суміші піску і цементу, визначається виразом
Q = c уд 1 m 1 Δ T + c уд 2 m 2 Δ T = (c уд 1 m 1 + c уд 2 m 2) Δ T .
Маса суміші є сума мас піску та цементу:
m = m1 + m2.
Підставимо отримані вирази для кількості теплоти та маси суміші у формулу питомої теплоємності суміші:
c уд = (c уд 1 m 1 + c уд 2 m 2) T (m 1 + m 2) Δ T = c уд 1 m 1 + c уд 2 m 2 m 1 + m 2 .
Зробимо перетворення отриманого виразу з урахуванням співвідношення мас:
m 2 = 4m 1, тобто. c уд = c уд 1 m 1 + 4 c уд 2 m 1 m 1 + 4 m 1 = c уд 1 + 4 c уд 2 5 .
Розрахунок дає значення:
c уд = 960 + 4 ⋅ 810 5 = 840 Дж/(кг ⋅ К).
Отже, питома теплоємність суміші становить 840 Дж/(кг К).
