წყალბადის სულფიდის თბოტევადობა სხვადასხვა ტემპერატურაზე. ბუნებრივი აირის სპეციფიკური თბოტევადობა
არა სპეციფიკური, მაგრამ მთლიანი თერმული სიმძლავრე, ზოგადად მიღებული ფიზიკური გაგებით, არის ნივთიერების გაცხელების უნარი. ყოველ შემთხვევაში, ასე გვეუბნება თერმული ფიზიკის ნებისმიერი სახელმძღვანელო - ეს არის კლასიკური განმარტებასითბოს სიმძლავრე(სწორი ფორმულირება). სინამდვილეში, ეს არის საინტერესო ფიზიკური თვისება. ჩვენთვის ნაკლებად ცნობილი ყოველდღიურ ცხოვრებაში "მონეტის მხარე". გამოდის, რომ როდესაც სითბო მიეწოდება გარედან (გათბობა, დათბობა), ყველა ნივთიერება არ რეაგირებს თანაბრად სითბოზე ( თერმული ენერგია) და გაცხელეთ სხვანაირად. უნარი ბუნებრივი წარმოშობის გაზი გამოიყენება საწვავადთერმული ენერგიის მიღება, მიღება, შენარჩუნება და დაგროვება (დაგროვება). ეწოდება ნატურალური წვადი აირის თბოტევადობა. და თვითონაც მეთანის სითბოს სიმძლავრე, არის ფიზიკური მახასიათებელი, რომელიც აღწერს გაზის საწვავის თერმოფიზიკურ თვისებებს. ამავდროულად, სხვადასხვა გამოყენებითი ასპექტით, კონკრეტული პრაქტიკული შემთხვევიდან გამომდინარე, ერთი რამ შეიძლება აღმოჩნდეს ჩვენთვის მნიშვნელოვანი. მაგალითად: ნივთიერების მიღების უნარი თბილიან დაგროვების უნარი თერმული ენერგიაან „ნიჭი“ რომ შეინარჩუნო. თუმცა, გარკვეული განსხვავების მიუხედავად, ფიზიკური გაგებით, ჩვენთვის საჭირო თვისებები იქნება აღწერილი მეთანის სითბოს სიმძლავრე.
ფუნდამენტური ბუნების პატარა, მაგრამ ძალიან "საზიზღარი ნაკლი" არის გაცხელების უნარი - მეთანის თერმული ტევადობა, პირდაპირ კავშირშია არა მარტო ქიმიური შემადგენლობა, ნივთიერების მოლეკულური აგებულება, არამედ მისი რაოდენობა (წონა, მასა, მოცულობა). ასეთი „უსიამოვნო“ კავშირის გამო გენერალმა მეთანის სითბოს სიმძლავრეხდება ნივთიერების ძალიან მოუხერხებელი ფიზიკური მახასიათებელი. ვინაიდან ერთი გაზომილი პარამეტრი ერთდროულად აღწერს "ორ განსხვავებულ რამეს". კერძოდ: ნამდვილად ახასიათებს ბუნებრივი აირის თერმოფიზიკური თვისებები, თუმცა „გადასვლისას“ მის რაოდენობასაც ითვალისწინებს. ერთგვარი ინტეგრალური მახასიათებლის ფორმირება, რომელშიც "მაღალი" თერმული ფიზიკა და მატერიის "ბანალური" რაოდენობა (ჩვენს შემთხვევაში: გაზის საწვავი) ავტომატურად არის დაკავშირებული.
აბა, რატომ გვჭირდება ასეთი თერმოფიზიკური მახასიათებლები, რომლებშიც ნათლად არის მიკვლეული „არაადეკვატური ფსიქიკა“? ფიზიკის თვალსაზრისით, სულ მეთანის სითბოს სიმძლავრე(ყველაზე მოუხერხებელი გზით), ცდილობს არა მხოლოდ აღწეროს თერმული ენერგიის რაოდენობა, რომელსაც შეუძლია დაგროვდეს გაზის საწვავში, არამედ ასევე "შეგვატყობინოს" ოდენობის შესახებ. ბუნებრივი წვადი გაზი. გამოდის აბსურდი და არა ნათელი, გასაგები, სტაბილური, სწორი მეთანის თერმოფიზიკური მახასიათებელი. პრაქტიკულისთვის შესაფერისი სასარგებლო მუდმივის ნაცვლად თერმოფიზიკური გამოთვლები, გვეძლევა მცურავი პარამეტრი, რომელიც არის მიღებული სითბოს რაოდენობის ჯამი (ინტეგრალი). ბუნებრივი აირიდა მისი მასა ან მეთანის მოცულობა.
მადლობა, რა თქმა უნდა, ასეთი "ენთუზიაზმისთვის", მაგრამ რაოდენობა ბუნებრივი საწვავი გაზიშემიძლია გავზომო საკუთარი თავი. მიღებული შედეგები ბევრად უფრო მოსახერხებელი, "ადამიანური" ფორმით. რაოდენობა ბუნებრივი წვადი გაზიარ მინდა მათემატიკური მეთოდებით და გამოთვლებით "ამოვწერო" ზოგადიდან რთული ფორმულის გამოყენებით მეთანის სითბოს სიმძლავრე, სხვადასხვა ტემპერატურაზე და გაარკვიეთ წონა (მასა) გრამებში (გ, გ), კილოგრამებში (კგ), ტონებში (ტონა), კუბებში (კუბური მეტრი, კუბური მეტრი, მ3), ლიტრი (ლ) ან მილილიტრი (მლ). ). მითუმეტეს მას შემდეგ ჭკვიანი ხალხიდიდი ხნის წინ გამოვიდა ამ მიზნებისათვის საკმაოდ შესაფერისი საზომი ხელსაწყოები. მაგალითად: სასწორი ან სხვა მოწყობილობები.
განსაკუთრებით პარამეტრის „შემაშფოთებელი მცურავი ბუნება“: გენერალი ბუნებრივი აირის სითბოს სიმძლავრე. მისი არასტაბილური, ცვალებადი „განწყობა“. "სერვის ზომის ან დოზის" შეცვლისას, ბუნებრივი აირის თბოტევადობა სხვადასხვა ტემპერატურაზედაუყოვნებლივ იცვლება. უფრო აალებადი აირის ნარევი, ფიზიკური რაოდენობა, აბსოლუტური მნიშვნელობა მეთანის სითბოს სიმძლავრე- იზრდება. წვადი აირის ნარევის ნაკლები რაოდენობა, ღირებულება მეთანის თერმული ტევადობამცირდება. "სირცხვილი" ზოგიერთი თურმე! სხვა სიტყვებით რომ ვთქვათ, ის, რაც „გვაქვს“ არანაირად არ შეიძლება ჩაითვალოს მუდმივ აღწერად ბუნებრივი აირის თერმოფიზიკური მახასიათებლები სხვადასხვა ტემპერატურაზე. და ჩვენთვის სასურველია "გვქონდეს" გასაგები, მუდმივი კოეფიციენტი, საცნობარო პარამეტრი, რომელიც ახასიათებს თერმული თვისებებიგაზის საწვავი, მეთანის რაოდენობის (წონა, მასა, მოცულობა) „მინიშნებების“ გარეშე. Რა უნდა ვქნა?
სწორედ აქ გვეშველება ძალიან მარტივი, მაგრამ „ძალიან მეცნიერული“ მეთოდი. საქმე ეხება არა მხოლოდ აღმასრულებელს "უდ. - კონკრეტული", ადრე ფიზიკური რაოდენობა, მაგრამ ელეგანტური გადაწყვეტა, რომელიც მოიცავს მატერიის რაოდენობის გამორიცხვას განხილვისგან. ბუნებრივია, "არასასიამოვნო, ზედმეტი" პარამეტრები: მასა ან მოცულობა ბუნებრივი წვადი გაზიაბსოლუტურად შეუძლებელია გამორიცხვა. ყოველ შემთხვევაში, იმ მიზეზით, რომ თუ არ არის მეთანის რაოდენობა, მაშინ თავად არ იქნება "განხილვის საგანი". და ნივთიერება უნდა იყოს. ამიტომ ვირჩევთ მასის ან მოცულობის რაიმე პირობით სტანდარტს, რომელიც შეიძლება ჩაითვალოს ჩვენთვის საჭირო კოეფიციენტის „C“ მნიშვნელობის დასადგენად შესაფერის ერთეულად. ამისთვის ბუნებრივი აირის საწვავის წონამეთანის მასის ასეთი ერთეული, მოსახერხებელი პრაქტიკული გამოყენებისას, აღმოჩნდა 1 კილოგრამი (კგ).
Ახლა ჩვენ ერთ კილოგრამ ბუნებრივ აირს ვათბობთ 1 გრადუსით, ხოლო სითბოს რაოდენობას (თერმული ენერგია)ჩვენ გვჭირდება გათბობა გაზის ნარევიერთი ხარისხი - ეს არის ჩვენი სწორი ფიზიკური პარამეტრი, კოეფიციენტი "C"კარგად, საკმაოდ სრულად და ნათლად აღწერს ერთ-ერთს ბუნებრივი აირის თერმოფიზიკური თვისებები სხვადასხვა ტემპერატურაზე. გთხოვთ გაითვალისწინოთ, რომ ახლა საქმე გვაქვს მახასიათებელთან ფიზიკური ქონებანივთიერება, მაგრამ არ ცდილობს „დამატებით გვაცნობოს“ მისი რაოდენობის შესახებ. კომფორტული? სიტყვები არ არის. სულ სხვა საქმეა. სხვათა შორის, ახლა გენერალზე არ არის საუბარი მეთანის თერმული ტევადობა. Ყველაფერი შეიცვალა. ეს არის ბუნებრივი აირის სპეციფიკური სიცხე, რომელსაც ზოგჯერ სხვა სახელითაც უწოდებენ. Როგორ? უბრალოდ მასიური ბუნებრივი წვადი აირის თბოტევადობა. სპეციფიკური (უდ.) და მასა (მ.) - ამ შემთხვევაში: სინონიმები, აქ იგულისხმება ის, რაც ჩვენ გვჭირდება. კოეფიციენტი "C".
ცხრილი 1. კოეფიციენტი: ბუნებრივი აირის სპეციფიკური თბოტევადობა (სპ.). ბუნებრივი წვადი აირის მასობრივი თერმული ტევადობა. საცნობარო მონაცემები.
მარტივად რომ ვთქვათ, სითბოს მოცულობა FROMსხეული ეწოდება სითბოს რაოდენობას, რომელიც უნდა დაიხარჯოს ეს პროცესისხეულის ერთი გრადუსით გაცხელება: .
ჩვეულებრივ, სითბოს სიმძლავრე მოიხსენიება ნივთიერების რაოდენობის ერთეულზე და, არჩეული ერთეულიდან გამომდინარე, განასხვავებენ:
სპეციფიკური მასის სითბოს მოცულობა თან, იგულისხმება 1 კგ აირი, J/(kgK);
სპეციფიკური მოცულობითი სითბოს მოცულობა თან´, იგულისხმება გაზის რაოდენობა, რომელიც შეიცავს 1 მ 3 მოცულობის ნორმალურ ფიზიკურ პირობებში, J / (m 3 K);
სპეციფიკური მოლური სითბოს სიმძლავრე μ თან, მოხსენიებულია ერთ კილომოლზე, J / (kmolK).
სპეციფიკური სითბოს სიმძლავრეებს შორის კავშირი დადგენილია აშკარა ურთიერთობებით:
თან= μ თან/μ; თან´= თანρ n. (2.13)
აქ ρ n არის გაზის სიმკვრივე ნორმალურ პირობებში.
შესაბამისად, სხეულის ტემპერატურის ცვლილება მიწოდებული სითბოს იგივე რაოდენობით დამოკიდებულია მიმდინარე პროცესის ბუნებაზე სითბოს სიმძლავრე პროცესის ფუნქციაა. ეს ნიშნავს, რომ ერთი და იგივე სამუშაო სითხე, პროცესიდან გამომდინარე, საჭიროებს სითბოს სხვადასხვა რაოდენობას მისი გასათბობად 1 კ-ით. რიცხობრივად სიდიდე თანმერყეობს + ∞-დან – ∞-მდე.
თერმოდინამიკურ გამოთვლებში დიდი მნიშვნელობააქვს:
სითბოს სიმძლავრე მუდმივი წნევის დროს
თან p = δ ქპ/ dT, (2.14)
ქ p , ორგანიზმში მიყვანილი ამ პროცესში მუდმივი წნევით, სხეულის ტემპერატურის ცვლილებამდე dT;
სითბოს სიმძლავრე მუდმივი მოცულობით
თან ვ = δ ქ ვ /dT, (2.15)
უდრის δ სითბოს რაოდენობის შეფარდებას ქ ვ, ორგანიზმში მიყვანილია ამ პროცესში მუდმივი მოცულობით, სხეულის ტემპერატურის ცვლილებამდე dT.
დახურული სისტემების თერმოდინამიკის პირველი კანონის შესაბამისად δ ქ = დუ + pdf.
იმის გათვალისწინებით, რომ 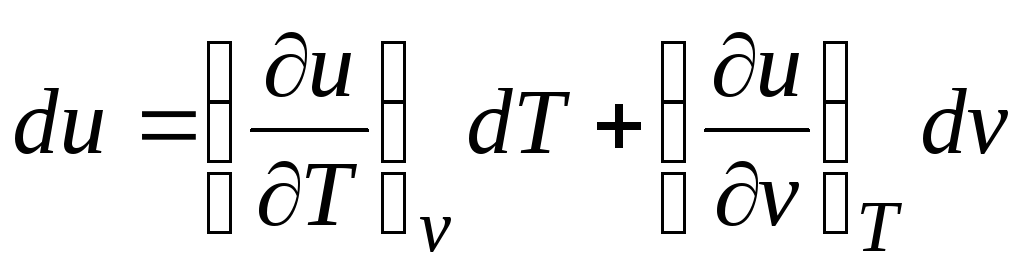 (ურთიერთობები (2.1))
(ურთიერთობები (2.1))
Δ ქ = (∂u/∂თ) ვ dT + [(∂u/∂ვ) თ + გვ]dv. (2.16)
იზოქორული პროცესისთვის ( ვ=const) ეს განტოლება იღებს ფორმას 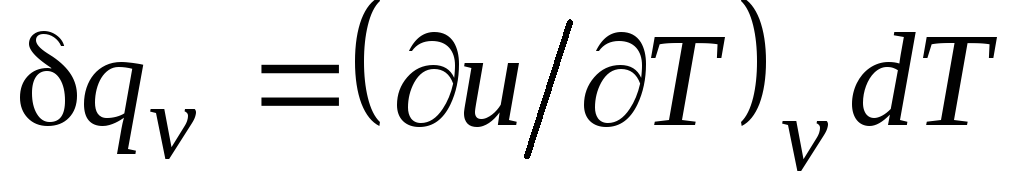 და, (2.15) გათვალისწინებით, მივიღებთ იმას
და, (2.15) გათვალისწინებით, მივიღებთ იმას
გ ვ = (∂u/∂თ) ვ . (2.17)
იდეალური გაზისთვის
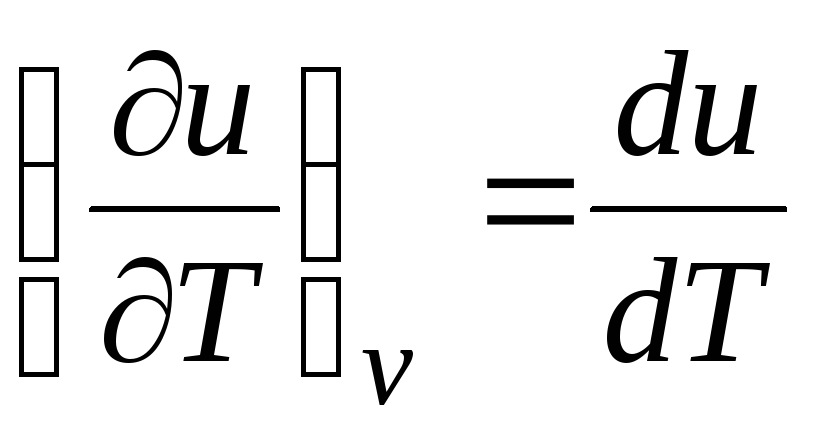 (განტოლება 2.2), ასე
(განტოლება 2.2), ასე
გ ვ = დუ/dT. (2.18)
იზობარული პროცესისთვის ( რ=const) (2.16) და (2.14) განტოლებიდან ვიღებთ
გ p = (∂ u/∂თ) ვ + [(∂u/∂ვ) თ + გვ](dv/dT) გვ
ვინაიდან შინაგანი ენერგია იდეალური გაზიგანისაზღვრება მხოლოდ მისი ტემპერატურით და არ არის დამოკიდებული კონკრეტულ მოცულობაზე, მაშინ
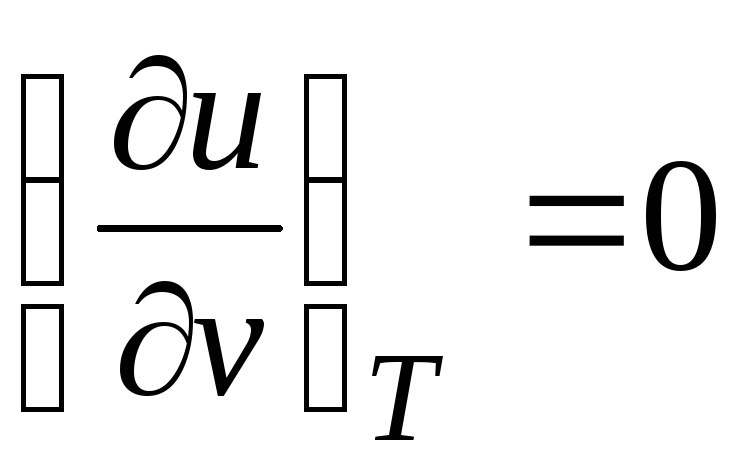 .
(2.19)
.
(2.19)
კლაპეირონის განტოლებიდან (1.4) pv
= RT(1.3) მოყვება 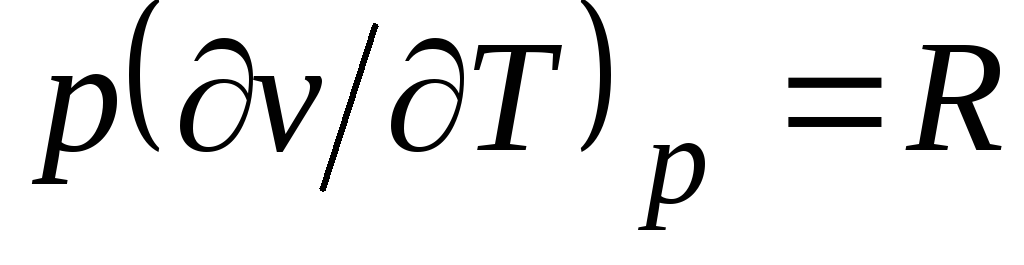 , სად
, სად
გ p= თან ვ + რ. (2.20)
მიმართებას (2.20) ეწოდება მაიერის განტოლება და ერთ-ერთი მთავარია იდეალური აირების ტექნიკურ თერმოდინამიკაში.
Პროცესში ვ\u003d const, გაზზე გადაცემული სითბო მიდის მხოლოდ მისი შიდა ენერგიის შესაცვლელად, ხოლო პროცესის p \u003d const, სითბო იხარჯება როგორც შიდა ენერგიის გასაზრდელად, ასევე გაფართოების სამუშაოს შესასრულებლად. Ამიტომაც გგვ მეტი თან v ამ სამუშაოს მოცულობით.
ფორმულა ![]() განსაზღვრავს ეგრეთ წოდებულ ნამდვილ თბოტევადობას, ანუ სითბოს სიმძლავრის მნიშვნელობას მოცემულ ტემპერატურაზე. პრაქტიკაში, სითბოს სიმძლავრე ფართოდ გამოიყენება სითბოს რაოდენობის გამოსათვლელად ქ 12, რომელიც უნდა დაიხარჯოს სხეულის გასათბობად ერთი ტემპერატურისგან ( ტ 1) მეორეს ( ტ 2) (ან რომელიც გამოიყოფა გაციებისთანავე ტ 2-მდე ტ 1).
განსაზღვრავს ეგრეთ წოდებულ ნამდვილ თბოტევადობას, ანუ სითბოს სიმძლავრის მნიშვნელობას მოცემულ ტემპერატურაზე. პრაქტიკაში, სითბოს სიმძლავრე ფართოდ გამოიყენება სითბოს რაოდენობის გამოსათვლელად ქ 12, რომელიც უნდა დაიხარჯოს სხეულის გასათბობად ერთი ტემპერატურისგან ( ტ 1) მეორეს ( ტ 2) (ან რომელიც გამოიყოფა გაციებისთანავე ტ 2-მდე ტ 1).
თუ სითბოს სიმძლავრე არ იცვლება მითითებულ ტემპერატურულ დიაპაზონში, მაშინ
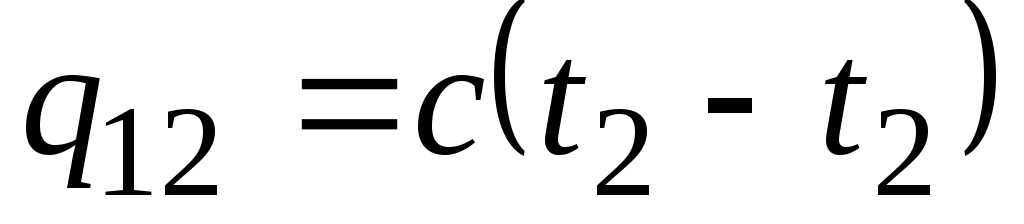 , კჯ/კგ და
, კჯ/კგ და 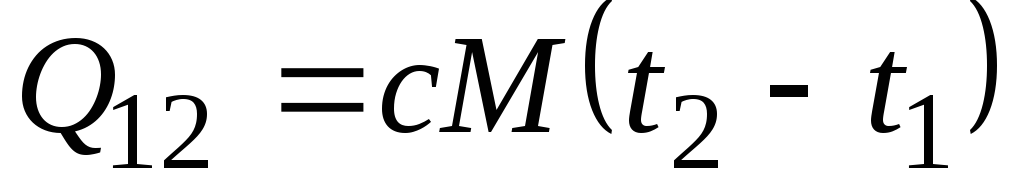 , კჯ. (2.21)
, კჯ. (2.21)
ეს ფორმულა ასევე შეიძლება გამოყენებულ იქნას სავარაუდო (არა ძალიან ზუსტი) გამოთვლებისთვის. მაგალითად, ოთახის ტემპერატურაზე წყლის სპეციფიკური თბოტევადობა არის 4,187 კჯ/(კგC), ხოლო ჰაერი 1 კჯ/(კგC). იმის გამო, რომ თითქმის ყველა ნივთიერების სითბოს მოცულობა იცვლება (ყველაზე ხშირად იზრდება) ტემპერატურის მატებასთან ერთად, აუცილებელია, მკაცრად რომ ვთქვათ, ფორმულის გამოყენება
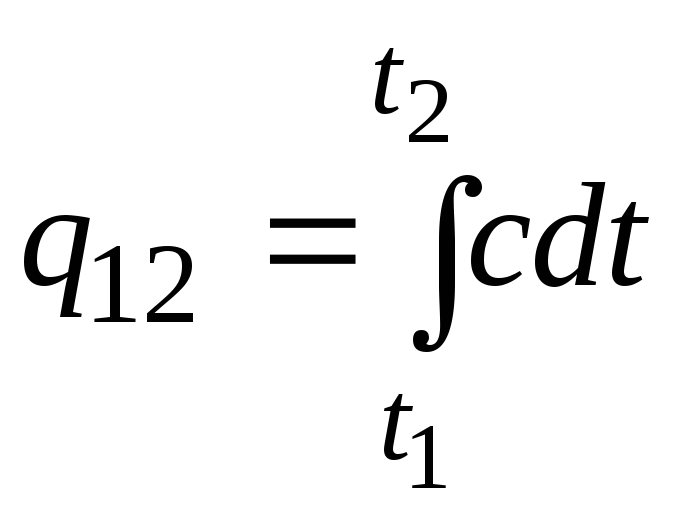 .
(2.21ა)
.
(2.21ა)
ნახ. 2.2 მაგნიტუდა ქ 12 ნაჩვენებია როგორც დაჩრდილული ადგილი. როგორც ჩანს, ყველაზე მარტივი გზა, საშუალო მნიშვნელობის თეორემის გამოყენებით, არის დაწერა
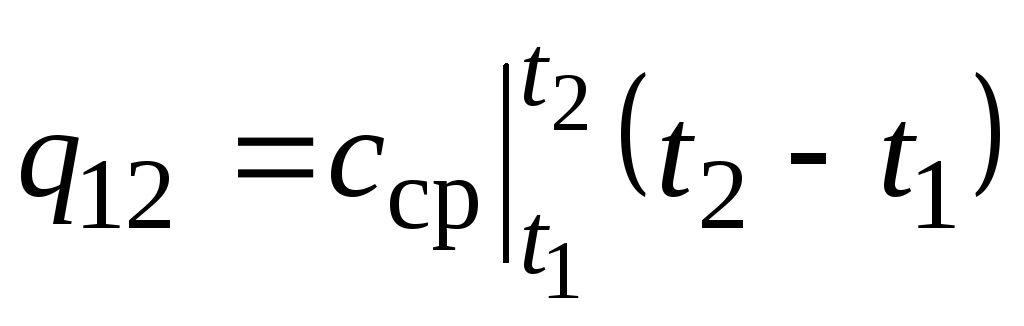 ,
(2.22)
,
(2.22)
სადაც 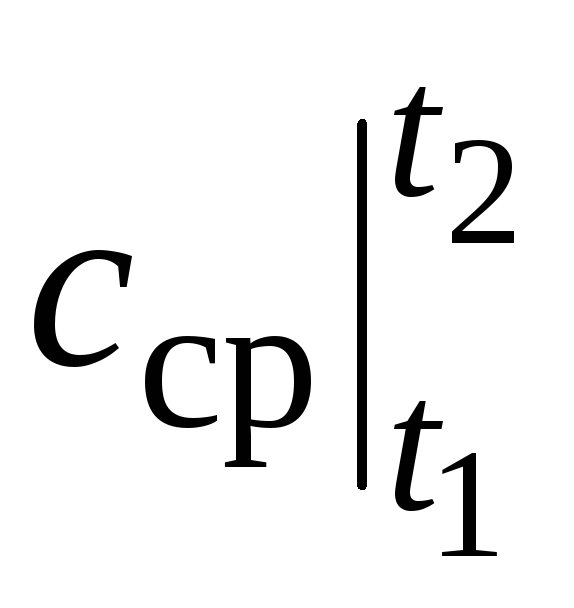 არის საშუალო სითბოს სიმძლავრე ტემპერატურის დიაპაზონში ტ 1 …ტ 2 .
არის საშუალო სითბოს სიმძლავრე ტემპერატურის დიაპაზონში ტ 1 …ტ 2 .
ბრინჯი. 2.2. ჭეშმარიტი სითბოს სიმძლავრის დამოკიდებულება ტემპერატურაზე
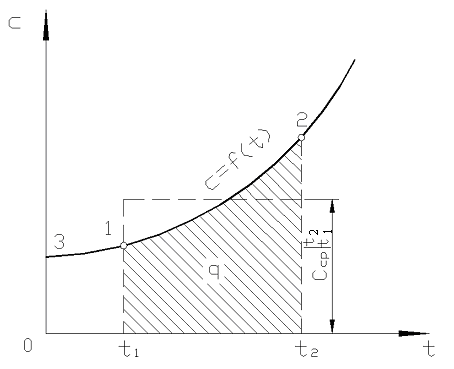
თუმცა, რეალური გამოთვლებისთვის, ასეთი აღნიშვნა ძალიან მოუხერხებელია, რადგან სითბოს სიმძლავრე არჩეულია ცხრილებიდან და 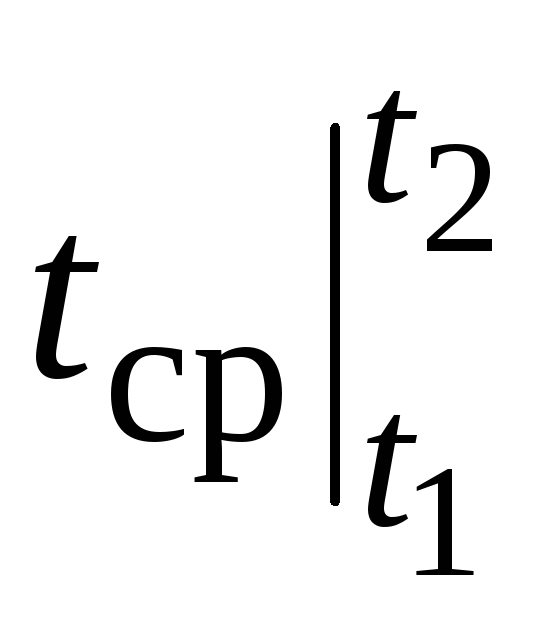 დამოკიდებულია იმაზე, თუ როგორ ტ 1 და დან ტ 2. ორი არგუმენტის ფუნქციის ცხრილი ძალიან რთული იქნება.
დამოკიდებულია იმაზე, თუ როგორ ტ 1 და დან ტ 2. ორი არგუმენტის ფუნქციის ცხრილი ძალიან რთული იქნება.
პრაქტიკაში, გააგრძელეთ შემდეგნაირად. სითბოს სასურველი რაოდენობა წარმოდგენილია როგორც სხვაობა მის რაოდენობას შორის, რომელიც საჭიროა სხეულის გასათბობად 0 С ტემპერატურამდე. ტ 2 და ტ 1 შესაბამისად (ნახ. 2.2)
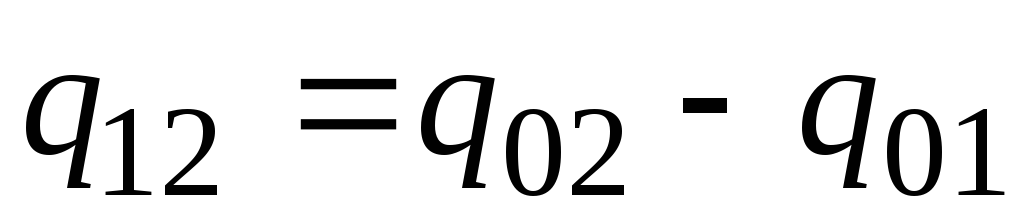 . (2.23)
. (2.23)
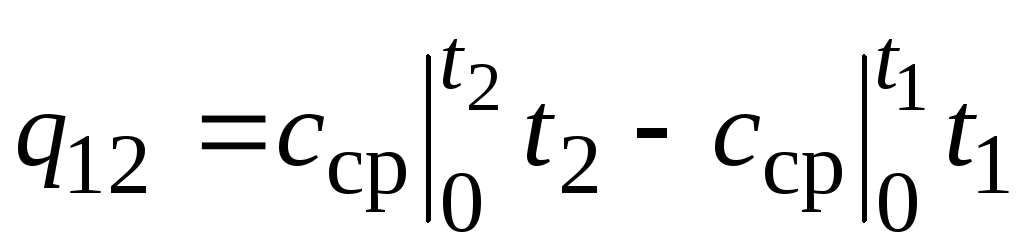 ,
(2.24)
,
(2.24)
სადაც 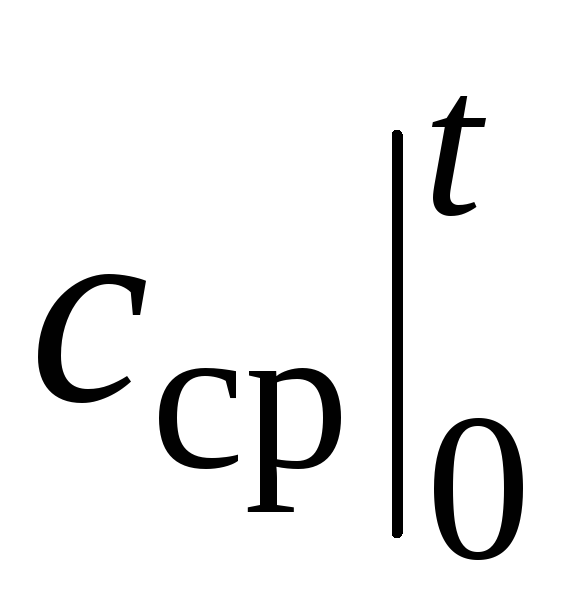 - საშუალო სითბოს სიმძლავრე ტემპერატურის დიაპაზონში 0… ტC.
- საშუალო სითბოს სიმძლავრე ტემპერატურის დიაპაზონში 0… ტC.
საშუალო სითბოს სიმძლავრის მნიშვნელობა 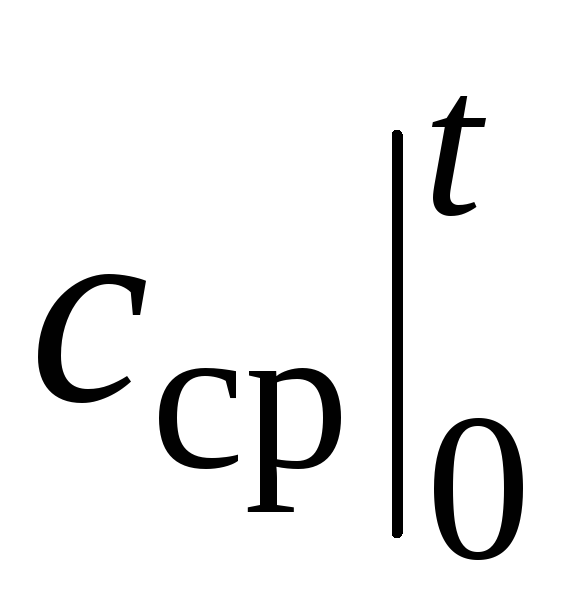 მოცემული ნივთიერებისთვის (და მოცემული პროცესისთვის, ე.ი. თან რან გ ვ) დამოკიდებულია მხოლოდ ერთ ტემპერატურაზე ტ. ეს არის სითბოს სიმძლავრეები, რომლებიც მოცემულია ყველა ცხრილში "საშუალო" სახელწოდებით. რაც ითქვა სიმართლეა თან
(თან რდა გ ვ), ასევე ამისთვის თან და თან. მაგალითად, ქვემოთ მოყვანილი ცხრილი გვიჩვენებს სითბოს სიმძლავრეს ტემპერატურის წინააღმდეგ ზოგიერთი ყველაზე გავრცელებული გაზისთვის. ხაზგასმით უნდა აღინიშნოს, რომ ფორმულაში (2.24) ტემპერატურა ჩანაცვლებულია გრადუს ცელსიუსში.
მოცემული ნივთიერებისთვის (და მოცემული პროცესისთვის, ე.ი. თან რან გ ვ) დამოკიდებულია მხოლოდ ერთ ტემპერატურაზე ტ. ეს არის სითბოს სიმძლავრეები, რომლებიც მოცემულია ყველა ცხრილში "საშუალო" სახელწოდებით. რაც ითქვა სიმართლეა თან
(თან რდა გ ვ), ასევე ამისთვის თან და თან. მაგალითად, ქვემოთ მოყვანილი ცხრილი გვიჩვენებს სითბოს სიმძლავრეს ტემპერატურის წინააღმდეგ ზოგიერთი ყველაზე გავრცელებული გაზისთვის. ხაზგასმით უნდა აღინიშნოს, რომ ფორმულაში (2.24) ტემპერატურა ჩანაცვლებულია გრადუს ცელსიუსში.
სხვადასხვა გაზების საშუალო მოლური სითბოს სიმძლავრე ზე რ=კონსტ
(მ.პ. ვუკალოვიჩის, ვ.ა. კირილინის, ვ.ნ. ტიმოფეევის მიხედვით)
|
ტ, C |
თან რ, kJ/(kmolK) |
|||||||
|
N 2 ატმოსფერული | ||||||||
ამ ცხრილში არის მნიშვნელობები თან p მოცემულია 100 С-მდე. ვინაიდან ისინი დიდად არ იცვლებიან ტემპერატურასთან ერთად, შუალედური მნიშვნელობების პოვნა შესაძლებელია ხაზოვანი ექსტრაპოლაციით. გაიხსენეთ როგორ კეთდება ეს. არსებობს ცხრილური ფუნქციის მნიშვნელობები წ
= ვ(x) ზე 1 (როდესაც X= X 1) და ზე 2 (როდესაც X= X 2). ფუნქციის ღირებულება ზე(X) ზე X 1 <X<X 2 უდრის 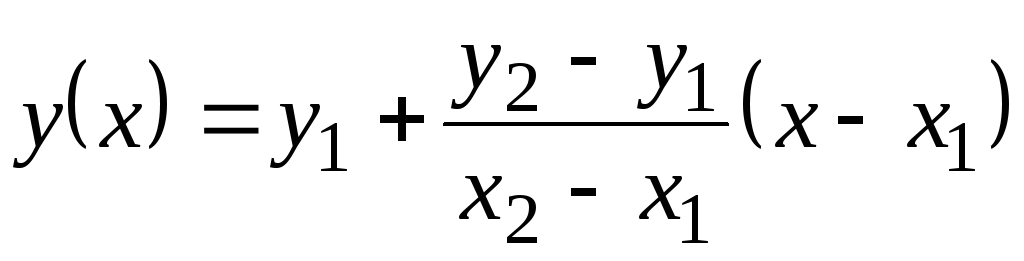 . ეს ფორმულა მართალია როგორც მონოტონურად მზარდი ფუნქციისთვის (როდესაც ზე 2 >ზე 1) და მონოტონურად შემცირებისთვის ( ზე 2 <ზეერთი); ამ შემთხვევაში, წილადი უარყოფითი იქნება, ვინაიდან X 2 > X 1 ყოველთვის.
. ეს ფორმულა მართალია როგორც მონოტონურად მზარდი ფუნქციისთვის (როდესაც ზე 2 >ზე 1) და მონოტონურად შემცირებისთვის ( ზე 2 <ზეერთი); ამ შემთხვევაში, წილადი უარყოფითი იქნება, ვინაიდან X 2 > X 1 ყოველთვის.
ცხრილი გვიჩვენებს აირების თბოგამტარობის მნიშვნელობებს ტემპერატურისა და წნევის მიხედვით.
თბოგამტარობის მნიშვნელობები მითითებულია ტემპერატურებისთვის 20 K (-253 °C) 1500 K (1227 °C) დიაპაზონში და წნევა 1-დან 1000 ატმოსფერომდე.
მაგიდა შემდეგი გაზების თბოგამტარობის გათვალისწინებით: , , ფრეონი-14 CF 4 , ეთილენი C 2 H 4 . თბოგამტარობის ერთეულია W/(m deg).
უნდა აღინიშნოს, რომ გაზების თბოგამტარობა იზრდება ტემპერატურისა და წნევის მატებასთან ერთად. მაგალითად, ამიაკის გაზის თერმული კონდუქტომეტრი ოთახის ტემპერატურაზე და ნორმალურ ატმოსფერულ წნევაზე არის 0,024 ვტ/(მ გრადუსი), ხოლო როდესაც ის თბება 300 გრადუსით, თბოგამტარობა იზრდება 0,067 ვტ/(მ გრადუსი). თუ ამ გაზის წნევა გაიზრდება 300 ატმოსფერომდე, მაშინ თბოგამტარობის მნიშვნელობა კიდევ უფრო მაღალი გახდება და ექნება მნიშვნელობა 0,108 ვტ/(მ გრადუსი).
შენიშვნა: ფრთხილად! ცხრილის თბოგამტარობა მითითებულია 10 3 კოეფიციენტით. არ დაგავიწყდეთ 1000-ზე გაყოფა!
არაორგანული აირების თბოგამტარობა დამოკიდებულია ტემპერატურაზე
ცხრილში მოცემულია არაორგანული აირების თბოგამტარობის მნიშვნელობები, რაც დამოკიდებულია ტემპერატურაზე ნორმალურ ატმოსფერულ წნევაზე. აირების თერმული კონდუქტომეტრის მნიშვნელობები მითითებულია 80-დან 1500 K ტემპერატურაზე (-193 ... 1227 ° C).
ცხრილში მოცემულია შემდეგი გაზების თბოგამტარობა: აზოტის ოქსიდი N 2 O, გოგირდის ჰექსაფტორიდი SF 6, აზოტის ოქსიდი NO, წყალბადის სულფიდი H 2 S, ამიაკი NH 3, გოგირდის დიოქსიდი SO 2, ორთქლი H 2 O, ნახშირორჟანგი CO 2 , მძიმე წყლის ორთქლი D 2 O, ჰაერი.
უნდა აღინიშნოს, რომ არაორგანული აირების თბოგამტარობა იზრდება გაზის ტემპერატურის მატებასთან ერთად.
შენიშვნა: ცხრილში აირების თბოგამტარობა მითითებულია 10 3 კოეფიციენტით. არ დაგავიწყდეთ 1000-ზე გაყოფა!
ორგანული აირების თბოგამტარობა ტემპერატურის ფუნქციის მიხედვით
ცხრილი გვიჩვენებს ორგანული აირების და ზოგიერთი სითხის ორთქლის თბოგამტარობის მნიშვნელობებს, რაც დამოკიდებულია ტემპერატურაზე ნორმალურ ატმოსფერულ წნევაზე. აირების თბოგამტარობის მნიშვნელობები მოცემულია ცხრილში 120-დან 800 კ-მდე ტემპერატურის დიაპაზონში.
მოცემულია შემდეგი ორგანული აირებისა და სითხეების თბოგამტარობა:აცეტონი CH 3 COCH 3, ოქტანი C 8 H 18, პენტანი C 5 H 12, ბუტანი C 4 H 10, ჰექსანი C 6 H 14, პროპილენი C 3 H 6, ჰეპტანი C 7 H 16, ამილის სპირტი C 5 H 11 OH, ქსილენი C 8 H 10, იზოპროპილის სპირტი C 2 H 7 OH, მეთანი CH 4, მეთილის სპირტი CH 3 OH, ნახშირბადის ტეტრაქლორიდი CCl 4, ციკლოჰექსანი C 6 H 12, ეთანი C 2 H 6, ნახშირბადის ტეტრაფტორი CF 4, ფრეონ-11 3, ეთილის ქლორიდი C 2 H 5 Cl, ფრეონი-12 CF 2 Cl 2, ეთილენი C 2 H 4, ფრეონი-13 CF 3 Cl, ეთილის ფორმატი HCOOC 2 H 5, ფრეონ-21 CHFCl 2, დიეთილის ეთერი (C 2 H 5) 2O.
როგორც ცხრილიდან ჩანს, ორგანული აირების თბოგამტარობის მნიშვნელობა ასევე იზრდება გაზის ტემპერატურის მატებასთან ერთად.
Ფრთხილად იყავი! ცხრილის თბოგამტარობა მითითებულია 10 3 კოეფიციენტით. არ დაგავიწყდეთ 1000-ზე გაყოფა!მაგალითად, აცეტონის ორთქლის თბოგამტარობა 400 K (127°C) ტემპერატურაზე არის 0,0204 W/(m deg).
