Mjeri se količina topline u sustavu. Metode i sredstva za mjerenje količine topline
Toplina- energija koja se prenosi s jače zagrijanog tijela na manje zagrijano izravnim kontaktom ili zračenjem.
Temperatura je mjera intenziteta molekularnog gibanja.
Količina topline koju posjeduje tijelo pri određenoj temperaturi ovisi o njegovoj masi; na primjer, pri istoj temperaturi, velika šalica vode sadrži više topline od male, a kanta hladne vode može sadržavati više topline od šalice Vruća voda(iako je temperatura vode u kanti niža).
Toplina ima važnu ulogu u životu čovjeka, pa tako i u funkcioniranju njegovog tijela. Dio kemijske energije sadržane u hrani pretvara se u toplinu, čime se održava tjelesna temperatura oko 37°C. Toplinska ravnoteža ljudskog tijela također ovisi o temperaturi okoliš, a ljudi su prisiljeni trošiti puno energije grijući stambene i industrijske prostore zimi i hladeći ih ljeti. Većinu te energije dobivaju toplinski strojevi, poput kotlova i parnih turbina u elektranama koje izgaraju fosilna goriva (ugljen, nafta) i proizvode električnu energiju.
Sve do kraja 18.st. toplinu smatrao materijalnom tvari, smatrajući da je temperatura tijela određena količinom koju ono sadrži<калорической жидкости>, ili<теплорода>. Kasnije su B. Rumford, J. Joule i drugi tadašnji fizičari domišljatim pokusima i razmišljanjima pobili<калорическую>teoriju, dokazujući da je toplina bestežinska i da se može dobiti u bilo kojoj količini jednostavnim mehaničkim kretanjem. Sama toplina nije tvar - to je samo energija kretanja njezinih atoma ili molekula. Upravo takvo shvaćanje topline zastupa moderna fizika.
U ovom ćemo članku pogledati kako su toplina i temperatura povezani i kako se te količine mjere. Predmet naše rasprave bit će i sljedeća pitanja: prijenos topline s jednog dijela tijela na drugi; prijenos topline u vakuumu (prostor bez tvari); uloga topline u suvremenom svijetu.
Toplina i temperatura
Količina toplinske energije u tvari ne može se odrediti promatranjem gibanja svake njezine molekule pojedinačno. Naprotiv, samo proučavanjem makroskopskih svojstava tvari mogu se pronaći karakteristike mikroskopskog gibanja mnogih molekula u prosjeku tijekom određenog vremenskog razdoblja. Temperatura tvari je prosječni pokazatelj intenziteta molekularnog gibanja, čija je energija Termalna energija tvari.
Jedan od najčešćih, ali i najmanje točnih načina za procjenu temperature je dodir. Pri dodiru predmeta procjenjujemo je li vruć ili hladan, fokusirajući se na svoje osjete. Naravno, ti osjeti ovise o temperaturi našeg tijela, što nas dovodi do pojma toplinske ravnoteže - jedne od najvažnijih pri mjerenju temperature.
Toplinska ravnoteža
Toplinska ravnoteža između tijela A i B
Očito, ako su dva tijela A i B čvrsto pritisnuta jedno uz drugo, tada ćemo nakon dovoljno dugog dodira primijetiti da im je temperatura jednaka. U tom slučaju kaže se da su tijela A i B međusobno u toplinskoj ravnoteži. No, tijela se, općenito govoreći, ne moraju nužno dodirivati da bi među njima postojala toplinska ravnoteža – dovoljno je da su im temperature iste. To se može provjeriti pomoću trećeg tijela C, prvo ga dovodeći u toplinsku ravnotežu s tijelom A, a zatim uspoređujući temperature tijela C i B. Tijelo C ovdje ima ulogu termometra. U svojoj strogoj formulaciji, ovo se načelo naziva nulti zakon termodinamike: ako su tijela A i B u toplinskoj ravnoteži s trećim tijelom C, tada su i ta tijela međusobno u toplinskoj ravnoteži. Ovaj zakon je temelj svih metoda mjerenja temperature.
Mjerenje temperature

Temperaturne ljestvice

Termometri
Termometri temeljeni na električnim efektima
Ako želimo provesti točne pokuse i izračune, onda takve ocjene temperature kao što su vruće, toplo, hladno, hladno nisu dovoljne - potrebna nam je stupnjevana temperaturna ljestvica. Postoji nekoliko takvih ljestvica, a obično se kao referentne točke uzimaju temperature smrzavanja i vrenja vode. Na slici su prikazane četiri najčešće ljestvice. Celzijeva ljestvica, prema kojoj ledište vode odgovara 0°, a vrelište 100°, zove se Celzijeva ljestvica nazvana po A. Celsiusu, švedskom astronomu koji ju je opisao 1742. Vjeruje se da je švedski prirodoslovac C. Linnaeus prvi je upotrijebio ovu ljestvicu. Sada je Celzijeva ljestvica najčešća na svijetu. Fahrenheitovu temperaturnu ljestvicu, u kojoj točke smrzavanja i vrelišta vode odgovaraju krajnje nezgodnim brojevima od 32 i 212°, predložio je Fahrenheit 1724. godine. Fahrenheitova ljestvica je raširena u zemljama engleskog govornog područja, ali se gotovo nikad ne koristi u znanstvenoj literaturi. Za pretvorbu Celzijeve temperature (°C) u temperaturu Fahrenheita (°F) postoji formula °F = (9/5)°C + 32, a za obrnutu pretvorbu postoji formula °C = (5/9)( °F- 32).
Obje ljestvice - i Fahrenheit i Celsius - vrlo su nezgodne kada se izvode pokusi u uvjetima kada temperatura pada ispod točke ledišta vode i izražava se negativnim brojem. Za takve slučajeve uvedene su apsolutne temperaturne ljestvice koje se temelje na ekstrapolaciji na tzv. apsolutnu nulu - točku u kojoj bi se molekularno gibanje trebalo zaustaviti. Jedna od njih naziva se Rankineova ljestvica, a druga apsolutna termodinamička ljestvica; Temperature se mjere u stupnjevima Rankinea (°R) i kelvinima (K). Obje ljestvice počinju na temperaturi apsolutne nule, a ledište vode odgovara 491,7°R i 273,16 K. Broj stupnjeva i kelvina između točaka smrzavanja i vrelišta vode na Celzijevoj ljestvici i apsolutnoj termodinamičkoj ljestvici isti su i jednako 100; za Fahrenheitovu i Rankineovu ljestvicu također je ista, ali jednaka 180. Celzijevi stupnjevi pretvaraju se u kelvine pomoću formule K = °C + 273,16, a stupnjevi Fahrenheita pretvaraju se u Rankineove stupnjeve pomoću formule °R = °F + 459.7.
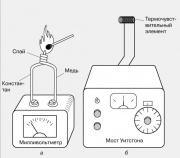
Rad instrumenata dizajniranih za mjerenje temperature temelji se na različitim fizičkim pojavama povezanim s promjenama toplinske energije tvari - promjenama u električnom otporu, volumenu, tlaku, karakteristikama emisije i termoelektričnim svojstvima. Jedan od najjednostavnijih i najpoznatijih alata za mjerenje temperature je stakleni termometar, prikazan na slici. Kuglica na dnu termometra stavi se u medij ili pritisne na predmet čija se temperatura mjeri, a ovisno o tome prima li ili odaje toplinu, širi se ili skuplja te se njezin stupac diže ili spušta u kapilari. . Ako je termometar prethodno kalibriran i opremljen ljestvicom, tada možete izravno saznati tjelesnu temperaturu.
Drugi uređaj čiji se rad temelji na toplinskom širenju je bimetalni termometar, prikazan na slici. Njegov glavni element je spiralna ploča izrađena od dva zavarena metala s različitim koeficijentima toplinskog širenja. Kada se zagrije, jedan od metala se širi više od drugog, spirala se uvija i okreće strelicu u odnosu na ljestvicu. Takvi se uređaji često koriste za mjerenje unutarnje i vanjske temperature zraka, ali nisu prikladni za određivanje lokalnih temperatura.
Lokalna temperatura obično se mjeri pomoću termoelementa, koji se sastoji od dvije žice od različitih metala zalemljene na jednom kraju. Kad se takav spoj zagrije, na slobodnim krajevima žica nastaje emf, koji obično iznosi nekoliko milivolti. Termoparovi se izrađuju od različitih metalnih parova: željezo i konstantan, bakar i konstantan, kromel i alumel. Njihova termo-emf varira gotovo linearno s temperaturom u širokom temperaturnom rasponu.
Poznat je i drugi termoelektrični učinak - ovisnost otpora vodljivog materijala o temperaturi. U osnovi je rada električnih termometara otpora, od kojih je jedan prikazan na slici. Otpor malog elementa osjetljivog na temperaturu (toplinski pretvarač) - obično zavojnica fine žice - uspoređuje se s otporom kalibriranog promjenjivog otpornika pomoću Wheatstoneovog mosta. Izlazni uređaj može se izravno kalibrirati u stupnjevima.
Optički pirometri koriste se za mjerenje temperature vrućih tijela koja emitiraju vidljivu svjetlost. U jednoj izvedbi ovog uređaja, svjetlost koju emitira tijelo uspoređuje se sa emisijom žarne niti žarulje sa žarnom niti postavljene u žarišnoj ravnini dalekozora kroz koji se gleda tijelo koje emitira. Električna struja koja grije žarnu nit mijenja se sve dok se vizualnom usporedbom sjaja žarne niti i tijela ne utvrdi da je između njih uspostavljena toplinska ravnoteža. Skala instrumenta može se kalibrirati izravno u temperaturnim jedinicama.
Tehnički napredak zadnjih godina omogućio stvaranje novih temperaturnih senzora. Na primjer, u slučajevima kada je potrebna posebno visoka osjetljivost, umjesto termoelementa ili konvencionalnog termometra otpora, koristi se poluvodički uređaj - termistor. Boje i tekući kristali koji mijenjaju svoje fazno stanje također se koriste kao toplinski pretvarači, posebno u slučajevima kada temperatura površine tijela varira u širokom rasponu. Na kraju, koristi se infracrvena termografija, koja proizvodi infracrvenu sliku objekta u lažnim bojama, pri čemu svaka boja odgovara određenoj temperaturi. Ova metoda mjerenja temperature nalazi najširu primjenu - od medicinska dijagnostika prije provjere toplinske izolacije prostorija.
Mjerenje topline
Vodeni kalorimetar
Toplinska energija (količina topline) tijela može se izravno izmjeriti pomoću onoga što se zove kalorimetar; jednostavna verzija takvog uređaja prikazana je na slici. Ovo je pažljivo izolirana zatvorena posuda, opremljena uređajima za mjerenje temperature unutar nje i ponekad ispunjena radnom tekućinom s poznatim svojstvima, poput vode. Za mjerenje količine topline u malom zagrijanom tijelu ono se stavlja u kalorimetar i čeka se dok sustav ne postigne toplinsku ravnotežu. Količina topline predana kalorimetru (točnije vodi koja ga puni) određena je porastom temperature vode.
Količina topline koja se oslobađa tijekom kemijske reakcije, kao što je izgaranje, može se izmjeriti stavljanjem male<бомбу>. U<бомбе>postoji uzorak na koji su spojene električne žice za paljenje i odgovarajuća količina kisika. Nakon što uzorak potpuno izgori i uspostavi se toplinska ravnoteža, utvrđuje se koliko je porasla temperatura vode u kalorimetru, a time i količina oslobođene topline.
Toplinske jedinice
Toplina je oblik energije i stoga se mora mjeriti u energetskim jedinicama. SI jedinica za energiju je džul (J). Također je moguće koristiti nesustavne jedinice količine topline - kalorije: međunarodna kalorija je 4,1868 J, termokemijska kalorija - 4,1840 J. U stranim laboratorijima rezultati istraživanja često se izražavaju pomoću tzv. Kalorija od 15 stupnjeva jednaka je 4,1855 J. Britanska termalna jedinica izvan sustava (BTU) postupno se ukida: BTU prosječno = 1,055 J.
Izvori topline
Glavni izvori topline su kemijske i nuklearne reakcije, kao i razni procesi pretvorbe energije. Primjeri kemijskih reakcija koje oslobađaju toplinu su izgaranje i razgradnja komponenti hrane. Gotovo svu toplinu koju prima Zemlja dobivaju nuklearne reakcije koje se odvijaju u dubinama Sunca. Čovječanstvo je naučilo dobivati toplinu koristeći kontrolirane procese nuklearne fisije, a sada pokušava koristiti reakcije termonuklearne fuzije za istu svrhu. Druge vrste energije, poput mehaničkog rada i električne energije, također se mogu pretvoriti u toplinu. Važno je zapamtiti da se toplinska energija (kao i svaka druga) može samo pretvoriti u drugi oblik, ali se ne može primiti<из ничего>, niti uništiti. Ovo je jedno od osnovnih načela znanosti zvane termodinamika.
Termodinamika
Termodinamika je znanost o odnosu između topline, rada i materije. Suvremene ideje o tim odnosima formirane su na temelju radova tako velikih znanstvenika prošlosti kao što su Carnot, Clausius, Gibbs, Joule, Kelvin itd. Termodinamika objašnjava značenje toplinskog kapaciteta i toplinske vodljivosti tvari, toplinskog širenja tijela. , i toplina faznih prijelaza. Ova znanost temelji se na nekoliko eksperimentalno utvrđenih zakona – principa.
Toplina i svojstva tvari
Razne tvari imaju različite sposobnosti akumulacije toplinske energije; to ovisi o njihovoj molekularnoj strukturi i gustoći. Količina topline potrebna za povećanje temperature jedinice mase tvari za jedan stupanj naziva se njezin specifični toplinski kapacitet. Toplinski kapacitet ovisi o uvjetima u kojima se tvar nalazi. Na primjer, za zagrijavanje jednog grama zraka u balonu za 1 K potrebno je više topline nego za isto zagrijavanje u zatvorenoj posudi s krutim stijenkama, budući da se dio energije predane balonu troši na širenje zraka, a ne na zagrijavanju. Stoga se posebno mjeri toplinski kapacitet plinova pri stalnom tlaku i pri stalnom volumenu.
S porastom temperature povećava se i intenzitet kaotičnog kretanja molekula – većina tvari se zagrijavanjem širi. Naziva se stupanj širenja tvari pri porastu temperature za 1 K koeficijent toplinske ekspanzije.
Da bi tvar prešla iz jednog faznog stanja u drugo, na primjer iz krutog u tekuće (a ponekad i izravno u plinovito), mora primiti određenu količinu topline. Ako se grije čvrsta, tada će mu temperatura rasti dok se ne počne topiti; dok se topljenje ne završi, temperatura tijela ostat će konstantna, unatoč dodavanju topline. Količina topline potrebna za taljenje jedinice mase tvari naziva se toplina taljenja. Ako dalje zagrijavate, rastaljena će se tvar zagrijati do vrenja. Količina topline potrebna za isparavanje jedinice mase tekućine pri određenoj temperaturi naziva se toplina isparavanja.
Uloga topline i njezino korištenje
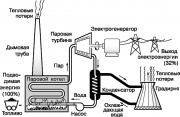
Shema rada parnoturbinske elektrane
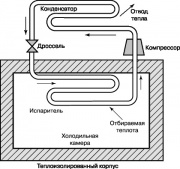
Dijagram ciklusa hlađenja
Globalni procesi izmjene topline nisu ograničeni na zagrijavanje Zemlje sunčevim zračenjem. Masivna konvekcijska strujanja u atmosferi određuju dnevne promjene vremenskih uvjeta diljem svijeta. Promjene temperature u atmosferi između ekvatorijalnih i polarnih područja, zajedno s Coriolisovim silama uzrokovanim rotacijom Zemlje, dovode do pojave kontinuirano promjenjivih konvekcijskih struja, kao što su pasati, mlazne struje te tople i hladne fronte.
Prijenos topline (zbog toplinske vodljivosti) iz rastaljene jezgre Zemlje na njezinu površinu dovodi do vulkanskih erupcija i pojave gejzira. U nekim se regijama geotermalna energija koristi za grijanje prostora i proizvodnju električne energije.
Toplina je neizostavan dio gotovo svakoga proizvodni procesi. Spomenimo najvažnije među njima, kao što su taljenje i obrada metala, rad motora, proizvodnja hrane, kemijska sinteza, prerada nafte te proizvodnja najrazličitijih predmeta – od opeke i posuđa do automobila i elektroničkih uređaja.
Mnoge industrijske proizvodnje i transporta, kao i termoelektrane, ne bi mogle raditi bez toplinskih strojeva – uređaja koji toplinu pretvaraju u koristan rad. Primjeri takvih strojeva uključuju kompresore, turbine, parne, benzinske i mlazne motore.
Jedan od najpoznatijih toplinskih motora je parna turbina, koja implementira dio Rankineovog ciklusa koji se koristi u modernim elektranama. Pojednostavljeni dijagram ovog ciklusa prikazan je na slici. Radni fluid – voda – pretvara se u pregrijanu paru u parnom kotlu, koja se zagrijava izgaranjem fosilnih goriva (ugljen, nafta ili prirodni plin). Velika para
Gazovik - industrijska plinska oprema Priručnik GOST, SNiP, PB Jedinice fizičkih veličina, fizički i kemijski koncepti, odnosi, sastav i karakteristike plinova
Mjerne jedinice za temperaturu i količinu topline
Osnovna jedinica za mjerenje temperature bio je stupanj Međunarodne temperaturne ljestvice, što je gotovo jednako Celzijevom stupnju. Ova vrijednost jednaka je 1/100 temperaturnog intervala između 0 i 100 °C, tj. između temperature taljenja leda i vrelišta vode pri tlaku od 760 mm Hg. Umjetnost.
Apsolutna temperatura je temperatura mjerena od apsolutne nule, tj. –273,16 °C, i mjerena u stupnjevima Kelvina (°K). Kelvinov stupanj ne razlikuje se po veličini od Celzijusovog stupnja. Stoga se apsolutna temperatura izražava u stupnjevima Celzijusa na ljestvici kako slijedi:
T, °K = t, °C + 273,16
SI jedinica za temperaturu je Kelvinov stupanj. Dopušteno je koristiti stupanj Celzijusa uz stupanj Kelvina za izražavanje praktičnih rezultata mjerenja temperature, ovisno o ishodištu (nulti položaj) na ljestvici.
Primjer: 250 ±5 °C = 523,16 ±5 °K.
U SI sustavu rad, energija i toplina mjere se u džulima (J). Ponekad se koristi veća i praktičnija jedinica za praktične svrhe - kilojoule (kJ), jednaka 1000 J. SI jedinica za rad uzima se kao rad koji izvrši sila od 1 N da se pomakne 1 m. Energija - fizička količina, pokazujući koliki rad tijelo može obaviti.
Kalorije i kilokalorije mogu se koristiti kao izvansistemske toplinske jedinice. Kalorija je količina topline potrebna za zagrijavanje 1 g vode za 1 °C (od 19,5 do 20,5 °C).
1 kal (kalorija) = 4,1868 J;
1 kcal (kilokalorija) = 1000 cal = 4186,8 J = 4,187 kJ;
1 Mcal (megakalorija) = 10 6 cal = 4,1868 MJ;
1 Gcal (gigakalorija) = 10 9 cal = 4186,8 MJ.
Za usporedbu, pri procjeni goriva koristi se takozvana konvencionalna toplina, čija se kalorijska vrijednost za izračun pretpostavlja uvjetno jednakom 7 Mcal/kg ili 7 Gcal/t. U takvim slučajevima govorimo o 1 kg odnosno 1 toni standardnog goriva (t.e.f.).
Toplina ima važnu ulogu u životu čovjeka, pa tako i u funkcioniranju njegovog tijela. Dio kemijske energije sadržane u hrani pretvara se u toplinu, čime se održava tjelesna temperatura oko 37
° C. Toplinska ravnoteža ljudskog tijela također ovisi o temperaturi okoline, a ljudi su prisiljeni trošiti mnogo energije grijući stambene i industrijske prostore zimi i hladeći ih ljeti. Većinu te energije dobivaju toplinski strojevi, poput kotlova i parnih turbina u elektranama koje izgaraju fosilna goriva (ugljen, nafta) i proizvode električnu energiju.Sve do kraja 18.st. toplinu su smatrali materijalnom supstancom, vjerujući da je temperatura tijela određena količinom "kalorične tekućine" ili "kalorija" koje sadrži. Kasnije su B. Rumford, J. Joule i drugi tadašnji fizičari domišljatim pokusima i zaključivanjem opovrgnuli “kaloričnu” teoriju, dokazujući da je toplina bestežinska i da se jednostavno mehaničkim kretanjem može dobiti u bilo kojoj količini. Sama toplina nije tvar; to je samo energija kretanja njezinih atoma ili molekula. Upravo takvo shvaćanje topline zastupa moderna fizika. vidi također FIZIKA.
U ovom ćemo članku pogledati kako su toplina i temperatura povezani i kako se te količine mjere. Predmet naše rasprave bit će i sljedeća pitanja: prijenos topline s jednog dijela tijela na drugi; prijenos topline u vakuumu (prostor bez tvari); uloga topline u suvremenom svijetu.
TOPLINA I TEMPERATURA Količina toplinske energije u tvari ne može se odrediti promatranjem gibanja svake njezine molekule pojedinačno. Naprotiv, samo proučavanjem makroskopskih svojstava tvari mogu se pronaći karakteristike mikroskopskog gibanja mnogih molekula u prosjeku tijekom određenog vremenskog razdoblja. Temperatura tvari je prosječni pokazatelj intenziteta molekularnog gibanja, čija je energija toplinska energija tvari.Jedan od najčešćih, ali i najmanje točnih načina za procjenu temperature je dodir. Pri dodiru predmeta procjenjujemo je li vruć ili hladan, fokusirajući se na svoje osjete. Naravno, ti osjeti ovise o temperaturi našeg tijela, što nas dovodi do pojma toplinske ravnoteže, jednog od najvažnijih kod mjerenja temperature.
Toplinska ravnoteža. Očito, ako dva tijela A i B (Sl. 1) čvrsto pritisnuti jedan uz drugi, tada ćemo nakon dovoljno dugog vremena dodirivanja primijetiti da im je temperatura jednaka. U ovom slučaju kažu da tijela A i B međusobno su u toplinskoj ravnoteži. No, tijela se, općenito govoreći, ne moraju nužno dodirivati da bi među njima postojala toplinska ravnoteža, dovoljno je da su im temperature iste. To se može provjeriti pomoću trećeg tijela C , dovodeći ga prvo u toplinsku ravnotežu s tijelom A , a zatim uspoređujući tjelesne temperature C i B. Tijelo C ovdje igra ulogu termometra. U strogoj formulaciji, ovo se načelo naziva nulti zakon termodinamike: ako su tijela A i B u toplinskoj ravnoteži s trećim tijelom C, tada su i ta tijela međusobno u toplinskoj ravnoteži. Ovaj zakon je temelj svih metoda mjerenja temperature.Mjerenje temperature. Ako želimo provoditi točne pokuse i izračune, onda temperaturne ocjene kao što su vruće, toplo, hladno, hladno nisu dovoljne; potrebna nam je stupnjevana temperaturna ljestvica. Postoji nekoliko takvih ljestvica, a obično se kao referentne točke uzimaju temperature smrzavanja i vrenja vode. Četiri najčešće ljestvice prikazane su na sl. 2. Celzijeva ljestvica, na kojoj ledište vode odgovara 0° , a vrelište je 100° , naziva se Celzijeva ljestvica po A. Celsiusu, švedskom astronomu koji ju je opisao 1742. godine. Vjeruje se da je švedski prirodoslovac C. Linnaeus prvi upotrijebio ovu ljestvicu. Sada je Celzijeva ljestvica najčešća na svijetu. Fahrenheitova temperaturna ljestvica, u kojoj točke smrzavanja i vrelišta vode odgovaraju krajnje nezgodnim brojevima 32 i 212° , predložio je 1724. G. Fahrenheit. Fahrenheitova ljestvica je raširena u zemljama engleskog govornog područja, ali se gotovo nikad ne koristi u znanstvenoj literaturi. Za pretvaranje temperature u Celzijuse (° C) na temperaturu Fahrenheita (° F) postoji formula°F = (9/5) ° C + 32, a za formulu obrnutog prijevoda°C = (5/9) (°F - 32). Obje ljestvice, Fahrenheit i Celsius, vrlo su nezgodne kada se izvode pokusi u uvjetima kada temperatura pada ispod točke ledišta vode i izražava se negativnim brojem. Za takve slučajeve uvedene su apsolutne temperaturne ljestvice koje se temelje na ekstrapolaciji na takozvanu apsolutnu nulu, točku u kojoj bi molekularno gibanje trebalo prestati. Jedna od njih naziva se Rankineova ljestvica, a druga apsolutna termodinamička ljestvica; njihove se temperature mjere u Rankineovim stupnjevima (° R) i kelvina (K). Obje ljestvice počinju na apsolutnoj nuli, a ledište vode odgovara 491,7° R i 273,16 K. Broj stupnjeva i kelvina između ledišta i vrelišta vode na Celzijevoj ljestvici i apsolutnoj termodinamičkoj ljestvici isti su i jednaki 100; za Fahrenheitovu i Rankineovu ljestvicu također je ista, ali jednaka 180. Celzijevi stupnjevi pretvaraju se u kelvine pomoću formule K =° C + 273,16, i stupnjeva Fahrenheita do stupnjeva Rankinea prema formuli°R = °F + 459,7. Rad instrumenata dizajniranih za mjerenje temperature temelji se na različitim fizičkim pojavama povezanim s promjenama toplinske energije tvari, promjenama u električnom otporu, volumenu, tlaku, karakteristikama emisije i termoelektričnim svojstvima. Jedan od najjednostavnijih i najpoznatijih instrumenata za mjerenje temperature je živin stakleni termometar, prikazan na sl. 3, A. Kuglica žive u donjem dijelu termometra stavi se u medij ili pritisne na predmet čija se temperatura mjeri, a ovisno o tome prima li kuglica ili odaje toplinu, živa se širi ili skuplja te se njezin stupac diže ili pada u kapilaru. Ako je termometar prethodno kalibriran i opremljen ljestvicom, tada možete izravno saznati tjelesnu temperaturu.Drugi uređaj čiji se rad temelji na toplinskom širenju je bimetalni termometar prikazan na sl.
3, b. Njegov glavni element spiralna ploča od dva zavarena metala s različitim koeficijentima toplinskog rastezanja. Kada se zagrije, jedan od metala se širi više od drugog, spirala se uvija i okreće strelicu u odnosu na ljestvicu. Takvi se uređaji često koriste za mjerenje unutarnje i vanjske temperature zraka, ali nisu prikladni za određivanje lokalnih temperatura.Lokalna temperatura obično se mjeri pomoću termopara, koji se sastoji od dvije žice od različitih metala zalemljene na jednom kraju (Sl.
4, A). Kada se takav spoj zagrijava, na slobodnim krajevima žica stvara se EMF, obično u iznosu od nekoliko milivolti. Termoparovi se izrađuju od različitih metalnih parova: željezo i konstantan, bakar i konstantan, kromel i alumel. Njihova termo-emf varira gotovo linearno s temperaturom u širokom temperaturnom rasponu.Poznat je i drugi termoelektrični učinak: ovisnost otpora vodljivog materijala o temperaturi. U osnovi je rada termometara električnog otpora, od kojih je jedan prikazan na sl.
4, b. Otpor malog elementa osjetljivog na temperaturu (toplinskog pretvarača), obično zavojnice tanke žice, uspoređuje se s otporom kalibriranog promjenjivog otpornika pomoću Wheatstoneovog mosta. Izlazni uređaj može se izravno kalibrirati u stupnjevima.Optički pirometri koriste se za mjerenje temperature vrućih tijela koja emitiraju vidljivu svjetlost. U jednoj izvedbi ovog uređaja, svjetlost koju emitira tijelo uspoređuje se sa emisijom žarne niti žarulje sa žarnom niti postavljene u žarišnoj ravnini dalekozora kroz koji se gleda tijelo koje emitira. Električna struja koja grije žarnu nit mijenja se sve dok se vizualnom usporedbom sjaja žarne niti i tijela ne utvrdi da je između njih uspostavljena toplinska ravnoteža. Skala instrumenta može se kalibrirati izravno u temperaturnim jedinicama.
Tehnički napredak posljednjih godina omogućio je stvaranje novih temperaturnih senzora. Na primjer, u slučajevima kada je potrebna posebno visoka osjetljivost, umjesto termoelementa ili konvencionalnog otpornog termometra, koristi se poluvodički uređaj, termistor. Boje i tekući kristali koji mijenjaju svoje fazno stanje također se koriste kao toplinski pretvarači, posebno u slučajevima kada temperatura površine tijela varira u širokom rasponu. Na kraju, koristi se infracrvena termografija, koja proizvodi infracrvenu sliku objekta u lažnim bojama, pri čemu svaka boja odgovara određenoj temperaturi. Ova metoda mjerenja temperature nalazi najširu primjenu od medicinske dijagnostike do provjere toplinske izolacije prostorija. vidi također FIZIKA ČVRSTOG STANJA; TEKUĆI KRISTAL.
Mjerenje količine topline. Toplinska energija (količina topline) tijela može se izravno mjeriti pomoću tzv. kalorimetra; jednostavna verzija takvog uređaja prikazana je na sl. 5. Ovo je pažljivo izolirana zatvorena posuda, opremljena uređajima za mjerenje temperature unutar nje i ponekad ispunjena radnom tekućinom s poznatim svojstvima, poput vode. Za mjerenje količine topline u malom zagrijanom tijelu ono se stavlja u kalorimetar i čeka se dok sustav ne postigne toplinsku ravnotežu. Količina topline predana kalorimetru (točnije vodi koja ga puni) određena je porastom temperature vode.Količina topline koja se oslobađa tijekom kemijske reakcije, kao što je izgaranje, može se izmjeriti stavljanjem male "bombe" u kalorimetar. “Bomba” sadrži uzorak na koji su spojene električne žice za paljenje i odgovarajuću količinu kisika. Nakon što uzorak potpuno izgori i uspostavi se toplinska ravnoteža, utvrđuje se koliko je porasla temperatura vode u kalorimetru, a time i količina oslobođene topline. vidi također KALORIMETRIJA.
Mjerne jedinice topline. Toplina je oblik energije i stoga se mora mjeriti u energetskim jedinicama. SI jedinica za energiju je džul (J). Također je moguće koristiti nesistemske jedinice količine topline kalorije: međunarodna kalorija je 4,1868 J, termokemijska kalorija 4,1840 J. U inozemnim laboratorijima rezultati istraživanja često se izražavaju pomoću tzv. Kalorija od 15 stupnjeva jednaka je 4,1855 J. Britanska termalna jedinica izvan sustava (BTU) postupno se ukida: BTU prosječno = 1,055 J. Glavni izvori topline su kemijske i nuklearne reakcije, kao i razni procesi pretvorbe energije. Primjeri kemijskih reakcija koje oslobađaju toplinu su izgaranje i razgradnja komponenti hrane. Gotovo svu toplinu koju prima Zemlja dobivaju nuklearne reakcije koje se odvijaju u dubinama Sunca. Čovječanstvo je naučilo dobivati toplinu koristeći kontrolirane procese nuklearne fisije, a sada pokušava koristiti reakcije termonuklearne fuzije za istu svrhu. Druge vrste energije, poput mehaničkog rada i električne energije, također se mogu pretvoriti u toplinu. Važno je zapamtiti da se toplinska energija (kao i svaka druga) može samo pretvoriti u drugi oblik, ali se ne može dobiti “ni iz čega” ili uništiti. Ovo je jedno od osnovnih načela znanosti zvane termodinamika. TERMODINAMIKA Termodinamika je znanost o odnosu između topline, rada i materije. Suvremene ideje o tim odnosima formirane su na temelju radova tako velikih znanstvenika prošlosti kao što su Carnot, Clausius, Gibbs, Joule, Kelvin itd. Termodinamika objašnjava značenje toplinskog kapaciteta i toplinske vodljivosti tvari, toplinskog širenja tijela. , i toplina faznih prijelaza. Ova se znanost temelji na nekoliko eksperimentalno utvrđenih zakona i principa.Počeci termodinamike. Gore formulirani nulti zakon termodinamike uvodi koncepte toplinske ravnoteže, temperature i termometrije. Prvi zakon termodinamike tvrdnja je od ključne važnosti za cjelokupnu znanost u cjelini: energija se ne može niti uništiti niti dobiti „ni iz čega“, stoga je ukupna energija Svemira konstantna veličina. U svom najjednostavnijem obliku, prvi zakon termodinamike može se izraziti na sljedeći način: energija koju sustav prima minus energija koju daje jednaka je energiji koja ostaje u sustavu. Na prvi pogled ova izjava izgleda očita, ali nije tako, na primjer, situacijama kao što je izgaranje benzina u cilindrima automobilskog motora: ovdje je primljena energija kemijska, otpuštena energija je mehanička (rad), a energija koja ostaje u sustavu je toplinska.Dakle, jasno je da se energija može transformirati iz jednog oblika u drugi i da se takve transformacije stalno događaju u prirodi i tehnologiji. Prije više od sto godina J. Joule je to dokazao za slučaj pretvaranja mehaničke energije u toplinsku pomoću uređaja prikazanog na Sl. 6, A. U ovom uređaju, utezi koji su se spuštali i dizali okretali su osovinu s oštricama u kalorimetru ispunjenom vodom, uzrokujući zagrijavanje vode. Precizna mjerenja omogućila su Jouleu da utvrdi da je jedna kalorija topline ekvivalentna 4,186 J mehaničkog rada. Uređaj prikazan na Sl.
6, b, korišten je za određivanje toplinskog ekvivalenta električne energije.Prvi zakon termodinamike objašnjava mnoge svakodnevne pojave. Na primjer, postaje jasno zašto ne možete hladiti kuhinju s otvorenim hladnjakom. Pretpostavimo da smo kuhinju izolirali od okoline. Energija se kontinuirano dovodi u sustav preko žice za napajanje hladnjaka, ali sustav ne oslobađa nikakvu energiju. Tako se njegova ukupna energija povećava, a kuhinja postaje sve toplija: samo dotaknite cijevi izmjenjivača topline (kondenzatora) na stražnjoj stijenci hladnjaka i shvatit ćete beskorisnost toga kao uređaja za "hlađenje". Ali ako se te cijevi izvedu izvan sustava (na primjer, izvan prozora), tada bi kuhinja dala više energije nego što je primila, tj. hladio bi, a hladnjak bi radio kao prozorski klima uređaj.
Prvi zakon termodinamike je zakon prirode koji isključuje stvaranje ili uništavanje energije. Međutim, ne govori ništa o tome kako se odvijaju procesi prijenosa energije u prirodi. Dakle, znamo da će vruće tijelo zagrijati hladno ako se ta tijela dovedu u kontakt. Ali može li hladno tijelo samo prenijeti svoju toplinsku rezervu na vruće? Posljednja prilika kategorički odbacuje drugi zakon termodinamike.
Prvi zakon također isključuje mogućnost stvaranja motora s koeficijentom korisna radnja(učinkovitost) više od 100% (slično
"vječni" motor bi proizvoljno dugo mogao opskrbljivati više energije nego što sam troši). Nemoguće je izgraditi motor čak i s učinkovitošću od 100%, budući da dio energije koja mu se isporučuje mora nužno biti izgubljen u obliku manje korisne toplinske energije. Dakle, kotač se neće dugo vrtjeti bez napajanja energijom, jer će se zbog trenja u ležajevima energija mehaničkog kretanja postupno pretvarati u toplinu sve dok se kotač ne zaustavi.Tendencija pretvaranja "korisnog" rada u manje korisnu energiju toplinu može se usporediti s drugim procesom koji se događa kada se spoje dvije posude koje sadrže različite plinove. Nakon dovoljno dugog čekanja nalazimo homogenu smjesu plinova u obje posude, priroda djeluje tako da se red sustava smanjuje. Termodinamička mjera tog poremećaja naziva se entropija, a drugi zakon termodinamike može se drugačije formulirati: procesi u prirodi uvijek se odvijaju tako da entropija sustava i okoline raste. Dakle, energija svemira ostaje konstantna, ali njegova entropija kontinuirano raste.
Toplina i svojstva tvari. Različite tvari imaju različite sposobnosti pohranjivanja toplinske energije; to ovisi o njihovoj molekularnoj strukturi i gustoći. Količina topline potrebna da se jedinica mase tvari povisi za jedan stupanj temperature naziva se njezina specifični toplinski kapacitet. Toplinski kapacitet ovisi o uvjetima u kojima se tvar nalazi. Na primjer, za zagrijavanje jednog grama zraka u balonu za 1 K potrebno je više topline nego za isto zagrijavanje u zatvorenoj posudi s krutim stijenkama, budući da se dio energije predane balonu troši na širenje zraka, a ne na zagrijavanju. Stoga se posebno mjeri toplinski kapacitet plinova pri stalnom tlaku i pri stalnom volumenu.Kako temperatura raste, intenzitet kaotičnog kretanja molekula raste, većina tvari se širi kada se zagrijava. Stupanj širenja tvari pri porastu temperature za 1 K naziva se koeficijent toplinskog širenja.
Da bi tvar prešla iz jednog faznog stanja u drugo, na primjer iz krutog u tekuće (a ponekad i izravno u plinovito), mora primiti određenu količinu topline. Ako zagrijete krutinu, njezina temperatura će se povećavati sve dok se ne počne topiti; dok se topljenje ne završi, temperatura tijela ostat će konstantna, unatoč dodavanju topline. Količina topline potrebna za taljenje jedinice mase tvari naziva se toplina taljenja. Ako dalje zagrijavate, rastaljena će se tvar zagrijati do vrenja. Količina topline potrebna za isparavanje jedinice mase tekućine pri određenoj temperaturi naziva se toplina isparavanja.
Molekularno kinetička teorija. Molekularno-kinetička teorija objašnjava makroskopska svojstva tvari razmatrajući na mikroskopskoj razini ponašanje atoma i molekula koje čine tu tvar. U ovom slučaju koristi se statistički pristup i donose se neke pretpostavke o samim česticama i prirodi njihova kretanja. Stoga se molekule smatraju čvrstim kuglicama, koje su u plinovitim medijima u kontinuiranom kaotičnom gibanju i prelaze znatne udaljenosti od jednog sudara do drugog. Sudari se smatraju elastičnima i događaju se između čestica čija je veličina mala, ali njihov broj je vrlo velik. Niti jedan od stvarnih plinova ne odgovara potpuno ovom modelu, ali većina plinova mu je prilično blizu, što određuje praktičnu vrijednost molekularne kinetičke teorije.Na temelju tih ideja i korištenjem statističkog pristupa, Maxwell je izveo distribuciju brzina molekula plina u ograničenom volumenu, koja je kasnije nazvana po njemu. Ova raspodjela je grafički prikazana na sl. 7 za određenu masu vodika na temperaturama 100 i 1000
° C. Os ordinata predstavlja broj molekula koje se kreću brzinom naznačenom na osi apscisa. Ukupan broj čestica jednak je površini ispod svake krivulje i isti je u oba slučaja. Grafikon pokazuje da većina čestica ima brzine blizu neke prosječne vrijednosti, a samo mali broj ima vrlo velike ili niske brzine. Prosječne brzine pri navedenim temperaturama leže u rasponu od 20003000 m/s, tj. vrlo velika.Velik broj tako brzih molekula plina djeluje prilično mjerljivom silom na okolna tijela. Mikroskopske sile kojima brojne molekule plina udaraju o stijenke spremnika čine makroskopsku veličinu koja se naziva tlak. Kada se plinu dovede energija (temperatura raste), prosječna kinetička energija njegovih molekula se povećava, čestice plina češće i jače udaraju o stijenke, raste tlak, a ako stijenke nisu potpuno krute, onda se istežu i volumen se povećava. plina se povećava. Dakle, mikroskopski statistički pristup koji je u osnovi molekularne kinetičke teorije omogućuje nam da objasnimo fenomen toplinskog širenja o kojem smo raspravljali.
Drugi rezultat molekularne kinetičke teorije je zakon koji opisuje svojstva plina koji zadovoljava gore navedene zahtjeve. To je takozvana jednadžba stanja idealni plin povezuje tlak, volumen i temperaturu jednog mola plina i ima oblik jednakosti
PV = RT, gdje je P pritisak, V volumen, T temperatura, i R univerzalna plinska konstanta jednaka (8,31441± 0,00026) J/(mol H DO). vidi također MOLEKULARNA KINETIČKA TEORIJA; TERMODINAMIKA. PRIJENOS TOPLINE Prijenos topline je proces prijenosa topline unutar tijela ili s jednog tijela na drugo zbog temperaturnih razlika. Intenzitet prijenosa topline ovisi o svojstvima tvari, temperaturnoj razlici i pokorava se eksperimentalno utvrđenim zakonima prirode. Da biste stvorili učinkovite sustave grijanja ili hlađenja, različite motore, elektrane i sustave toplinske izolacije, morate poznavati principe prijenosa topline. U nekim slučajevima izmjena topline je nepoželjna (toplinska izolacija peći za taljenje, svemirskih brodova i sl.), dok u drugima treba biti što veća (parni kotlovi, izmjenjivači topline, kuhinjsko posuđe).Postoje tri glavne vrste prijenosa topline: kondukcija, konvekcija i prijenos topline zračenjem.
Toplinska vodljivost. Ako unutar tijela postoji temperaturna razlika, tada toplinska energija prelazi iz toplijeg dijela tijela u hladniji dio. Ova vrsta prijenosa topline, uzrokovana toplinskim gibanjima i sudarima molekula, naziva se toplinska vodljivost; s dovoljno visoke temperature u krutim tvarima može se uočiti vizualno. Dakle, kada se čelična šipka zagrije s jednog kraja u plamenu plinskog plamenika, toplinska energija se prenosi duž šipke, a sjaj se širi na određenoj udaljenosti od zagrijanog kraja (sve slabijim s udaljenošću od mjesta zagrijavanja). ).Intenzitet prijenosa topline zbog toplinske vodljivosti ovisi o temperaturnom gradijentu, tj. odnos
D T/D x temperaturna razlika na krajevima štapa do udaljenosti između njih. Također ovisi o površini poprečnog presjeka šipke (u m 2 ) i koeficijent toplinske vodljivosti materijala[ u odgovarajućim jedinicama W/(m CH K) ] . Odnos između ovih veličina izveo je francuski matematičar J. Fourier i ima sljedeći oblik: Gdje q protok topline, k koeficijent toplinske vodljivosti, i A poprečni presjek područja. Taj se odnos naziva Fourierov zakon toplinske vodljivosti; znak minus u njemu označava da se toplina prenosi u smjeru suprotnom od temperaturnog gradijenta.Iz Fourierovog zakona proizlazi da se protok topline može smanjiti smanjenjem jedne od veličina: koeficijenta toplinske vodljivosti, površine ili temperaturnog gradijenta. Za zgradu u zimskim uvjetima, posljednje vrijednosti su praktički konstantne, pa stoga, kako bi se održala željena temperatura u prostoriji, ostaje smanjiti toplinsku vodljivost zidova, tj. poboljšati njihovu toplinsku izolaciju.
U tablici su prikazani koeficijenti toplinske vodljivosti nekih tvari i materijala. Iz tablice je vidljivo da neki metali puno bolje provode toplinu od drugih, ali su svi znatno bolji vodiči topline od zraka i poroznih materijala.
|
TOPLINSKA VODLJIVOST NEKIH TVARI I MATERIJALA |
|
|
Supstance i materijali |
Toplinska vodljivost, W/(m× K) |
| Aluminij | |
| bronca | |
| Bizmut | |
| Volfram | |
| Željezo | |
| Zlato | |
| Kadmij | |
| Magnezij | |
| Bakar | |
| Arsen | |
| nikal | |
| Platina | |
| Merkur | |
| voditi | |
| Cinkov | |
|
Ostali materijali |
|
| Azbest | |
| Beton | |
| Zrak | |
| puhasto gaga (labavo) | |
| orah) | |
| magnezij (MgO) | |
| Piljevina | |
| Guma (spužva) | |
| tinjac | |
| Staklo | |
| Ugljik (grafit) | |
Toplinski i električni otpor mnogih tvari naglo opada kada temperatura padne ispod temperature tekućeg helija (1,8 K). Ovaj fenomen, nazvan supravodljivost, koristi se za poboljšanje učinkovitosti mnogih uređaja, od mikroelektroničkih uređaja do dalekovoda i velikih elektromagneta. vidi također SUPRAVODLJIVOST.
Konvekcija. Kao što smo već rekli, kada se toplina dovodi u tekućinu ili plin, povećava se intenzitet molekularnog kretanja, a kao rezultat toga, povećava se tlak. Ako tekućina ili plin nisu ograničeni volumenom, tada se šire; lokalna gustoća tekućine (plina) postaje manja, a zahvaljujući silama uzgona (Arhimedovim) zagrijani dio medija se pomiče prema gore (zbog čega se topli zrak u prostoriji diže od radijatora do stropa). Ova pojava se naziva konvekcija. Kako ne biste gubili toplinu sustava grijanja, morate koristiti moderne grijače koji osiguravaju prisilnu cirkulaciju zraka.Konvekcijski tok topline od grijača do grijanog medija ovisi o početnoj brzini gibanja molekula, gustoći, viskoznosti, toplinskoj vodljivosti i toplinskom kapacitetu i medija; Veličina i oblik grijača također su vrlo važni. Odnos između odgovarajućih veličina pokorava se Newtonovom zakonu
q = hA ( T W- TҐ ), gdje q protok topline (mjereno u vatima), A površina izvora topline (u m 2), T W I TҐ temperatura izvora i okoline (u Kelvinima). Koeficijent konvektivnog prolaza topline h ovisi o svojstvima medija, početnoj brzini njegovih molekula, kao i o obliku izvora topline, a mjeri se u jedinicama W/(m 2 H DO).Veličina
h nije isto za slučajeve kada zrak oko grijača miruje (slobodna konvekcija) i kada je isti grijač u struji zraka (prisilna konvekcija). U jednostavnim slučajevima strujanja fluida kroz cijev ili strujanja oko ravne površine, koeficijent h može se teoretski izračunati. Međutim, još nije bilo moguće pronaći analitičko rješenje problema konvekcije za turbulentno strujanje medija. Turbulencija je složeno kretanje tekućine (plina), kaotično u mjerilu znatno većem od molekularnog.Ako se zagrijano (ili, obrnuto, hladno) tijelo postavi u stacionarni medij ili u struju, tada se oko njega formiraju konvektivne struje i granični sloj. Temperatura, tlak i brzina kretanja molekula u ovom sloju imaju važnu ulogu u određivanju koeficijenta konvektivnog prijenosa topline.
Konvekcija se mora uzeti u obzir pri projektiranju izmjenjivača topline, klimatizacijskih sustava, zrakoplova velikih brzina i mnogih drugih primjena. U svim takvim sustavima, toplinska vodljivost se javlja istovremeno s konvekcijom, kako između čvrstih tijela tako iu njihovoj okolini. Na povišene temperature Prijenos topline zračenjem također može igrati značajnu ulogu.
Prijenos topline zračenjem. Treći tip prijenosa topline, prijenos topline zračenjem, razlikuje se od kondukcije i konvekcije po tome što se toplina u ovom slučaju može prenositi kroz vakuum. Njegova sličnost s drugim metodama prijenosa topline je u tome što je također uzrokovan temperaturnim razlikama. Toplinsko zračenje je jedna od vrsta elektromagnetska radijacija. Ostale vrste radio valova, ultraljubičastog i gama zračenja nastaju u odsutnosti temperaturne razlike.Na sl. Na slici 8 prikazana je ovisnost energije toplinskog (infracrvenog) zračenja o valnoj duljini. Toplinsko zračenje može biti popraćeno emisijom vidljive svjetlosti, ali je njegova energija mala u usporedbi s energijom zračenja iz nevidljivog dijela spektra.
Intenzitet prijenosa topline kondukcijom i konvekcijom proporcionalan je temperaturi, a toplinski tok zračenjem proporcionalan je četvrtoj potenciji temperature i pridržava se zakona Stefana Boltzmanna
Stambeni i poslovni prostori često se griju malim električnim raspršivačima topline; crvenkasti sjaj njihovih spirala je vidljivo toplinsko zračenje, blizu ruba infracrvenog dijela spektra. Prostorija se zagrijava toplinom, koju prenosi uglavnom nevidljivi, infracrveni dio zračenja. U uređajima za noćno gledanje
^ Ovi uređaji koriste izvor toplinskog zračenja i prijemnik osjetljiv na infracrveno zračenje, što omogućuje da se vidi u mraku.Sunce je snažan emiter toplinske energije; zagrijava Zemlju i na udaljenosti od 150 milijuna km. Intenzitet sunčevog zračenja koji iz godine u godinu bilježe postaje u mnogim dijelovima svijeta iznosi približno 1,37 W
/ m 2 . Sunčeva energija je izvor života na Zemlji. U tijeku je potraga za načinima kako ga najučinkovitije iskoristiti. Solarni paneli stvoreni su za grijanje kuća i proizvodnju električne energije za kućne potrebe. ULOGA TOPLINE I NJENA UPORABA Globalni procesi izmjene topline nisu ograničeni na zagrijavanje Zemlje sunčevim zračenjem. Masivna konvekcijska strujanja u atmosferi određuju dnevne promjene vremenskih uvjeta diljem svijeta. Promjene temperature u atmosferi između ekvatorijalnih i polarnih područja, zajedno s Coriolisovim silama uzrokovanim rotacijom Zemlje, dovode do pojave kontinuirano promjenjivih konvekcijskih struja, kao što su pasati, mlazne struje te tople i hladne fronte. vidi također KLIMA; METEOROLOGIJA I KLIMATOLOGIJA.Prijenos topline (zbog toplinske vodljivosti) iz rastaljene jezgre Zemlje na njezinu površinu dovodi do vulkanskih erupcija i pojave gejzira. U nekim se regijama geotermalna energija koristi za grijanje prostora i proizvodnju električne energije.
Toplina je neizostavan sudionik u gotovo svim proizvodnim procesima. Spomenimo najvažnije među njima, kao što su taljenje i obrada metala, rad motora, proizvodnja hrane, kemijska sinteza, prerada nafte te proizvodnja najrazličitijih predmeta – od opeke i posuđa do automobila i elektroničkih uređaja.
Mnoge industrijske proizvodnje i transporta, kao i termoelektrane, ne bi mogle raditi bez toplinskih strojeva – uređaja koji toplinu pretvaraju u koristan rad. Primjeri takvih strojeva uključuju kompresore, turbine, parne, benzinske i mlazne motore.
Jedan od najpoznatijih toplinskih strojeva je parna turbina, koja implementira dio Rankineovog ciklusa koji se koristi u modernim elektranama. Pojednostavljeni dijagram ovog ciklusa prikazan je na sl. 9. Radni fluid voda pretvara se u pregrijanu paru u parnom kotlu koji se zagrijava izgaranjem fosilnih goriva (ugljen, nafta ili prirodni plin). Steam visokotlačni vrti osovinu parne turbine, koja pokreće generator koji proizvodi električnu energiju. Ispušna para se kondenzira kada se ohladi tekućom vodom, koja apsorbira dio topline koja se ne koristi u Rankineovom ciklusu. Zatim se voda dovodi u rashladni toranj, odakle se dio topline ispušta u atmosferu. Kondenzat se pomoću pumpe vraća u parni kotao, te se cijeli ciklus ponavlja.
Svi procesi u Rankineovom ciklusu ilustriraju gore opisana načela termodinamike. Konkretno, prema drugom zakonu, dio energije koju troši elektrana mora se raspršiti u okolišu u obliku topline. Ispada da se otprilike 68% energije izvorno sadržane u fosilnim gorivima gubi na ovaj način. Osjetno povećanje učinkovitosti elektrane moglo bi se postići samo povećanjem temperature parnog kotla (koja je ograničena toplinskom otpornošću materijala) ili snižavanjem temperature medija u koji odlazi toplina, tj. atmosfera.
Još jedan termodinamički ciklus koji ima veliki značaj u našem Svakidašnjica, ovo je Rankineov ciklus rashladnog kompresora pare, čiji je dijagram prikazan na sl. 10. U hladnjacima i klimatizacijskim uređajima za kućanstvo, energija za njezino osiguravanje dolazi izvana. Kompresor povećava temperaturu i tlak radne tvari hladnjaka: freona, amonijaka ili ugljičnog dioksida. Pregrijani plin dovodi se u kondenzator, gdje se hladi i kondenzira, oslobađajući toplinu u okolinu. Tekućina koja napušta cijevi kondenzatora prolazi kroz prigušni ventil u isparivač, a dio isparava, što je popraćeno oštrim padom temperature. Isparivač uzima toplinu iz komore hladnjaka, koja zagrijava radni fluid u cijevima; ovu tekućinu kompresor dovodi u kondenzator i ciklus se ponovno ponavlja.
Ciklus hlađenja prikazan na sl. 10, također se može koristiti u toplinskoj pumpi. Takve dizalice topline ljeti predaju toplinu vrućem atmosferskom zraku i kondicioniraju prostoriju, a zimi, naprotiv, uzimaju toplinu hladnom zraku i zagrijavaju prostoriju.
Nuklearne reakcije važan su izvor topline za potrebe poput proizvodnje električne energije i transporta. Godine 1905. A. Einstein je pokazao da su masa i energija povezani odnosom
E = mc 2 , tj. mogu transformirati jedno u drugo. Brzina svjetlosti c vrlo velik: 300 tisuća km/ S. To znači da čak i mala količina tvari može dati ogromnu količinu energije. Tako je iz 1 kg fisibilnog materijala (primjerice urana) teoretski moguće dobiti energiju koju elektrana snage 1 MW daje u 1000 dana neprekidnog rada. vidi također GRAĐA ATOMA; TEHNIKA PEĆI I LOŽIŠTA; ELEKTROMAGNETSKA RADIJACIJA; IZMJENJIVAČ TOPLINE; TURBINA; MJERNE JEDINICE FIZIKALNIH VELIČINA.KNJIŽEVNOST Zemanski M. Temperature su vrlo visoke i vrlo niske. M., 1968Paul R. Mehanika, akustika i proučavanje topline. M., 1971
Smorodinski Ya.A. Temperatura. M., 1981
Fen J. Strojevi, energija i entropija. M., 1986
Atkins P.V. Red i nered u prirodi. M., 1987
Tekući kalorimetri
Ovaj tip kalorimetra, koji se najviše koristi u tehnologiji, jednostavnog je dizajna i jednostavan za održavanje. Količina topline proizvedena reakcijom induciranom izvana prvo se prenosi u reakcijsku posudu (u kojoj se odvijala reakcija), a zatim u tekuću kupelj. Tekućina u kupelji kontinuirano se miješa pomoću impelera, vijka za podizanje ili pumpi, što ubrzava izjednačavanje temperature. Kada je u najvećoj mogućoj mjeri toplinski izolirana (zaštićena) od okoline. Promjena temperature tekuće kupelji mjera je količine topline koja se detektira. Toplinski kapacitet grijanih masa ne smije biti prevelik kako bi se osigurala dovoljna promjena temperature i kako proces mjerenja ne bi trajao predugo (što povećava gubitke topline).
Slika Uređaj tekućinskog kalorimetra.
Ako postoje visoki zahtjevi za stalnim uvjetima okoline, cijeli kalorimetar se može staviti u drugu kadu i temperatura u njoj se može stabilizirati s visokom točnošću pomoću kontrolne petlje. To je prije svega potrebno u slučajevima kada je potrebno provoditi pokuse na temperaturama koje se znatno razlikuju od temperature okoline.
Za izvođenje analiza na niskim temperaturama (do približno -150°C), tekući dušik se koristi kao rashladni medij. U tom slučaju potrebno je obratiti pozornost da se na uzorcima ili posudama s uzorcima ne taloži inje iz okolnog vlažnog zraka prilikom njihove izmjene, jer njegov sloj može utjecati na proces mjerenja. Kako bi se to izbjeglo, kada je kalorimetar otvoren, uzorak i spremnik za uzorak se pročišćavaju hladnim plinovitim dušikom.
Kalorimetri s metalnim tijelom
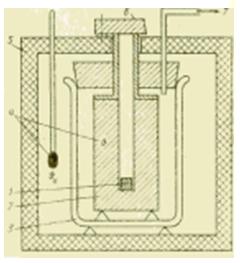
Slika Dijagram izvedbe metalnog kalorimetra.
Ako je potrebno provesti kalorimetrijska istraživanja u širem temperaturnom rasponu, tada tekući kalorimetri više nisu prikladni. U odgovarajućim kalorimetrima s metalnim tijelom prenesenu količinu topline očitava metalni blok (srebro, bakar, aluminij), koji je obično na sobnoj temperaturi. Ovaj kalorimetar je prvenstveno namijenjen za određivanje specifičnog toplinskog kapaciteta c, J/(kg*K), tekućih i čvrstih tvari.
Uzorak se prvo ohladi izvan kalorimetra rashladna jedinica ili zagrijati u pećnici i nakon postizanja stabilnog stanja spustiti (ispustiti) u rupu metalnog bloka. Prema načinu rada takav se uređaj naziva kalorimetar slobodnog pada, a prema prirodi termodinamičkih procesa u njemu ponekad se naziva i kalorimetar pomaka.
Količina topline prenesena tijekom takvog miješanja s uzorka (s parametrima m1, c1, ) na metalni blok (m2, c2, ) uzrokuje mjerljivu promjenu temperature bloka. To omogućuje određivanje obično nepoznatog specifičnog toplinskog kapaciteta uzorka za idealni uvjeti(u nedostatku izmjene topline s okolinom) iz izraza:
Sam metalni blok nalazi se u vakuumiranoj Dewarovoj tikvici, a ponekad i u kupelji s tekućinom. U potonjem slučaju, da bi se dobio toplinski kapacitet kalorimetra Ck, toplinski kapacitet kupke Cw mora se dodati toplinskom kapacitetu metalnog bloka C2:
CK=C2+CW=c2m2+cWmW .
KALORIMETRIJSKE METODE MJERENJA
Najčešće se kalorimetri koriste u režimu stalnih uvjeta okoline. Ovo se prvenstveno odnosi na većinu kalorimetara izgaranja, kod kojih je vrijeme reakcije vrlo kratko. Dok se temperatura unutarnjih dijelova kalorimetra mijenja zbog reakcije, temperatura okoline ostaje konstantna. U mnogim slučajevima, termostatska kupelj se koristi kao okoline kako bi se izbjegao utjecaj vanjskih smetnji na izmjerenu vrijednost - temperaturne fluktuacije u prostoriji, zračenje, propuh itd.
Prednost ove mjerne sheme je relativno niska cijena opreme, s kojom se može izvesti većina kalorimetrijskih mjerenja. Glavnim nedostatkom treba smatrati izmjenu topline kalorimetra s okolinom, što komplicira interpretaciju rezultata. Ova metoda mjerenja uvijek se naziva izoperibol (dijatermički). U svakom slučaju, ne može se nazvati izotermnim, čija je bit da temperatura kalorimetra ostaje konstantna tijekom reakcije, kao što su, na primjer, kalorimetri namijenjeni mjerenju faznih transformacija.
Adijabatska metoda
Ako je moguće isključiti izmjenu topline s okolinom, odnosno osigurati adijabatski tijek procesa, tada je provođenje eksperimenta i interpretacija rezultata pojednostavljena, a rezultat mjerenja točniji, jer nema potrebe za kontinuiranim bilježenjem temperature. promjene i izračunati korekcije. Osim toga, u ovom slučaju može se dopustiti nešto veći porast temperature u kalorimetrijskoj posudi; Za neadijabatske uređaje to je neprihvatljivo zbog povećanih gubitaka topline.
Kako bi se eliminirala izmjena topline između kalorimetrijske posude i njezine neposredne okoline (obično tekuće kupelji), temperatura kupelji mora se stalno podešavati u skladu s promjenama temperature unutar posude. Pomoću elektroničkog regulatora (nadzorni krug) možete stalno održavati razliku između ovih temperatura gotovo jednaku nuli. To povećava cijenu mjerne opreme ovisno o potrebnoj točnosti mjerenja.
Elementi opreme moraju biti brzodjelujući i dugotrajno stabilni (imati minimalno zanošenje). Mrtva zona servo upravljačke petlje trebala bi biti u rasponu od ± 10-3 do ± 10-5 K. Kao mjerni uređaji možete koristiti bilo koje električne kontaktne termometre niske inercije, koji, kada su spojeni na strujni krug mosta, daju impuls regulatoru za promjenu snage grijanja. Zagrijavanje se provodi pomoću zavojnice s električnim otporom ili izravno u tekućoj kupelji, koja zahvaljujući slaboj disocijaciji djeluje kao otpor za zagrijavanje (tzv. elektrolitičko zagrijavanje). Ova druga metoda je praktički bez inercije. Rezultat se može dobiti postojećim sredstvima za električno mjerenje temperature ili pomoću dodatno ugrađenog termometra za tekućinu (Beckman).
Metoda adijabatskog mjerenja prikladna je za proučavanje uglavnom sporih procesa koji uključuju toplinske učinke. S brzim promjenama u količini topline (u kalorimetrima izgaranja), inercija temperaturnog izjednačavanja ima toliko negativan učinak da se ne postiže čak ni točnost konvencionalnih neadijabatskih metoda. Međutim, osiguravanjem niskog toplinskog kapaciteta grijaćih elemenata i temperaturnih senzora te intenzivnim miješanjem tekućine kupke, moguće je dobiti male vrijednosti različitih vremenskih konstanti (smanjiti inerciju).
Metoda kompenzacije
Korištenjem diferencijalnih ili dvojnih kalorimetara koji se temelje na principu kompenzacije, moguće je značajno eliminirati vanjske utjecaje na proces mjerenja. Dvije identične kalorimetrijske posude s identičnim pomoćnim uređajima smještene su u okolinu s istim uvjetima. U jednoj posudi, proces koji se proučava odvija se s toplinskim učinkom, a druga se posuda, pomoću sustava upravljanja praćenjem, zagrijava na način da je gubitak topline u okoliš jednak za obje posude. Stoga se isporučena snaga grijanja može staviti u izravnu ovisnost o količini topline koja se oslobađa tijekom procesa koji se proučava. U tom se slučaju zadatak eksperimentalnog mjerenja seli na drugo područje i svodi se na vrlo točno određivanje dovedene električne snage grijanja (W*s, J):
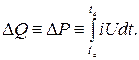
Diferencijalni kalorimetar posebno se koristi u adijabatskim uvjetima okoline, posebno kada se očekuju vrlo male ili vrlo spore promjene u količini topline. Za endotermne procese dovoljna je jedna kalorimetrijska posuda. Dovod topline se kontrolira tako da temperatura u posudi ostaje cijelo vrijeme ista (izotermna metoda). Nedostatak diferencijalnih kalorimetara je visoka cijena opreme i mjerne tehnologije.
KALORIMETRI IZGARANJA
Gorivu koje se koristi u termoenergetskim objektima ispituje se njegova ogrjevna vrijednost H (J/kg). Ovaj pokazatelj je potreban za određivanje faktora učinkovitosti, proučavanje učinkovitosti i izračunavanje potrošene energije u različitim instalacijama, kao i za optimalnu kontrolu procesa izgaranja. Značajne fluktuacije u sastavu zapaljivih komponenti često zahtijevaju kontinuirano određivanje kalorijske vrijednosti.
Kada tvar potpuno izgori, oslobađa se određena količina topline Q (toplina izgaranja). Ako ga podijelite s masom t (ili s volumenom u normalnim uvjetima Vn), dobit ćete (specifičnu) toplinu izgaranja:
Ovisno o stanju produkata izgaranja, razlikuju se dvije vrste topline izgaranja: viša H0 i niža H0, koje se još nazivaju i toplina izgaranja i ogrjevna vrijednost. Pri određivanju donje topline izgaranja Ni voda nastala tijekom kemijske reakcije, mora biti u stanju pare. Razlika između obje topline H0 - Ni odgovara toplini isparavanja kondenzirane vode (CO - indeks kondenzata) r koja iznosi 2,441 MJ/kg.
Za kruta i tekuća goriva rezultirajuća količina vode može se odrediti na temelju elementarne analize, a kod izgaranja plinovitih goriva mjerenjem količine kondenzata.
U industrijskim pećima temperatura produkata izgaranja uvijek premašuje vrelište vode. Stoga je obično od interesa samo niža ogrjevna vrijednost Ni, budući da se toplina kondenzacije vode ne može iskoristiti.
Kalorimetri izgaranja za krutine i tekućine
Za brze procese izgaranja razvijen je poseban oblik tekućeg kalorimetra - tzv. kalorimetar Berthelotove bombe (slika 3).
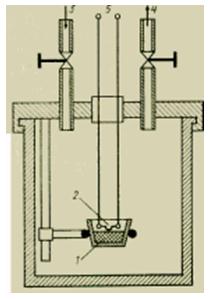
Crtež Dizajn kalorimetrijske bombe.
Izgaranje male, precizno izmjerene količine tvari događa se pri konstantnom volumenu u zatvorenoj bombi u atmosferi najčišćeg mogućeg kisika pod tlakom od ~30 atm (3 MPa). Napunjena bomba stavlja se u tekuću kupelj kalorimetra, koja apsorbira oslobođenu toplinu izgaranja.
Krutine obično prešane u male brikete (tablete) i vrlo precizno izvagane. Preporučljivo je pomiješati slabo goruće tvari s dobro gorućim tekućinama s poznatom kalorijskom vrijednošću (na primjer, benzojeva kiselina). Tekuće tvari stavljaju se u čašice (čamce) od platine ili kvarca ili u male plastične kapsule. Na poklopcu koji je vijcima pričvršćen za tijelo bombe nalaze se svi uređaji potrebni za istraživanje: ventili za dovod kisika i odvod produkata izgaranja, držači za uzorke i električni upaljač. Paljenje se provodi dovodom struje na tanku platinastu žicu. Toplina dovedena za paljenje mora se točno izmjeriti kako bi se mogla uzeti u obzir pri tumačenju eksperimentalnih rezultata. U kalorimetru bombe određuje se viša toplina izgaranja H0. Tijekom provjere toplinski ekvivalent kalorimetra C određuje se spaljivanjem referentne tvari (na primjer, benzojeve kiseline) ili korištenjem električnog uređaja za grijanje.
Kalorimetar izgaranja za plinovite tvari
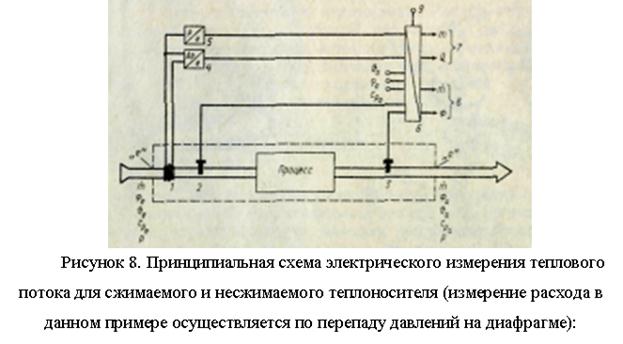
Postoje različite metode za određivanje topline izgaranja plinovitih medija. Svi oni, za razliku od kalorimetra bombe za čvrste i tekuće tvari, temelje se na kontinuiranom mjerenju. Princip mjerenja koji se koristi je vrlo jednostavan. Ispitni plin kontinuirano izgara u plameniku pri konstantnom tlaku. Sva toplina nastala izgaranjem apsorbira se ili protokom rashladne tekućine u izmjenjivaču topline (kalorimetar s mokrom ili izmjenom topline) ili miješanjem produkata izgaranja sa strujom zraka pri poznatoj brzini protoka (kalorimetar sa suhim ili miješanjem). Obično se određuje donja kalorična vrijednost Nu. Za određivanje veće ogrjevne vrijednosti H0 potrebno je kondenzirati vodenu paru (CO indeks) sadržanu u ispušnim plinovima. Poznavajući maseni protok i temperaturnu razliku na ulazu (indeks e) i izlazu (indeks a) kalorimetra, moguće je izračunati odgovarajuću toplinu izgaranja pomoću jednadžbe toplinske bilance.
Potrebna priprema plina u svim plinskim kalorimetrima je u osnovi ista. Prije izgaranja, plin (indeks G) se najprije očisti od čvrstih mehaničkih nečistoća (u filtru) i ovlaži (do zasićenja vlagom, 100%), a zatim se dovede do zadanih vrijednosti prethodnog tlaka (pomoću reducirnog ventila). ) i temperatura rashladnog medija (indeks K) . Zrak potreban za izgaranje (indeks L) također se ovlažuje i dovodi na temperaturu rashladnog medija.
Ovisno o potrebnoj točnosti i prihvatljivoj cijeni mjerne opreme, neki od ovih uvjeta možda neće biti ispunjeni. Kalorimetre treba ispitati na referentnom plinu (npr. vodiku) kako bi se utvrdilo odstupanje od jednadžbe za idealno stanje kalorimetra. Za (mokri) kalorimetar izmjene topline navedena jednadžba ima oblik
gdje su i maseni protok rashladnog medija i goriva, kg/s; sk - specifični toplinski kapacitet rashladnog medija, J/(kg*K); - povećanje temperature rashladnog medija, K.
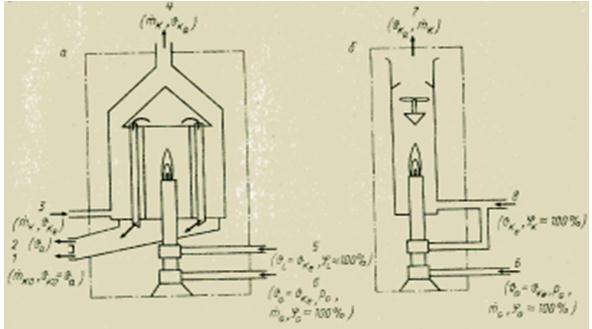
Slika Projektiranje mokrog (a) i suhog (b) kalorimetra za plinovito gorivo.
Porast temperature je obično 5-15 K. Zbog velike toplinske mase kalorimetri izmjene topline imaju vrlo dugu vremensku konstantu, koja može doseći i nekoliko minuta. Stoga su manje prikladni za korištenje u zatvorenoj regulacijskoj petlji kao senzor nego suhi (miješajući) kalorimetri, čija je vremenska konstanta samo nekoliko sekundi. Ali postižna točnost kalorimetara za izmjenu topline je relativno visoka. Njihova pogreška ne prelazi ±0,25-1%, pa se mogu koristiti i za laboratorijski rad i provjeru. Suhi kalorimetri (mješački) imaju pogrešku od ±1 do ±2% od gornje granice mjernog područja.
Izvedbe kalorimetara različitih proizvođača razlikuju se prvenstveno po pomoćnim i sigurnosnim uređajima, osjetljivim elementima i računalnim sklopovima koji omogućuju kompenzaciju pogreške. Tako se u kalorimetrima izmjenjivača topline na različite načine održava konstantan omjer protoka plina i rashladnog medija (vidi gornju jednadžbu kalorimetra), zbog čega viša ogrjevna vrijednost H0 izravno ovisi samo o porastu temperature.
U suhim kalorimetrima, porast temperature mjeri se izravno pomoću električnih kontaktnih termometara ili neizravno pomoću dilatometrijskog senzora - ekspandirajuće cijevi koja se nalazi u struji dimnih plinova. U ADOS kalorimetru, toplinsko produljenje dilatometrijske cijevi izravno odgovara toplini izgaranja i može se pretvoriti u bilo koji signal pomoću prijenosa poluge i mjerača duljine. U Reineckeovom kalorimetru produžetak šipke koristi se kao mjerni signal u kontrolnom krugu koji kontrolira protok zraka za hlađenje tako da porast temperature ostaje praktički konstantan. U ovom slučaju, upravljačka petlja ispada da je čisto proporcionalna, ali neka zaostala odstupanja su u njoj neizbježna. U tom slučaju, brzina protoka rashladnog zraka ili istezanje dilatometrijske cijevi (šipke) su mjera utvrđene kalorične vrijednosti. Nužan preduvjet za postizanje dovoljne točnosti kod svih suhih kalorimetara je dobro miješanje rashladnog zraka i produkata izgaranja.
MJERENJE TOPLINSKOG PROTOKA
Toplina se kao vrsta energije prenosi na tri načina: preko čvrstog tijela (toplinska kondukcija), tekućih ili plinovitih medija (konvekcija) i bez sudjelovanja tvari (zračenje). U tehnologiji prijenos topline gotovo uvijek uključuje sve tri komponente; međutim, u mnogim slučajevima moguće je dobiti rezultate prihvatljive točnosti mjerenjem samo jedne komponente.
Mjerenje protok topline s toplinskom vodljivošću
Prijenos topline kroz stijenke koje provode toplinu važan je u mnogim područjima tehnike (izmjenjivači topline svih vrsta, toplinska izolacija itd.). U ovom slučaju, nije toliko od interesa trenutno praćenje proizvodnih vrijednosti koliko rezultati pojedinačnih mjerenja koji se koriste za procjenu opterećenja, provjeru ispunjavanja zajamčenih pokazatelja i učinkovitosti.
Prema zakonima stacionarne toplinske vodljivosti, protok topline se određuje prema sljedećim formulama (J/s):
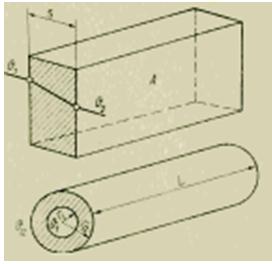
Budući da su poznati koeficijent toplinske vodljivosti zida [J/(m*s*K)] i njegove geometrijske dimenzije, mjerenje toplinskog toka svodi se na mjerenje temperaturne razlike. Međutim, ova tehnika zahtijeva vrlo precizno određivanje površinskih temperatura. Pogreške povezane s promjenama uvjeta prijenosa topline prilikom postavljanja temperaturno osjetljivih elemenata na površine mogu biti prilično velike. Stoga se za točnija mjerenja preporučuju dolje navedene metode koje istovremeno koriste i toplinsku vodljivost i prijenos topline.
Mjerenje protoka topline tijekom prijenosa topline (prijenos topline u kombinaciji s toplinskom vodljivošću)
Za ravnu stijenku spomenutu u prethodnom odjeljku vrijedi sljedeći zakon prijenosa topline (J/s):
![]() ,
,
gdje je u koeficijentu prolaza topline k 1J/(m2*s*K)], uz koeficijent toplinske vodljivosti [J/Dm*s*K)], koeficijenti prolaza topline i [J/(m2*s*K) ] obje strane zida također se uzimaju u obzir.
Na ravnu stijenku postavlja se mala tanka ploča kroz koju prolazi izmjereni toplinski tok čija se površinska temperatura određuje pomoću ugrađenih tankoslojnih termoparova. Prednost ovakvog mjerenja je u tome što ne zahtijeva poznavanje toplinskih svojstava stijenke, a pripadajuća svojstva ploče mogu se tijekom kalibracije svesti na jednu konstantnu vrijednost. Takvi osjetljivi elementi imaju veličinu od približno 30x30x0,5 mm; raspon mjerenja pokriva toplinske tokove od 10 do 100 000 W/m2; greška je 2-5%.
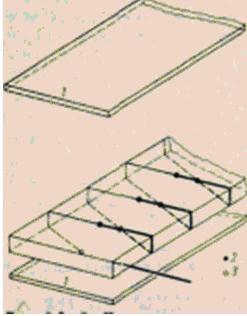
Slika Princip rada mjerača protoka topline.
Kod poboljšanja ove metode mjerenja umjesto aplicirane ploče koriste se gumene podloge. Njihovim lijepljenjem na neravne površine ili omotavanjem oko zakrivljene površine moguće je odrediti prijenos topline s površine relativno velike površine, npr. s cijevi, posude i sl. Termoparovi su ugrađeni u obje površine prostirku na način da se njihovi topli i hladni spojevi nalaze točno jedan naspram drugog (slika 6). I u ovom slučaju, gustoća toplinskog toka, u skladu s kalibracijom, proporcionalna je temperaturnoj razlici. No, primijenjene prostirke donekle remete početni prijenos topline, što postaje vidljivo točnim mjerenjima. Stoga se ova metoda mjerenja koristi uglavnom za određivanje termodinamičkih konstanti tvari, kada poremećaj toka topline ne utječe na rezultat mjerenja.
Mjerenje toplinskih tokova u tekućim medijima.
Značajan dio toplinske energije prenosi se tekućim ili plinovitim medijima (voda, para i dr.) koji se kreću u zatvorenoj cjevovodnoj mreži. Međutim, u usporedbi s prijenosom električne energije kroz žice, udaljenost preko koje se toplinska energija može prenijeti je ograničena. Za toplinskotehničke studije svih vrsta sustava grijanja i hlađenja potrebno je izmjeriti proizvodnju i potrošnju topline.
Protok topline F (J/s), strujio rashladni medij (kg/s) kroz kontrolni presjek površine A (m2) u određenoj zoni za koju se sastavlja toplinska bilanca (u zoni procesa, slika 7) jednak je
Količina topline dana u vremenskom intervalu t2 - t1 određena je kao integral (J):
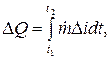
gdje je razlika u sadržaju topline (entalpija, J/kg) rashladnog sredstva na ulazu (indeks e) i na izlazu (indeks a) zone toplinske bilance.
Budući da je entalpija općenito od interesa samo u odnosu na određenu razinu, kao što je entalpija na temperaturi okoline, sva mjerenja protoka topline u biti su mjerenja razlike.
Pojedinačne entalpije uključene u opću jednadžbu mogu se izraziti u smislu odgovarajućih temperatura i specifičnih toplinskih kapaciteta;
Stoga se mjerenje protoka topline izravno svodi na mjerenje temperatura i masenih protoka. U mnogim slučajevima se ne mjeri maseni protok, već volumenski protok rashladnog sredstva; u tom će se slučaju dobiveni rezultat razlikovati samo za vrijednost gustoće rashladnog sredstva p. Specifični toplinski kapaciteti ci sami su funkcije temperature. Međutim, zbog uskog raspona mjerenja mnogih instrumenata, oni se obično mogu smatrati konstantnim vrijednostima bez velikog gubitka točnosti. Mora se znati specifični toplinski kapacitet. Za tekućine, jednadžba toka topline dodatno je pojednostavljena, budući da one specifični toplinski kapaciteti ne ovise o pritisku:
![]() , J/s.
, J/s.
U svim jednadžbama ovog tipa potrebno je voditi računa o predznacima veličina ovisno o tome da li se toplina dovodi ili odvodi, je li proces endoterman ili egzoterman, dolazi li do hlađenja ili zagrijavanja.
