Cara menentukan kapasitas panas spesifik air. Ensiklopedia bagus tentang minyak dan gas
PERANGKAT DAN AKSESORIS : kalorimeter, termometer, timbangan, badan uji, gelas kimia (satuan gram), alat pemanas listrik.
– mengkonfirmasi secara eksperimental validitas persamaan keseimbangan panas;
– menghitung kapasitas panas spesifik zat padat;
– menyusun hasil pengukuran dan perhitungan dalam bentuk tabel;
– tuliskan saran Anda untuk menyempurnakan teknik pengukuran dan perhitungan dalam karya ini.
TEORI PENGALAMAN SINGKAT
Salah satu konsep fisika dasar termodinamika adalah kapasitas panas.
Kapasitas panas tubuh ditelepon kuantitas fisik, secara numerik sama dengan panas, yang harus dikomunikasikan kepada suatu benda untuk mengubah suhunya sebesar 1 K dalam proses termodinamika yang sedang dipertimbangkan. Sebaliknya, kapasitas kalor suatu benda sama dengan perbandingan kalor dQ yang diberikan ke benda tersebut dengan perubahan dT suhu benda dalam proses termodinamika yang dipertimbangkan:
Kapasitas panas suatu benda bergantung padanya komposisi kimia, massa benda dan keadaan termodinamikanya, serta, seperti dapat dilihat dari definisi, jenis proses perubahan keadaan benda di mana panas dQ disuplai.
Sifat termal benda homogen dicirikan oleh nilai kapasitas panas spesifik dan molar (molar). Kapasitas panas spesifik suatu zat disebut besaran fisis Dengan, secara numerik sama dengan kalor yang harus diberikan kepada satu kilogram suatu zat untuk mengubah suhunya sebesar 1 K dalam proses termodinamika yang ditinjau. Kapasitas panas suatu benda homogen dapat didefinisikan sebagai hasil kali massa benda M untuk kapasitas panas spesifik Dengan zat-zatnya:
![]() atau (2.2).
atau (2.2).
Jadi, hubungan antara dQ dan dT untuk benda homogen berbentuk:
Kapasitas panas molar disebut besaran fisis C, yang secara numerik sama dengan kalor yang harus diberikan kepada satu mol suatu zat untuk mengubah suhunya sebesar 1 K dalam proses termodinamika yang ditinjau:
DENGAN = MS = (2.4),
dimana M adalah massa molar zat; DENGAN adalah kapasitas panas spesifiknya dalam proses yang sama.
Ekspresi (2.4) sekarang dapat ditulis dalam bentuk:
dimana = n adalah jumlah zat.
Satuan ukuran kapasitas panas suatu benda adalah 1 J/K, kapasitas panas spesifik– 1 J/kg. K, molar – 1 J/mol. KE.
Jika pemanasan terjadi pada kondisi dimana volumenya tetap, maka kapasitas panas molar yang bersangkutan disebut kapasitas panas pada volume konstan, atau kapasitas panas isokorik, dan dilambangkan dengan C v:
Jika tekanan selama pemanasan tetap konstan, maka kapasitas panas disebut kapasitas panas pada tekanan konstan C p (bisa juga disebut kapasitas panas isobarik):
Perhatikan bahwa untuk benda padat, hanya kapasitas panas pada tekanan konstan, dan bukan pada volume konstan, yang dapat diukur secara langsung, karena pemuaian termal tidak mungkin memastikan volume benda yang konstan. Namun karena perubahan volume yang kecil selama pemanasan, perbedaan antara kapasitas panas C p dan C v menjadi kecil.
Kapasitas panas suatu benda ditentukan secara eksperimental menggunakan persamaan keseimbangan panas. Biarkan tubuh dipanaskan hingga suhu yang lebih tinggi dari suhu tersebut lingkungan. Kemudian, saat tubuh mendingin, tubuh mengeluarkan sejumlah panas. Menurut hukum kekekalan energi dalam sistem tertutup, jumlah kalor yang diterima medium harus sama persis dengan jumlah kalor yang dikeluarkan benda. Dalam usaha ini, ketika benda uji mendingin, ia memindahkan panas ke air dalam kalorimeter dan ke kalorimeter itu sendiri.
Biarkan ini menguji massa benda M, dipanaskan sampai suhu t 0, diturunkan ke dalam kalorimeter dengan air yang suhunya t 1. Akibat pertukaran panas suhu air dan kalorimeter bertambah menjadi t 2, A Suhu tubuh turun ke t 2. Banyaknya panas yang dikeluarkan tubuh sama dengan:
Departemen Q = cm(t 0 - t 2) (2.6),
di mana c adalah kapasitas panas spesifik benda uji,
t 0– suhu tubuh awal,
t 2– suhu tubuh akhir,
M- massa tubuh.
Banyaknya kalor yang diterima kalorimeter dan air sama dengan:
dimana dan adalah massa dan kapasitas kalor jenis kalorimeter,
I – massal dan spesifik kapasitas panas air,
t 1– suhu air awal,
t 2– suhu akhir air.
Menurut hukum kekekalan energi dalam sistem tertutup:
Q terpisah = Q lantai (2.8).
Kemudian, substitusikan rumus 2.6 dan 2.7 ke dalam persamaan 2.8 dan nyatakan nilai yang diinginkan DENGAN , kita mendapatkan:
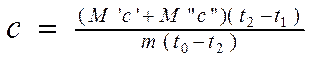 (2.9).
(2.9).
MENENTUKAN KAPASITAS PANAS SPESIFIK TIGA BADAN SILINDRI DARI LOGAM BERBEDA
1. Tentukan nilai massa benda - saya, massa kalorimeter – , kapasitas kalor jenis air – , kapasitas kalor jenis kalorimeter – .
2. Tuangkan sejumlah air dingin pada suhu kamar (kurang lebih 150 g) ke dalam kalorimeter.
3. Ukur suhu awal air dingin t 1.
4. Panaskan air dalam wadah hingga mendidih.
5. Masukkan salah satu benda uji ke dalam air mendidih selama beberapa waktu. Ambil suhu benda yang dipanaskan t 0 suhu yang sama Titik didih air pada kondisi normal adalah 100 °C.
6. Tempatkan benda yang dipanaskan ke dalam kalorimeter yang berisi air. Tunggu sampai pertukaran panas selesai dan ukur suhu akhir dalam kalorimeter – t 2 .
8. Tentukan kapasitas kalor jenis dua benda lainnya dengan cara yang sama.
9. Masukkan hasil pengukuran dan perhitungan pada tabel 3.
10. Dengan menggunakan nilai kapasitas kalor jenis, tentukan zat penyusun benda tersebut.
12. Setelah mengukur dimensi linier suatu benda, tentukan massa jenisnya.
13. Hitung kesalahan dan catat hasilnya sesuai dengan Gost.
14. Tuliskan kesimpulan dari pekerjaan laboratorium.
Tabel 3
| TIDAK. | M",kg | M",kg | m, kg | C", J/kg.K | C", J/kg.K | t 0,0 C | t 1,0 C | t 2,0 C | C, J/kg. KE |
Halaman 2
Keakuratan penentuan kapasitas kalor jenis menurut Sykes sangat tinggi. Namun, metode ini memiliki kesulitan eksperimen yang lebih besar daripada metode Smith, dan juga memberikan hasil yang akurat hanya untuk kurva pemanasan, meskipun metode ini juga dapat diterapkan untuk memperoleh kurva pendinginan. Metode Smith mempermudah mempelajari rentang suhu yang sempit, namun mungkin kurang akurat.
Oleh karena itu, untuk menentukan kapasitas kalor jenis c suatu zat, perlu mengukur kerja A yang dilakukan oleh gaya luar yang bekerja pada benda, dan mengukur perubahan suhu benda yang diamati sebagai akibat kerja tanpa adanya panas. pertukaran dengan badan lain.
Metode paling umum untuk menentukan kapasitas panas spesifik; disebut metode pencampuran. Kalorimeter (Regnault) terdiri dari bejana tembaga merah yang diletakkan di atas kaki kayu di dasar bejana tembaga lainnya, yang dipisahkan oleh lapisan udara, yang konduktivitas termal dan kapasitas panasnya, per satuan volume, dapat diabaikan. Bejana pertama diisi air.
Sekarang mari kita perhatikan metode untuk menentukan kapasitas panas spesifik suatu campuran gas.
Penentuan langsung (langsung) kapasitas panas spesifik Cy dan studi tentang perubahannya tergantung pada suhu dan volume spesifik adalah salah satunya cara yang efektif mempelajari keadaan kritis suatu zat. Oleh karena itu, penentuan kapasitas panas secara eksperimental merupakan kepentingan teoritis dan praktis yang besar dalam studi fenomena kritis.
Apa rumus untuk menentukan kapasitas panas spesifik larutan.
Saat melakukan percobaan untuk menentukan kapasitas panas spesifik dengan metode pencampuran, sampel yang diteliti perlu dipanaskan hingga suhu tetap yang tepat. Untuk tujuan ini, pemanas portabel digunakan, yang dipasang di atas kalorimeter untuk waktu singkat yang diperlukan untuk segera memindahkan sampel yang dipanaskan ke kalorimeter.
| Diagram perangkat. |
Inti dari metode stasioner absolut paling sederhana untuk menentukan kapasitas panas spesifik adalah sebagai berikut: sampel bahan uji dengan ketebalan h dan luas penampang 5 ditempatkan di antara pemanas dan pendingin. Pemanasnya bisa berupa bejana dengan air panas atau elemen pemanas listrik sehingga dayanya dapat diatur sesuka hati dengan memvariasikan tegangannya. Pendingin adalah badan logam berongga yang dilalui air dingin. Suhu pada permukaan sampel yang dipanaskan dan didinginkan (tj dan, karenanya, /2) diukur dengan termokopel.
Di bawah ini adalah contoh pengolahan data eksperimen dalam menentukan kapasitas kalor jenis suatu sampel batupasir. Sebuah silinder berongga berisi bubuk sampel batuan yang diteliti dipanaskan hingga 40 C dan didinginkan dalam ruang udara diam hingga suhu 18 - 20 C.
Pada Gambar. 3 - 6 menunjukkan nomogram untuk menentukan kapasitas panas spesifik hidrokarbon individu cair dan campuran minyak, serta larutan metanol dan etanol dalam air.
Sebagai contoh, mari kita buat persamaan keseimbangan panas yang digunakan untuk menentukan kapasitas kalor jenis suatu zat menggunakan kalorimeter. Secara kasar dapat diasumsikan bahwa dalam kasus ini tiga benda berpartisipasi dalam pertukaran panas: kalorimeter, cairan dan benda yang kapasitas panas spesifiknya ditentukan.
6.4. Pertukaran panas antar benda
6.4.1. Kapasitas panas tubuh, spesifik kapasitas kalor suatu zat, kapasitas kalor molar suatu zat
Untuk meningkatkan suhu tubuh, diperlukan sejumlah panas tertentu.
1 kg zat ini per 1 K disebut kapasitas panas spesifik suatu zat dan dihitung dengan rumus
c ketukan = Q m Δ T ,
dimana Q adalah jumlah kalor yang diperlukan untuk memanaskan suatu massa zat tertentu; m adalah massa zat; ΔT adalah perubahan suhu suatu zat bila dipanaskan.
Dalam Sistem Satuan Internasional, kapasitas kalor jenis suatu zat diukur dalam joule dibagi kilogram kelvin (1 J/(kg ⋅ K)).
Jumlah panas yang dibutuhkan untuk pemanasan beberapa massa materi, ditentukan oleh produk
Q = c kalahkan m ∆T .
Banyaknya kalor yang diperlukan untuk menghangatkan suatu benda sebesar 1 K disebut kapasitas panas tubuh dan dihitung dengan rumus
C = QΔT,
di mana Q adalah jumlah panas yang dibutuhkan untuk memanaskan suatu benda; ΔT adalah perubahan suhu tubuh saat dipanaskan.
Dalam Sistem Satuan Internasional, kapasitas panas suatu benda diukur dalam joule dibagi kelvin (1 J/K).
Jumlah panas yang dibutuhkan untuk memanaskan suatu benda ditentukan oleh produknya
Q = CΔT,
dimana C adalah kapasitas panas tubuh.
Kapasitas kalor suatu benda dan kapasitas kalor zat penyusun benda tersebut adalah saling berhubungan ekspresi
C = mc mengalahkan,
dimana C adalah kapasitas panas suatu benda; m - berat badan; csp adalah kapasitas panas spesifik zat yang membentuk benda tersebut.
Banyaknya kalor yang diperlukan untuk memanaskan 1 mol suatu zat sebesar 1 K disebut kapasitas panas molar suatu zat dan dihitung dengan rumus
c μ = Q ν Δ T ,
dimana Q adalah jumlah kalor yang diperlukan untuk memanaskan sejumlah zat; ν - jumlah zat; ΔT adalah perubahan suhu sejumlah tertentu suatu zat ketika dipanaskan.
Dalam Sistem Satuan Internasional, kapasitas panas molar suatu zat diukur dalam joule per mol kelvin (1 J/(mol ⋅ K)).
Jumlah panas yang dibutuhkan untuk pemanasan sejumlah zat, ditentukan oleh produk
Q = c µ νΔT .
Kapasitas molar dan panas spesifik suatu zat saling berhubungan ekspresi
cµ = Nona mengalahkan,
dimana c µ adalah kapasitas panas molar zat; M adalah massa molar suatu zat; csp adalah kapasitas panas spesifik suatu zat.
Contoh 14. Bola besi dan bola timah mempunyai diameter yang sama. Berapa kali kapasitas kalor bola besi lebih besar dari kapasitas kalor bola timah? Kapasitas kalor jenis besi dan timbal adalah 0,46 dan 0,13 kJ/(kg ⋅ K), dan massa jenisnya masing-masing adalah 7,80 dan 11,5 g/cm 3.
Solusi. Kapasitas panas bola ditentukan dengan rumus berikut:
- bola besi -
C 1 = m 1 c ud1,
dimana m 1 adalah massa bola besi; csp1 - kapasitas panas spesifik besi;
- bola timah -
C 2 = m 2 c ketukan2,
dimana m 2 adalah massa bola utama; csp2 - kapasitas panas spesifik timbal.
Rasio kapasitas panas yang dibutuhkan adalah:
C 1 C 2 = m 1 c ketukan 1 m 2 c ketukan 2,
yang ditentukan oleh perbandingan massa bola besi dan timah serta perbandingan kapasitas kalor jenis besi dan timbal.
Massa bola ditentukan oleh ukuran dan kepadatannya:
- bola besi -
m 1 = ρ 1 V 1,
dimana ρ 1 adalah massa jenis besi; V 1 - volume bola besi;
- bola timah -
m 2 = ρ 2 V 2,
di mana ρ 2 adalah massa jenis timbal; V 2 adalah volume bola utama.
Bola-bola tersebut mempunyai diameter yang sama, sehingga volumenya sama:
V 1 = V 2 = V = π d 2 6,
dimana d adalah diameter bola besi dan timah.
Dengan mempertimbangkan keadaan terakhir, rasio massa adalah:
m 1 m 2 = ρ 1 V 1 ρ 2 V 2 = ρ 1 ρ 2 .
Mari kita substitusikan m 1 /m 2 ke dalam rumus perbandingan kapasitas panas bola besi dan bola timah:
C 1 C 2 = ρ 1 c mengalahkan 1 ρ 2 c mengalahkan 2 .
Mari kita lakukan perhitungan:
C 1 C 2 = 7,80 ⋅ 10 3 ⋅ 0,46 ⋅ 10 3 11,5 ⋅ 10 3 ⋅ 0,13 ⋅ 10 3 = 2,4.
Kapasitas panas bola besi 2,4 kali lebih tinggi dibandingkan kapasitas panas bola timah.
Contoh 15. Saat menyiapkan campuran, sejumlah pasir dan empat kali massa semen dituangkan ke dalam bunker. Kapasitas kalor jenis semen dan pasir masing-masing adalah 810 dan 960 J/(kg ⋅ K). Tentukan kapasitas panas spesifik campuran.
Solusi. Kapasitas panas spesifik campuran ditentukan oleh rumus
c ketukan = Q m Δ T ,
dimana Q adalah jumlah kalor yang diperlukan untuk menaikkan suhu campuran sebesar ΔT; m adalah massa campuran.
Banyaknya kalor yang diperlukan untuk memanaskan campuran tersebut adalah -
Q = Q 1 + Q 2,
dimana Q 1 adalah jumlah kalor yang diperlukan untuk memanaskan pasir yang termasuk dalam campuran sebesar T; Q 2 adalah banyaknya kalor yang diperlukan untuk memanaskan semen yang termasuk dalam campuran sebesar ΔT.
Jumlah panas yang dibutuhkan untuk pemanasan:
- pasir -
Q 1 = c sp1 m 1 ∆T ,
dimana csp1 adalah kapasitas panas spesifik pasir; m 1 - massa pasir;
- semen -
Q 2 = c sp2 m 2 T,
dimana csp2 adalah kapasitas panas spesifik semen; m 2 - massa semen.
Banyaknya kalor yang diperlukan untuk memanaskan campuran pasir dan semen diberikan oleh
Q = c pukul 1 m 1 Δ T + c pukul 2 m 2 Δ T = (c pukul 1 m 1 + c pukul 2 m 2) Δ T.
Massa campuran adalah jumlah massa pasir dan semen:
m = m 1 + m 2 .
Mari kita substitusikan persamaan yang diperoleh untuk jumlah kalor dan massa campuran ke dalam rumus kapasitas kalor jenis campuran:
c ketukan = (c ketukan 1 m 1 + c ketukan 2 m 2) Δ T (m 1 + m 2) Δ T = c ketukan 1 m 1 + c ketukan 2 m 2 m 1 + m 2.
Mari kita ubah ekspresi yang dihasilkan dengan mempertimbangkan rasio massa:
m 2 = 4m 1, mis. c ketukan = c ketukan 1 m 1 + 4 c ketukan 2 m 1 m 1 + 4 m 1 = c ketukan 1 + 4 c ketukan 2 5 .
Perhitungannya memberikan nilai:
c ketukan = 960 + 4 ⋅ 810 5 = 840 J/(kg ⋅ K).
Jadi, kapasitas kalor jenis campuran tersebut adalah 840 J/(kg ⋅ K).
