A quantidade de calor que Quantidade de calor. Unidades de calor. Calor específico

Que processo é chamado de condução de calor? Em que ambientes é possível? É o mesmo para várias substâncias? Que processo é chamado de convecção? Em que ambientes é possível? O que determina a taxa de convecção? Que processo é chamado de radiação. Quais características desse tipo de transferência de calor você conhece?

A energia que o calor recebe ou perde durante a transferência de calor é chamada de quantidade de calor. Símbolo: Q Unidades: joule (J) (kJ) caloria (cal) 1 cal=4,19 J 1 kcal= 4190 J 4,2 kJ Caloria é a quantidade de calor necessária para aquecer 1 g de água em 1°C.

Etapa 1 do experimento 1. Despeje água nos frascos: o segundo é 2 vezes mais que o primeiro. 2. Fixe os frascos nas pernas dos tripés. 3. Meça a temperatura inicial do líquido em cada frasco. 4. Acenda lamparinas. 5. Simultaneamente, comece a aquecer os frascos. 6. Meça a temperatura em cada frasco após 2 minutos. 7. Faça uma conclusão.
![]()
Um experimento para determinar a dependência da quantidade de calor transferida para uma substância na massa dessa substância. m 1 
Etapa 2 do experimento 1. Despeje uma quantidade igual de água em 2 frascos. 2. Fixe os frascos nas pernas dos tripés. 3. Meça a temperatura inicial do líquido em cada frasco. 4. Acenda lamparinas. 5. Simultaneamente, comece a aquecer os frascos. 6. Sem retirar o termômetro do líquido, pare o aquecimento quando a temperatura no primeiro frasco subir 20°C e no segundo 25°C. 7. Meça o tempo que levou para cada processo. 8. Tire conclusões.

Um experimento para determinar a dependência da quantidade de calor transferida para uma substância em uma mudança em sua temperatura. m 1 = m t 1 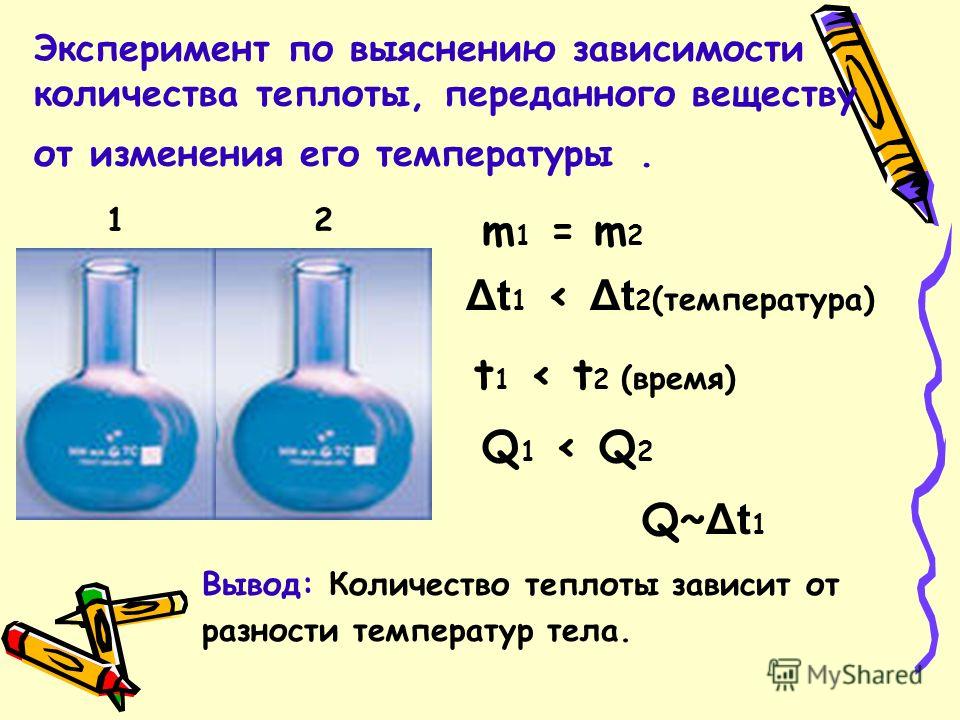
Etapa 3 do experimento 1. Despeje uma quantidade igual de água e óleo em 2 frascos. 2. Fixe os frascos nas pernas dos tripés. 3. Meça a temperatura inicial do líquido em cada frasco. 4. Acenda lamparinas. 5. Simultaneamente, comece a aquecer os frascos. 6. Meça a temperatura em cada frasco após 2 minutos. 7. Faça uma conclusão.

T 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 transferido de seu tipo m 1 = m 2 1 2 t 1 > t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância" class="link_thumb"> 11 !} Um experimento para determinar a dependência da quantidade de calor transferida em seu tipo. m 1 = m t 1 > t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância. 1 2 Q ~ sobre o tipo de substância t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância "> t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância. 1 2 Q ~ do tipo de substância "> t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância" title="(!LANG: Um experimento para determinar a dependência do quantidade de calor transferida em sua espécie. m 1 = m 2 1 2 t 1 > t 2 (tempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende do tipo de substância"> title="Um experimento para determinar a dependência da quantidade de calor transferida em seu tipo. m 1 \u003d m 2 1 2 t 1\u003e t 2 (tempo) Δt 1 \u003d Δt 2 (temperatura) Q 1 > Q 2 Conclusão: a quantidade de calor necessária para aquecer (resfriar) o corpo depende da tipo de substância"> !}
Designado: s unidade de medida: J/kg °C Quantidade física, numericamente igual à quantidade de calor que deve ser transferida a um corpo de massa 1 kg para que sua temperatura varie 1 ° C, é chamado calor específico substâncias. Calor específico substâncias.

O calor específico do aço é igual a 500 J/kg °C. Isso significa que para aquecer (resfriar) o aço m = 1 kg por 1ºС, é necessária uma quantidade de calor igual a 500 J. A capacidade de calor específico de uma substância em diferentes estados de agregação é diferente. por exemplo, para água c = 4200 J/kg °C; para gelo c = 2100 J/kg °C


Fixação Qual é a quantidade de calor? O que é medido? O que determina a quantidade de calor? Qual é o calor específico de uma substância? Qual é a unidade de capacidade de calor específico. O calor específico do chumbo é 140 J/kg °C. O que isto significa?

Qual é a capacidade de calor específico de zinco, tijolo, água? Quanto calor deve ser transmitido a essas substâncias com uma massa de 1 kg para aquecer em 1 ºС. Calcule a quantidade de calor (em calorias e quilocalorias). Necessário para aquecer a água em 1°C, cuja massa é 3; 4kg.


