Ջրածնի սուլֆիդի ջերմային հզորությունը տարբեր ջերմաստիճաններում: Բնական գազի տեսակարար ջերմային հզորությունը
Ոչ թե կոնկրետ, այլ ընդհանուր ջերմային հզորությունը, ընդհանուր ընդունված ֆիզիկական իմաստով, նյութի տաքանալու ունակությունն է։ Համենայն դեպս դա մեզ ասում է ջերմային ֆիզիկայի ցանկացած դասագիրք. սա դասական սահմանումջերմային հզորություն(ճիշտ ձևակերպում): Իրականում սա հետաքրքիր ֆիզիկական հատկանիշ է: Մեզ քիչ հայտնի է առօրյա կյանքում «մետաղադրամի կողմը»: Պարզվում է, որ երբ ջերմությունը մատակարարվում է դրսից (տաքացում, տաքացում), ոչ բոլոր նյութերը հավասարապես են արձագանքում ջերմությանը ( ջերմային էներգիա) և տաքացնել այլ կերպ: Կարողություն Բնական ծագման ԳԱԶ, որն օգտագործվում է որպես վառելիքստանալ, ստանալ, պահպանել և կուտակել (կուտակել) ջերմային էներգիա կոչվում է ԲՆԱԿԱՆ այրվող գազի ջերմունակություն. Եվ ինքն իրեն մեթանի ջերմային հզորությունը, ֆիզիկական բնութագիր է, որը նկարագրում է գազի վառելիքի ջերմաֆիզիկական հատկությունները։ Միևնույն ժամանակ, կիրառական տարբեր ասպեկտներում, կախված կոնկրետ գործնական դեպքից, մեզ համար կարող է կարևոր լինել մի բան. Օրինակ՝ նյութի ընդունման ունակությունը տաքկամ կուտակելու կարողություն ջերմային էներգիակամ «տաղանդ» պահել այն։ Այնուամենայնիվ, չնայած որոշակի տարբերությանը, ֆիզիկական իմաստով նկարագրվելու են մեզ անհրաժեշտ հատկությունները մեթանի ջերմային հզորությունը.
Ֆունդամենտալ բնույթի փոքրիկ, բայց շատ «գարշելի խայթոցն» այն է, որ տաքանալու ունակությունը. մեթանի ջերմային հզորությունը, ուղղակիորեն կապված է ոչ միայն քիմիական բաղադրությունը, նյութի մոլեկուլային կառուցվածքը, այլև նրա քանակով (քաշ, զանգված, ծավալ)։ Նման «տհաճ» կապի պատճառով գեներալ մեթանի ջերմային հզորությունըդառնում է նյութի չափազանց անհարմար ֆիզիկական բնութագիր: Քանի որ մեկ չափված պարամետրը միաժամանակ նկարագրում է «երկու տարբեր բաներ»: Այսինքն՝ իրոք բնութագրում է ԲՆԱԿԱՆ ԳԱԶԻ ջերմաֆիզիկական հատկությունները, սակայն, «անցնող»-ը հաշվի է առնում նաև դրա քանակը։ Մի տեսակ ինտեգրալ բնութագրի ձևավորում, որում ավտոմատ կերպով միացված են «բարձր» ջերմային ֆիզիկան և նյութի «բանալ» քանակությունը (մեր դեպքում՝ գազի վառելիքը)։
Լավ, ինչի՞ն են մեզ պետք այնպիսի ջերմաֆիզիկական բնութագրեր, որոնցում հստակ երևում է «ոչ ադեկվատ հոգեկանը»։ Ֆիզիկայի տեսանկյունից ընդհանուր մեթանի ջերմային հզորությունը(ամենաանշնորհք ձևով), փորձում է ոչ միայն նկարագրել ջերմային էներգիայի քանակությունը, որը կարող է կուտակվել գազի վառելիքում, այլ նաև «մեզ տեղեկացնել» քանակի մասին. ԲՆԱԿԱՆ Այրվող ԳԱԶ. Ստացվում է աբսուրդ, և ոչ պարզ, հասկանալի, կայուն, ճիշտ մեթանի ջերմաֆիզիկական բնութագիրը. Գործնականի համար հարմար օգտակար հաստատունի փոխարեն ջերմաֆիզիկական հաշվարկներ, մեզ տրվում է լողացող պարամետր, որը ստացված ջերմության քանակի գումարն է (ինտեգրալը)։ ԲՆԱԿԱՆ ԳԱԶև դրա զանգվածը կամ մեթանի ծավալը։
Շնորհակալ եմ, իհարկե, նման «ոգեւորության», բայց քանակի ԲՆԱԿԱՆ ՎԱՌԵԼԻՔ ԳԱԶԵս կարող եմ ինձ չափել. Արդյունքներ ստանալով շատ ավելի հարմար, «մարդկային» տեսքով։ Քանակ ԲՆԱԿԱՆ Այրվող ԳԱԶԵս կցանկանայի «չհանել» մաթեմատիկական մեթոդներով և հաշվարկներով՝ օգտագործելով բարդ բանաձևը ընդհանուրից մեթանի ջերմային հզորությունը, տարբեր ջերմաստիճաններում, բայց պարզեք քաշը (զանգվածը) գրամներով (գ, գ), կիլոգրամներով (կգ), տոննաներով (տոննաներով), խորանարդներով (խմ, խորանարդ մետր, մ3), լիտրով (լ) կամ միլիլիտրներով (մլ): ) Մանավանդ որ խելացի մարդիկվաղուց հայտնվեց այս նպատակների համար բավականին հարմար չափիչ գործիքներ: Օրինակ՝ կշեռքներ կամ այլ սարքեր։
Հատկապես պարամետրի «նյարդայնացնող լողացող բնույթը»՝ ընդհանուր բնականորեն առաջացող ԳԱԶ-ի ջերմային հզորությունը. Նրա անկայուն, փոփոխական «տրամադրությունը». «Սպասարկման չափը կամ չափաբաժինը» փոխելիս. ԲՆԱԿԱՆ ԳԱԶԻ ջերմունակությունը տարբեր ջերմաստիճաններումանմիջապես փոխվում է. Ավելի այրվող գազային խառնուրդ, ֆիզիկական քանակություն, բացարձակ արժեք մեթանի ջերմային հզորությունը- ավելանում է. Ավելի քիչ քանակությամբ այրվող գազային խառնուրդ, արժեքը մեթանի ջերմային հզորությունընվազում է. «Խայտառակություն» ոմանք պարզվում է. Այսինքն՝ այն, ինչ «ունենք», ոչ մի կերպ չի կարելի մշտական բնութագրում համարել ԲՆԱԿԱՆ ԳԱԶԻ ջերմաֆիզիկական բնութագրերը տարբեր ջերմաստիճաններում. Եվ մեզ համար ցանկալի է, որ «ունենանք» հասկանալի, հաստատուն գործակից, հղման պարամետր, որը բնութագրում է. ջերմային հատկություններգազային վառելիք՝ առանց մեթանի քանակի «հղումների» (քաշ, զանգված, ծավալ): Ինչ անել?
Այստեղ է, որ մեզ օգնության է հասնում մի շատ պարզ, բայց «շատ գիտական» մեթոդ։ Դա վերաբերում է ոչ միայն կարգադրիչին «ud. - կոնկրետ», նախքան ֆիզիկական քանակություն, բայց նրբագեղ լուծմանը, որը ներառում է նյութի քանակի բացառումը քննարկումից: Բնականաբար, «անհարմար, ավելորդ» պարամետրեր՝ զանգված կամ ծավալ ԲՆԱԿԱՆ Այրվող ԳԱԶբացառել բացարձակապես անհնար է. Գոնե այն պատճառով, որ եթե մեթանի քանակ չկա, ապա ինքնին «քննարկման առարկա» չի լինի։ Իսկ նյութը պետք է լինի. Ուստի մենք ընտրում ենք զանգվածի կամ ծավալի ինչ-որ պայմանական ստանդարտ, որը կարելի է համարել մեզ անհրաժեշտ «C» գործակցի արժեքը որոշելու համար հարմար միավոր։ Համար ԲՆԱԿԱՆ ԳԱԶԻ վառելիքի քաշը, մեթանի զանգվածի նման միավորը, որը հարմար է գործնական օգտագործման համար, պարզվել է 1 կիլոգրամ (կգ)։
Հիմա մենք մեկ կիլոգրամ ԲՆԱԿԱՆ ԳԱԶԸ տաքացնում ենք 1 աստիճանով, իսկ ջերմության քանակը (ջերմային էներգիա)մենք պետք է տաքացնենք գազի խառնուրդմեկ աստիճան - սա մեր ճիշտ ֆիզիկական պարամետրն է, գործակից «C», լավ, բավականին լիարժեք և հստակ նկարագրելով մեկը ԲՆԱԿԱՆ ԳԱԶԻ ջերմաֆիզիկական հատկությունները տարբեր ջերմաստիճաններում. Խնդրում ենք նկատի ունենալ, որ այժմ մենք գործ ունենք բնութագրիչի հետ ֆիզիկական սեփականություննյութ, բայց չփորձելով «լրացուցիչ տեղեկացնել մեզ» դրա քանակի մասին։ Հարմարավետ? Խոսքեր չկան։ Դա բոլորովին այլ հարց է։ Ի դեպ, հիմա խոսքը գեներալի մասին չէ մեթանի ջերմային հզորությունը. Ամեն ինչ փոխվել է. ՍԱ ԲՆԱԿԱՆ ԳԱԶԻ ՀԱՏՈՒԿ ՋԵՐՄԱՆ Է, որը երբեմն կոչվում է այլ անունով։ Ինչպե՞ս: Ուղղակի ԶԱՆԳԱՎՈՐ ԲՆԱԿԱՆ Այրվող ԳԱԶԻ ՋԵՐՄԱԿԱՆ ԿԱՐՈՂՈՒԹՅՈՒՆԸ. Հատուկ (ud.) Եվ զանգված (մ.) - այս դեպքում՝ հոմանիշներ, այստեղ նկատի ունեն մեզ անհրաժեշտը։ գործակից «C».
Աղյուսակ 1. Գործակից. ԲՆԱԿԱՆ ԳԱԶԻ տեսակարար ջերմունակությունը (sp.): ԲՆԱԿԱՆ այրվող ԳԱԶԻ զանգվածային ջերմային հզորությունը։ Հղման տվյալներ.
Պարզ ասած, ջերմային հզորություն ԻՑմարմինը կոչվում է ջերմության այն քանակությունը, որը պետք է ծախսվի այս գործընթացըմարմինը մեկ աստիճանով տաքացնել.
Սովորաբար ջերմային հզորությունը վերաբերում է նյութի քանակի միավորին և, կախված ընտրված միավորից, նրանք առանձնացնում են.
հատուկ զանգվածային ջերմային հզորություն Հետ, վերաբերում է 1 կգ գազին, J/(kgK);
հատուկ ծավալային ջերմային հզորություն Հետ´, վերաբերում է գազի քանակին, որը պարունակվում է 1 մ 3 ծավալում նորմալ ֆիզիկական պայմաններում, J / (m 3 K);
հատուկ մոլային ջերմային հզորություն μ Հետ, վերաբերում է մեկ կիլոմոլին, J / (kmolK):
Հատուկ ջերմային հզորությունների միջև կապը հաստատվում է ակնհայտ հարաբերություններով.
Հետ= μ Հետ/μ; Հետ´= Հետρ n. (2.13)
Այստեղ ρ n-ն գազի խտությունն է նորմալ պայմաններում:
Մարմնի ջերմաստիճանի փոփոխությունը մատակարարվող ջերմության նույն քանակով կախված է տեղի ունեցող գործընթացի բնույթից, հետևաբար ջերմային հզորությունը գործընթացի գործառույթ է. Սա նշանակում է, որ նույն աշխատանքային հեղուկը, կախված գործընթացից, իր տաքացման համար պահանջում է տարբեր քանակությամբ ջերմություն 1 Կ-ով։ Թվային մեծություն Հետտատանվում է + ∞-ից – ∞:
Ջերմոդինամիկական հաշվարկներում մեծ նշանակությունունեն՝
ջերմային հզորություն մշտական ճնշման տակ
Հետ p = δ ք p/ dT, (2.14)
ք p , մարմնին բերված գործընթացում մշտական ճնշման տակ, մարմնի ջերմաստիճանի փոփոխության dT;
ջերմային հզորություն մշտական ծավալով
Հետ v = δ ք v /dT, (2.15)
հավասար է δ ջերմության քանակի հարաբերակցությանը ք v, մարմնին բերված գործընթացում հաստատուն ծավալով, մարմնի ջերմաստիճանի փոփոխության dT.
Փակ համակարգերի թերմոդինամիկայի առաջին օրենքի համաձայն δ ք = դու + pdf.
Հաշվի առնելով այն հանգամանքը, որ 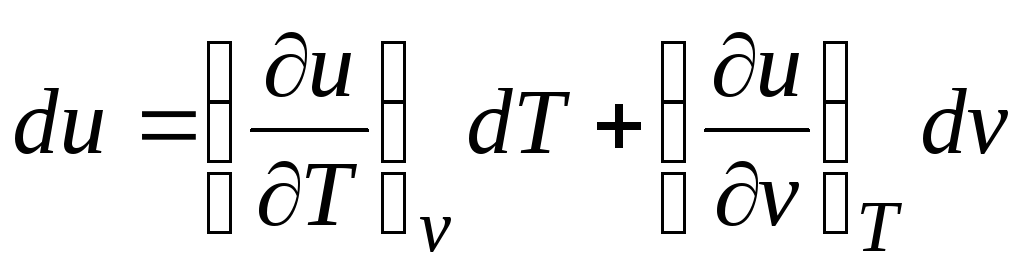 (հարաբերություններ (2.1))
(հարաբերություններ (2.1))
Δ ք = (∂u/∂Տ) v dT + [(∂u/∂v) Տ + էջ]dv. (2.16)
Իզոխորիկ գործընթացի համար ( v=const) այս հավասարումը ստանում է ձև 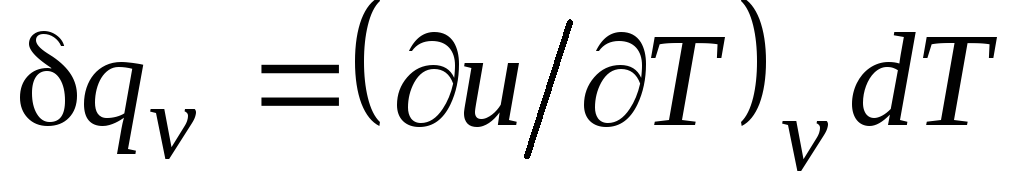 , և, հաշվի առնելով (2.15), ստանում ենք, որ
, և, հաշվի առնելով (2.15), ստանում ենք, որ
գ v = (∂u/∂Տ) v . (2.17)
Իդեալական գազի համար
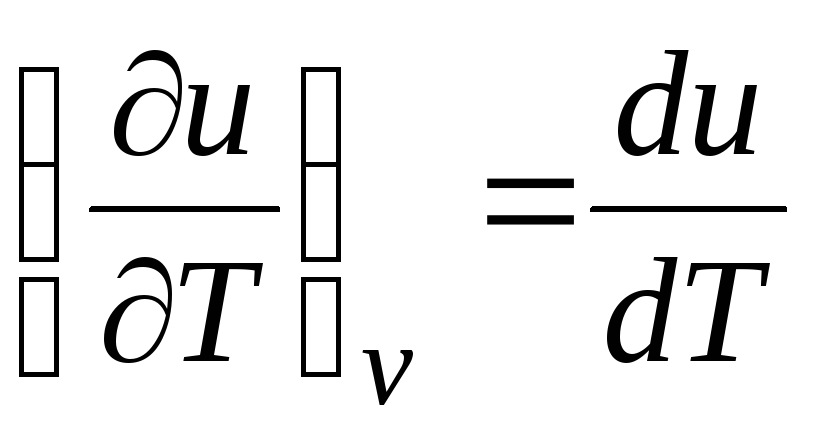 (հավասարում 2.2), այսպես
(հավասարում 2.2), այսպես
գ v = դու/dT. (2.18)
Իզոբարային գործընթացի համար ( Ռ=const) (2.16) և (2.14) հավասարումներից ստանում ենք
գ p = (∂ u/∂Տ) v + [(∂u/∂v) Տ + էջ](dv/dT) էջ
Քանի որ ներքին էներգիան իդեալական գազորոշվում է միայն իր ջերմաստիճանով և կախված չէ կոնկրետ ծավալից, ապա
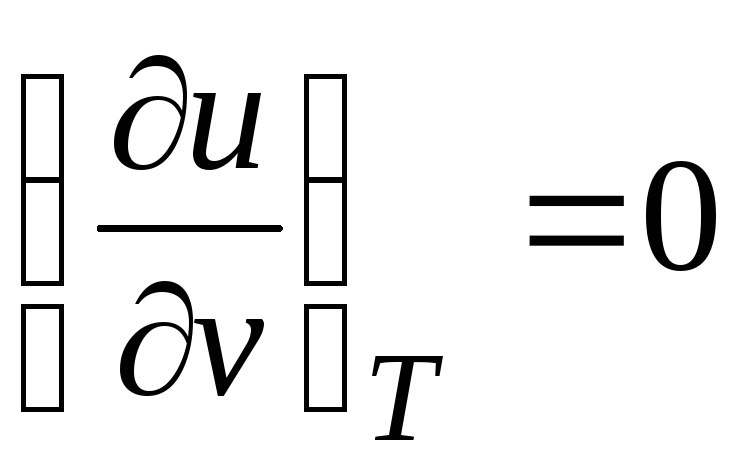 .
(2.19)
.
(2.19)
Կլապեյրոնի հավասարումից (1.4) pv
= RT(1.3) հետևում է 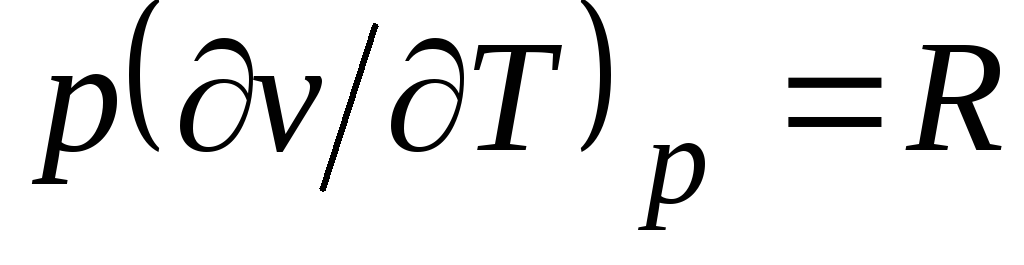 , որտեղ
, որտեղ
գ p= Հետ v + Ռ. (2.20)
Հարաբերությունը (2.20) կոչվում է Մայերի հավասարում և գլխավորներից է իդեալական գազերի տեխնիկական թերմոդինամիկայի մեջ։
Ընթացքում v\u003d կոնստ, գազին փոխանցվող ջերմությունը գնում է միայն նրա ներքին էներգիան փոխելու համար, մինչդեռ p \u003d const գործընթացում ջերմությունը ծախսվում է ինչպես ներքին էներգիան ավելացնելու, այնպես էլ ընդլայնման աշխատանքը կատարելու համար: Ահա թե ինչու գ p ավելին Հետ v այս աշխատանքի ծավալով.
Բանաձև ![]() որոշում է, այսպես կոչված, իրական ջերմային հզորությունը, այսինքն, ջերմային հզորության արժեքը տվյալ ջերմաստիճանում: Գործնականում ջերմային հզորությունը լայնորեն օգտագործվում է ջերմության քանակությունը հաշվարկելու համար ք 12, որը պետք է ծախսվի մարմինը մեկ ջերմաստիճանից տաքացնելու համար ( տ 1) մյուսին ( տ 2) (կամ որը կթողարկվի սառչելուց հետո տ 2 դեպի տ 1).
որոշում է, այսպես կոչված, իրական ջերմային հզորությունը, այսինքն, ջերմային հզորության արժեքը տվյալ ջերմաստիճանում: Գործնականում ջերմային հզորությունը լայնորեն օգտագործվում է ջերմության քանակությունը հաշվարկելու համար ք 12, որը պետք է ծախսվի մարմինը մեկ ջերմաստիճանից տաքացնելու համար ( տ 1) մյուսին ( տ 2) (կամ որը կթողարկվի սառչելուց հետո տ 2 դեպի տ 1).
Եթե ջերմային հզորությունը չի փոխվում նշված ջերմաստիճանի միջակայքում, ապա
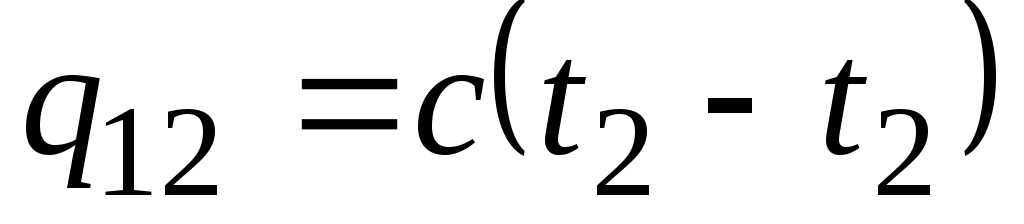 , կՋ/կգ եւ
, կՋ/կգ եւ 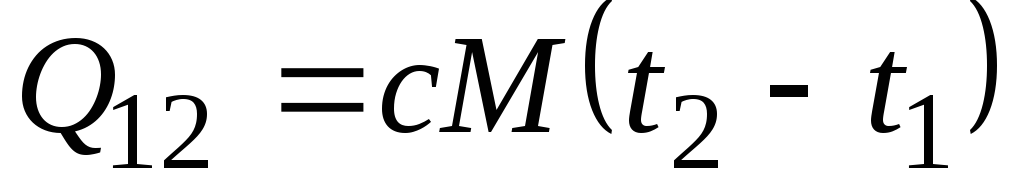 , կՋ. (2.21)
, կՋ. (2.21)
Այս բանաձևը կարող է օգտագործվել նաև մոտավոր (ոչ շատ ճշգրիտ) հաշվարկների համար։ Օրինակ՝ ջրի տեսակարար ջերմային հզորությունը սենյակային ջերմաստիճանում կազմում է 4,187 կՋ/(կգC), իսկ օդը՝ 1 կՋ/(կգC): Քանի որ գրեթե բոլոր նյութերի ջերմային հզորությունը փոխվում է (առավել հաճախ ավելանում) ջերմաստիճանի բարձրացման հետ, անհրաժեշտ է, խստորեն ասած, օգտագործել բանաձևը.
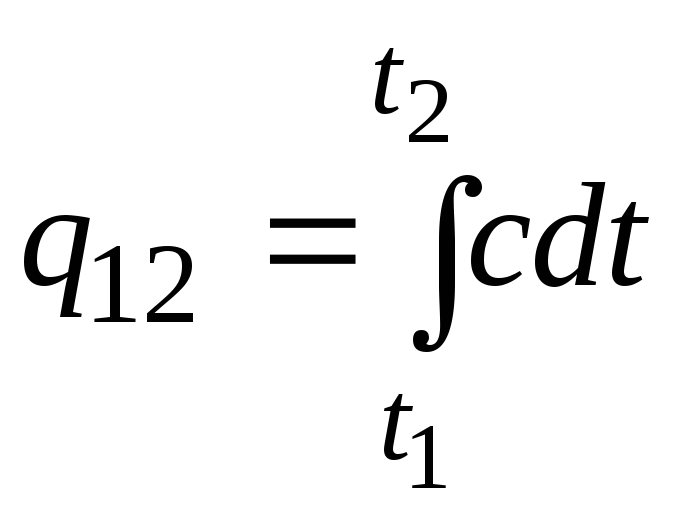 .
(2.21ա)
.
(2.21ա)
Նկ. 2.2 մագնիտուդ ք 12-ը ցուցադրվում է որպես ստվերավորված տարածք: Թվում է, որ ամենահեշտ ձևը, կիրառելով միջին արժեքի թեորեմը, գրելն է
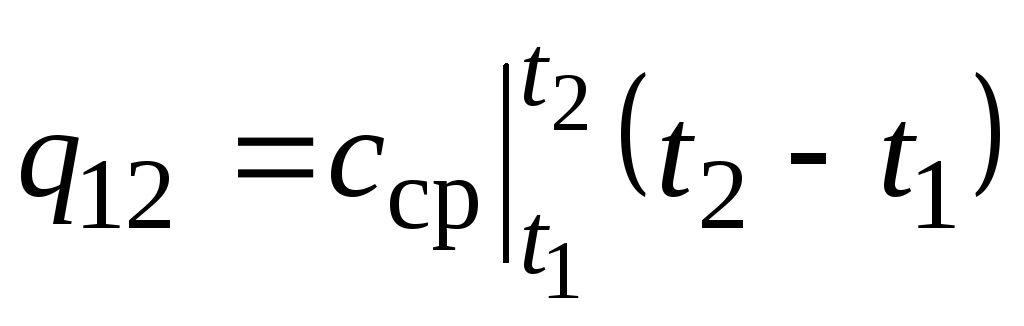 ,
(2.22)
,
(2.22)
որտեղ 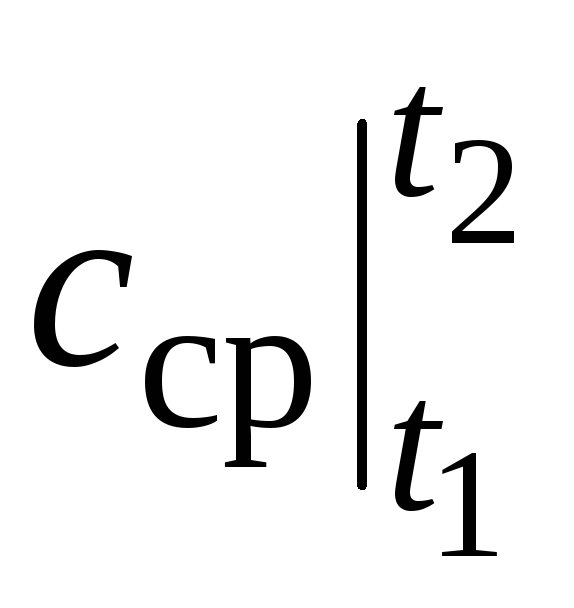 ջերմաստիճանի միջակայքում միջին ջերմային հզորությունն է տ 1 …տ 2 .
ջերմաստիճանի միջակայքում միջին ջերմային հզորությունն է տ 1 …տ 2 .
Բրինձ. 2.2. Իրական ջերմային հզորության կախվածությունը ջերմաստիճանից
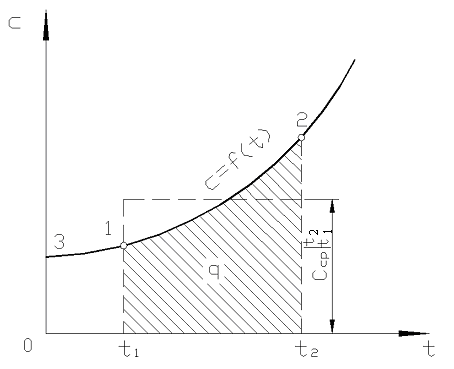
Այնուամենայնիվ, իրական հաշվարկների համար նման նշումը շատ անհարմար է, քանի որ ջերմային հզորությունը ընտրվում է աղյուսակներից, և 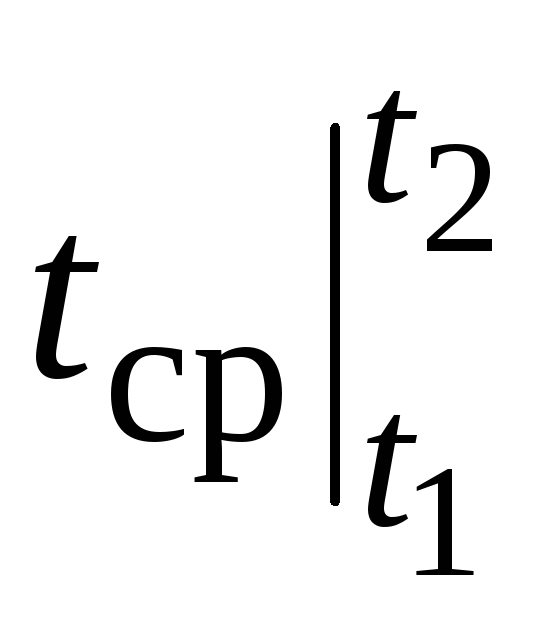 կախված է նրանից, թե ինչպես տ 1-ից և տ 2. Երկու արգումենտներից բաղկացած ֆունկցիաների աղյուսակը շատ դժվար կլինի:
կախված է նրանից, թե ինչպես տ 1-ից և տ 2. Երկու արգումենտներից բաղկացած ֆունկցիաների աղյուսակը շատ դժվար կլինի:
Գործնականում վարվեք հետևյալ կերպ. Ջերմության ցանկալի քանակությունը ներկայացվում է որպես մարմնին 0 С-ից մինչև ջերմաստիճան տաքացնելու համար պահանջվող քանակությունների տարբերություն։ տ 2 և տ 1 համապատասխանաբար (նկ. 2.2)
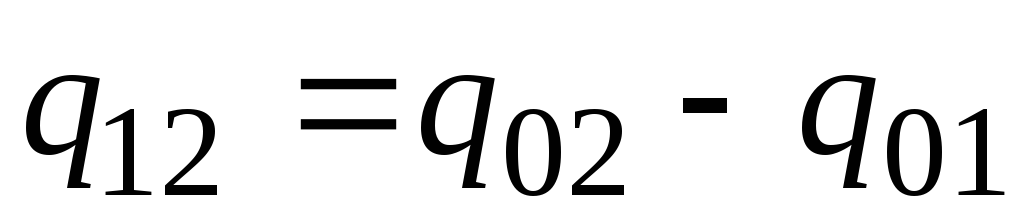 . (2.23)
. (2.23)
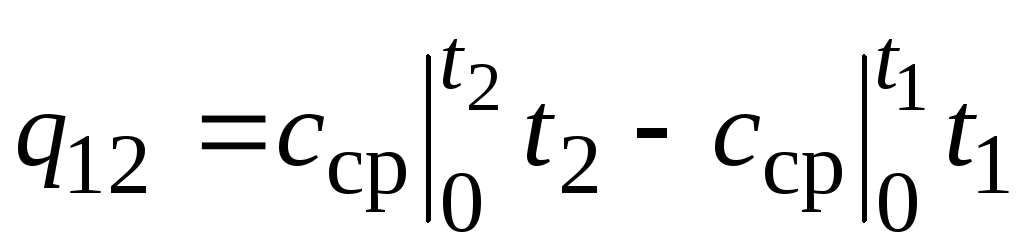 ,
(2.24)
,
(2.24)
որտեղ 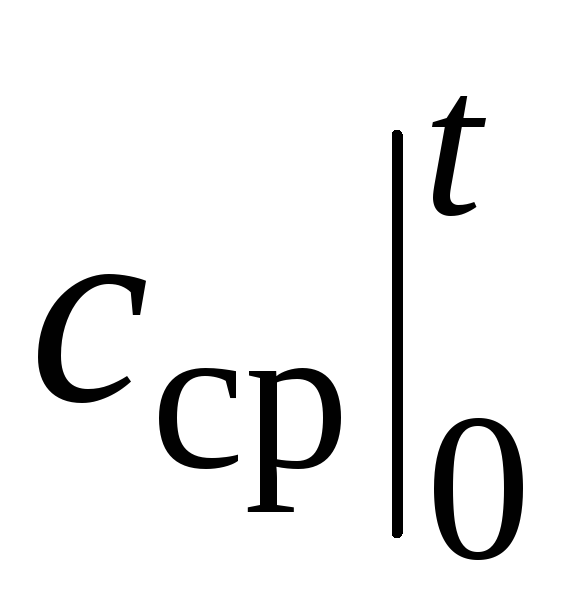 - միջին ջերմային հզորությունը ջերմաստիճանի միջակայքում 0… տC.
- միջին ջերմային հզորությունը ջերմաստիճանի միջակայքում 0… տC.
Միջին ջերմային հզորության արժեքը 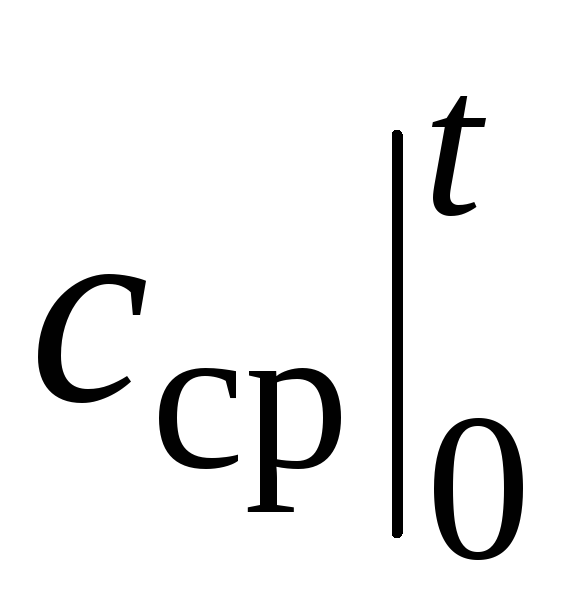 տվյալ նյութի համար (և տվյալ գործընթացի համար, այսինքն. Հետ Ռկամ գ v) կախված է միայն մեկ ջերմաստիճանից տ. Հենց այս ջերմային հզորություններն են բոլոր աղյուսակներում տրված «միջին» անվան տակ։ Ասվածը ճիշտ է Հետ
(Հետ Ռև գ v), ինչպես նաև համար Հետ և Հետ. Որպես օրինակ՝ ստորև բերված աղյուսակը ցույց է տալիս որոշ ամենատարածված գազերի ջերմային հզորությունը՝ համեմատած ջերմաստիճանի հետ: Հարկ է ընդգծել, որ (2.24) բանաձեւում ջերմաստիճանը փոխարինվում է Ցելսիուսի աստիճաններով։
տվյալ նյութի համար (և տվյալ գործընթացի համար, այսինքն. Հետ Ռկամ գ v) կախված է միայն մեկ ջերմաստիճանից տ. Հենց այս ջերմային հզորություններն են բոլոր աղյուսակներում տրված «միջին» անվան տակ։ Ասվածը ճիշտ է Հետ
(Հետ Ռև գ v), ինչպես նաև համար Հետ և Հետ. Որպես օրինակ՝ ստորև բերված աղյուսակը ցույց է տալիս որոշ ամենատարածված գազերի ջերմային հզորությունը՝ համեմատած ջերմաստիճանի հետ: Հարկ է ընդգծել, որ (2.24) բանաձեւում ջերմաստիճանը փոխարինվում է Ցելսիուսի աստիճաններով։
Տարբեր գազերի միջին մոլային ջերմային հզորությունը ժամը Ռ=կոնստ
(ըստ Մ.Պ. Վուկալովիչի, Վ.Ա. Կիրիլինի, Վ.Ն. Տիմոֆեևի)
|
տ, C |
Հետ Ռ, կՋ/(kmolK) |
|||||||
|
N 2 մթնոլորտային | ||||||||
Այս աղյուսակում արժեքները Հետ p տրված են 100 С-ի միջոցով: Քանի որ դրանք շատ չեն փոխվում ջերմաստիճանի հետ, միջանկյալ արժեքները կարելի է գտնել գծային էքստրապոլացիայի միջոցով: Հիշեք, թե ինչպես է դա արվում: Կան աղյուսակային ֆունկցիայի արժեքներ y
= զ(x) ժամը 1 (երբ X= X 1) և ժամը 2 (երբ X= X 2). Ֆունկցիայի արժեքը ժամը(X) ժամը X 1 <X<X 2 հավասար է 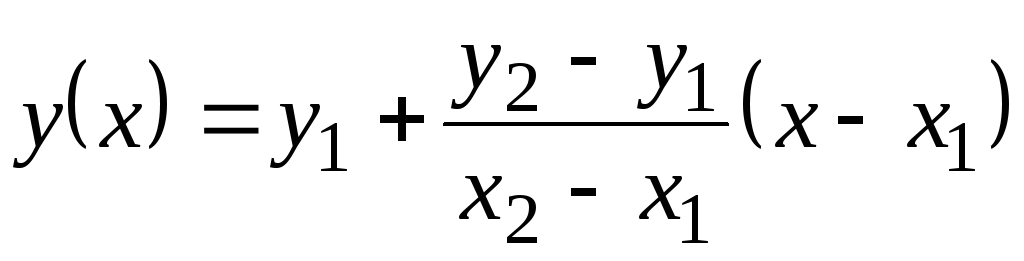 . Այս բանաձևը ճիշտ է ինչպես միապաղաղ աճող ֆունկցիայի դեպքում (երբ ժամը 2 >ժամը 1) և միապաղաղ նվազման համար ( ժամը 2 <ժամըմեկ); Այս դեպքում կոտորակը բացասական կլինի, քանի որ X 2 > X 1 միշտ.
. Այս բանաձևը ճիշտ է ինչպես միապաղաղ աճող ֆունկցիայի դեպքում (երբ ժամը 2 >ժամը 1) և միապաղաղ նվազման համար ( ժամը 2 <ժամըմեկ); Այս դեպքում կոտորակը բացասական կլինի, քանի որ X 2 > X 1 միշտ.
Աղյուսակում ներկայացված են գազերի ջերմային հաղորդունակության արժեքները՝ կախված ջերմաստիճանից և ճնշումից:
Ջերմային հաղորդունակության արժեքները նշվում են 20 K (-253 °C) մինչև 1500 K (1227 °C) և 1-ից մինչև 1000 մթնոլորտ ճնշման միջակայքում գտնվող ջերմաստիճանների համար:
Աղյուսակ հաշվի առնելով հետևյալ գազերի ջերմահաղորդականությունը, , ֆրեոն-14 CF 4 , էթիլեն C 2 H 4 : Ջերմային հաղորդունակության միավորը W/(m deg) է։
Հարկ է նշել, որ գազերի ջերմային հաղորդունակությունը մեծանում է ջերմաստիճանի և ճնշման բարձրացմամբ. Օրինակ, ամոնիակ գազի ջերմային հաղորդունակությունը սենյակային ջերմաստիճանում և նորմալ մթնոլորտային ճնշման դեպքում կազմում է 0,024 Վտ / (մ deg), իսկ երբ այն տաքացվում է 300 աստիճանով, ջերմային հաղորդունակությունը մեծանում է մինչև 0,067 Վտ / (մ աստիճան): Եթե այս գազի ճնշումը հասցվի 300 մթնոլորտի, ապա ջերմահաղորդականության արժեքը կբարձրանա և կունենա 0,108 Վտ/(մ աստիճան):
Նշում. Զգույշ եղեք. Աղյուսակում ջերմահաղորդականությունը նշված է 10 3 գործակցով: Մի մոռացեք բաժանել 1000-ի:
Անօրգանական գազերի ջերմահաղորդականությունը՝ կախված ջերմաստիճանից
Աղյուսակը տալիս է անօրգանական գազերի ջերմային հաղորդունակության արժեքները՝ կախված նորմալ մթնոլորտային ճնշման ջերմաստիճանից: Գազերի ջերմային հաղորդունակության արժեքները նշվում են 80-ից 1500 Կ (-193 ... 1227 ° C) ջերմաստիճանում:
Աղյուսակում ներկայացված են հետևյալ գազերի ջերմահաղորդականությունը՝ ազոտի օքսիդ N 2 O, ծծմբի հեքսաֆտորիդ SF 6, ազոտի օքսիդ NO, ջրածնի սուլֆիդ H 2 S, ամոնիակ NH 3, ծծմբի երկօքսիդ SO 2, գոլորշու H 2 O, ածխածնի երկօքսիդ CO 2։ , ծանր ջրի գոլորշի D 2 O, օդ.
Հարկ է նշել, որ անօրգանական գազերի ջերմային հաղորդունակությունը մեծանում է գազի ջերմաստիճանի բարձրացման հետ։
Ծանոթագրություն. Աղյուսակում գազերի ջերմահաղորդականությունը նշված է 10 3 գործակցով: Մի մոռացեք բաժանել 1000-ի:
Օրգանական գազերի ջերմահաղորդականությունը՝ կախված ջերմաստիճանից
Աղյուսակը ցույց է տալիս օրգանական գազերի և որոշ հեղուկների գոլորշիների ջերմահաղորդականության արժեքները՝ կախված նորմալ մթնոլորտային ճնշման ջերմաստիճանից: Գազերի ջերմային հաղորդունակության արժեքները տրված են աղյուսակում 120-ից 800 Կ ջերմաստիճանի միջակայքում:
Տրված է հետևյալ օրգանական գազերի և հեղուկների ջերմահաղորդականությունը.ացետոն CH 3 COCH 3, օկտան C 8 H 18, պենտան C 5 H 12, բութան C 4 H 10, հեքան C 6 H 14, պրոպիլեն C 3 H 6, հեպտան C 7 H 16, ամիլ սպիրտ C 5 H 11 OH, քսիլեն C 8 H 10, իզոպրոպիլային սպիրտ C 2 H 7 OH, մեթան CH 4, մեթիլ սպիրտ CH 3 OH, ածխածնի տետրաքլորիդ CCl 4, ցիկլոհեքսան C 6 H 12, էթան C 2 H 6, ածխածնի տետրաֆտորիդ CF 4, ֆրեոն-11 3, էթիլ քլորիդ C 2 H 5 Cl, ֆրեոն-12 CF 2 Cl 2, էթիլեն C 2 H 4, ֆրեոն-13 CF 3 Cl, էթիլ ֆորմատ HCOOC 2 H 5, ֆրեոն-21 CHFCl 2, դիէթիլ եթեր (C 2 H 5) 2Օ.
Ինչպես երևում է աղյուսակից. Օրգանական գազերի ջերմահաղորդականության արժեքը նույնպես մեծանում է գազի ջերմաստիճանի բարձրացման հետ.
Զգույշ եղիր! Աղյուսակում ջերմահաղորդականությունը նշված է 10 3 գործակցով: Մի մոռացեք բաժանել 1000-ի:Օրինակ, ացետոնի գոլորշու ջերմային հաղորդունակությունը 400 Կ (127°C) ջերմաստիճանում կազմում է 0,0204 Վտ/(մ աստիճան):
