Suyun özgül ısı kapasitesi nasıl belirlenir? Büyük petrol ve gaz ansiklopedisi
CİHAZLAR VE AKSESUARLAR: kalorimetre, termometre, terazi, test gövdeleri, beher (gram cinsinden derecelendirilmiş), elektrikli ısıtma cihazı.
– ısı dengesi denkleminin geçerliliğinin deneysel olarak doğrulanması;
– katıların spesifik ısı kapasitelerini hesaplamak;
– ölçüm ve hesaplama sonuçlarını bir tablo şeklinde düzenlemek;
– Bu çalışmada ölçüm ve hesaplama tekniklerinin geliştirilmesine yönelik önerilerinizi yazın.
KISA DENEY TEORİSİ
Termodinamiğin temel fiziksel kavramlarından biri ısı kapasitesidir.
Vücudun ısı kapasitesi isminde fiziksel miktar, sayısal olarak ısıya eşit Söz konusu termodinamik süreçte sıcaklığını 1 K değiştirmek için vücuda iletilmesi gerekir. Öte yandan, bir cismin ısı kapasitesi, söz konusu termodinamik süreçte vücuda verilen dQ ısısının vücut sıcaklığındaki dT değişimine oranına eşittir:
Bir cismin ısı kapasitesi ona bağlıdır. kimyasal bileşim, vücut kütlesi ve onun termodinamik durumu ve ayrıca tanımdan da görülebileceği gibi, dQ ısısının sağlandığı vücudun durumunu değiştirme işleminin türü.
Termal özellikler homojen cisimler, spesifik ve molar (molar) ısı kapasitesi değerleriyle karakterize edilir. Bir maddenin özgül ısı kapasitesi fiziksel büyüklük denir İle, sayısal olarak, söz konusu termodinamik süreçte bir maddenin bir kilogramının sıcaklığını 1 K değiştirmek için verilmesi gereken ısıya eşittir. Homojen bir cismin ısı kapasitesi, cismin kütlesinin çarpımı olarak tanımlanabilir. M spesifik ısı kapasitesi için İle içindeki maddeler:
![]() veya (2.2).
veya (2.2).
Dolayısıyla homojen bir cisim için dQ ve dT arasındaki ilişki şu şekildedir:
Molar ısı kapasitesi Söz konusu termodinamik işlemde bir maddenin bir molünün sıcaklığını 1 K değiştirmek için verilmesi gereken ısıya sayısal olarak eşit olan fiziksel bir miktar C olarak adlandırılır:
İLE = Hanım = (2.4),
burada M maddenin molar kütlesidir; İLE aynı süreçteki özgül ısı kapasitesidir.
İfade (2.4) artık şu şekilde yazılabilir:
burada = n madde miktarıdır.
Bir cismin ısı kapasitesinin ölçü birimi 1 J/K'dir. spesifik ısı kapasitesi– 1J/kg. K, molar – 1 J/mol. İLE.
Hacmin sabit kaldığı koşullar altında ısıtma meydana gelirse, buna karşılık gelen molar ısı kapasitesi denir. sabit hacimde ısı kapasitesi veya izokorik ısı kapasitesidir ve Cv ile gösterilir:
Isıtma sırasında basınç sabit kalırsa, ısı kapasitesine denir. sabit basınçta ısı kapasitesi C p (izobarik ısı kapasitesi olarak da adlandırılabilir):
Katılar için, sabit hacimde değil, yalnızca sabit basınçta ısı kapasitesinin doğrudan ölçülebileceğini unutmayın, çünkü termal genleşme nedeniyle vücudun sabit bir hacmini sağlamak imkansızdır. Ancak ısıtma sırasında hacimdeki küçük değişiklik nedeniyle ısı kapasiteleri Cp ve Cv arasındaki fark küçüktür.
Bir cismin ısı kapasitesi, ısı dengesi denklemi kullanılarak deneysel olarak belirlenir. Vücudun sıcaklıktan daha yüksek bir sıcaklığa ısıtılmasına izin verin çevre. Daha sonra vücut soğudukça bir miktar ısı yayar. Kapalı bir sistemde enerjinin korunumu kanununa göre ortamın aldığı ısı miktarının cismin verdiği ısı miktarına tam olarak eşit olması gerekir. Bu çalışmada test gövdesi soğudukça ısıyı kalorimetredeki suya ve kalorimetrenin kendisine aktarıyor.
Bu kütle kütlesini test edelim M, sıcaklığa kadar ısıtılır t 0 sıcaklığına sahip su ile bir kalorimetreye indirildi. t 1. Isı değişiminin bir sonucu olarak su sıcaklığı ve kalorimetre artar t 2, A Vücut ısısı aşağı iner t 2. Vücudun verdiği ısı miktarı şuna eşittir:
Q bölümü = santimetre(t 0 - t 2) (2.6),
burada c test gövdesinin özgül ısı kapasitesidir,
t 0– başlangıç vücut ısısı,
t 2– son vücut ısısı,
M- vücut kütlesi.
Kalorimetre ve suyun aldığı ısı miktarı şuna eşittir:
kalorimetrenin kütlesi ve özgül ısı kapasitesi nerede ve nerede,
I – kütle ve spesifik suyun ısı kapasitesi,
t 1– başlangıç su sıcaklığı,
t 2– son su sıcaklığı.
Kapalı bir sistemde enerjinin korunumu yasasına göre:
Q ayrı = Q katı (2.8).
Daha sonra formül 2.6 ve 2.7'yi denklem 2.8'de yerine koyarak istenen değeri ifade ederiz. İLE , şunu elde ederiz:
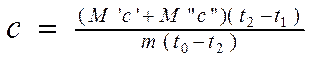 (2.9).
(2.9).
FARKLI METALLERDEN ÜÇ SİLİNDİRİK GÖVDESİN ÖZEL ISI KAPASİTELERİNİN BELİRLENMESİ
1. Vücut kütlelerinin değerlerini belirleyin – ben ben, kalorimetrenin kütlesi – , suyun özgül ısı kapasitesi – , kalorimetrenin özgül ısı kapasitesi – .
2. Kalorimetreye tartılmış miktarda oda sıcaklığında soğuk su (yaklaşık 150 g) dökün.
3. Soğuk suyun başlangıç sıcaklığını ölçün t 1.
4. Kaptaki suyu kaynayana kadar ısıtın.
5. Test gövdelerinden birini bir süre kaynar suya koyun. Isıtılan cismin sıcaklığını alın t 0 eşit sıcaklık Normal şartlarda suyun kaynama noktası 100°C'dir.
6. Isıtılmış gövdeyi su dolu bir kalorimetreye yerleştirin. Isı değişiminin sonuna kadar bekleyin ve kalorimetredeki son sıcaklığı ölçün – t 2 .
8. Diğer iki cismin özgül ısı kapasitelerini benzer şekilde belirleyiniz.
9. Ölçümlerin ve hesaplamaların sonuçlarını tablo 3'e girin.
10. Spesifik ısı kapasitelerinin değerlerini kullanarak gövdelerin yapıldığı maddeleri belirleyin.
12. Cisimlerin doğrusal boyutlarını ölçerek yoğunluklarını belirleyin.
13. Hataları hesaplayın ve sonucu GOST'a göre kaydedin.
14. Laboratuvar çalışmalarından elde edilen sonuçları yazın.
Tablo 3
| HAYIR. | M", kg | M", kg | m, kg | C", J/kg. K | C", J/kg. K | t 0,0 C | t 1,0 C | t 2,0 C | C, J/kg. İLE |
Sayfa 2
Sykes'e göre spesifik ısı kapasitesinin belirlenmesinin doğruluğu çok yüksektir. Ancak bu yöntem, Smith yöntemine göre daha büyük deneysel zorluklarla ilişkilidir ve soğuma eğrilerinin elde edilmesi için de uygulanabilmesine rağmen, yalnızca ısıtma eğrileri için doğru sonuçlar verir. Smith'in yöntemi dar sıcaklık aralıklarının incelenmesini kolaylaştırır, ancak muhtemelen daha az doğrudur.
Sonuç olarak, bir maddenin özgül ısı kapasitesini c belirlemek için, cisme etki eden dış kuvvetlerin yaptığı A işinin ölçülmesi ve ısı olmadığında yapılan iş sonucunda vücut sıcaklığında gözlenen değişimin ölçülmesi gerekir. diğer kurumlarla değişim.
Spesifik ısı kapasitesinin belirlenmesinde en yaygın yöntem; karıştırma yöntemi denir. Kalorimetre (Regault), birim hacim başına termal iletkenliği ve ısı kapasitesi ihmal edilebilir olan bir hava tabakası ile ayrıldığı, başka bir bakır kabın tabanındaki ahşap ayaklar üzerine yerleştirilen kırmızı bakır bir kaptan oluşur. Birinci kap su ile doldurulur.
Şimdi bir gaz karışımının özgül ısı kapasitesini belirleme yöntemlerini ele alalım.
Spesifik ısı kapasitesi Cy'nin doğrudan (doğrudan) belirlenmesi ve sıcaklığa ve spesifik hacme bağlı olarak değişiminin seyrinin incelenmesi, Etkili araçlar Maddelerin kritik durumunun incelenmesi. Bu nedenle, ısı kapasitesinin deneysel olarak belirlenmesi, kritik olayların incelenmesinde teorik ve pratik açıdan büyük önem taşımaktadır.
Çözeltilerin özgül ısı kapasitesini belirleme formülü nedir?
Karıştırma yöntemiyle spesifik ısı kapasitesini belirlemek için deneyler yaparken, incelenen numunenin kesin olarak sabit bir sıcaklığa ısıtılması gerekir. Bu amaçla, ısıtılan numunenin hızlı bir şekilde kalorimetreye aktarılması için gereken kısa süre için kalorimetrenin üzerine monte edilen portatif ısıtıcılar kullanılır.
| Cihaz diyagramı. |
Spesifik ısı kapasitesini belirlemek için en basit mutlak sabit yöntemin özü şuna iner: ısıtıcı ve soğutucu arasına h kalınlığında ve 5 kesit alanına sahip bir test malzemesi örneği yerleştirilir. Isıtıcı bir kap olabilir sıcak su veya bir elektrikli ısıtma elemanı, böylece voltajı değiştirerek gücü isteğe göre ayarlanabilir. Soğutucu, içinden soğuk suyun geçtiği içi boş bir metal gövdedir. Numunenin ısıtılan ve soğutulan yüzeylerindeki sıcaklıklar (tj ve buna bağlı olarak /2) termokupllar ile ölçülür.
Aşağıda bir kumtaşı numunesinin spesifik ısı kapasitesini belirlerken deneysel verilerin işlenmesine bir örnek verilmiştir. İncelenen kaya örneğinin tozuyla doldurulmuş içi boş bir silindir, 40°C'ye ısıtıldı ve sakin bir hava odasında 18-20°C sıcaklığa soğutuldu.
İncirde. Şekil 3 - 6, sıvı ayrı hidrokarbonların ve yağ karışımlarının yanı sıra metanol ve etanolün sulu çözeltilerinin spesifik ısı kapasitesinin belirlenmesine yönelik nomogramları göstermektedir.
Örneğin kalorimetre kullanarak bir maddenin özgül ısı kapasitesini belirlemek için kullanılan bir ısı dengesi denklemi oluşturalım. Bu durumda yaklaşık olarak üç cismin ısı alışverişine katıldığı varsayılabilir: kalorimetre, sıvı ve özgül ısı kapasitesi belirlenen cisim.
6.4. Vücutlar arasındaki ısı alışverişi
6.4.1. Vücudun ısı kapasitesi, spesifik Bir maddenin ısı kapasitesi, bir maddenin molar ısı kapasitesi
Vücut ısısını arttırmak için belli miktarda ısı vermesi gerekir.
Bu maddenin 1 K başına 1 kg'ına denir bir maddenin özgül ısı kapasitesi ve formülle hesaplanır
c vuruş = Q m Δ T ,
burada Q, belirli bir madde kütlesini ısıtmak için gereken ısı miktarıdır; m, maddenin kütlesidir; ΔT, bir maddenin ısıtıldığında sıcaklığındaki değişikliktir.
Uluslararası Birim Sisteminde, bir maddenin özgül ısı kapasitesi joule cinsinden kilogram kelvin'e (1 J/(kg ⋅ K)) bölünerek ölçülür.
Isıtma için gerekli ısı miktarı bir miktar madde kütlesi, ürüne göre belirlenir
Q = c yendi m ∆T .
Belirli bir cismi 1 K kadar ısıtmak için gereken ısı miktarına denir. vücudun ısı kapasitesi ve formülle hesaplanır
C = QΔT,
burada Q, belirli bir cismi ısıtmak için gereken ısı miktarıdır; ΔT ısıtıldığında vücut sıcaklığındaki değişikliktir.
Uluslararası Birim Sisteminde bir cismin ısı kapasitesi joule bölü kelvin (1 J/K) cinsinden ölçülür.
Belirli bir cismi ısıtmak için gereken ısı miktarı ürüne göre belirlenir.
Q = CΔT,
burada C vücudun ısı kapasitesidir.
Bir cismin ısı kapasitesi ile cismi oluşturan maddenin ısı kapasitesi birbirine bağlı ifade
C = mc atım,
burada C vücudun ısı kapasitesidir; m - vücut ağırlığı; csp, bu cismin yapıldığı maddenin özgül ısı kapasitesidir.
Belirli bir maddenin 1 molünü 1 K ısıtmak için gereken ısı miktarına denir. Bir maddenin molar ısı kapasitesi ve formülle hesaplanır
c μ = Q ν Δ T ,
burada Q, bir maddenin belirli bir miktarını ısıtmak için gereken ısı miktarıdır; ν - madde miktarı; ΔT, belirli miktardaki bir maddenin ısıtıldığında sıcaklığındaki değişikliktir.
Uluslararası Birim Sisteminde, bir maddenin molar ısı kapasitesi mol kelvin başına joule (1 J/(mol ⋅ K)) cinsinden ölçülür.
Isıtma için gerekli ısı miktarı bir miktar madde, ürüne göre belirlenir
Q = c µ νΔT .
Bir maddenin molar ve özgül ısı kapasitesi birbirine bağlı ifade
c µ = Ms atım,
burada c µ maddenin molar ısı kapasitesidir; M, maddenin molar kütlesidir; csp, maddenin özgül ısı kapasitesidir.
Örnek 14. Demir ve kurşun topların çapları aynıdır. Demir topun ısı kapasitesi kurşun topun ısı kapasitesinin kaç katıdır? Demir ve kurşunun özgül ısı kapasiteleri sırasıyla 0,46 ve 0,13 kJ/(kg ⋅ K) ve yoğunlukları sırasıyla 7,80 ve 11,5 g/cm3'tür.
Çözüm . Topların ısı kapasiteleri aşağıdaki formüllerle belirlenir:
- demir top -
C 1 = m 1 c ud1,
burada m1 demir topun kütlesidir; csp1 - demirin özgül ısı kapasitesi;
- kurşun top -
C 2 = m 2 c vuruş2,
burada m2 kurşun topun kütlesidir; csp2 - kurşunun özgül ısı kapasitesi.
Gerekli ısı kapasitesi oranı:
C 1 C 2 = m 1 c atım 1 m 2 c atım 2,
demir ve kurşun bilyaların kütlelerinin oranı ve demir ve kurşunun özgül ısı kapasitelerinin oranı ile belirlenir.
Topların kütleleri boyutlarına ve yoğunluklarına göre belirlenir:
- demir top -
m 1 = ρ 1 V 1,
burada ρ 1 demirin yoğunluğudur; V 1 - demir topun hacmi;
- kurşun top -
m2 = ρ2V2,
burada ρ2 kurşunun yoğunluğudur; V2 kurşun topun hacmidir.
Topların çapları aynı olduğundan hacimleri de aynıdır:
V 1 = V 2 = V = π d 2 6,
burada d demir ve kurşun bilyaların çaplarıdır.
Son durum dikkate alındığında kütle oranı şuna eşittir:
m 1 m 2 = ρ 1 V 1 ρ 2 V 2 = ρ 1 ρ 2 .
Demir ve kurşun bilyaların ısı kapasitelerinin oranı formülünde m 1 /m 2'yi yazalım:
C 1 C 2 = ρ 1 c 1'i yendi ρ 2 c 2'yi yendi .
Hesaplamayı yapalım:
C 1 C 2 = 7,80 ⋅ 10 3 ⋅ 0,46 ⋅ 10 3 11,5 ⋅ 10 3 ⋅ 0,13 ⋅ 10 3 = 2,4.
Demir topun ısı kapasitesi kurşun topun ısı kapasitesinden 2,4 kat daha fazladır.
Örnek 15. Karışımı hazırlarken bir bunkerin içine belirli bir kütle kum ve dört katı çimento kütlesi döküldü. Çimento ve kumun özgül ısı kapasiteleri sırasıyla 810 J/(kg ⋅ K)'dir. Karışımın özgül ısı kapasitesini belirleyiniz.
Çözüm . Karışımın özgül ısı kapasitesi formülle belirlenir.
c vuruş = Q m Δ T ,
burada Q, karışımın sıcaklığını ΔT kadar artırmak için gereken ısı miktarıdır; m karışımın kütlesidir.
Karışımı ısıtmak için gereken ısı miktarı;
S = Ç 1 + Ç 2,
burada Q1, karışıma dahil edilen kumu ΔT kadar ısıtmak için gereken ısı miktarıdır; Q2, karışıma dahil edilen çimentoyu ΔT kadar ısıtmak için gereken ısı miktarıdır.
Isıtma için gerekli ısı miktarı:
- kum -
Q 1 = c sp1 m 1 ∆T ,
burada csp1 kumun özgül ısı kapasitesidir; m 1 - kum kütlesi;
- çimento -
Q 2 = c sp2 m 2 ∆T,
burada csp2 çimentonun özgül ısı kapasitesidir; m 2 - çimento kütlesi.
Kum ve çimento karışımını ısıtmak için gereken ısı miktarı şu şekilde verilir:
Q = c 1 m 1'i yendi Δ T + c 2 m 2'yi yendi Δ T = (c 1 m 1'i yendi + c 2 m 2'yi yendi) Δ T.
Karışımın kütlesi kum ve çimento kütlelerinin toplamıdır:
m = m1 + m2 .
Karışımın ısı miktarı ve kütlesi için elde edilen ifadeleri karışımın özgül ısı kapasitesi formülünde yerine koyalım:
c atım = (c atım 1 m 1 + c atım 2 m 2) Δ T (m 1 + m 2) Δ T = c atım 1 m 1 + c atım 2 m 2 m 1 + m 2.
Ortaya çıkan ifadeyi kütle oranını dikkate alarak dönüştürelim:
m2 = 4m1, yani. c atım = c atım 1 m 1 + 4 c atım 2 m 1 m 1 + 4 m 1 = c atım 1 + 4 c atım 2 5.
Hesaplama değeri verir:
c vuruş = 960 + 4 ⋅ 810 5 = 840 J/(kg ⋅ K).
Dolayısıyla karışımın özgül ısı kapasitesi 840 J/(kg ⋅ K)'dir.
