La unidad para medir la cantidad de calor es la fórmula. Cantidad de calor. Unidades de cantidad de calor. Calor especifico

¿Qué proceso se llama conducción térmica? ¿En qué entornos es posible? ¿Es lo mismo para varias sustancias? ¿Qué proceso se llama convección? ¿En qué entornos es posible? ¿De qué depende la velocidad de convección? ¿Qué proceso se llama radiación? ¿Qué características de este tipo de transferencia de calor conoces?

La energía que el calor gana o pierde durante la transferencia de calor se llama cantidad de calor. Designación: Q Unidades de medida: julio (J) (kJ) caloría (cal) 1 cal=4,19 J 1 kcal= 4190 J 4,2 kJ Caloría es la cantidad de calor necesaria para calentar 1 g de agua en 1 °C.

Etapa 1 del experimento 1. Vierta agua en los matraces: 2 veces más en el segundo matraz que en el primero. 2. Asegure los matraces en las patas de los trípodes 3. Mida la temperatura inicial del líquido en cada matraz. 4. Enciende las lámparas de alcohol. 5. Al mismo tiempo, empezar a calentar los matraces. 6. Mida la temperatura en cada matraz después de 2 minutos. 7. Saca una conclusión.
![]()
Un experimento para determinar la dependencia de la cantidad de calor transferido a una sustancia de la masa de esta sustancia. metro 1 
Etapa 2 del experimento 1. Vierta la misma cantidad de agua en 2 matraces. 2. Asegure los matraces en las patas de los trípodes 3. Mida la temperatura inicial del líquido en cada matraz. 4. Enciende las lámparas de alcohol. 5. Al mismo tiempo, empezar a calentar los matraces. 6. Sin sacar el termómetro del líquido, dejar de calentar cuando la temperatura en el primer matraz suba 20°C y en el segundo 25°C. 7. Mide el tiempo que tomó cada proceso. 8. Sacar conclusiones.

Un experimento para determinar la dependencia de la cantidad de calor transferida a una sustancia de los cambios en su temperatura. metro 1 = metro t 1 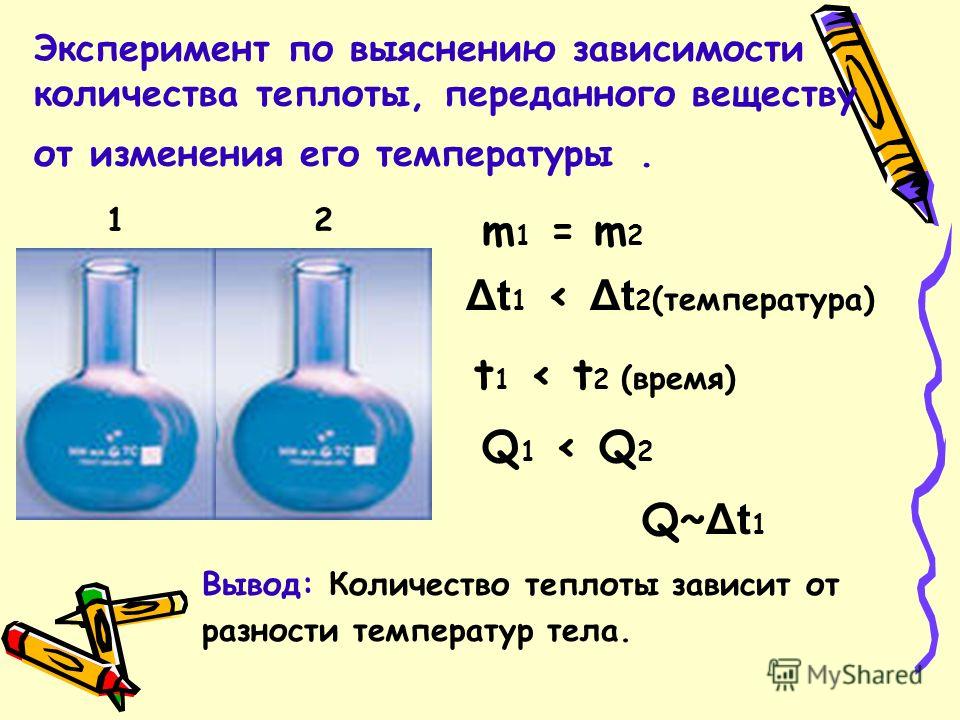
Etapa 3 del experimento 1. Vierta cantidades iguales de agua y aceite en 2 matraces. 2. Asegure los matraces en las patas de los trípodes 3. Mida la temperatura inicial del líquido en cada matraz. 4. Enciende las lámparas de alcohol. 5. Al mismo tiempo, empezar a calentar los matraces. 6. Mida la temperatura en cada matraz después de 2 minutos. 7. Saca una conclusión.

T 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia" title=" Experimento para determinar la dependencia de la cantidad de calor transmitida por su tipo m 1 = m 2 1 2 t 1 > t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar ( genial) un cuerpo depende del tipo de sustancia" class="link_thumb"> 11 !} Un experimento para determinar la dependencia de la cantidad de calor transferido de su tipo. m 1 = m t 1 > t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia. 1 2 Q ~ dependiendo del tipo de sustancia t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia "> t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia. 1 2 Q ~ del tipo de sustancia "> t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia" title=" Un experimento para determinar la dependencia de la cantidad de calor transferido de su tipo m 1 = m 2 1 2 t 1 > t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia"> title="Un experimento para determinar la dependencia de la cantidad de calor transferido de su tipo. m 1 = m 2 1 2 t 1 > t 2 (tiempo) Δt 1 = Δt 2 (temperatura) Q 1 > Q 2 Conclusión: la cantidad de calor necesaria para calentar (enfriar) un cuerpo depende del tipo de sustancia"> !}
Indicado por: s unidad de medida: J/kg °C Cantidad física, numéricamente igual a la cantidad de calor que se debe transferir a un cuerpo que pesa 1 kg para que su temperatura cambie 1ºC, se llama capacidad calorífica específica sustancias. Calor especifico sustancias.

La capacidad calorífica específica del acero es de 500 J/kg °C. Esto significa que para calentar (enfriar) acero m = 1 kg por 1ºC, se requiere una cantidad de calor igual a 500 J. La capacidad calorífica específica de una sustancia en diferentes estados de agregación es diferente. por ejemplo, para agua c = 4200 J/kg °C; para hielo c = 2100 J/kg °C


Consolidación ¿Cuál es la cantidad de calor? ¿En qué se mide? ¿De qué depende la cantidad de calor? ¿Cuál es la capacidad calorífica específica de una sustancia? ¿Cuál es la unidad de capacidad calorífica específica? La capacidad calorífica específica del plomo es de 140 J/kg °C. ¿Qué quiere decir esto?

¿Cuál es la capacidad calorífica específica del zinc, el ladrillo y el agua? ¿Qué cantidad de calor se debe impartir a estas sustancias que pesan 1 kg para calentarlas 1 ºС? Calcula la cantidad de calor (en calorías y kilocalorías). Se necesita para calentar agua a 1°C, cuya masa es 3; 4 kilogramos.


